Содержание
- 6. Пептизация - расщепление агрегатов, возникших при коагуляции дисперсных систем, на первичные частицы под действием жидкой среды
- 8. Любая химическая реакция может привести к образованию мицеллы при условии, что концентрация исходных веществ мала и
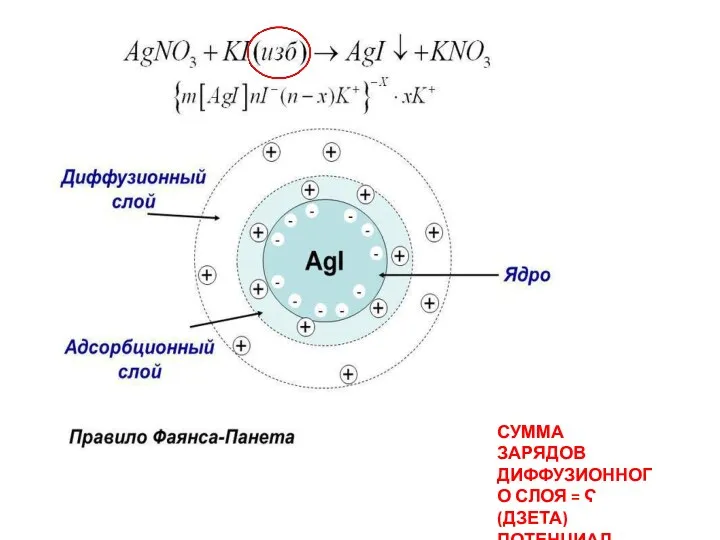
- 12. СУММА ЗАРЯДОВ ДИФФУЗИОННОГО СЛОЯ = Ϛ (ДЗЕТА) ПОТЕНЦИАЛ
- 13. Седиментация – осаждение частиц в растворе под действием силы тяжести, выпадение осадка. СЕДИМЕНТАЦИОННАЯ УСТОЙЧИВОСТЬ: - Размеры
- 14. Устойчивость коллоидных растворов
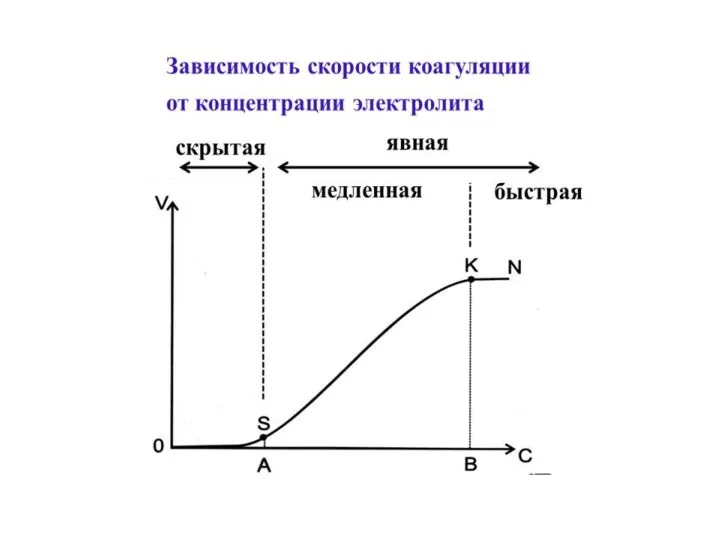
- 16. Электролитная коагуляция коллоидного раствора При добавлении любого электролита в раствор коллоидной системы происходит процесс коагуляции, в
- 19. Ионом коагулянтом в растворе электролита является тот ион, знак заряда которого противоположен знаку заряда гранулы (в
- 23. Организма человека и животных - коллоидные системы. Кровь является типичными примером ткани организма, где одни коллоиды
- 24. С точки зрения коллоидной химии плазма крови представляет собой сложную систему коллоидов. Белки - основная составляющая
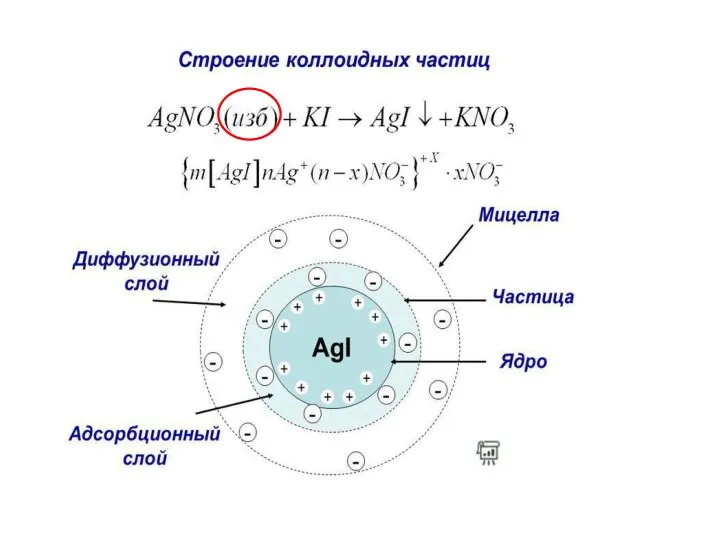
- 25. ? AgNO3 + KCl → AgCl↓ + KNO3 1) Нарисовать мицеллу 2) Заряд гранулы - ??
- 27. Скачать презентацию



















 Карбонові кислоти
Карбонові кислоти Молярна маса речовини
Молярна маса речовини Растворы. Общая характеристика растворов
Растворы. Общая характеристика растворов Скорость химической реакции
Скорость химической реакции Некоторые закономерности протекания химических реакций: тепловой эффект реакции, скорость реакции, химическое равновесие
Некоторые закономерности протекания химических реакций: тепловой эффект реакции, скорость реакции, химическое равновесие Степень окисления
Степень окисления Мыло. Мылящие вещества в природе
Мыло. Мылящие вещества в природе Виды и свойства текстильных материалов из химических волокон. 6 класс
Виды и свойства текстильных материалов из химических волокон. 6 класс Химико-аналитический контроль. Основы химико-аналитического контроля товаров
Химико-аналитический контроль. Основы химико-аналитического контроля товаров Қоспаларды бөлу әдістері
Қоспаларды бөлу әдістері Предельные углеводороды
Предельные углеводороды От кулинарии — к кулинохимии
От кулинарии — к кулинохимии Метали VI групи побічної підгрупи (Cr, Mo, W)
Метали VI групи побічної підгрупи (Cr, Mo, W) Классы неорганических соединений: Оксиды (8 класс)
Классы неорганических соединений: Оксиды (8 класс) Азот. Элемент V группы главной подгруппы
Азот. Элемент V группы главной подгруппы Номенклатура оснований. Классификация и примеры. Получение оснований. Химические свойства
Номенклатура оснований. Классификация и примеры. Получение оснований. Химические свойства Получение хлортетрациклина
Получение хлортетрациклина Реакции ионного обмена
Реакции ионного обмена Минеральные воды
Минеральные воды Химическое равновесие
Химическое равновесие Тепловой эффект химических реакций
Тепловой эффект химических реакций Химические элементы. Типы связей
Химические элементы. Типы связей Электротехнический фарфор – разновидность твердого фарфора
Электротехнический фарфор – разновидность твердого фарфора Химическая картина мира
Химическая картина мира Химические свойства кислот
Химические свойства кислот Производство метанола. Физико-химические основы синтеза метанола. Современные катализаторы
Производство метанола. Физико-химические основы синтеза метанола. Современные катализаторы Химическая организация клетки
Химическая организация клетки Формулы веществ. Относительная атомная масса. Относительная молекулярная масса. Массовая доля элементов в сложных веществах
Формулы веществ. Относительная атомная масса. Относительная молекулярная масса. Массовая доля элементов в сложных веществах