Содержание
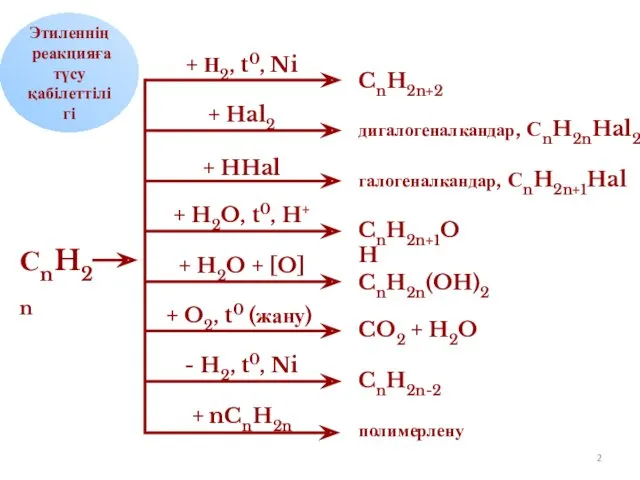
- 2. Этиленнің реакцияға түсу қабілеттілігі + Н2, t0, Ni + Hal2 + HHal + H2O, t0, H+
- 3. СН ОН 4. Гидратация: Pt, t Этиленнің химиялық қасиеттері 1. Гидрлеу: СН2 СН2 + Н2 СН3
- 4. Марковников ережесі Галогенсутектің сутек атомы сутегі көп көміртек атомына, ал галоген сутегі аз көміртек атомына қосылады.
- 5. Алкендердің алынуы 1)Катализдік дегидрлеу әдісі: CH3-CH3 CH2=CH2+H2 2)Спирттерді дегидратациялау: H3C-CH2-OH H2C=CH2+H2O 3)Дегидрогалогендеу: H3C-CH-CH2 H3C-CH=CH2 CI H
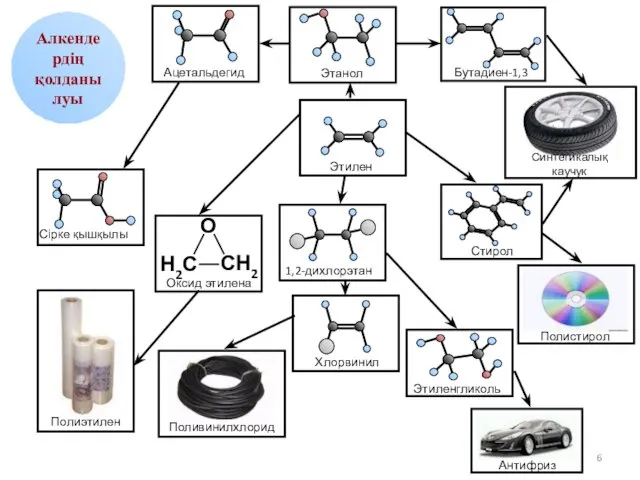
- 6. Алкендердің қолданылуы
- 7. Алкиндердің реакцияға түсу қабілеттілігі Қосылу реакциясы 1) Гидрлеу катализаторы (Ni, Pd немесе Pt), бірақ бұл реакция
- 8. 2) Галогендеу Алкиндер бром суын түссіздендіреді ( үш еселі байланыстың сапалық реакциясы).Реакция алкендермен салыстырғанда баяуырақ жүреді.
- 9. 4) Гидраттау (Кучеров реакциясы). Суды қосып алу реакциясы сынап сульфаты қатысында жүреді. Бұл реакцияны 1881 жылы
- 10. 5) Полимерлену. Ацетиленнің тримерленуі : kat HC≡CH + HC≡CH →CH2=CH–C≡CH kat CH2=CH–C≡CH + HC≡CH →CH2=CH–C≡C–CH=CH2 Cакт.,t
- 11. Алкиндердің қышқылдық қасиеттері. Ацетилендегі сутек атомдары ның орнын металл атомдары баса алады. Бұл кезде ацетиленидтер түзіледі.
- 12. Тотығу реакциясы Калий перманганаты әсерінен ацетилен қымыздық қышқылына дейін тотығып, KMnO4 ерітіндісін түссіздендіреді ( үш еселі
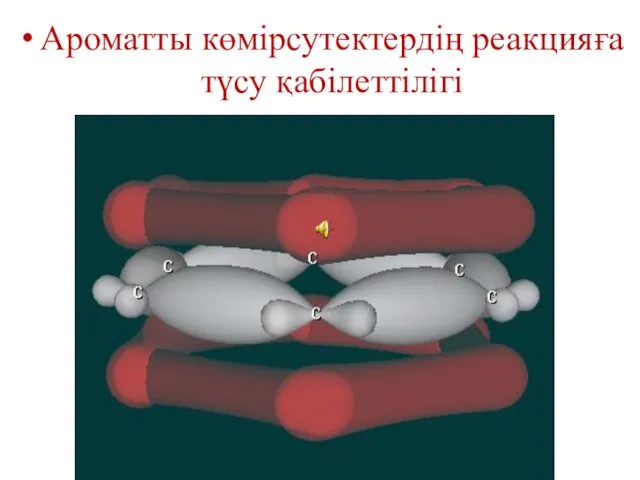
- 13. Ароматты көмірсутектердің реакцияға түсу қабілеттілігі
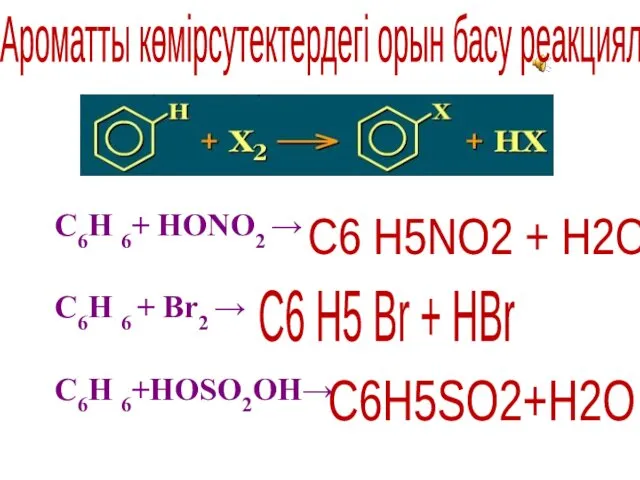
- 15. C6H 6+ HONO2 → C6H 6 + Br2 → C6H 6+HOSO2OH→ C6 H5NO2 + H2O C6
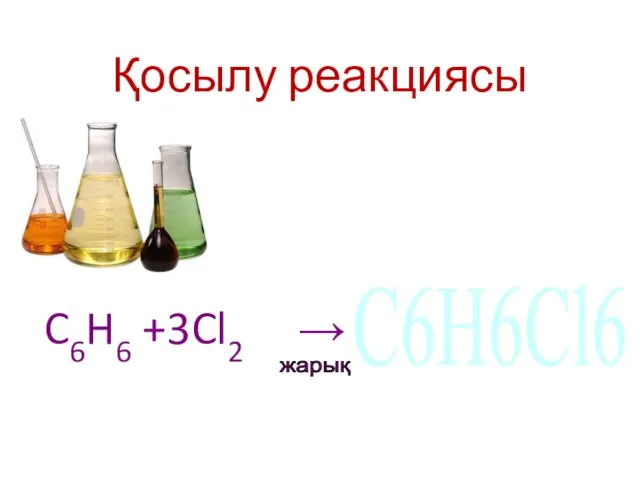
- 16. Қосылу реакциясы жарық C6H6 +3Cl2 → C6H6Cl6
- 17. Бензолдың қолданылуы
- 18. ҮЙГЕ ТАПСЫРМА: 1.Ә.Темірболатова, Н.Нұрахметов, Р.Жұмаділов, С.Әлімжанова Химия: -Алматы: Мектеп, 2011ж. §§ 3.1-4.6 қайталау 2. Ә. Темірболатова
- 20. Скачать презентацию












 Органикалық қышқылдарды алу. Тамақ өнеркәсібіндегі органикалық қышқылдардың тәжірибелік мәні
Органикалық қышқылдарды алу. Тамақ өнеркәсібіндегі органикалық қышқылдардың тәжірибелік мәні Чистые вещества и смеси
Чистые вещества и смеси Проект познавательно-исследовательской деятельности. Удивительная соль
Проект познавательно-исследовательской деятельности. Удивительная соль Нұсқа талдау
Нұсқа талдау Обмен липидов
Обмен липидов Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Подготовка к ГИА. А14. Определение характера среды раствора кислот и щелочей с помощью индикаторов. Реакции на ионы в растворе
Подготовка к ГИА. А14. Определение характера среды раствора кислот и щелочей с помощью индикаторов. Реакции на ионы в растворе Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Состав веществ. Причины многообразия веществ
Состав веществ. Причины многообразия веществ Протолитические равновесия и процессы. Лекция 3
Протолитические равновесия и процессы. Лекция 3 Технология выращивания кристаллов методом Чохральского
Технология выращивания кристаллов методом Чохральского Азот и его соединения. Повторение
Азот и его соединения. Повторение Пайдалы қазба
Пайдалы қазба Физические свойства минералов
Физические свойства минералов Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау
Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау Чистые вещества и смеси
Чистые вещества и смеси Рождение органической химии
Рождение органической химии Азотные удобрения
Азотные удобрения Алкандар. Метан молекуласының құрылысы Метан және оның гомологтарының қасиеттері
Алкандар. Метан молекуласының құрылысы Метан және оның гомологтарының қасиеттері Строение вещества. Строение атома и периодическая система элементов
Строение вещества. Строение атома и периодическая система элементов Водород. Строение, свойства, получение, применение
Водород. Строение, свойства, получение, применение Кремний и его соединения
Кремний и его соединения Маңызды химиялық өндірістер
Маңызды химиялық өндірістер Дефекты в твердых телах
Дефекты в твердых телах Хлор (лат. Chlorum, Cl)
Хлор (лат. Chlorum, Cl) Процессы нитрования
Процессы нитрования Синтетические моющие средства, порошки, омыление, выпадение в осадок мыла, жиров
Синтетические моющие средства, порошки, омыление, выпадение в осадок мыла, жиров Основные классы неорганических соединений
Основные классы неорганических соединений