Содержание
- 2. В электрохимии выделяют 2 основных вида процессов: 1) самопроизвольные процессы, которые реализуются в аккумуляторах, в гальванических
- 3. Взаимное превращение электрической и химической форм энергии происходит в электрохимических системах, состоящих из: проводников первого рода
- 4. Двойной электрический слой, его строение. Электродный потенциал.
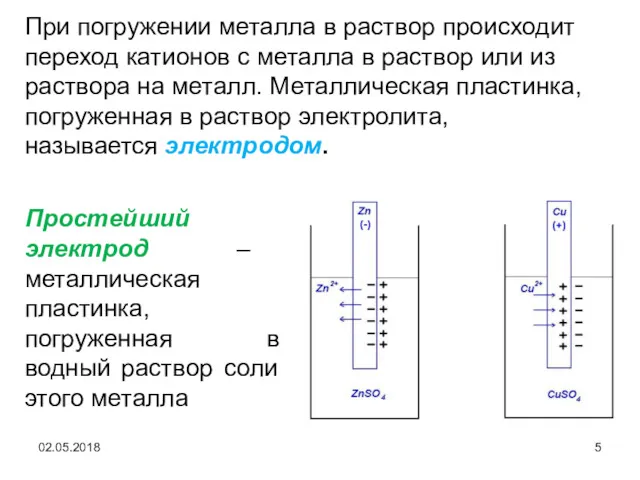
- 5. 02.05.2018 Простейший электрод – металлическая пластинка, погруженная в водный раствор соли этого металла При погружении металла
- 6. 02.05.2018 Цинковый и медный электроды. При погружении, цинковой пластинки, более активного металла, в раствор соли цинка
- 7. На границе раздела фаз возможны переходы поверхностных частиц из одной фазы в другую: Zn2+ + 2e
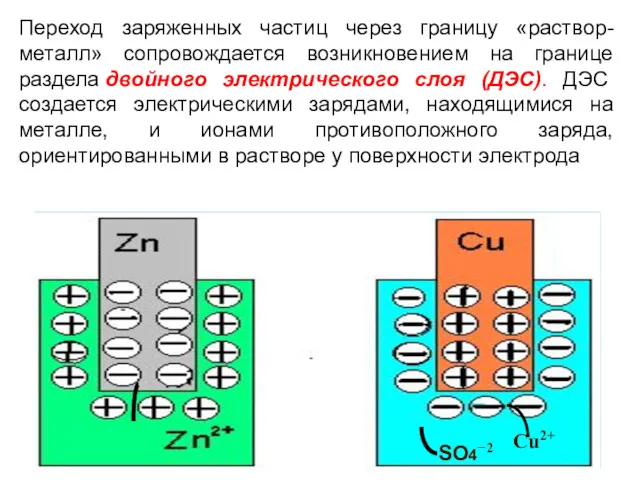
- 8. SO4−2 Cu2+ Переход заряженных частиц через границу «раствор-металл» сопровождается возникновением на границе раздела двойного электрического слоя
- 9. Между металлом и раствором возникает разность потенциалов, которая называется электродным потенциалом или потенциалом электрода (ϕ).
- 10. Электродный потенциал зависит от природы материала электрода, температуры, концентрации раствора и других свойств системы. Абсолютное значение
- 11. Стандартные электроды. Водородный электрод H+, H2 Pt Стандартный водородный электрод представляет собой платиновую пластинку, покрытую тонким
- 12. Электродный потенциал водородного электрода принят равным нулю Стандартные электродные потенциалы Потенциалы других электродов, измеренные в стандартных
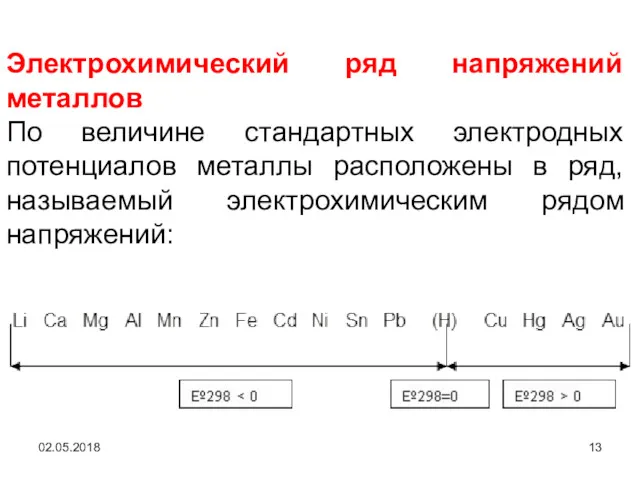
- 13. 02.05.2018 Электрохимический ряд напряжений металлов По величине стандартных электродных потенциалов металлы расположены в ряд, называемый электрохимическим
- 14. Ряд напряжений металлов: Электр. процесс ϕо, В Электр. процесс ϕо, В К - е- = К+
- 15. Свойства ряда напряжений металлов Восстановительная активность Ме в ряду напряжений уменьшается слева направо Окислительная способность катионов
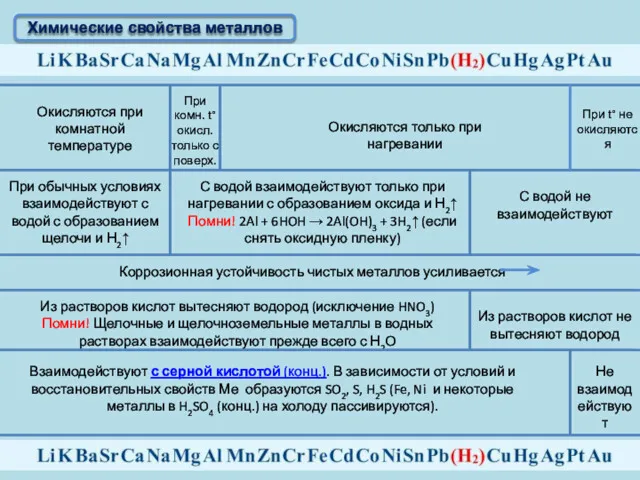
- 16. Химические свойства металлов Окисляются при комнатной температуре При комн. t°окисл. только с поверх. Окисляются только при
- 17. 02.05.2018 Расчет электродного потенциала. Уравнение Нернста Если условия отличаются от стандартных: E° - станд.эл.потенциал Ме, В
- 18. Ещё один вид уравнения Нернста: или
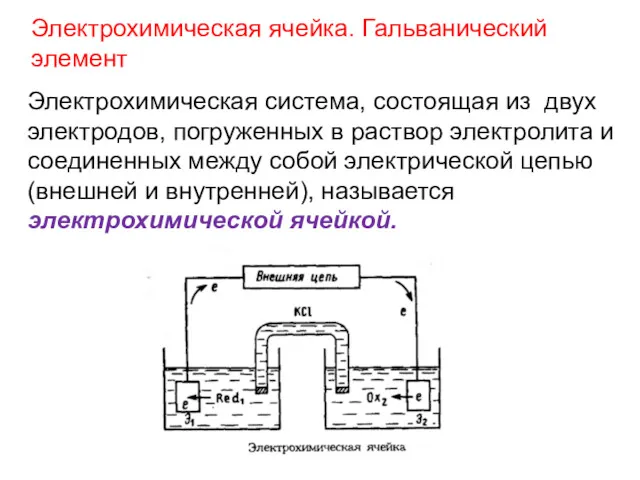
- 19. Электрохимическая ячейка. Гальванический элемент Электрохимическая система, состоящая из двух электродов, погруженных в раствор электролита и соединенных
- 20. 02.05.2018 Два основных типа электрохимических ячеек: гальванический элемент; электролитическая ячейка. В гальваническом элементе самопроизвольно протекает химическая
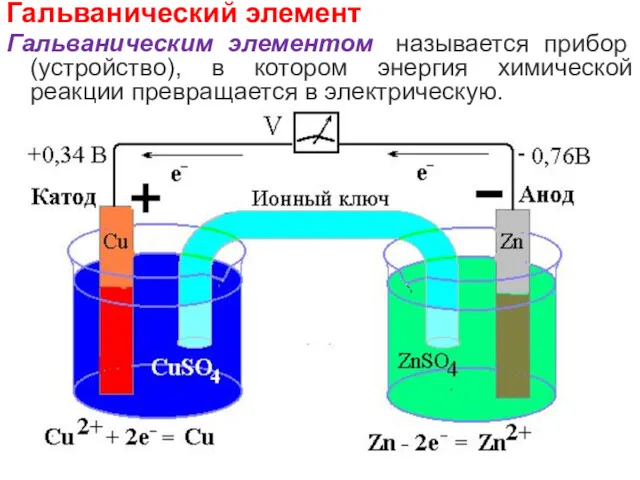
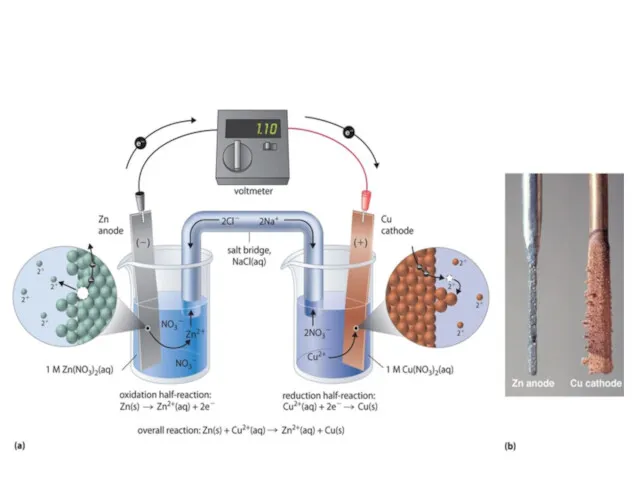
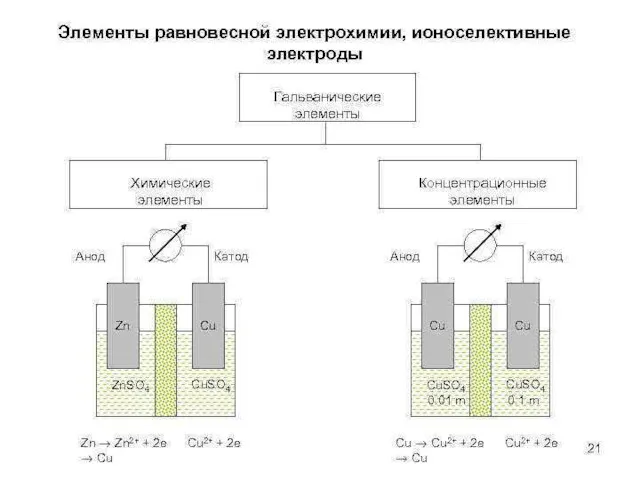
- 21. Гальванический элемент Гальваническим элементом называется прибор (устройство), в котором энергия химической реакции превращается в электрическую.
- 22. 02.05.2018 Накапливание ионов Zn+2 в первом сосуде и SO42− – во втором приведёт к остановке реакций.
- 24. Электроды гальванического элемента: Анод (отрицательный электрод, восстановитель, процесс окисления) – электрод, изготовленный из более активного Mе,
- 25. Электрохимическая схема гальванического элемента А(-) Zn/ZnSO4//CuSO4/Cu (+)К Токообразующая реакция: А(-): Zn – 2e = Zn2+ К(+):
- 26. Разность потенциалов катода и анода называется электродвижущей силой (ЭДС) гальванического элемента и вычисляется по формуле: ЭДС
- 27. 02.05.2018 Гальванический элемент, в котором источником энергии является не химическая реакция, а работа выравнивания концентраций (активностей)
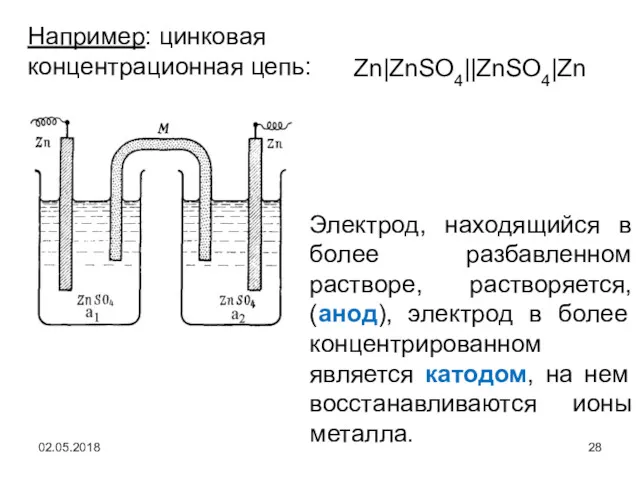
- 28. 02.05.2018 Zn|ZnSO4||ZnSO4|Zn Например: цинковая концентрационная цепь: Электрод, находящийся в более разбавленном растворе, растворяется, (анод), электрод в
- 29. 02.05.2018
- 30. 02.05.2018 Например для элемента Якоби-Даниэля ЭДС рассчитывается с помощью уравнения Нернста. ЭДС всегда является положительной величиной
- 31. 02.05.2018 ЭДС концентрационного гальванического элемента равна: При этом а1> a2
- 32. 02.05.2018 Диффузионные потенциалы возникают на границе соприкосновения двух растворов (растворы разных веществ или растворы одного и
- 33. 02.05.2018 Причина возникновения диффузионного потенциала заключается в неодинаковой подвижности ионов растворенных веществ. Если ионы электролита обладают
- 35. Скачать презентацию























 Метод нейтрализации. Расчёты в методе нейтрализации. Ионное произведение воды. Понятие Рн
Метод нейтрализации. Расчёты в методе нейтрализации. Ионное произведение воды. Понятие Рн Водород
Водород Применение гибридного биосорбента для очистки промышленных сточных вод от радиоактивных примесей
Применение гибридного биосорбента для очистки промышленных сточных вод от радиоактивных примесей 5.Алкины
5.Алкины 20230419_soli
20230419_soli Щелочноземельные металлы
Щелочноземельные металлы драгоценные и поделочные
драгоценные и поделочные Установка гидрокрекинга
Установка гидрокрекинга Кислотные дожди
Кислотные дожди Экстрагирование в химической промышленности
Экстрагирование в химической промышленности Своя игра. Химия. 7 класс
Своя игра. Химия. 7 класс Комплексные соединения
Комплексные соединения Основные постулаты квантовой механики
Основные постулаты квантовой механики Двовимірний ямр. Приклади
Двовимірний ямр. Приклади Гетероциклические соединения
Гетероциклические соединения Геохимия метасоматтческого процесса. (Лекция 7)
Геохимия метасоматтческого процесса. (Лекция 7) Процессы сульфирования в промышленности
Процессы сульфирования в промышленности Химическая промышленность России
Химическая промышленность России Основные классы неорганических соединений
Основные классы неорганических соединений Химиялық элементтер
Химиялық элементтер Периодический закон Д.И. Менделеева
Периодический закон Д.И. Менделеева Химический элемент цинк
Химический элемент цинк Значение периодического закона Д. И. Менделеева
Значение периодического закона Д. И. Менделеева Сахар - вред или польза?
Сахар - вред или польза? Периодический закон Д.И. Менделеева. Историческая формулировка периодического закона
Периодический закон Д.И. Менделеева. Историческая формулировка периодического закона Сущность процесса электролитической диссоциации
Сущность процесса электролитической диссоциации Органикалық қосылыстар. Көмірсутектерден жасалған
Органикалық қосылыстар. Көмірсутектерден жасалған Газохимия. Абсорбционно-газофракционирующая установка. (Лекция 5.2)
Газохимия. Абсорбционно-газофракционирующая установка. (Лекция 5.2)