Висновки:
зроблено літературний та патентний огляд існуючих та новітніх методів переробки діоксиду
вуглецю в органічні сполуки, каталізаторів конверсії СО2 , технології їх створення та властивості, фізико-хімічні основи процесу плазмової технології;
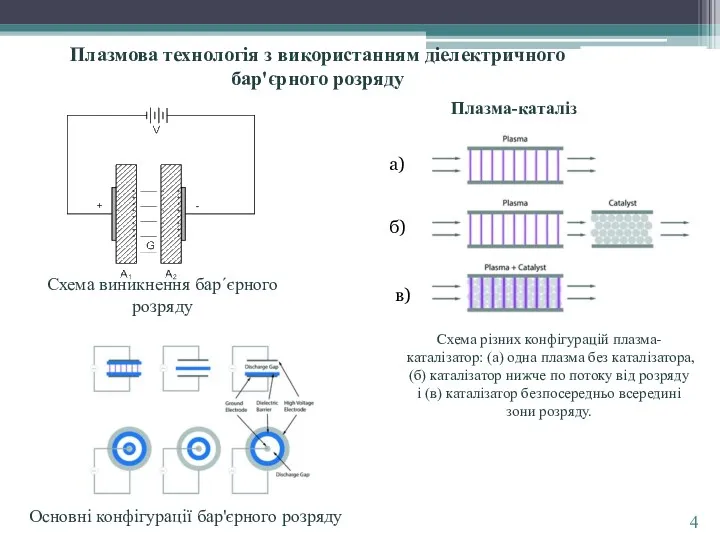
впроваджено компактну лабораторну установку конверсії СО2;
створений і досліджений нанесений каталізатор на основі природного сорбенту (глини);
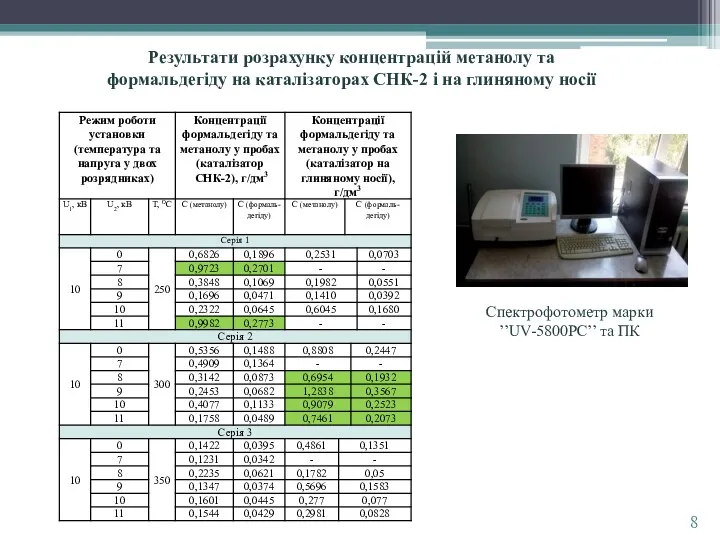
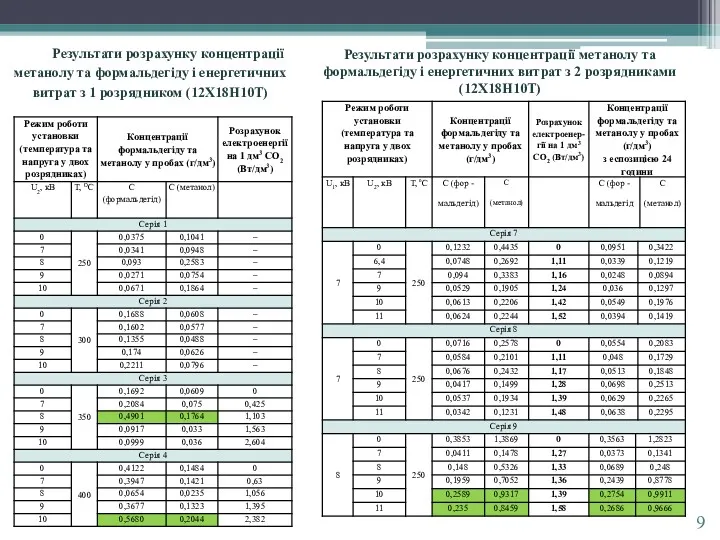
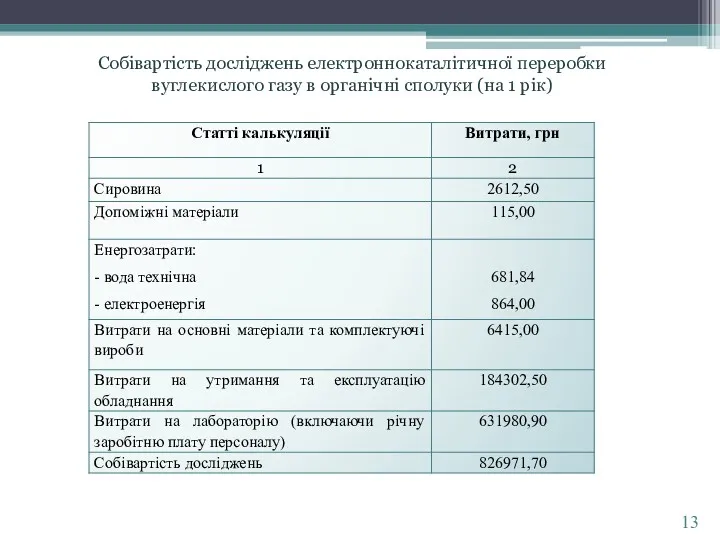
порівнюючи дані каталізатори, можна зазначити, що найкращі концентрації органічних сполук одержані: СНК-2: при 250 0С і 7 та 11 кВ вихід метанолу (0,97 і 1,0 г/дм3 відповідно), але вихід формальдегіду незначний (0,28 г/дм3, t = 250 0C, 11 кВ). Каталізатор на основі глиняного носія: при 300 0С і 9 кВ і 10кВ вихід метанолу (1,2838 і 0,91 г/дм3 відповідно), вихід формальдегіду значно кращий, ніж при використанні каталізатора СНК-2 - 0,36 г/дм3 при t = 300 0C, 9 кВ. Каталізатор 12Х18Н10Т: при 250 0С і 10 та 11 кВ вихід метанолу (0,99 і 0,97 г/дм3 відповідно), вихід формальдегіду 0,28 і 0,27 г/дм3 відповідно, при використанні 1 розрядника і температурі 400 0С вихід формальдегіду 0,57 г/дм3 .
14








 Хімічне виробництво сталі
Хімічне виробництво сталі Композиты как материалы конструкционного назначения
Композиты как материалы конструкционного назначения Химия в искусстве
Химия в искусстве Соли
Соли Кислородсодержащие соединения серы. Оксиды, кислоты, соли
Кислородсодержащие соединения серы. Оксиды, кислоты, соли Функциональные производные карбоновых кислот
Функциональные производные карбоновых кислот Xимия. Cr, Cu, Fe, Zn
Xимия. Cr, Cu, Fe, Zn Своя игра по химии
Своя игра по химии Мыло. Мылящие вещества в природе
Мыло. Мылящие вещества в природе Золото. История открытия
Золото. История открытия Сера и её соединения
Сера и её соединения Хімічний склад жувальної гумки
Хімічний склад жувальної гумки Рецепты литературы в химических опытах
Рецепты литературы в химических опытах Нуклеиновые кислоты
Нуклеиновые кислоты Горение топлива
Горение топлива Прикладные аспекты химии поверхностно-активных веществ
Прикладные аспекты химии поверхностно-активных веществ Гравиметрический метод анализа
Гравиметрический метод анализа Растворы ВМС
Растворы ВМС Основы коррозии и защиты металлов. Химическая коррозия
Основы коррозии и защиты металлов. Химическая коррозия Алюминий және оның қосылыстары
Алюминий және оның қосылыстары АТФ молекуласының құрылысы мен қызметтері
АТФ молекуласының құрылысы мен қызметтері алкадиены
алкадиены Монокристаллы CdTe и твердые растворы на его основе. Свойства, получение, применение
Монокристаллы CdTe и твердые растворы на его основе. Свойства, получение, применение Транспортное обеспечение внесения удобрений
Транспортное обеспечение внесения удобрений Щелочные металлы
Щелочные металлы 20230816_belki_2
20230816_belki_2 Электроотрицательность. Степень окисления. Валентность
Электроотрицательность. Степень окисления. Валентность Основные понятия органической химии. Лекция № 1
Основные понятия органической химии. Лекция № 1