Содержание
- 2. Галогены VII(A)
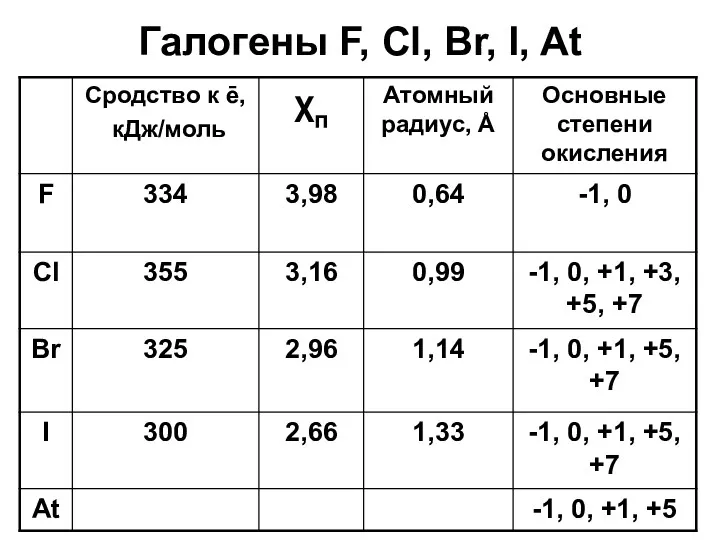
- 3. Галогены F, Cl, Br, I, At
- 4. Распространенность в природе F > Cl > Br > I >> At (τ1/2 (210At) = 8,1
- 5. Открытие элементов F2 – получен в 1886 г., Муассан (Франция) Cl2 – открыт в 1774 г.,
- 6. Происхождение названий F – от греч. фторос – разрушение, гибель; Cl – от греч. хлорос –
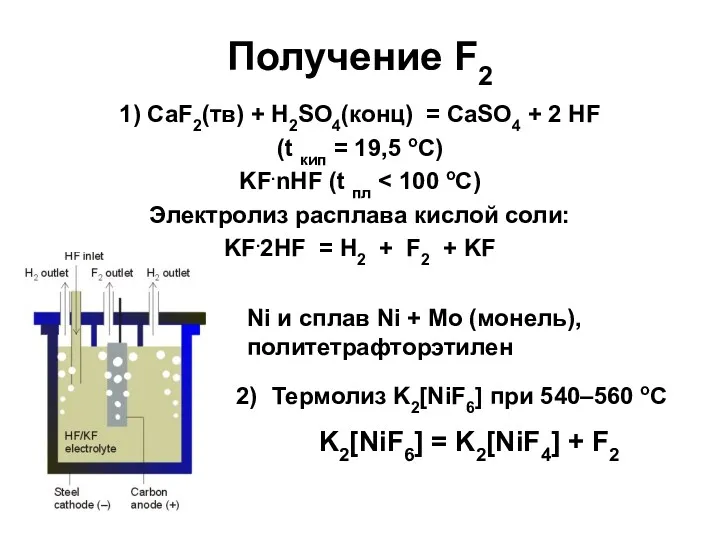
- 10. Получение F2 1) CaF2(тв) + H2SO4(конц) = CaSO4 + 2 HF (t кип = 19,5 оС)
- 11. Получение Cl2 Электролиз расплава: NaCl = Na + ½ Cl2 Электролиз раствора: анод: 2Cl- - 2ē
- 12. 2KMnO4 + 16HCl → 5Cl2⭡ + 2MnCl2 + 2KCl + 8H2O 2MnO2 + 8HCl → 2Cl2⭡
- 13. Получение Br2 Промышленный – хлорирование рассолов, содержащих Br- (морская вода и вода некоторых озер): 2Br- +
- 14. Получение I2 Лабораторный способ (редко): MnO2 + 2I- + 4H+ = Mn2+ + 2H2O + I2
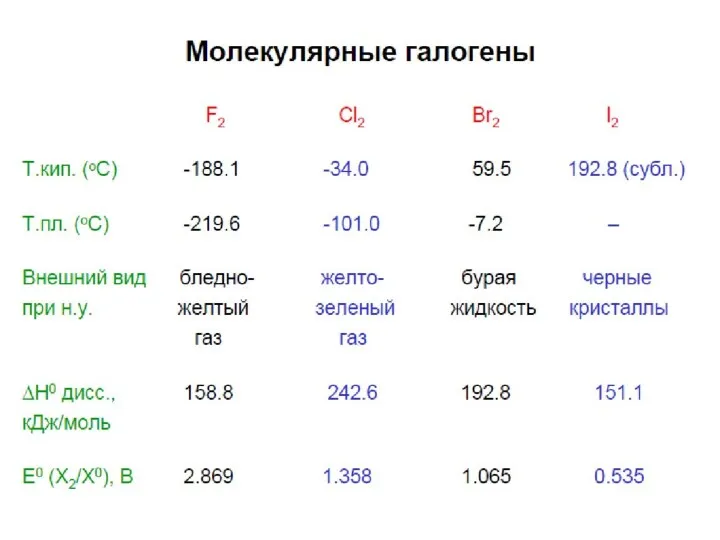
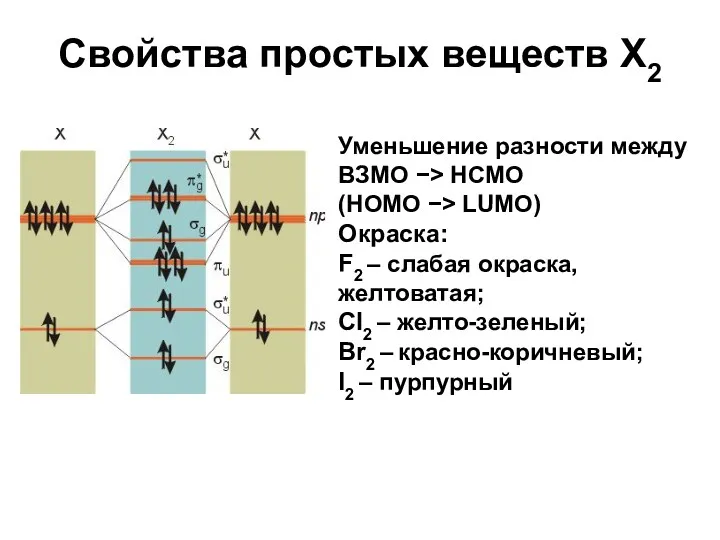
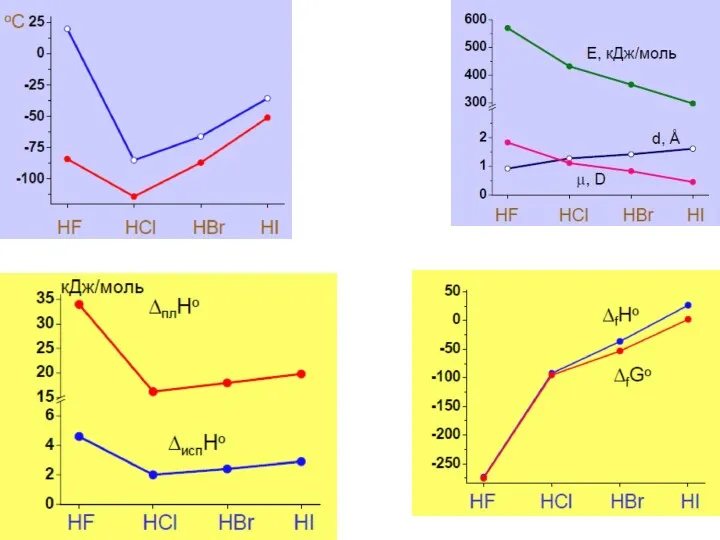
- 16. Свойства простых веществ X2 Уменьшение разности между ВЗМО −> НCМО (HOMO −> LUMO) Окраска: F2 –
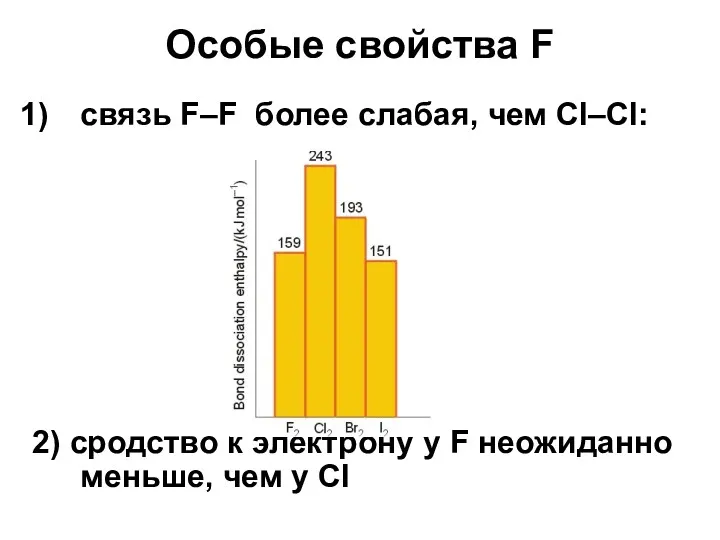
- 20. Особые свойства F связь F–F более слабая, чем Cl–Cl: 2) сродство к электрону у F неожиданно
- 21. Особые свойства F 3) соединения фтора более летучие по сравнению с соединениями хлора: t кип CF4
- 22. Особые свойства F 5) F – самый электроотрицательный элемент; 6) по способности стабилизировать высшие степени окисления
- 23. Галогениды неметаллов: газы: BF3, SiF4, PF3, PF5; жидкие: BCl3, SiCl4, PCl3, POCl3; твердые: BI3, PCl5: PCl3
- 24. Фторуглероды RH + 2CoF3 = RF + 2CoF2 + HF CoF3 регенерируют: 2CoF2 + F2 =
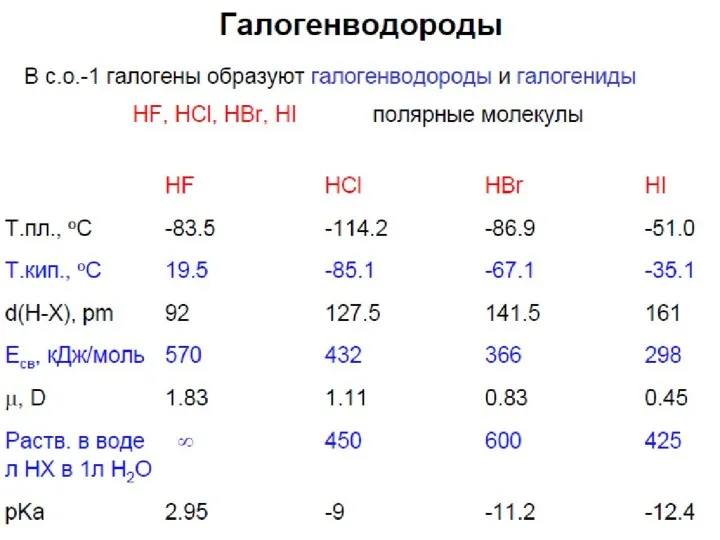
- 27. Галогенводороды НХ В газовой фазе: Hδ+ → Xδ- (полярная ковалентная связь) Кислотность в газе: HF >
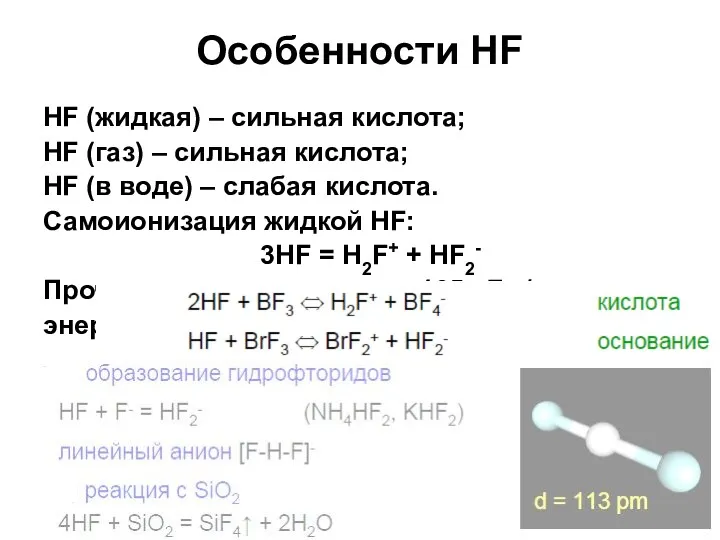
- 28. Особенности HF HF (жидкая) – сильная кислота; HF (газ) – сильная кислота; HF (в воде) –
- 29. Ox/red свойства HX
- 30. Получение HX а) синтез из простых веществ: H2 + X2 = 2 HX, ΔrH Для увеличения
- 31. Получение HX б) из солей реакцией ионного обмена: CaF2(тв) + H2SO4 (конц) = CaSO4 + 2HF
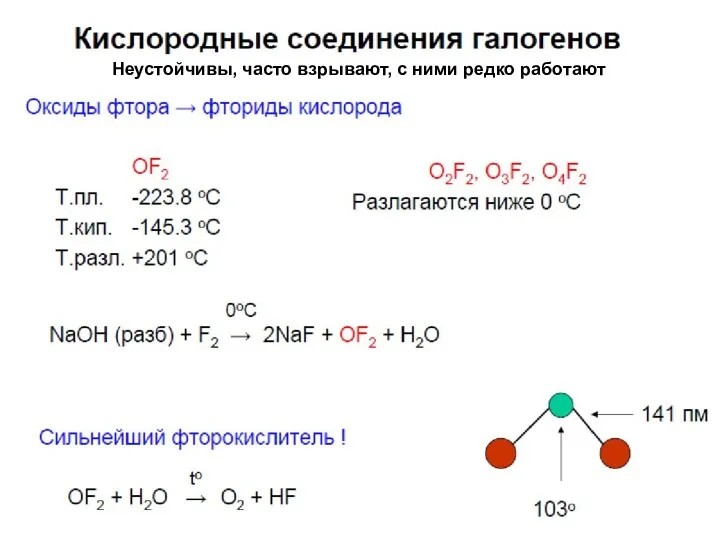
- 33. Оксиды фтора F2 + O2 – нет реакции при температурах 100–1000 оС; 2F2 + 2H2O =
- 34. Оксиды хлора: Cl2O Монооксид хлора Cl2O – желто-коричневый газ, при нагревании разлагается со взрывом. Ангидрид кислоты
- 35. Диокcид хлора ClO2 – желто-зеленый газ, парамагнитный (но не димеризуется!), термодинамически неустойчив (ΔfG = +121 кДж/моль).
- 36. Оксид хлора ClO2 Получение в промышленности: 2NaClO3 + SO2 + H2SO4 = 2NaHSO4 + 2ClO2 (в
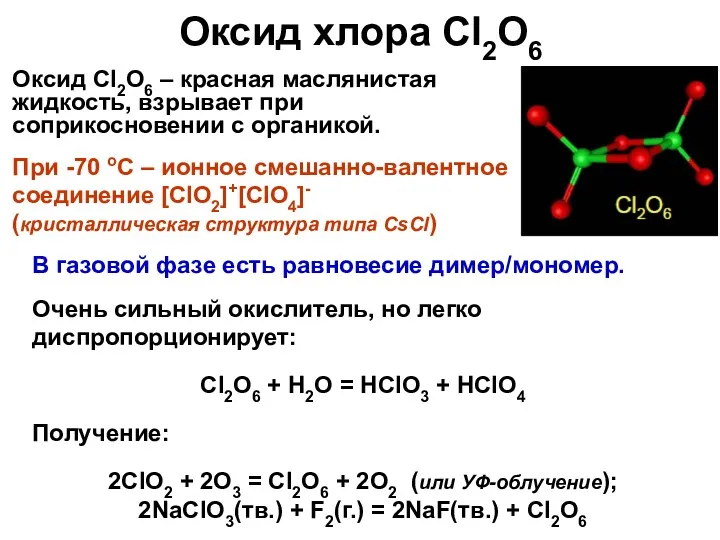
- 37. Оксид хлора Cl2O6 Оксид Cl2O6 – красная маслянистая жидкость, взрывает при соприкосновении с органикой. При -70
- 38. Оксид хлора (VII), хлорный ангидрид Cl2O7 Бесцветная маслянистая жидкость, наиболее устойчив среди оксидов хлора, но взрывает
- 39. Оксиды брома Br2O – красно-коричневая жидкость, разлагается выше -40оС. Получение: HgO(тв.) + 2Br2(г.) = Br2O +
- 40. Оксиды брома BrO2 – желтое кристаллическое вещество, разлагается выше -40оС (радикал) 2BrO2 = Br2 + 2O2
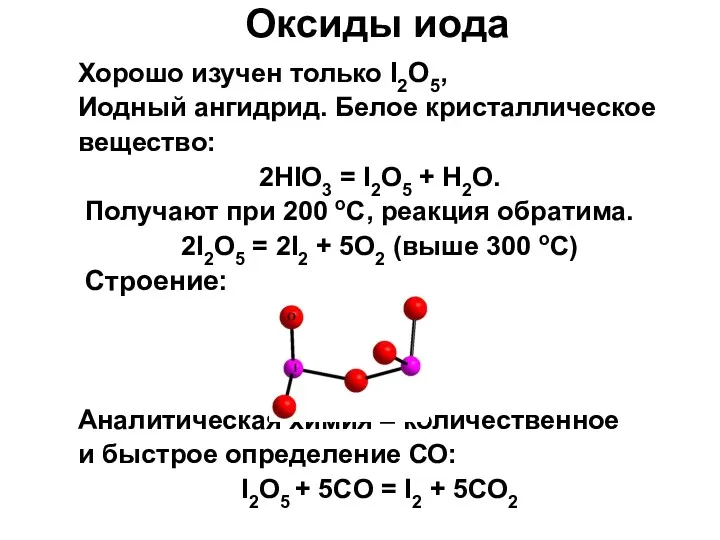
- 41. Хорошо изучен только I2O5, Иодный ангидрид. Белое кристаллическое вещество: 2HIO3 = I2O5 + H2O. Получают при
- 42. Взаимодействие Х2 с водой Особенности F2: Физическое растворение и химические реакции. При низких температурах можно выделить
- 43. Химическое взаимодействие с водой X2 + H2O = H+ + X- + HOX Реакция диспропорционирования обратима.
- 44. Использование в промышленности «Жавелева» вода: Cl2 + 2NaOH = NaCl + NaClO + H2O. Отбеливание тканей,
- 45. Диаграммы Латимера показывают стандартные потенциалы ox/red процессов в виде схемы: степени окисления элемента уменьшаются слева направо,
- 46. Диаграммы Латимера для галогенов (рН = 14)
- 47. Диаграммы Латимера для галогенов (рН = 0)
- 48. Задача: рассчитать Ео для полуреакции в кислой среде: HClO + H+ + 2ē = Cl- +H2O
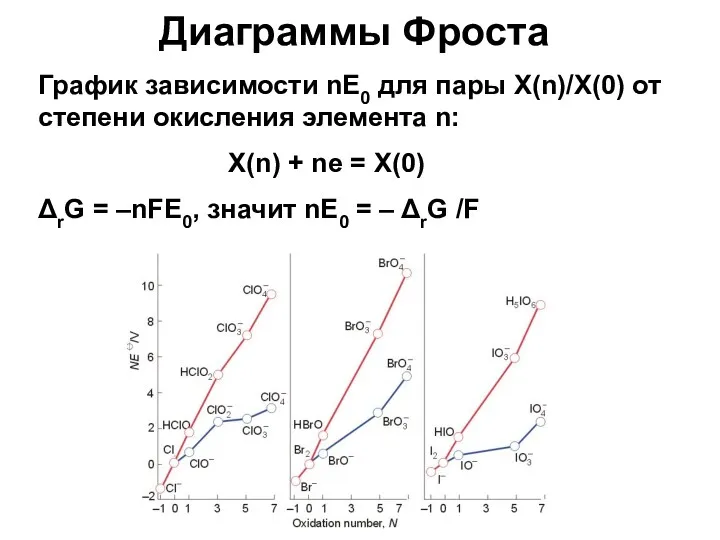
- 49. Диаграммы Фроста График зависимости nE0 для пары X(n)/X(0) от степени окисления элемента n: X(n) + ne
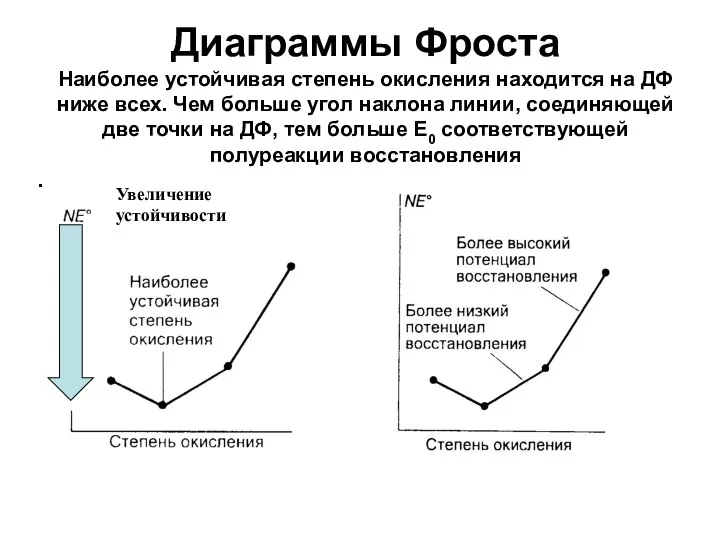
- 50. Увеличение устойчивости Диаграммы Фроста Наиболее устойчивая степень окисления находится на ДФ ниже всех. Чем больше угол
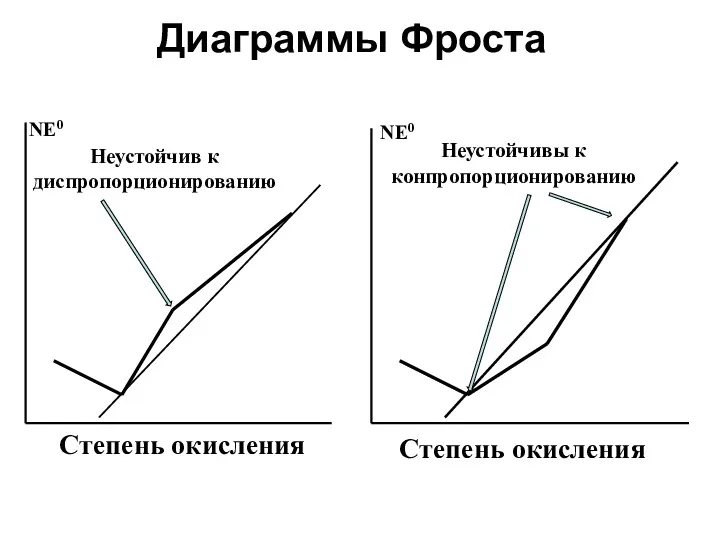
- 51. Диаграммы Фроста Степень окисления Неустойчив к диспропорционированию NE0 Степень окисления NE0 Неустойчивы к конпропорционированию
- 52. Общие замечания по ДЛ и ДФ 1. Ox/red реакции сильно зависят от рН и температуры. ДЛ
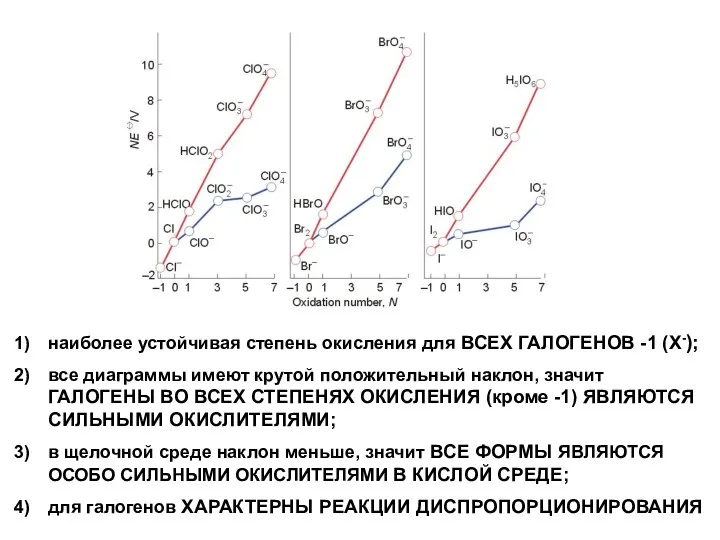
- 53. наиболее устойчивая степень окисления для ВСЕХ ГАЛОГЕНОВ -1 (Х-); все диаграммы имеют крутой положительный наклон, значит
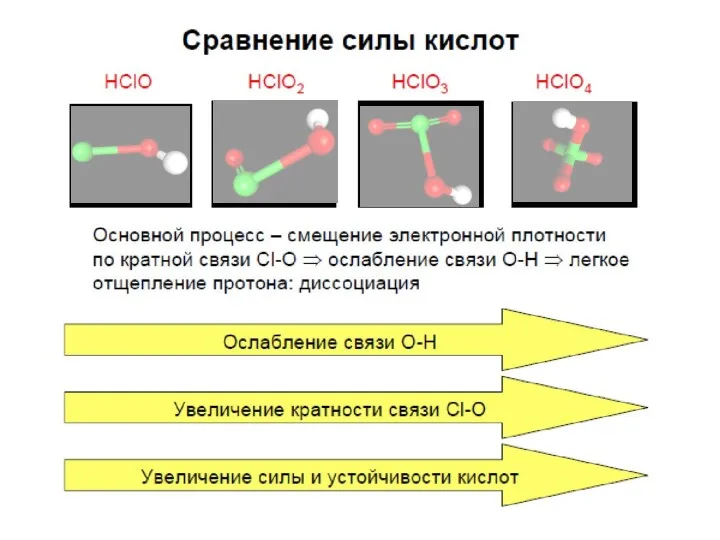
- 56. Кислородсодержащие кислоты и их соли HXO: HFO(?), HClO, HBrO, HIO; Ka = 10-8 (X = Cl),
- 57. Получение кислот HXO: X2 + H2O + CaCO3(тв) = CaX2 + CO2 + HXO (X =
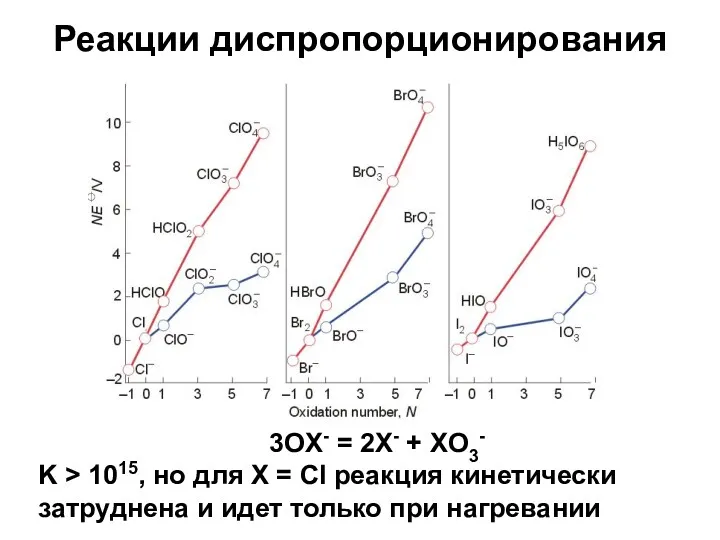
- 58. Реакции диспропорционирования 3OX- = 2X- + XO3- K > 1015, но для X = Cl реакция
- 59. Степень окисления +3 Нет HIO2 и нет примеров солей Нет HBrO2, только ДВА примера соли: Ba(BrO)2
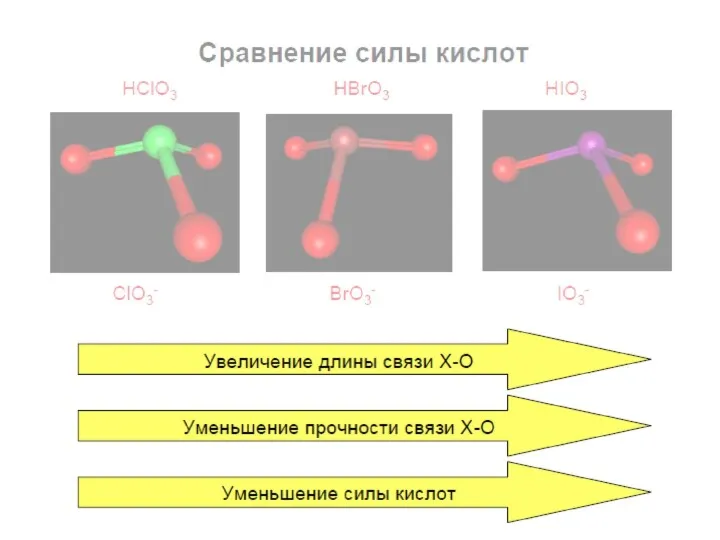
- 60. Степень окисления +5 Сильные кислоты HXO3 (X = Cl, Br, I) HClO3 и HBrO3 – только
- 61. Получение соединений X5+ ХЛОРАТЫ Электрохимическое окисление хлоридов: KCl + 3H2O = KClO3 (анод) + 3H2 ↑(катод)
- 62. Ox/red свойства соединений X5+ 1) все X5+ – сильные окислители; 2) в кислой среде более сильные
- 63. Ox/red свойства соединений X5+ Все соединения X5+ – сильные окислители, как правило, восстанавливаются до X- :
- 64. Разложение твердых солей при нагревании 4KClO3 = 3KClO4 + KCl (400 oC); 2KClO3 = 2KCl +
- 65. Соединения Х7+ HClO4 получена безводная (взрывоопасно!), сильная кислота; HBrO4 известна в растворах, сильная кислота; HIO4 –
- 66. Получение соединений X7+ Электролиз: XO3- + H2O = XO4-(анод) + H2(катод). Реакции в растворах: KBrO3 +
- 67. Свойства соединений X7+ ПЕРХЛОРАТЫ ВЗРЫВАЮТСЯ!!! KClO4 (тв) = KCl + 2O2 (выше 500 оС); 2NH4ClO4 (тв)
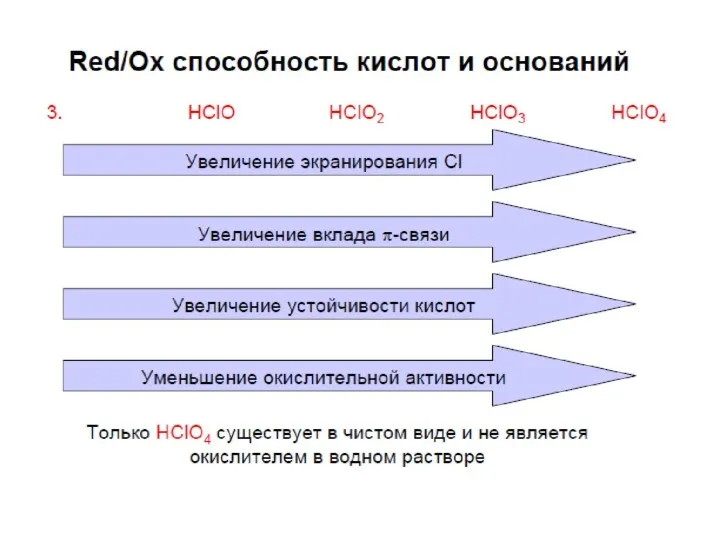
- 73. Особенности изменения окислительной способности кислот галогенов(VII) HBrO4 и ее соли более сильные окислители, чем соединения Cl(VII)
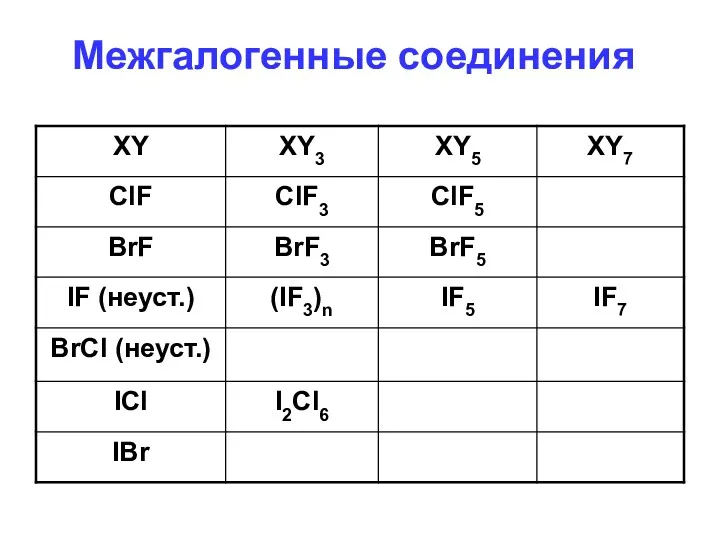
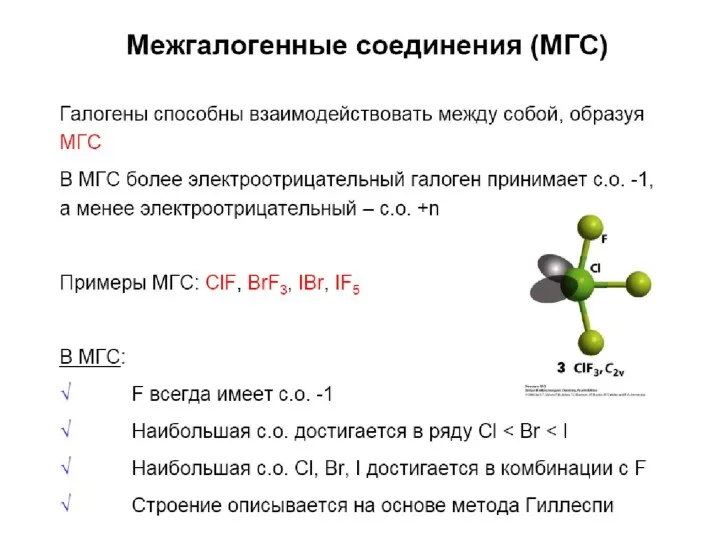
- 76. Межгалогенные соединения
- 78. (X =Cl: t=3500 (250 атм), X = Br: t >1500C, X = I: t = 200C)
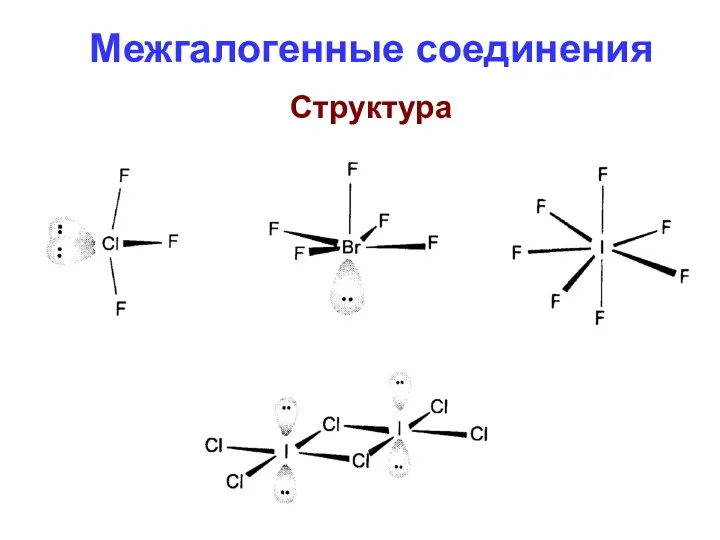
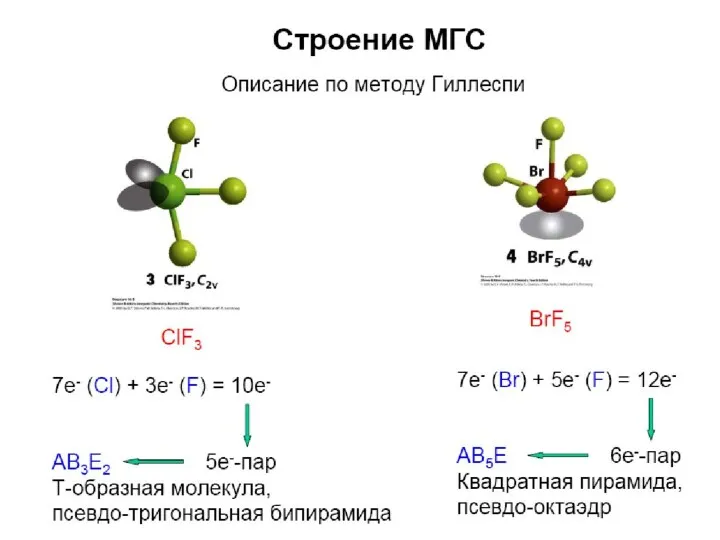
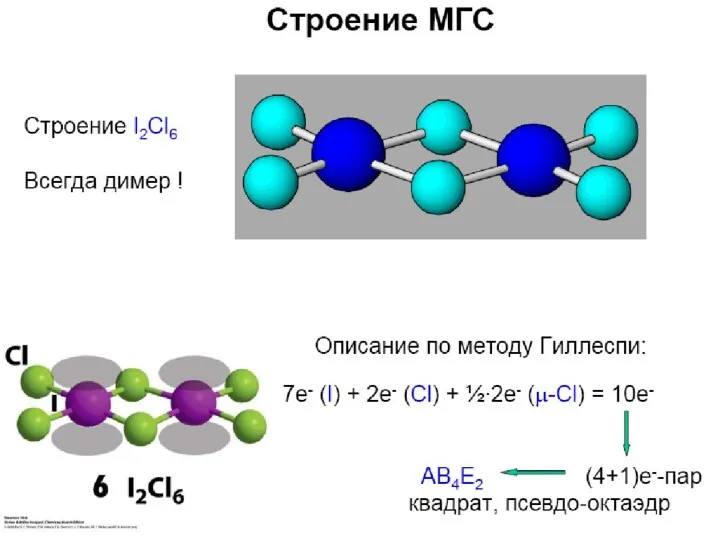
- 80. Межгалогенные соединения Структура
- 83. Межгалогенные соединения Чаще всего используют ClF3 и BrF3. Окислители, бурно реагируют с органикой (взрыв), горит асбест,
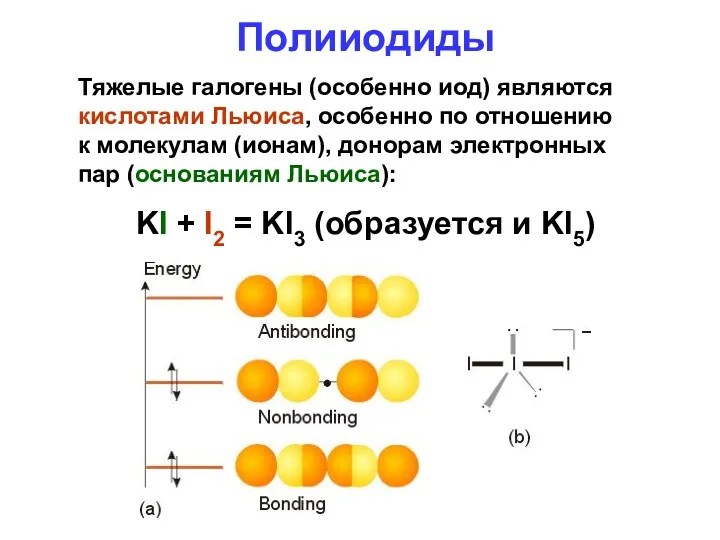
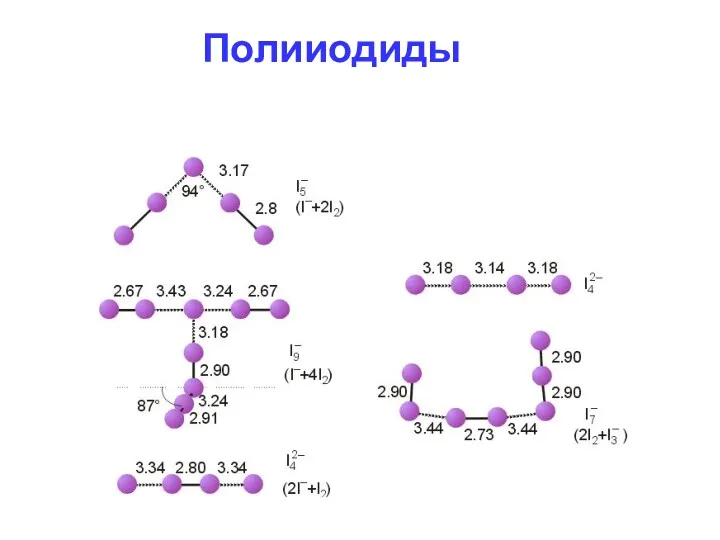
- 84. Полииодиды Тяжелые галогены (особенно иод) являются кислотами Льюиса, особенно по отношению к молекулам (ионам), донорам электронных
- 85. Полииодиды
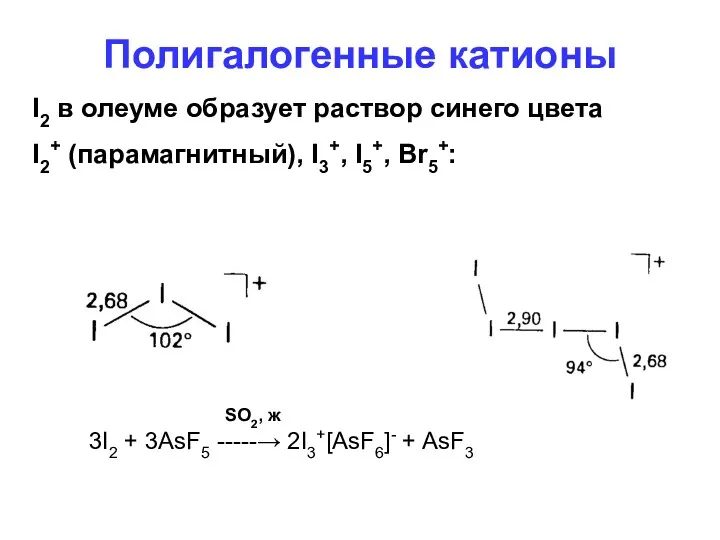
- 86. Полигалогенные катионы I2 в олеуме образует раствор синего цвета I2+ (парамагнитный), I3+, I5+, Br5+: 3I2 +
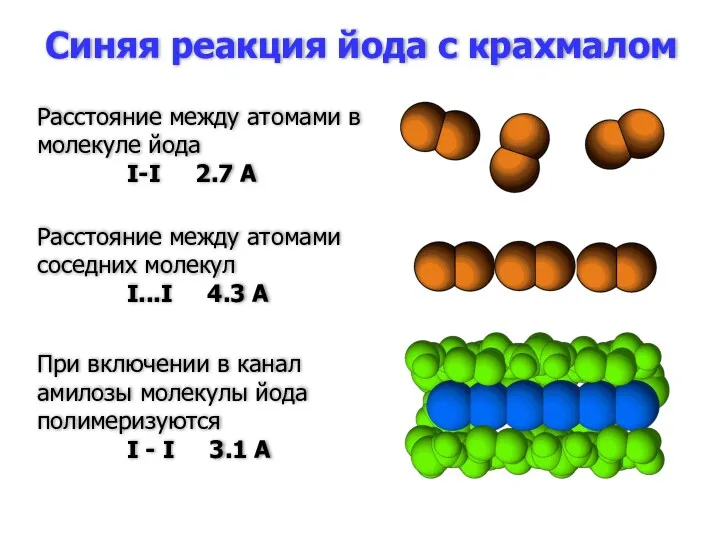
- 87. Синяя реакция йода с крахмалом Расстояние между атомами в молекуле йода I-I 2.7 A Расстояние между
- 89. Скачать презентацию
























































 Сталь, железо и чугун
Сталь, железо и чугун Прикладные аспекты химии поверхностно-активных веществ
Прикладные аспекты химии поверхностно-активных веществ Серная кислота. ОХТ, лекция №7
Серная кислота. ОХТ, лекция №7 Методы выделения и очистки продуктов биотехнологических производств
Методы выделения и очистки продуктов биотехнологических производств Алкани. Циклоалкани
Алкани. Циклоалкани Периодические системы химических элементов
Периодические системы химических элементов Цинк
Цинк Периодическая таблица Д.И. Менделеева. Своя игра
Периодическая таблица Д.И. Менделеева. Своя игра Кислоты и основания. (Лекция 16)
Кислоты и основания. (Лекция 16) Химические свойства кислот
Химические свойства кислот Констукционные и функциональные волокнистые композиты. Стекловолокно
Констукционные и функциональные волокнистые композиты. Стекловолокно Гидролиз. Применение гидролиза. (11 класс)
Гидролиз. Применение гидролиза. (11 класс) Химические формулы. Относительная молекулярная масса
Химические формулы. Относительная молекулярная масса Химические формулы. Относительная атомная и молекулярная масса
Химические формулы. Относительная атомная и молекулярная масса Лекция по химии
Лекция по химии Решение задач. Способы выражения состава раствора
Решение задач. Способы выражения состава раствора Методика “Кольоропис”
Методика “Кольоропис” Углеводы. Сn(H2O)m – общая формула углеводов
Углеводы. Сn(H2O)m – общая формула углеводов Кинетика химических реакций
Кинетика химических реакций Индикаторы. Круговорот воды в природе. Загрязнение природных вод. Охрана и очистка природных вод
Индикаторы. Круговорот воды в природе. Загрязнение природных вод. Охрана и очистка природных вод Классификация органических соединений. Теория химического строения вещества. 10 класс
Классификация органических соединений. Теория химического строения вещества. 10 класс Воспламенение (зажигание) газовых смесей
Воспламенение (зажигание) газовых смесей Тайна мыльного пузыря
Тайна мыльного пузыря Азот, фосфор и их соединения
Азот, фосфор и их соединения Природные источники углеводородов
Природные источники углеводородов Неметаллические и композиционные материалы
Неметаллические и композиционные материалы Флокуляційне очищення питної води за допомогою катіонних та аніонних флокулянтів
Флокуляційне очищення питної води за допомогою катіонних та аніонних флокулянтів Спирты. Обобщающий урок
Спирты. Обобщающий урок