Содержание
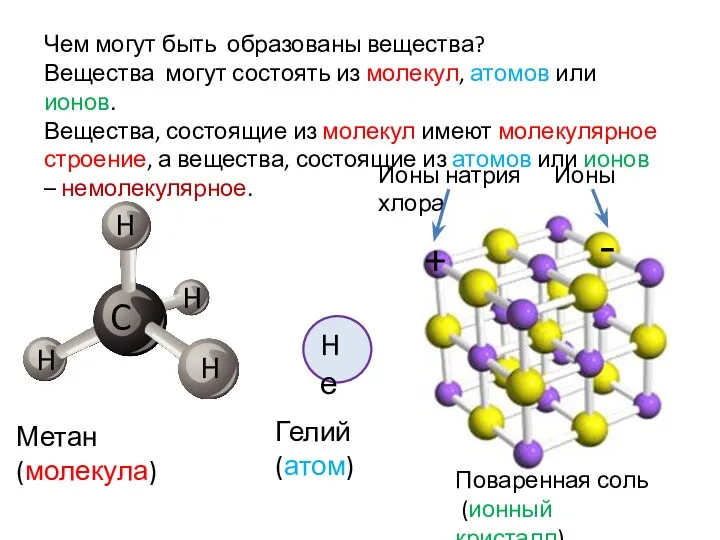
- 3. Поваренная соль (ионный кристалл) Чем могут быть образованы вещества? Вещества могут состоять из молекул, атомов или
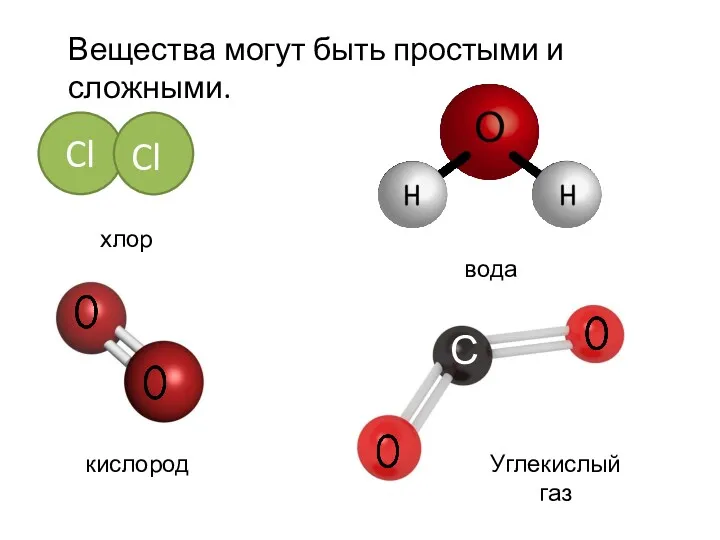
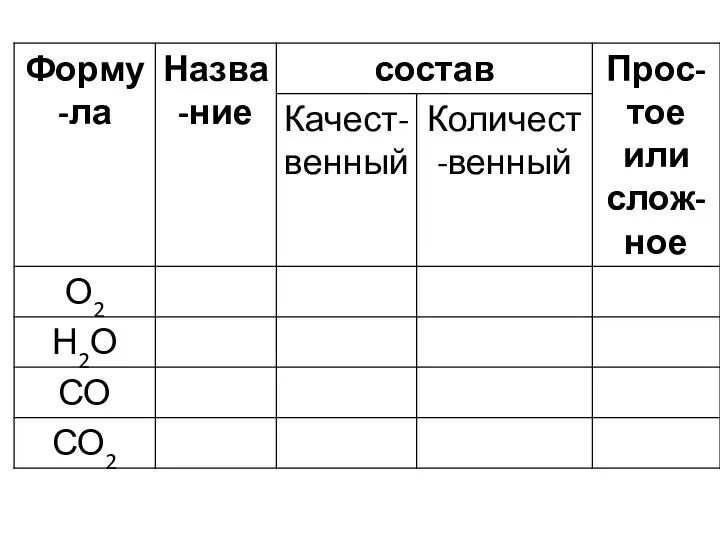
- 4. O2 кислород вода Н2О Cl2 хлор Cl Cl Вещества могут быть простыми и сложными. Углекислый газ
- 5. Вещества могут иметь постоянный и переменный состав. Химическая формула — запись качественного и количественного состава вещества
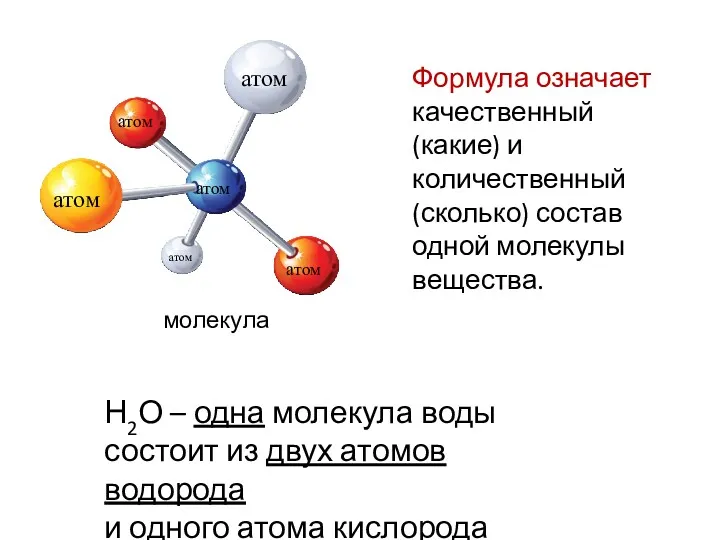
- 6. Формула означает качественный (какие) и количественный (сколько) состав одной молекулы вещества. Н2О – одна молекула воды
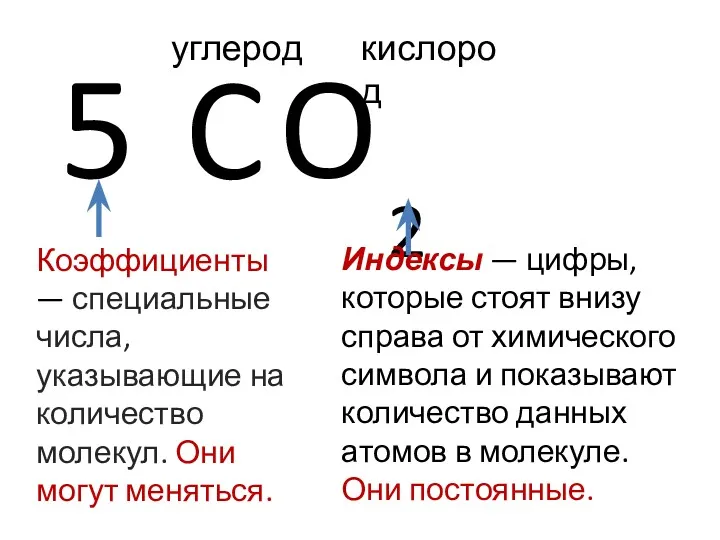
- 7. C O 2 Индексы — цифры, которые стоят внизу справа от химического символа и показывают количество
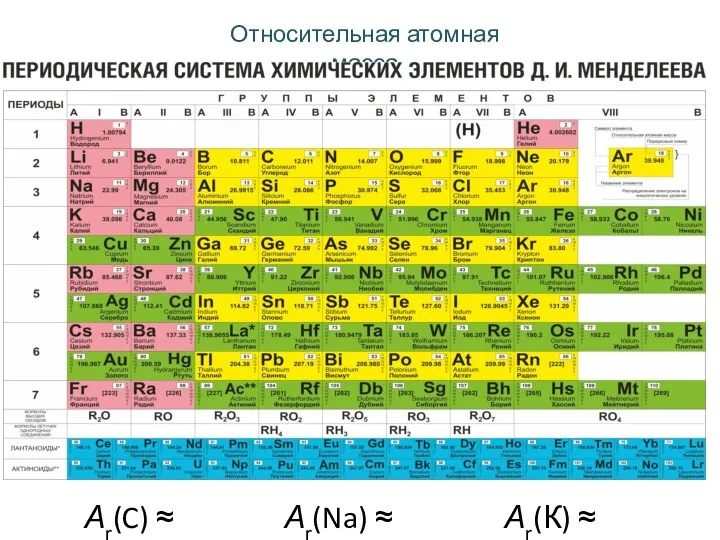
- 9. Относительная атомная масса показывает, во сколько раз масса его атома больше 1/12 массы атома углерода. Ar
- 10. Относительная атомная масса Аr(К) ≈ 39 Аr(Na) ≈ 23 Аr(C) ≈ 12
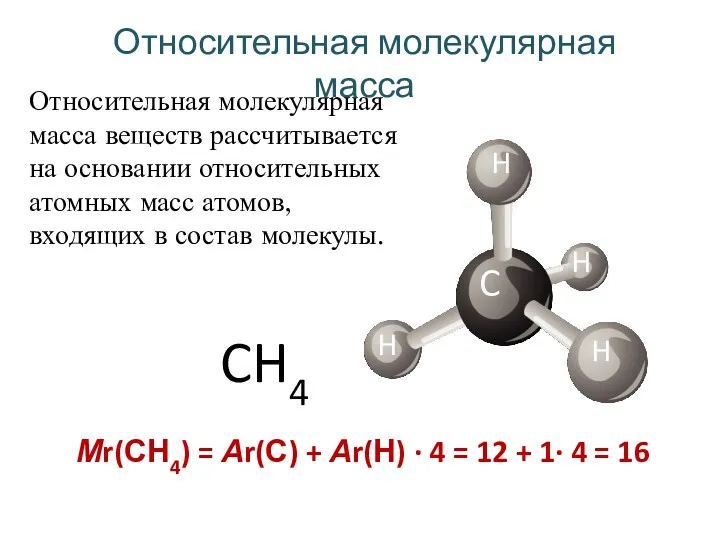
- 11. Mr Относительная молекулярная масса Зная относительные атомные массы, можно найти относительную молекулярную массу молекулы вещества. Относительная
- 12. Относительная молекулярная масса CH4 C H H H H Мr(СН4) = Аr(С) + Аr(Н) · 4
- 13. Mr (О2)= Mr(Н2О)= Mr(HNО3)= Mr(Ca(NО3)2=
- 15. Скачать презентацию



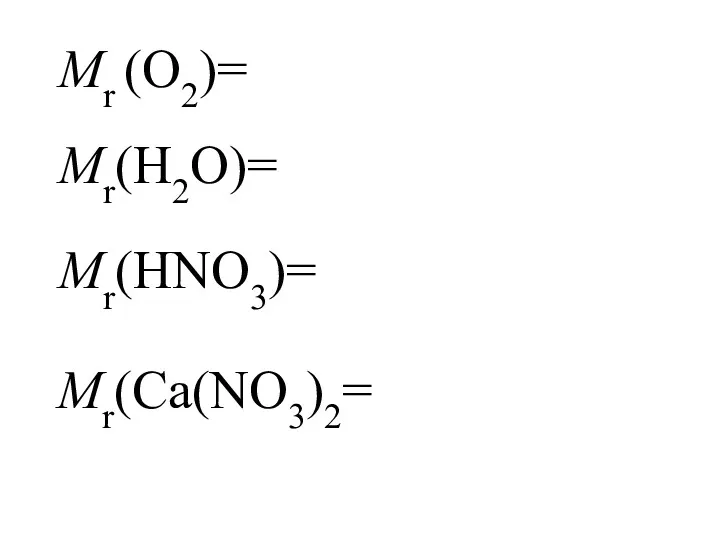
 Свойства кислот в свете теории электролитической диссоциации
Свойства кислот в свете теории электролитической диссоциации Химические реакции
Химические реакции Кислород. Озон. Получение кислорода
Кислород. Озон. Получение кислорода Монокристаллы CdTe и твердые растворы на его основе. Свойства, получение, применение
Монокристаллы CdTe и твердые растворы на его основе. Свойства, получение, применение Строение электронных оболочек атомов химических элементов
Строение электронных оболочек атомов химических элементов Типы химических реакций , признаки и условия их протекания
Типы химических реакций , признаки и условия их протекания Амінокислоти. Білки як біологічні полімери. Денатурація білка. Біологічна роль амінокислот та білків. 9 клас
Амінокислоти. Білки як біологічні полімери. Денатурація білка. Біологічна роль амінокислот та білків. 9 клас Класифікація, будова та номенклатура органічних сполук
Класифікація, будова та номенклатура органічних сполук Конструкционные материалы
Конструкционные материалы Алюміній
Алюміній Электролит және бейэлектролит ерітінділердің коллигативті қасие
Электролит және бейэлектролит ерітінділердің коллигативті қасие Комплексные соединения
Комплексные соединения Кислород и озон
Кислород и озон Интересные факты об углеводородах
Интересные факты об углеводородах Химическая связь
Химическая связь Теория сильных и слабых электролитов
Теория сильных и слабых электролитов Що ховається за цифрами? Харчові домішки
Що ховається за цифрами? Харчові домішки Топливо. Виды топлива. Химический состав топлива. Основные характеристики топлива. Марки топлива
Топливо. Виды топлива. Химический состав топлива. Основные характеристики топлива. Марки топлива Хімічні властивості металів
Хімічні властивості металів Качественные реакции
Качественные реакции Амины. Анилин
Амины. Анилин Пурин нуклеозидтері (аденозии 3-фосфор қышқылы, рибоксии). Сапасына Қойылантын талаптар, талдау әдістері
Пурин нуклеозидтері (аденозии 3-фосфор қышқылы, рибоксии). Сапасына Қойылантын талаптар, талдау әдістері Серебро. История
Серебро. История Дефекты в твердых телах
Дефекты в твердых телах Механическая смесь и растворы
Механическая смесь и растворы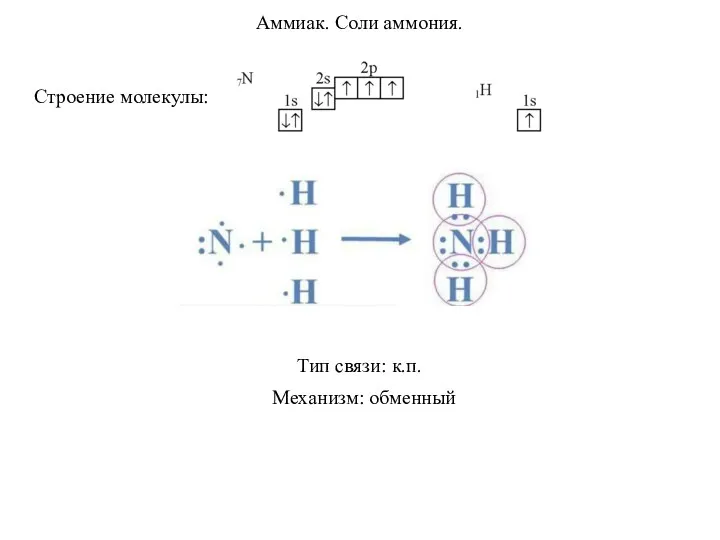 Аммиак. Соли аммония
Аммиак. Соли аммония Кислородсодержащие соединения серы
Кислородсодержащие соединения серы Биомакромолекулы. Нуклеиновые кислоты
Биомакромолекулы. Нуклеиновые кислоты