Содержание
- 2. Описание Неорганическое соединение гидроксид железа 3 имеет химическую формулу Fe(OH)2. Оно принадлежит к ряду амфотерных соединений
- 3. Свойства На вид это вещество представляет собой кристаллы белого цвета, которые при длительном пребывании на открытом
- 4. Свойства и сравнение с гидроксидом железа(2) Fe(OH)3 – более слабое основание, чем гидроксид железа (II). Это
- 6. Скачать презентацию
Слайд 2
Описание
Неорганическое соединение гидроксид железа 3 имеет химическую формулу Fe(OH)2. Оно принадлежит
Описание
Неорганическое соединение гидроксид железа 3 имеет химическую формулу Fe(OH)2. Оно принадлежит
к ряду амфотерных соединений железа, в которых преобладают свойства, характерные для оснований.
Слайд 3
Свойства
На вид это вещество представляет собой кристаллы белого цвета, которые при
Свойства
На вид это вещество представляет собой кристаллы белого цвета, которые при
длительном пребывании на открытом воздухе постепенно темнеют. Имеются варианты кристаллов зеленоватого оттенка. В повседневной жизни вещество может наблюдать каждый в виде зеленоватого налета на металлических поверхностях, что свидетельствует о начала процесса ржавления - гидроксид железа 3 выступает в качестве одной из промежуточных стадий этого процесса. Образуется при действии растворов щелочей на соли трёхвалентного железа: выпадает в виде красно–бурого осадка
Слайд 4
Свойства и сравнение с гидроксидом железа(2)
Fe(OH)3 – более слабое основание, чем
Свойства и сравнение с гидроксидом железа(2)
Fe(OH)3 – более слабое основание, чем
гидроксид железа (II).
Это объясняется тем, что у Fe2+ меньше заряд иона и больше его радиус, чем у Fe3+, а поэтому, Fe2+ слабее удерживает гидроксид-ионы, т.е. Fe(OH)2 более легко диссоциирует.
В связи с этим соли железа (II) гидролизуются незначительно, а соли железа (III) - очень сильно.
При нагревании окраска темнеет, а при прибавлении кислот становится более светлой вследствие подавления гидролиза. Fe(OH)3 обладает слабо выраженной амфотерностью: он растворяется в разбавленных кислотах и в концентрированных растворах щелочей
Соединения железа (III) - слабые окислители, реагируют с сильными восстановителями
Это объясняется тем, что у Fe2+ меньше заряд иона и больше его радиус, чем у Fe3+, а поэтому, Fe2+ слабее удерживает гидроксид-ионы, т.е. Fe(OH)2 более легко диссоциирует.
В связи с этим соли железа (II) гидролизуются незначительно, а соли железа (III) - очень сильно.
При нагревании окраска темнеет, а при прибавлении кислот становится более светлой вследствие подавления гидролиза. Fe(OH)3 обладает слабо выраженной амфотерностью: он растворяется в разбавленных кислотах и в концентрированных растворах щелочей
Соединения железа (III) - слабые окислители, реагируют с сильными восстановителями
- Предыдущая
Клуб виртуальной реальности. Бизнес-планСледующая -
Творчество Дэвида Финчера


 Аминокислоты 2
Аминокислоты 2 Магний. Нахождение в природе
Магний. Нахождение в природе Цветные металлы и сплавы
Цветные металлы и сплавы Концентрации растворов
Концентрации растворов Небезпечні хімічні речовини
Небезпечні хімічні речовини Медь и её соединения
Медь и её соединения Вода на Земле. Строение молекулы воды
Вода на Земле. Строение молекулы воды Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов
Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов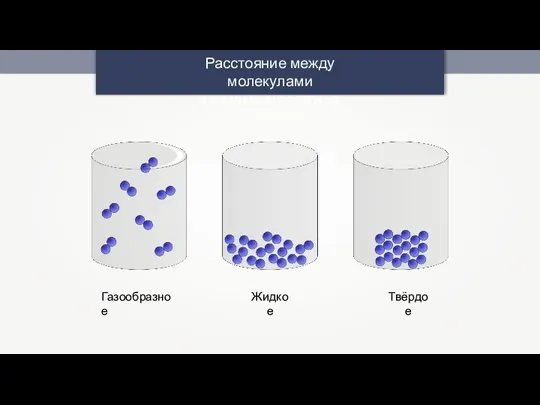 Расстояние между молекулами в разных агрегатных состояниях
Расстояние между молекулами в разных агрегатных состояниях Сущность процесса электролитической диссоциации
Сущность процесса электролитической диссоциации Азотовмісні сполуки
Азотовмісні сполуки Кристаллография, кристаллохимия, минералогия
Кристаллография, кристаллохимия, минералогия Знаки химических элементов. Химические формулы. Химический диктант
Знаки химических элементов. Химические формулы. Химический диктант Етери та естери. Хімічні властивості
Етери та естери. Хімічні властивості Физико-химические методы исследования биологически активных веществ
Физико-химические методы исследования биологически активных веществ Химическое равновесие в гомогенных системах. Ионное произведение воды. 12 класс
Химическое равновесие в гомогенных системах. Ионное произведение воды. 12 класс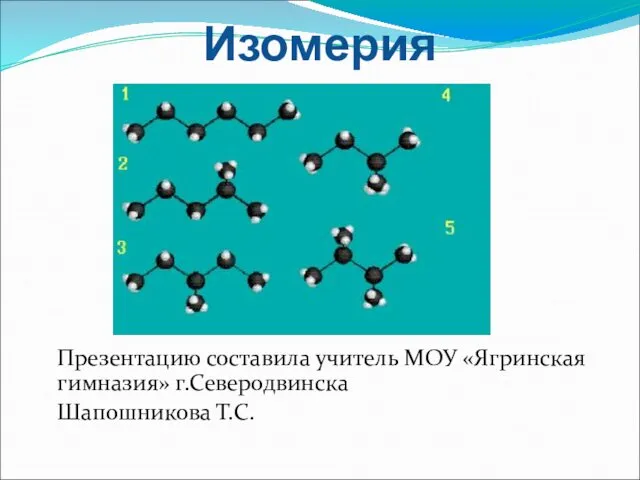 Изомерия и ее виды
Изомерия и ее виды Берилій
Берилій Новые интеллектуальные материалы на основе полимеров
Новые интеллектуальные материалы на основе полимеров Аммиак. Строение молекулы аммиака, его физические и химические свойства
Аммиак. Строение молекулы аммиака, его физические и химические свойства Вуглеводні. Лекція 11
Вуглеводні. Лекція 11 Алмазы. Бриллианты
Алмазы. Бриллианты Растворы. Общие свойства растворов
Растворы. Общие свойства растворов Химиялық элементтердің тірі және өлі табиғатта таралуы
Химиялық элементтердің тірі және өлі табиғатта таралуы Кислотно-основные (протолитические) равновесия
Кислотно-основные (протолитические) равновесия Методика изучения и описание вулканогенных обломочных пород
Методика изучения и описание вулканогенных обломочных пород Зеленая химия и проблемы устойчивого развития
Зеленая химия и проблемы устойчивого развития Кислород. Оксиды. Валентность
Кислород. Оксиды. Валентность