Содержание
- 2. Давно ли известен состав воздуха? Древнегреческий философ Анаксимен (560-450 до н.э.) первым предположил, что воздух является
- 3. Исследователи и первооткрыватели воздуха Джозеф Пристли К. Шееле Генри Кавендиш
- 4. Исследования Один из основоположников газовой химии шведский ученый К. Шееле в период с 1768 по 1773
- 5. Количественный состав воздуха Впервые установил количественный состав воздуха французский ученый Антуан Лоран Лавуазье. По результатам своего
- 6. Воздух Смесь газов Кислород Азот
- 7. Химический состав воздуха Воздух – это бесцветный газообразный раствор, плотность – 1,293г/л, при температуре -273С он
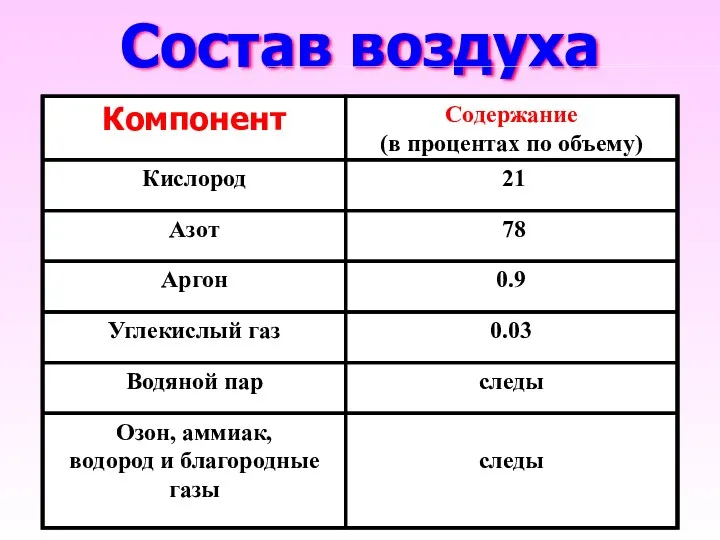
- 8. Состав воздуха
- 9. Кислород Жизненно важным газом атмосферы Земли является кислород. Его содержание составляет 21% воздуха. Хотя кислород является
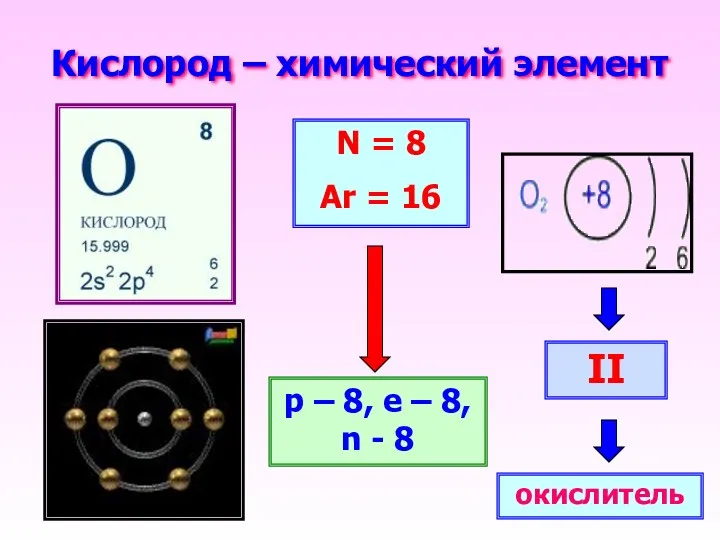
- 10. Кислород – химический элемент N = 8 Ar = 16 p – 8, e – 8,
- 11. Воздух – 21% Земная кора – 49% Гидросфера – 89% Живые организмы – 65% Самый распространенный
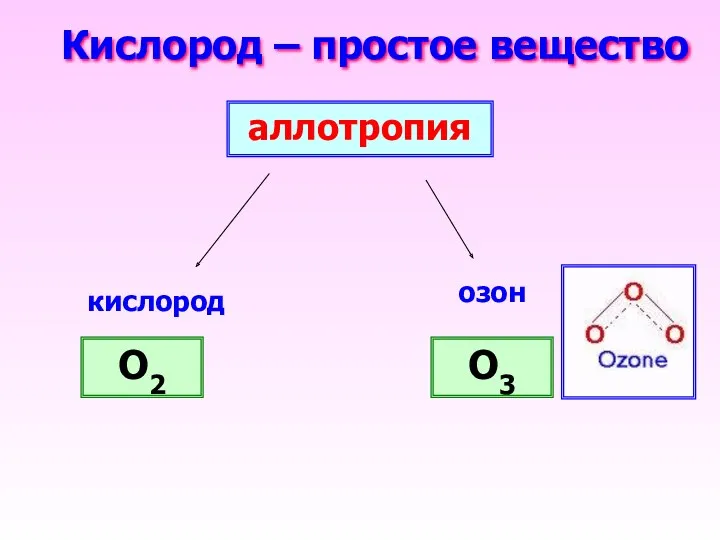
- 12. Кислород – простое вещество O2 O3 кислород озон аллотропия
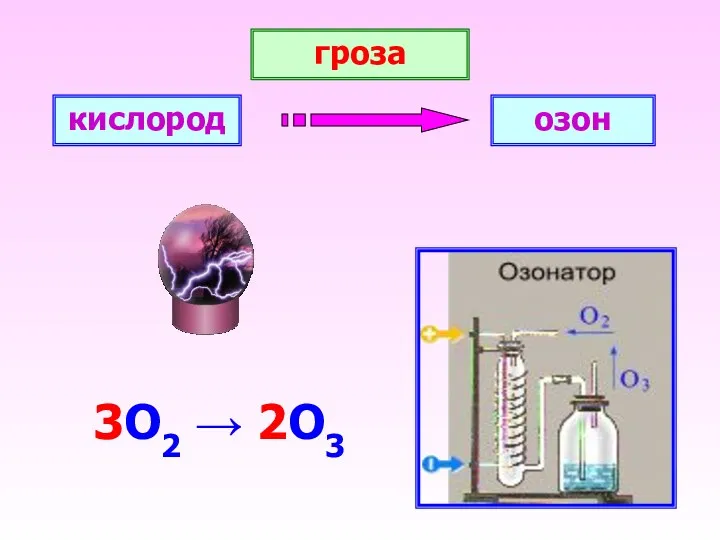
- 13. гроза 3О2 → 2О3 кислород озон
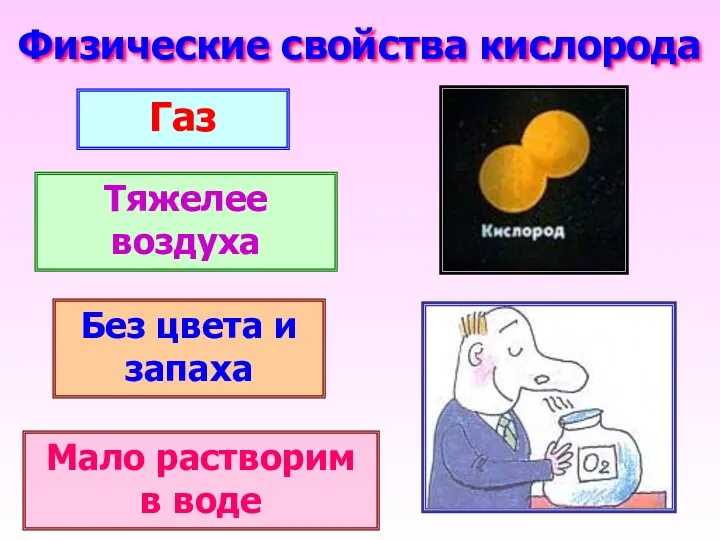
- 14. Физические свойства кислорода Газ Тяжелее воздуха Без цвета и запаха Мало растворим в воде
- 15. Способы получения кислорода В промышленности – перегонка жидкого воздуха Стальной баллон, Р – 15 МПа
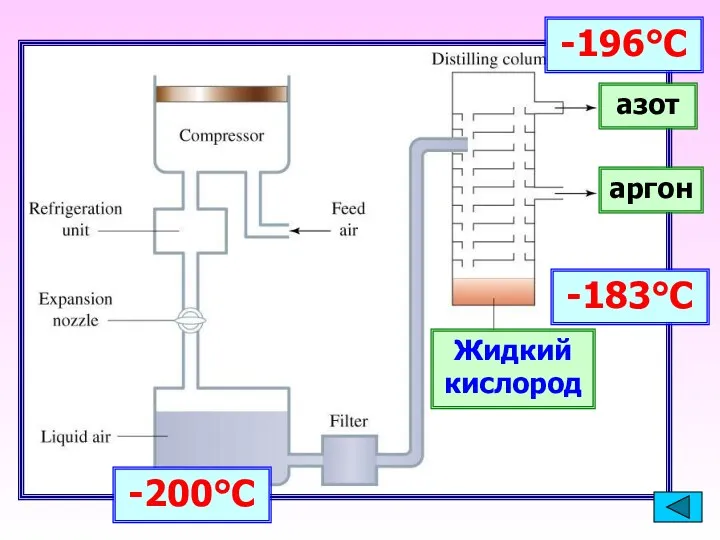
- 16. -200°С -183°С Жидкий кислород -196°С азот аргон
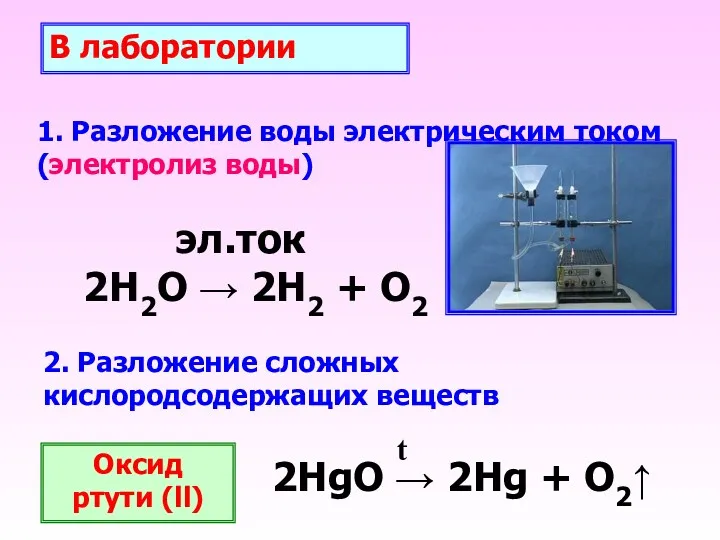
- 17. 1. Разложение воды электрическим током (электролиз воды) эл.ток 2Н2О → 2Н2 + О2 В лаборатории 2.
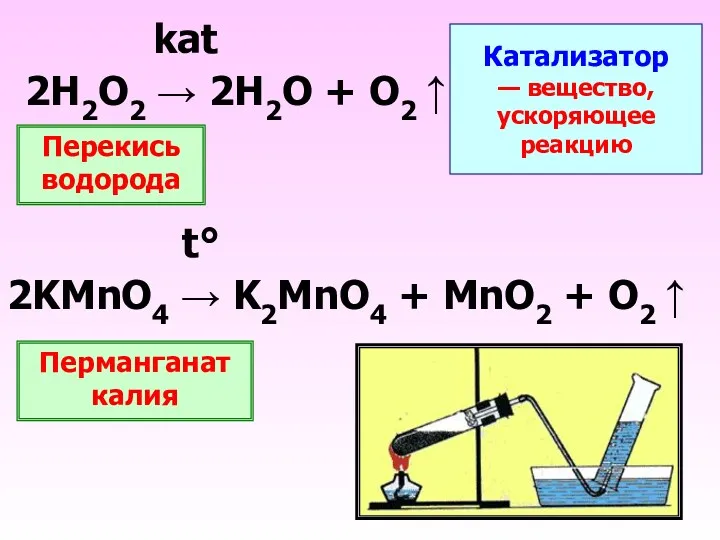
- 18. t° 2KMnO4 → K2MnO4 + MnO2 + O2 ↑ kat 2Н2О2 → 2Н2О + О2 ↑
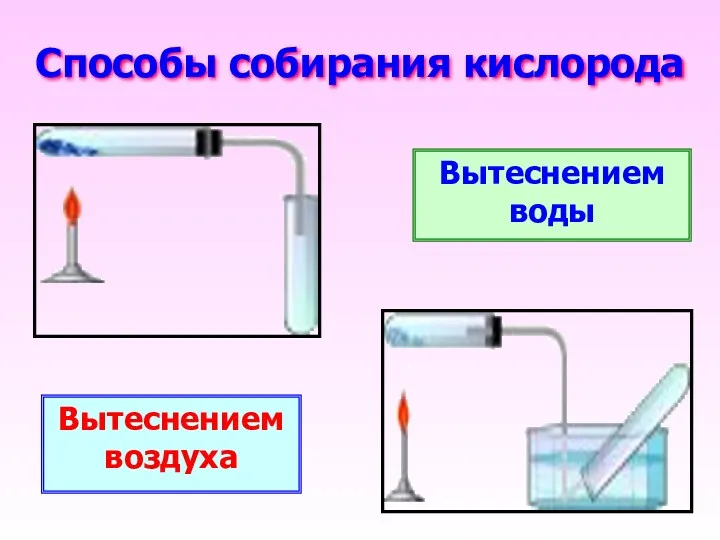
- 19. Способы собирания кислорода Вытеснением воздуха Вытеснением воды
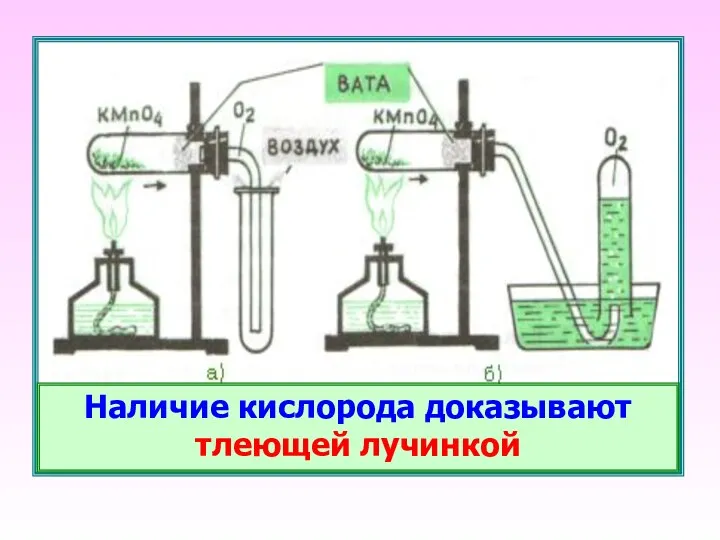
- 20. Наличие кислорода доказывают тлеющей лучинкой
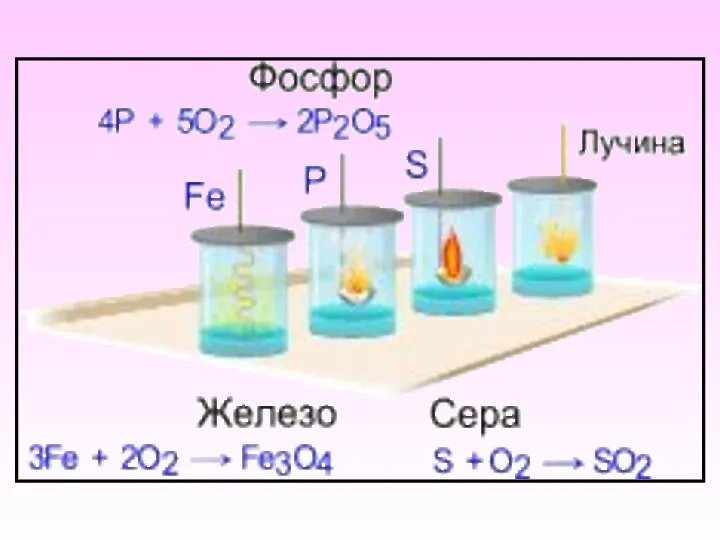
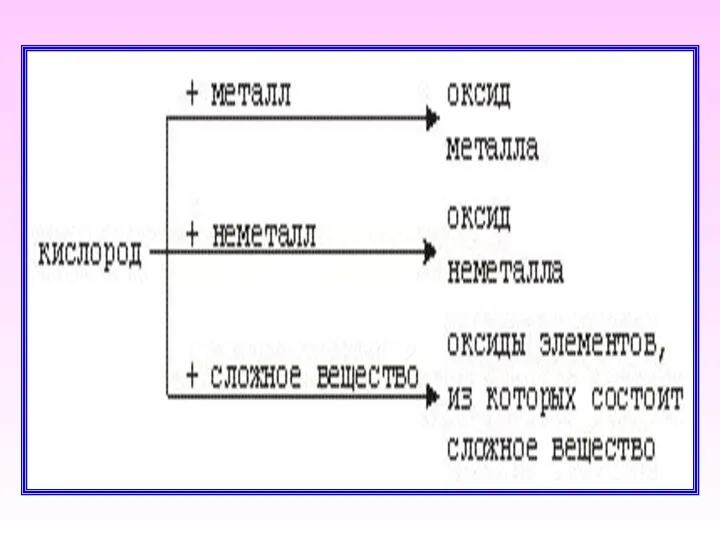
- 21. Химические свойства кислорода t° Al + O2 → Al O t° 3Fe + 2O2 → Fe3O4
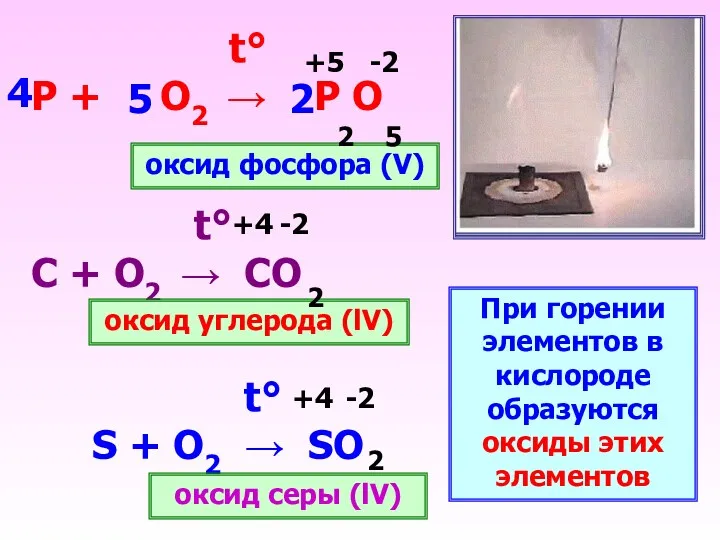
- 22. t° S + O2 → SO t° Р + О2 → Р О t° С +
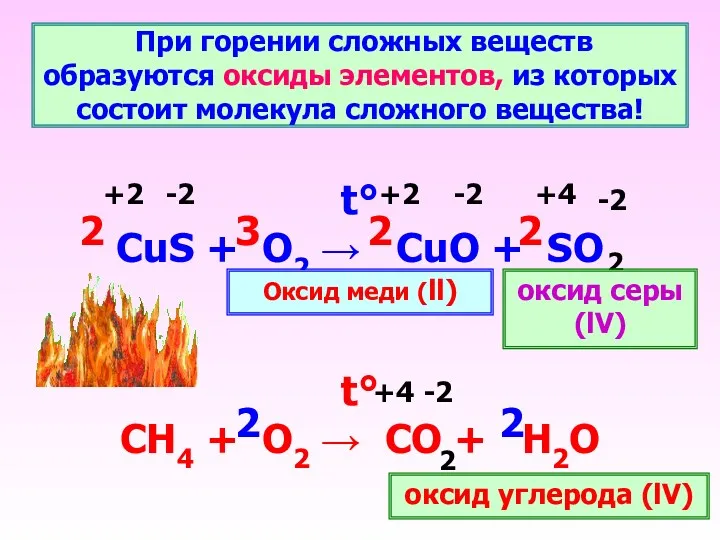
- 24. При горении сложных веществ образуются оксиды элементов, из которых состоит молекула сложного вещества! t° CuS +
- 25. 4FeS2 + 11O2 → 2Fe2O3 + 8SO2 2H2S + 3O2 → 2SO2 + 2H2O Для прекращения
- 27. 4Fe + 3O2 + 2nH2O = 2Fe2O3× nH2O (ржавчина – гидрат оксида железа (III) ) Медленное
- 28. Применение кислорода
- 29. Загрязнение воздуха деятельностью человека В наше время происходит активное загрязнение воздуха промышленной деятельностью человека, в частности
- 30. Имеются сообщения, что за последние полвека дымовые газы, выброшенные предприятиями Афин, а также выхлопные газы автомобилей
- 31. И не удивительно, что на улицах Токио можно подышать кислородом в специальных бутылках за плату, а
- 32. Вредное влияние на растения оказывает пыль, содержащаяся в загрязненном воздухе, постоянный уровень кислорода в воздухе 21%
- 33. Особенно опасна для здоровья людей загрязнённость воздуха радиоактивными производственными отходами и веществами, выделяющимися при испытании ядерного
- 35. Скачать презентацию

















 Кристаллография и основы кристаллохимии
Кристаллография и основы кристаллохимии Електронні і графічні електронні формули атомів s-, p-, d- елементів. Принцип Мінімальної енергії
Електронні і графічні електронні формули атомів s-, p-, d- елементів. Принцип Мінімальної енергії Скорость химических реакций
Скорость химических реакций Значение пищи и ее состав
Значение пищи и ее состав Введение в нефтепереработку. Переработка нефти и газа
Введение в нефтепереработку. Переработка нефти и газа Парфюмерно-косметическая продукция
Парфюмерно-косметическая продукция Кислоты
Кислоты Основания. (8 класс)
Основания. (8 класс) ПВХ
ПВХ Inert metals
Inert metals Закон Авогадро. Молярный объём газов
Закон Авогадро. Молярный объём газов Железо и его соединения
Железо и его соединения История и методология химии. Лекция 8
История и методология химии. Лекция 8 Метанол, етанол та їхнє застосування
Метанол, етанол та їхнє застосування Общая характеристика неметаллов
Общая характеристика неметаллов Свободные радикалы и болезни человека
Свободные радикалы и болезни человека Кристаллография, кристаллохимия, минералогия
Кристаллография, кристаллохимия, минералогия Окислительные свойства серной и азотной кислот
Окислительные свойства серной и азотной кислот Гетерофазный катализ. (Лекция 20)
Гетерофазный катализ. (Лекция 20) Полимерные материалы (ПМ). Классификация ПМ
Полимерные материалы (ПМ). Классификация ПМ Характеристика неметаллов. Галогены
Характеристика неметаллов. Галогены Влияние газированных напитков на организм человека
Влияние газированных напитков на организм человека Вредные вещества в продуктах питания
Вредные вещества в продуктах питания Тепловой эффект химических реакций. Расчёты по термохимическим уравнениям (ТХУ)
Тепловой эффект химических реакций. Расчёты по термохимическим уравнениям (ТХУ) Ациклические углеводороды
Ациклические углеводороды Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.)
Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.) Биохимия эритроцита
Биохимия эритроцита Кислород. Химия – 8 класс
Кислород. Химия – 8 класс