Содержание
- 2. План презентации: 1. Определение понятия «окислительно-восстановительные реакции» 2. Определение степени окисления атомов углерода в органических веществах
- 3. – реакции, сопровождающиеся изменением степени окисления атомов, входящих в состав реагирующих веществ, в результате перемещения электронов
- 4. Генетическая связь органических веществ Алехина Е.А.
- 5. Модифицированная генетическая связь органических и неорганических соединений C [O] CO [H] насыщенные ненасыщенные углеводороды -[H] углеводороды
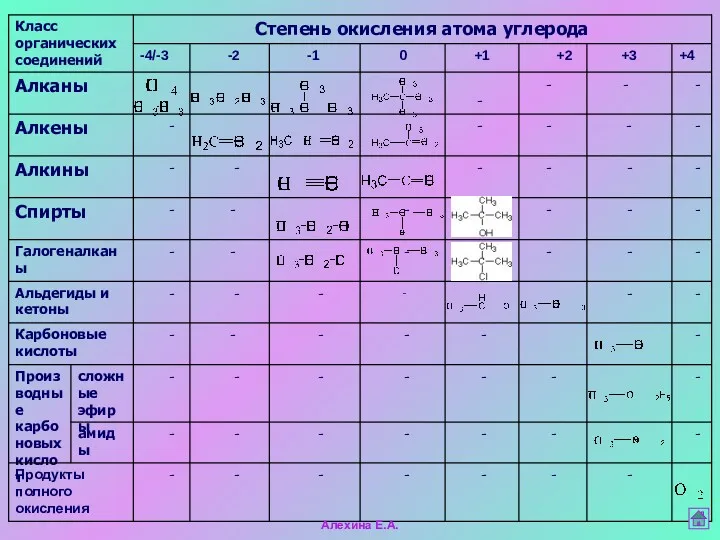
- 6. Н3С – СН2 – СН3 СН3 – СН2 – ОН Определение степени окисления атомов в органических
- 8. Алехина Е.А.
- 9. Изменение степени окисления углерода в органических соединениях Алехина Е.А.
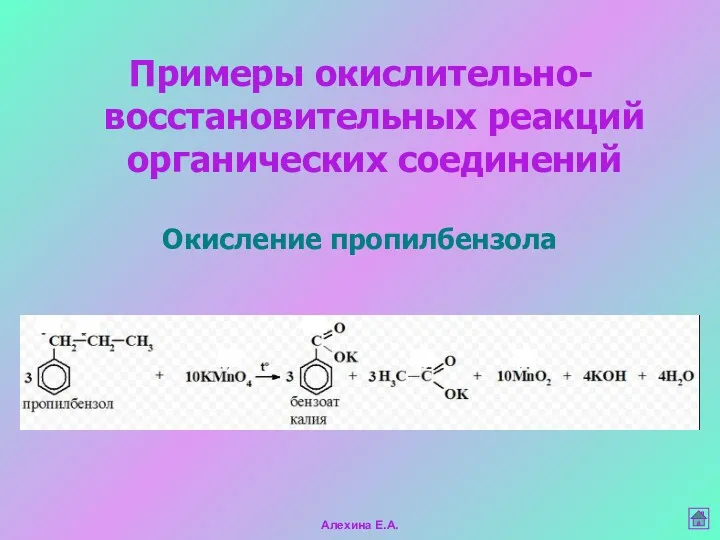
- 10. Алехина Е.А. Примеры окислительно-восстановительных реакций органических соединений Окисление пропилбензола
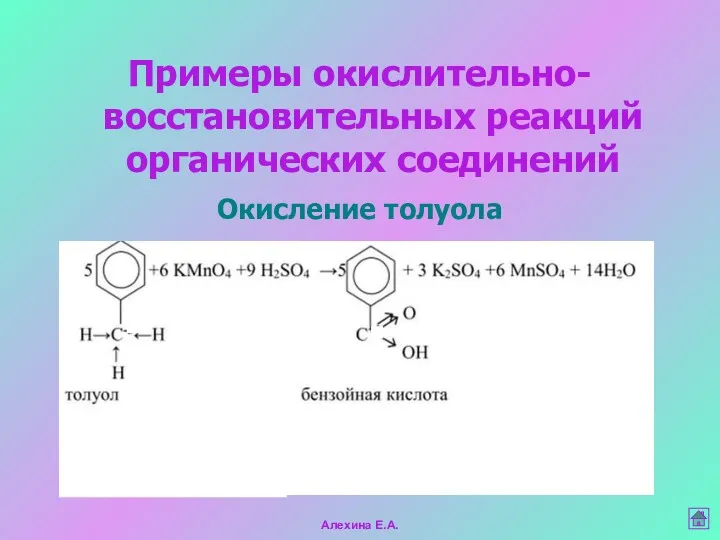
- 11. Алехина Е.А. Примеры окислительно-восстановительных реакций органических соединений Окисление толуола
- 12. Алехина Е.А. Примеры окислительно-восстановительных реакций органических соединений Окисление цимола
- 13. Алехина Е.А. Примеры окислительно-восстановительных реакций органических соединений
- 14. Алехина Е.А. Примеры окислительно-восстановительных реакций органических соединений
- 15. Реакции окисления процесс отдачи электронов атомом, молекулой или ионом (по Г.П. Хомченко, с. 168); образование новых
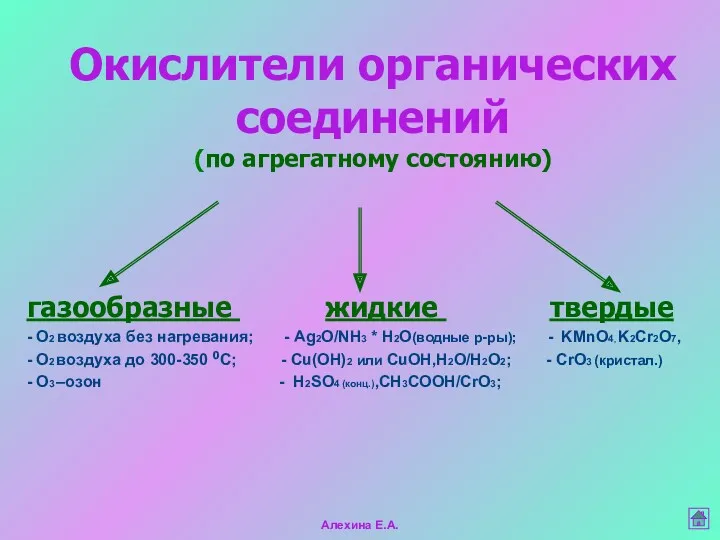
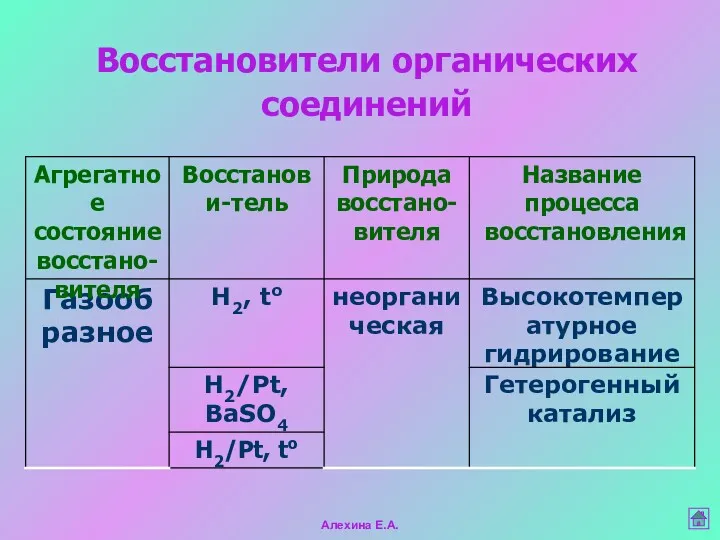
- 16. Окислители органических соединений (по агрегатному состоянию) газообразные жидкие твердые - O2 воздуха без нагревания; - Ag2O/NH3
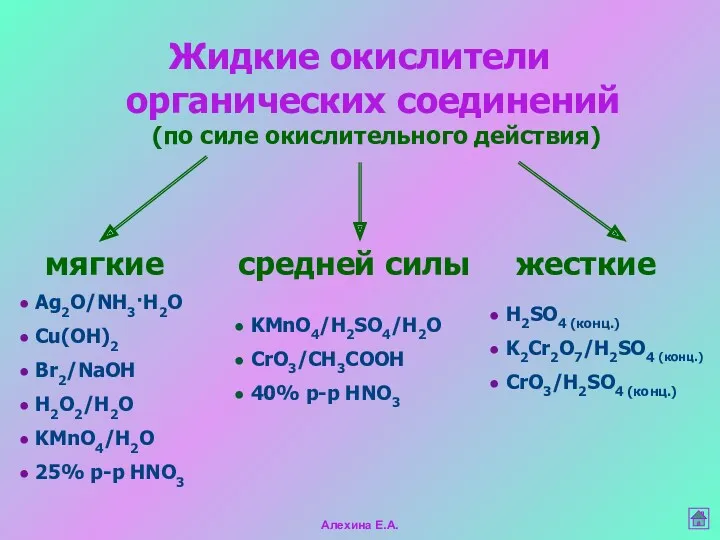
- 17. Жидкие окислители органических соединений (по силе окислительного действия) мягкие средней силы жесткие Ag2O/NH3·H2O Cu(OH)2 Br2/NaOH H2O2/H2O
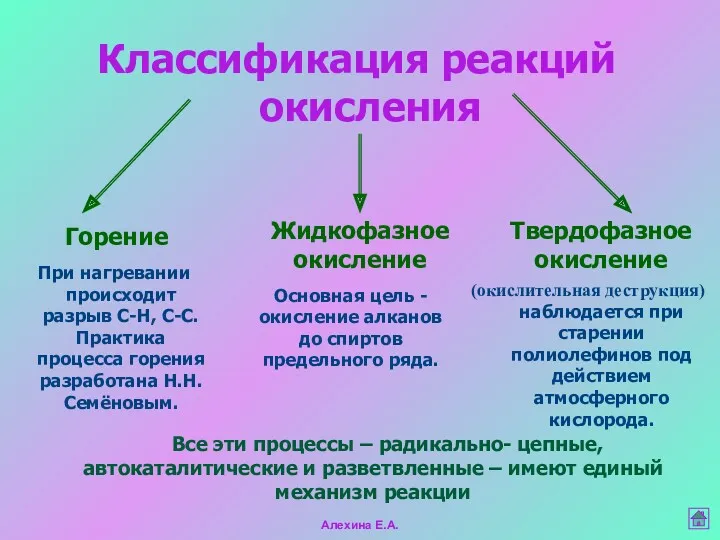
- 18. Классификация реакций окисления Горение Жидкофазное окисление Твердофазное окисление При нагревании происходит разрыв С-Н, С-С. Практика процесса
- 19. МЕХАНИЗМЫ ОКИСЛЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Алехина Е.А.
- 20. Радикальный механизм окисления органических соединений Инициирование + + t Рост цепи + + + + +
- 21. ГАЛОГЕНИРОВАНИЕ АЛКАНОВ hν Инициирование Рост цепи Обрыв цепи SR Алехина Е.А.
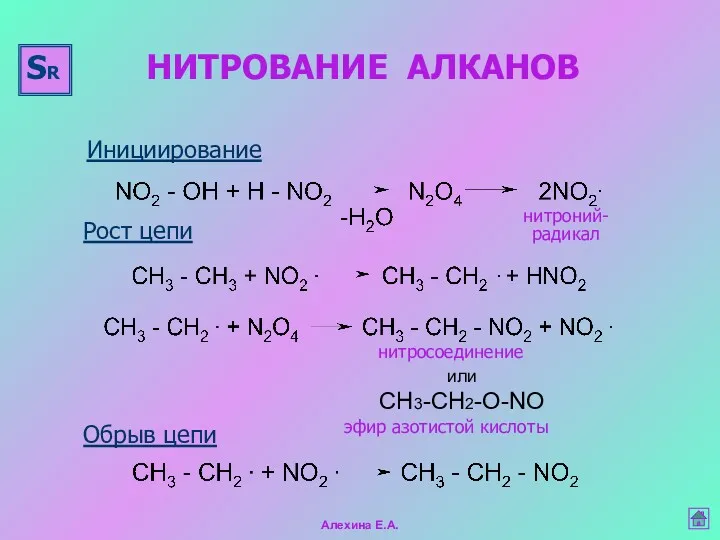
- 22. НИТРОВАНИЕ АЛКАНОВ Инициирование Рост цепи Обрыв цепи нитроний- радикал или СH3-СН2-О-NO нитросоединение эфир азотистой кислоты SR
- 23. СУЛЬФОХЛОРИРОВАНИЕ АЛКАНОВ Инициирование Рост цепи алкилсульфохлорид hν hν Например этилсульфохлорид СН3-СH3 + SO2 + Cl2 →
- 24. СУЛЬФООКИСЛЕНИЕ АЛКАНОВ алкилсульфокислота I способ II способ Например этилсульфокислота алкилсульфокислота 2R-H + 2SO2 + O2 →
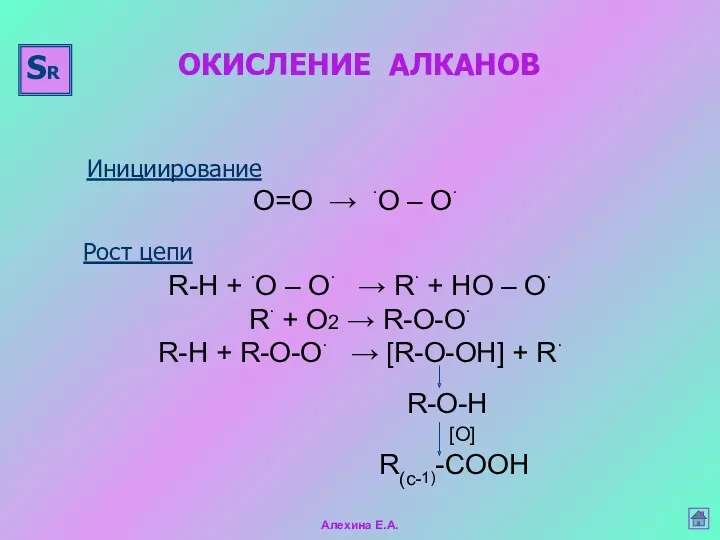
- 25. ОКИСЛЕНИЕ АЛКАНОВ Инициирование Рост цепи О=О → ∙О – О∙ R-H + ∙О – О∙ →
- 26. изобутан гидроперекись изобутана третбутанол Например (СН3)3СН + О2 → [(СН3)3С-О-О-Н] → (СН3)3С-ОН СН3-СН2-СН2-СН3 + О2 →
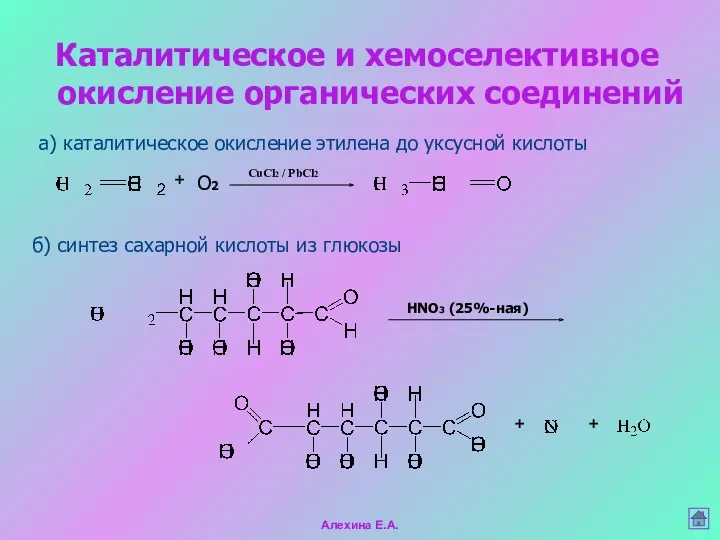
- 27. Каталитическое и хемоселективное окисление органических соединений а) каталитическое окисление этилена до уксусной кислоты + О2 CuCl2
- 28. Реакции восстановления процесс присоединения электронов атомом, молекулой или ионом (по Г.П. Хомченко, с. 168); образование новых
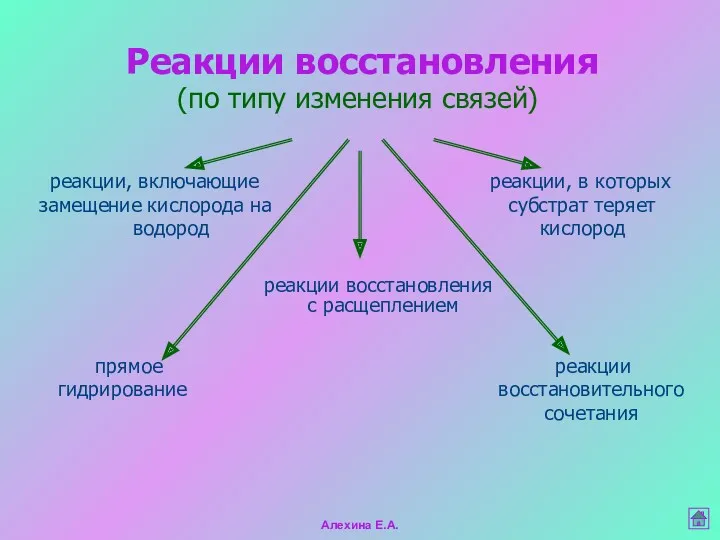
- 29. Реакции восстановления (по типу изменения связей) реакции, включающие реакции, в которых замещение кислорода на субстрат теряет
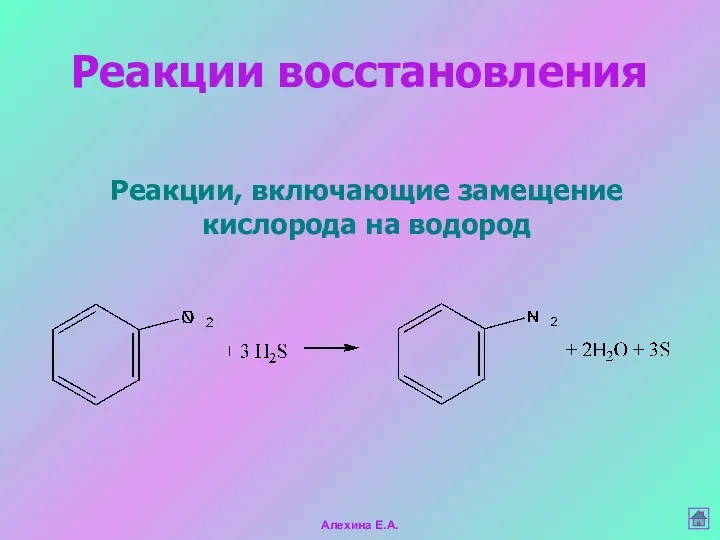
- 30. Реакции, включающие замещение кислорода на водород Реакции восстановления Алехина Е.А.
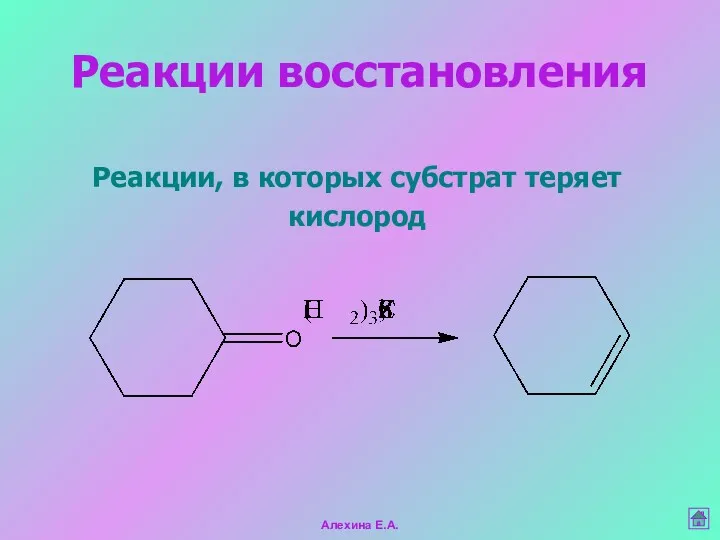
- 31. Реакции, в которых субстрат теряет кислород Реакции восстановления Алехина Е.А.
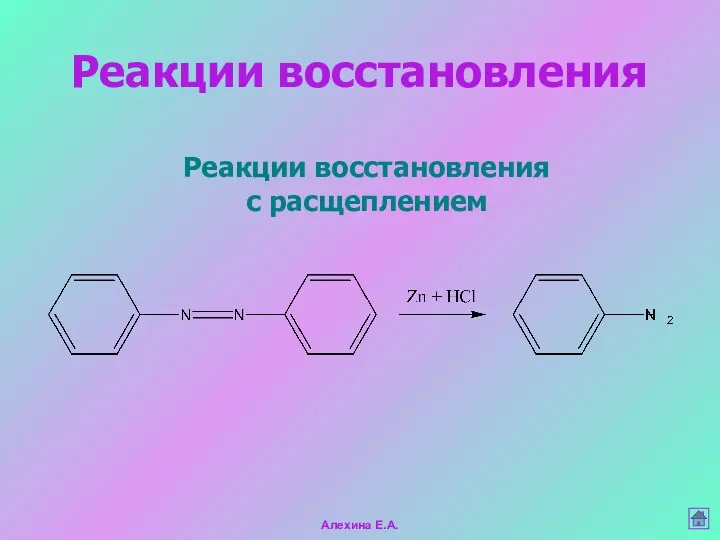
- 32. Реакции восстановления с расщеплением Реакции восстановления Алехина Е.А.
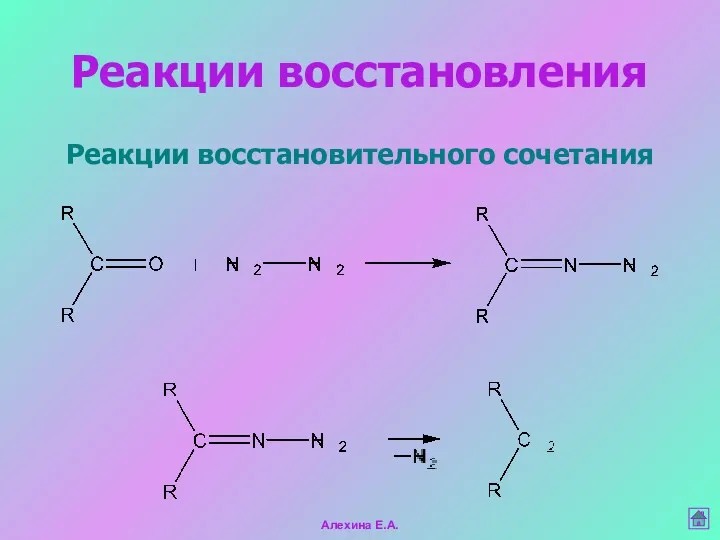
- 33. Реакции восстановления Реакции восстановительного сочетания Алехина Е.А.
- 34. Прямое гидрирование углеводородов Восстановление алифатических углеводородов Восстановление ароматических углеводородов Реакции восстановления Алехина Е.А.
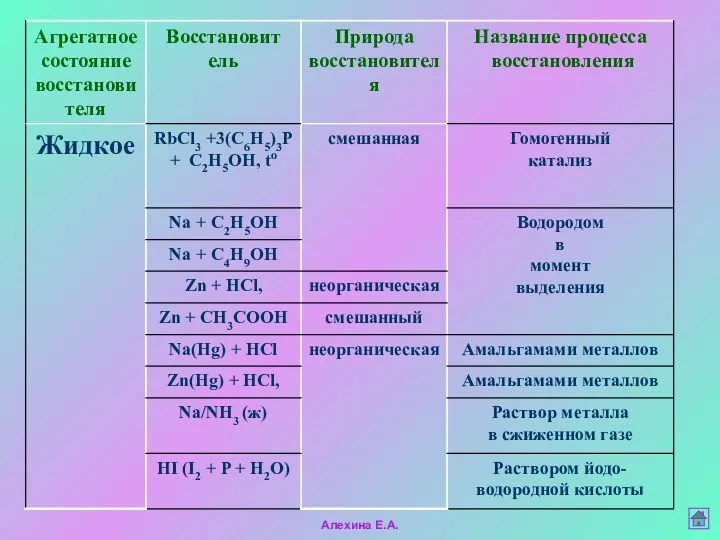
- 35. Восстановители органических соединений Алехина Е.А.
- 36. Алехина Е.А.
- 37. Алехина Е.А.
- 38. МЕХАНИЗМЫ ВОССТАНОВЛЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Алехина Е.А.
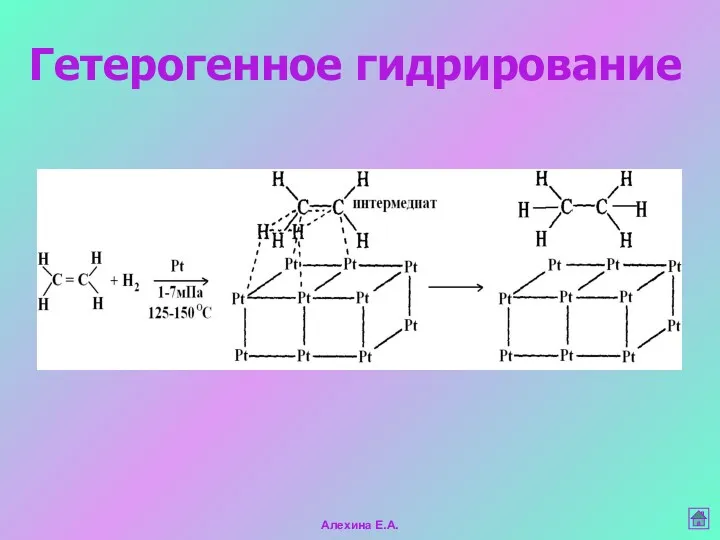
- 39. Гетерогенное гидрирование Алехина Е.А.
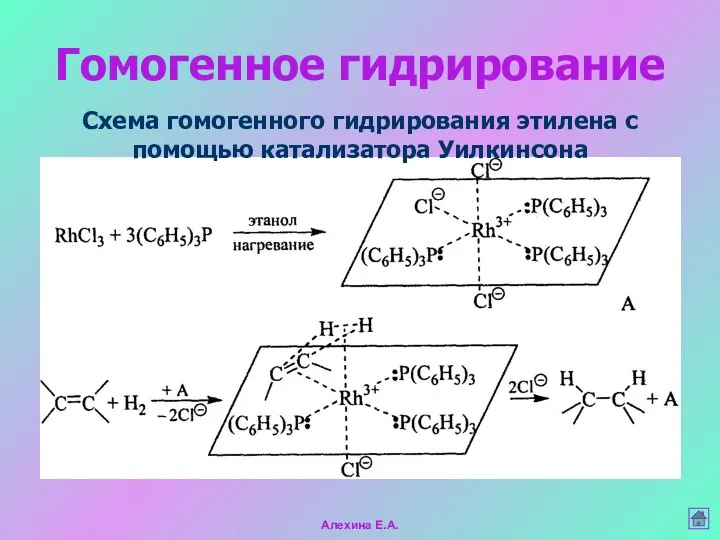
- 40. Гомогенное гидрирование Схема гомогенного гидрирования этилена с помощью катализатора Уилкинсона Алехина Е.А.
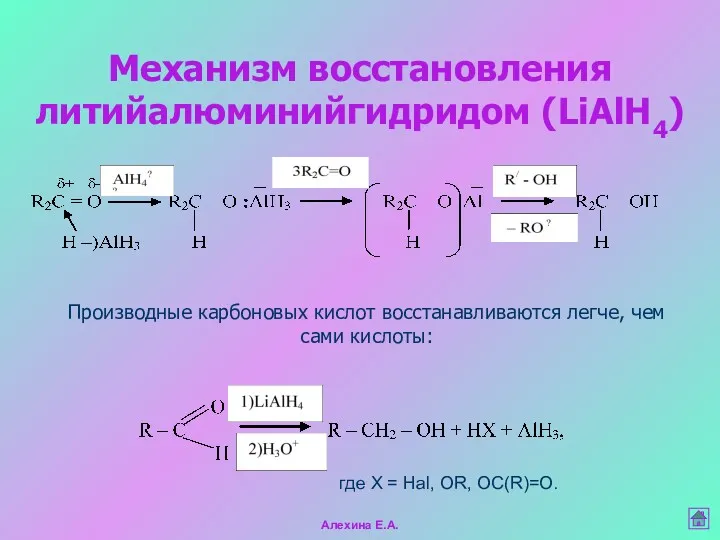
- 41. Механизм восстановления литийалюминийгидридом (LiAlH4) где Х = Hal, OR, OC(R)=O. Производные карбоновых кислот восстанавливаются легче, чем
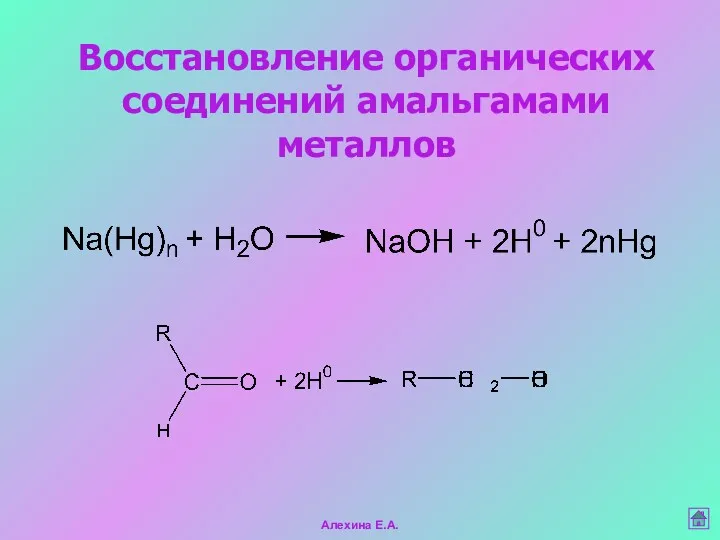
- 42. Восстановление органических соединений амальгамами металлов Амальгамами называют сплавы жидкой ртути с металлами – Zn, Co, Rb,
- 43. Восстановление органических соединений амальгамами металлов Алехина Е.А.
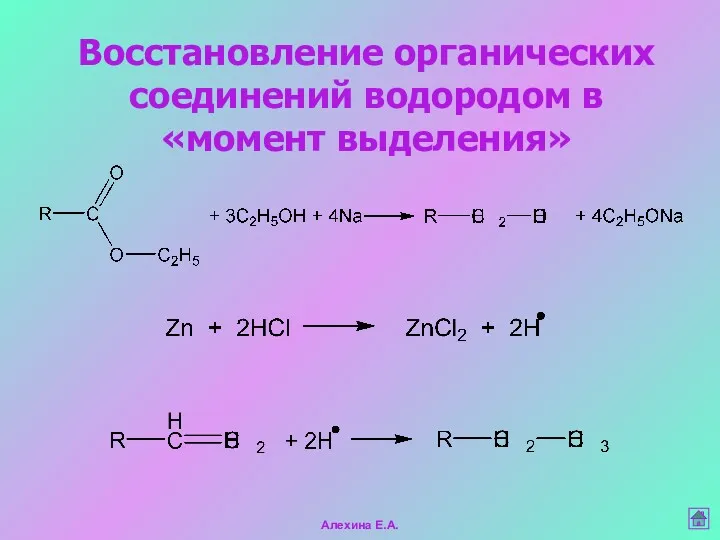
- 44. Восстановление органических соединений водородом в «момент выделения» Алехина Е.А.
- 46. Скачать презентацию



![Модифицированная генетическая связь органических и неорганических соединений C [O] CO](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/211957/slide-4.jpg)












![изобутан гидроперекись изобутана третбутанол Например (СН3)3СН + О2 → [(СН3)3С-О-О-Н]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/211957/slide-25.jpg)





 Аминокислоты 2
Аминокислоты 2 Магний. Нахождение в природе
Магний. Нахождение в природе Цветные металлы и сплавы
Цветные металлы и сплавы Концентрации растворов
Концентрации растворов Небезпечні хімічні речовини
Небезпечні хімічні речовини Медь и её соединения
Медь и её соединения Вода на Земле. Строение молекулы воды
Вода на Земле. Строение молекулы воды Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов
Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов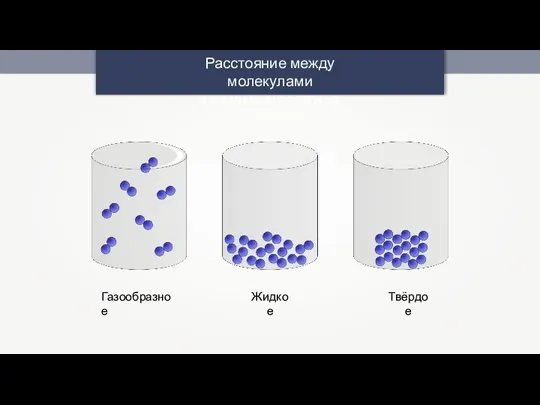 Расстояние между молекулами в разных агрегатных состояниях
Расстояние между молекулами в разных агрегатных состояниях Сущность процесса электролитической диссоциации
Сущность процесса электролитической диссоциации Азотовмісні сполуки
Азотовмісні сполуки Кристаллография, кристаллохимия, минералогия
Кристаллография, кристаллохимия, минералогия Знаки химических элементов. Химические формулы. Химический диктант
Знаки химических элементов. Химические формулы. Химический диктант Етери та естери. Хімічні властивості
Етери та естери. Хімічні властивості Физико-химические методы исследования биологически активных веществ
Физико-химические методы исследования биологически активных веществ Химическое равновесие в гомогенных системах. Ионное произведение воды. 12 класс
Химическое равновесие в гомогенных системах. Ионное произведение воды. 12 класс Изомерия и ее виды
Изомерия и ее виды Берилій
Берилій Новые интеллектуальные материалы на основе полимеров
Новые интеллектуальные материалы на основе полимеров Аммиак. Строение молекулы аммиака, его физические и химические свойства
Аммиак. Строение молекулы аммиака, его физические и химические свойства Вуглеводні. Лекція 11
Вуглеводні. Лекція 11 Алмазы. Бриллианты
Алмазы. Бриллианты Растворы. Общие свойства растворов
Растворы. Общие свойства растворов Химиялық элементтердің тірі және өлі табиғатта таралуы
Химиялық элементтердің тірі және өлі табиғатта таралуы Кислотно-основные (протолитические) равновесия
Кислотно-основные (протолитические) равновесия Методика изучения и описание вулканогенных обломочных пород
Методика изучения и описание вулканогенных обломочных пород Зеленая химия и проблемы устойчивого развития
Зеленая химия и проблемы устойчивого развития Кислород. Оксиды. Валентность
Кислород. Оксиды. Валентность