Слайд 2
Слайд 3

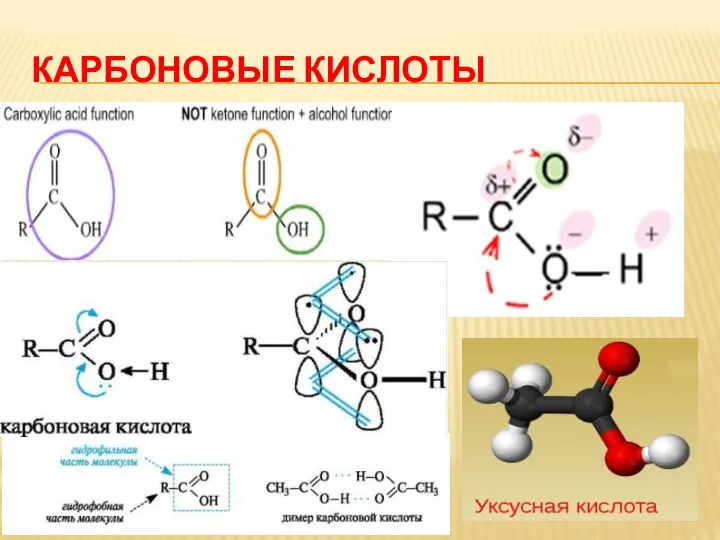
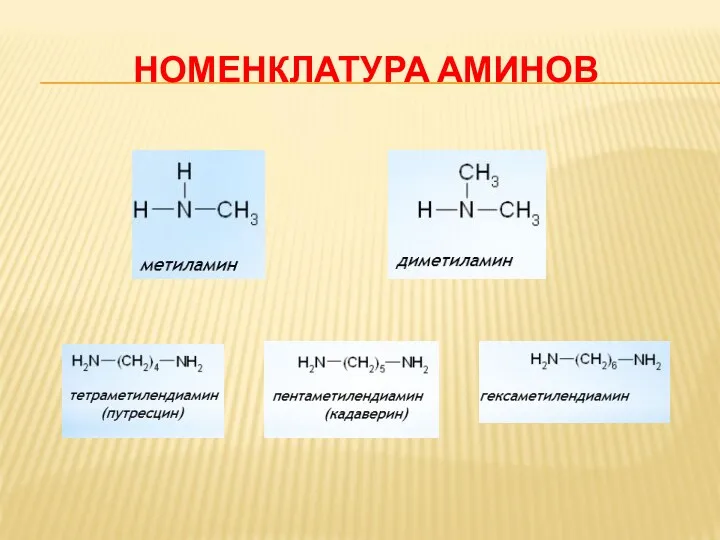
НОМЕНКЛАТУРА КАРБОНОВЫХ КИСЛОТ
Слайд 4

КЛАССИФИКАЦИЯ КАРБОНОВЫХ КИСЛОТ
По числу карбоксильных групп:
одноосновные(монокарбоновые)
многоосновные(ди-, трикарбоновые)
По характеру радикала:
предельные
непредельные
ароматические
Слайд 5

СПОСОБЫ ПОЛУЧЕНИЯ КАРБОНОВЫХ КИСЛОТ
1.Окисление спиртов:
2.Окисление альдегидов:
3.Окисление непредельных соединений:
Слайд 6
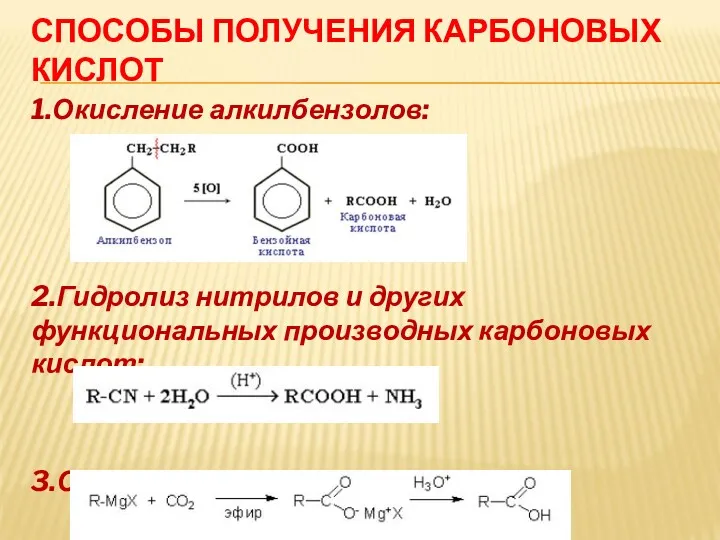
СПОСОБЫ ПОЛУЧЕНИЯ КАРБОНОВЫХ КИСЛОТ
1.Окисление алкилбензолов:
2.Гидролиз нитрилов и других функциональных производных карбоновых
кислот:
3.Синтез Гриньяра:
Слайд 7
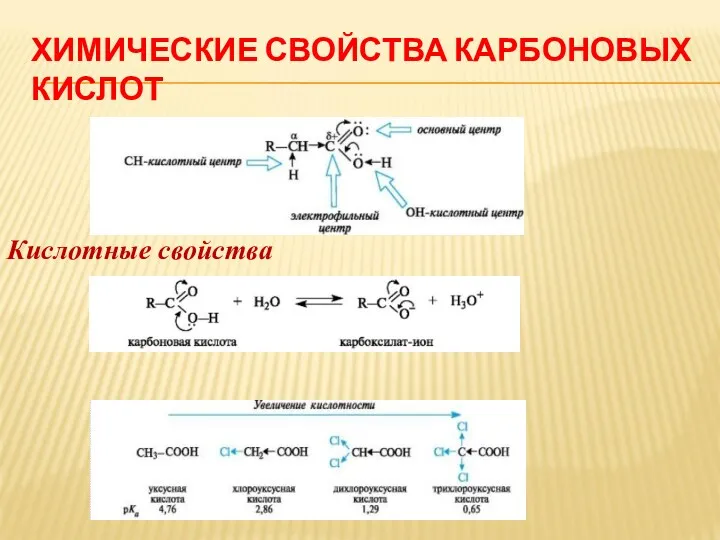
ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ
Кислотные свойства
Слайд 8

ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ
Взаимодействие с активными металлами:
2CH3COOH + Ca → (CH3COO)2Ca+H2
Взаимодействие
с оксидами металлов:
2CH3COOH+CaO → (CH3COO)2Ca+H2O
Реакция нейтрализации:
2CH3COOH+Ca(OH)2 → (CH3COO)2Ca+2H2O
Взаимодействие с солями:
2CH3COOH+CaCO3 → (CH3COO)2Ca+H2O+CO2
Слайд 9
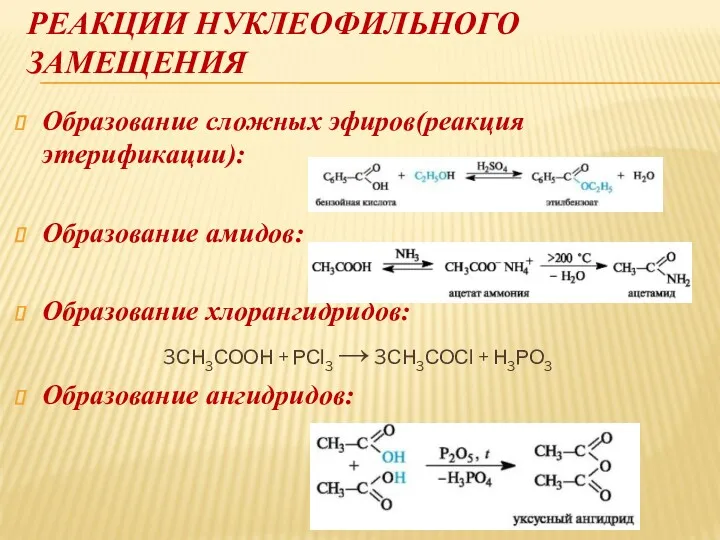
РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ
Образование сложных эфиров(реакция этерификации):
Образование амидов:
Образование хлорангидридов:
3СН3СООН + РСl3 →
3СН3СОСl + Н3РО3
Образование ангидридов:
Слайд 10
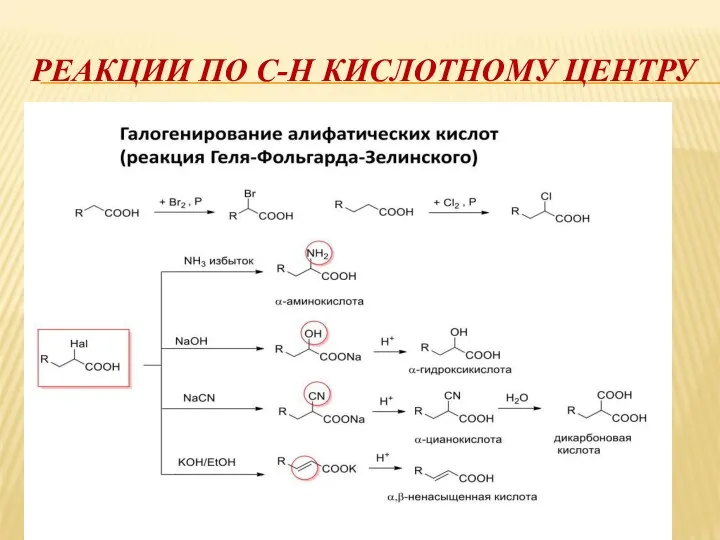
РЕАКЦИИ ПО С-Н КИСЛОТНОМУ ЦЕНТРУ
Слайд 11
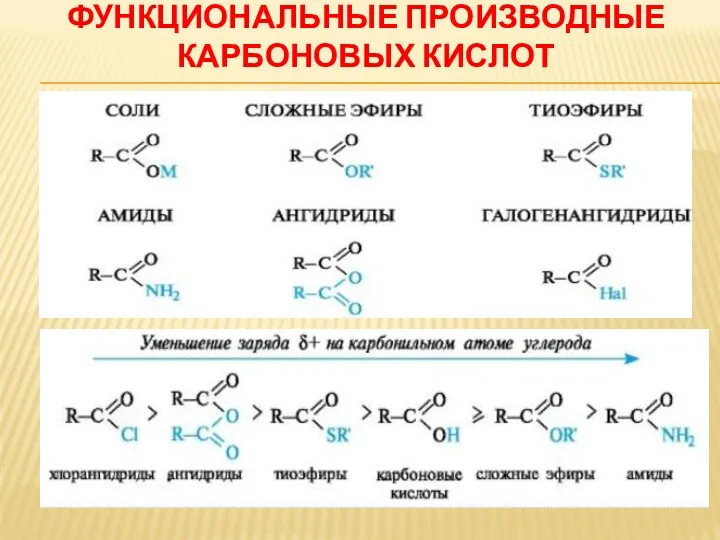
ФУНКЦИОНАЛЬНЫЕ ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
Слайд 12
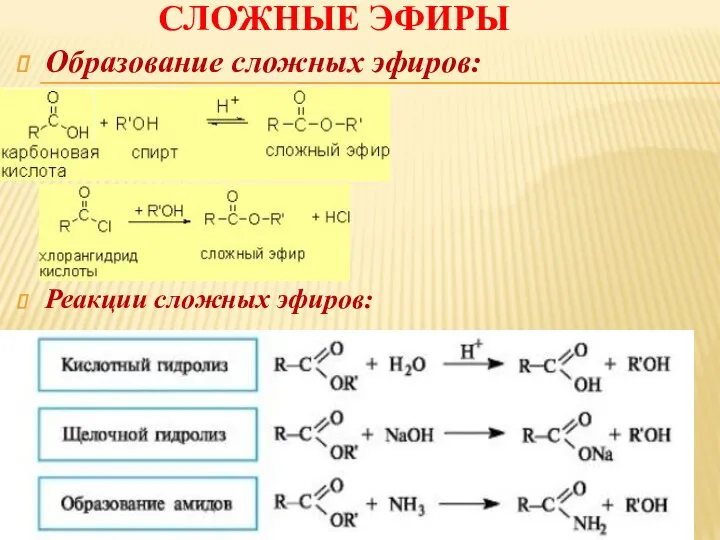
СЛОЖНЫЕ ЭФИРЫ
Образование сложных эфиров:
Реакции сложных эфиров:
Слайд 13
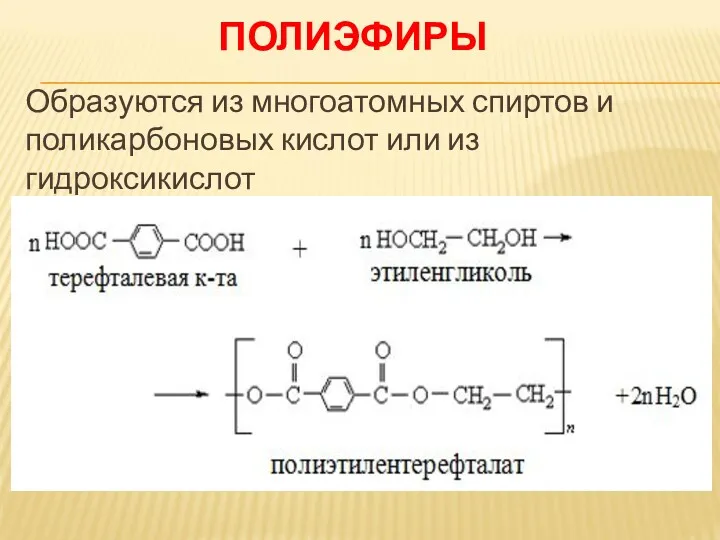
ПОЛИЭФИРЫ
Образуются из многоатомных спиртов и поликарбоновых кислот или из гидроксикислот
Слайд 14
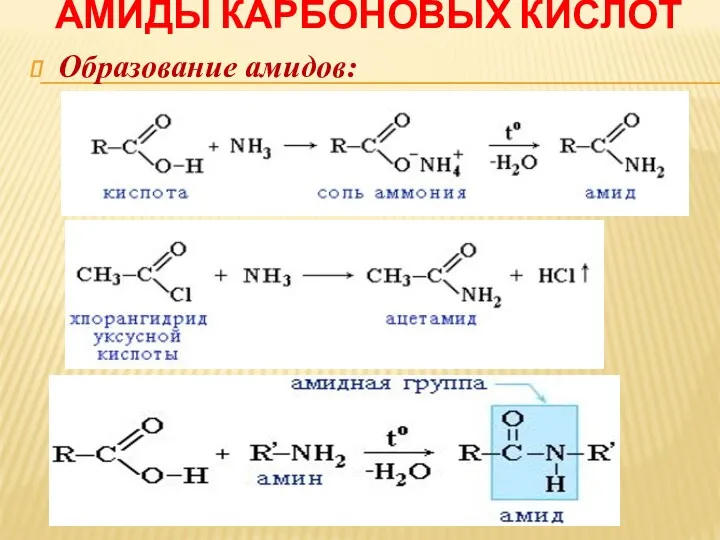
АМИДЫ КАРБОНОВЫХ КИСЛОТ
Образование амидов:
Слайд 15
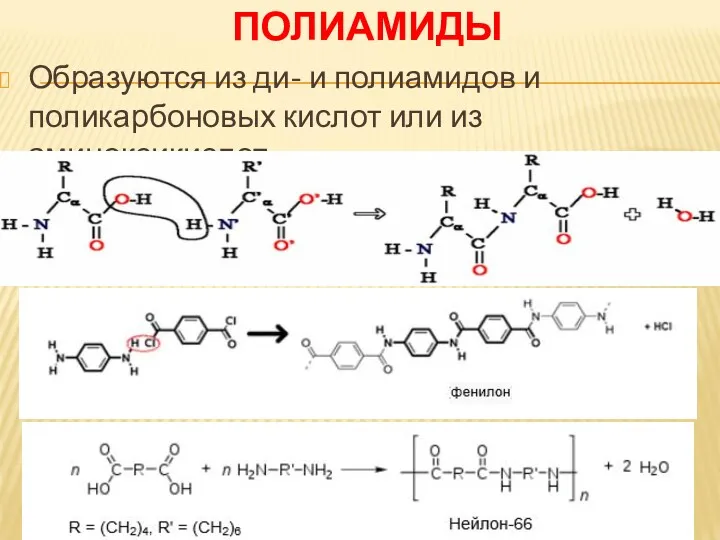
ПОЛИАМИДЫ
Образуются из ди- и полиамидов и поликарбоновых кислот или из аминоксикислот
Слайд 16
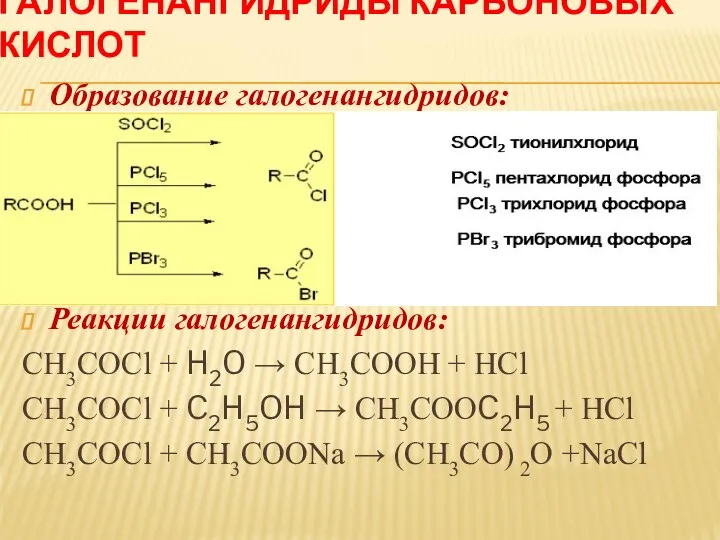
ГАЛОГЕНАНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
Образование галогенангидридов:
Реакции галогенангидридов:
CH3COCl + H2O → CH3COOH + HCl
CH3COCl
+ C2H5OH → CH3COOC2H5 + HCl
CH3COCl + CH3COONa → (CH3CO) 2O +NaCl
Слайд 17

АНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
Образование ангидридов:
CH3COCl + CH3COONa → (CH3CO) 2O +NaCl
2 CH3COOH
+ (H2SO4конц ) → (CH3CO) 2O +NaCl
Реакции ангидридов:
(CH3CO) 2O + 2H2O → 2CH3COOH
(CH3CO) 2O + 2C2H5OH → 2CH3COOC2H5 + H2O (CH3CO) 2O + 2NH3 → 2CH3CONH2+ H2O
Слайд 18
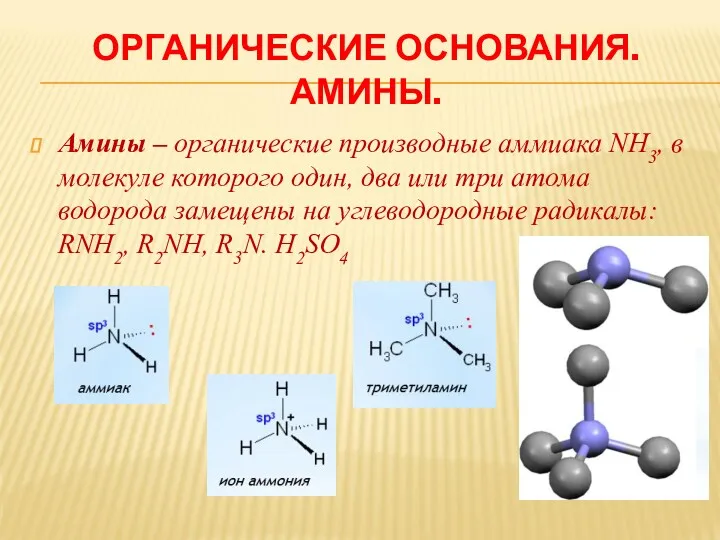
ОРГАНИЧЕСКИЕ ОСНОВАНИЯ. АМИНЫ.
Амины – органические производные аммиака NH3, в молекуле которого
один, два или три атома водорода замещены на углеводородные радикалы: RNH2, R2NH, R3N. H2SO4
Слайд 19
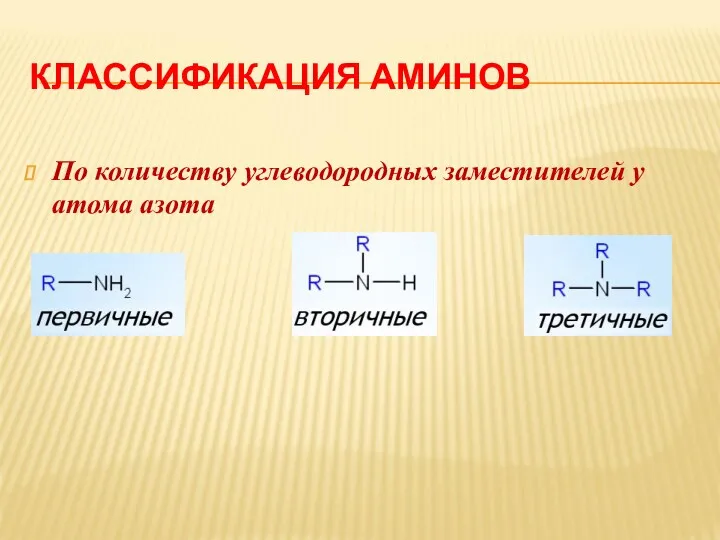
КЛАССИФИКАЦИЯ АМИНОВ
По количеству углеводородных заместителей у атома азота
Слайд 20
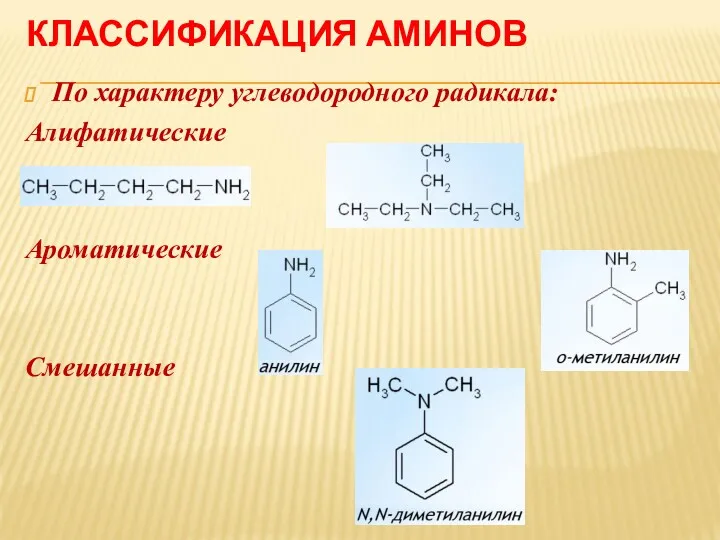
КЛАССИФИКАЦИЯ АМИНОВ
По характеру углеводородного радикала:
Алифатические
Ароматические
Смешанные
Слайд 21
Слайд 22
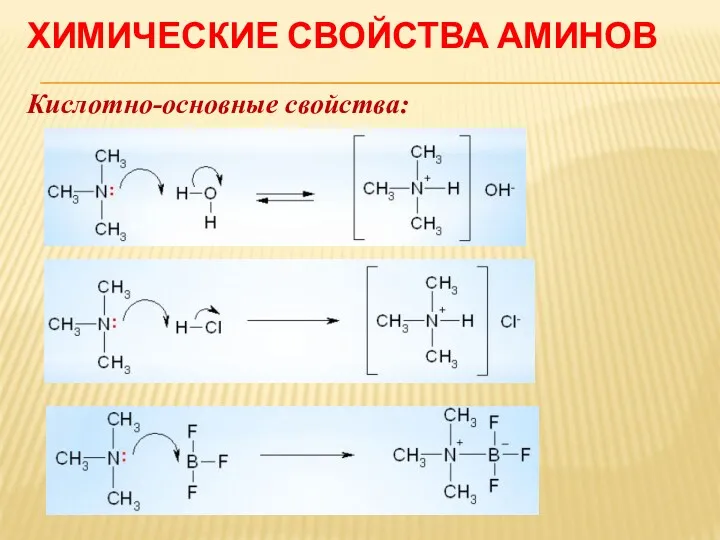
ХИМИЧЕСКИЕ СВОЙСТВА АМИНОВ
Кислотно-основные свойства:
Слайд 23
ХИМИЧЕСКИЕ СВОЙСТВА АМИНОВ
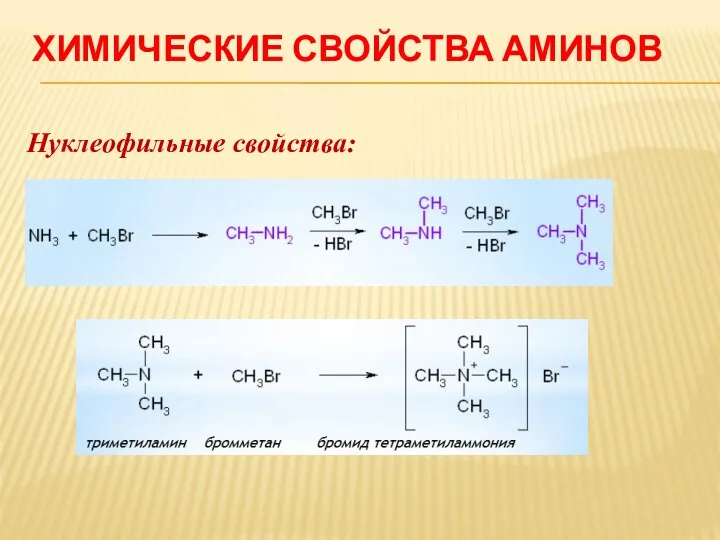
Нуклеофильные свойства:
Слайд 24
ХИМИЧЕСКИЕ СВОЙСТВА АМИНОВ
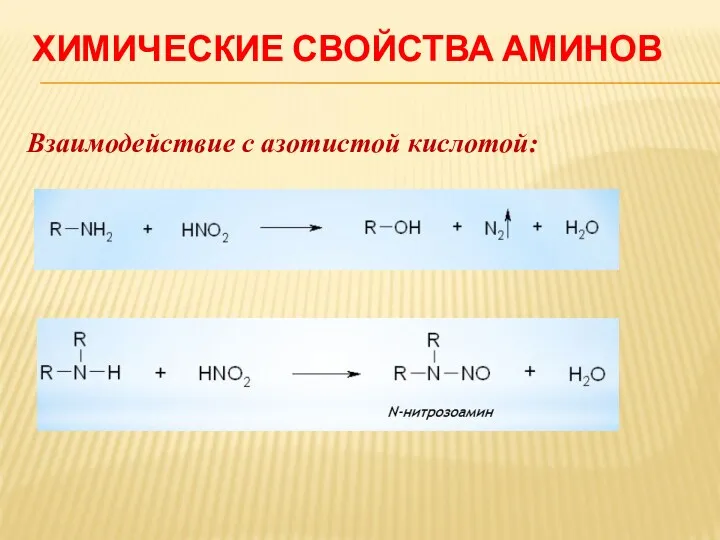
Взаимодействие с азотистой кислотой:
Слайд 25
ХИМИЧЕСКИЕ СВОЙСТВА АМИНОВ
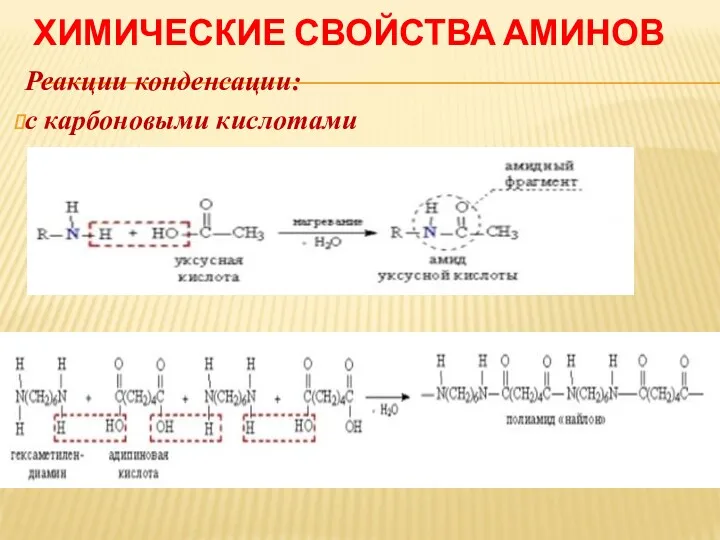
Реакции конденсации:
с карбоновыми кислотами
Слайд 26
ХИМИЧЕСКИЕ СВОЙСТВА АМИНОВ
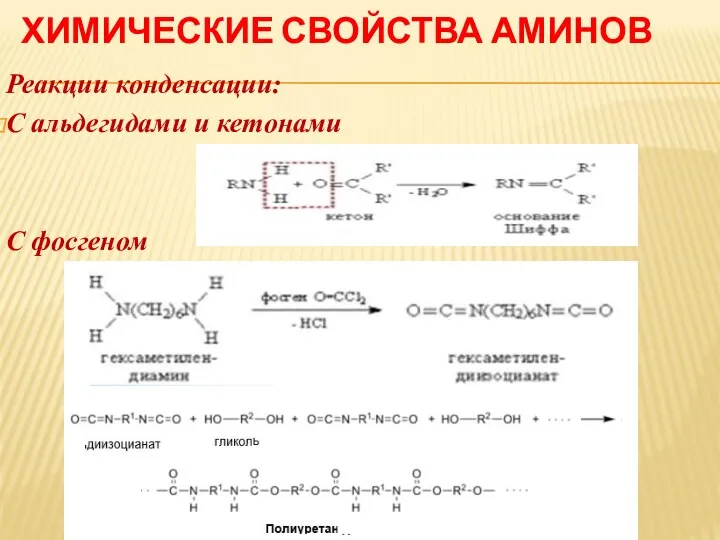
Реакции конденсации:
С альдегидами и кетонами
С фосгеном
Слайд 27
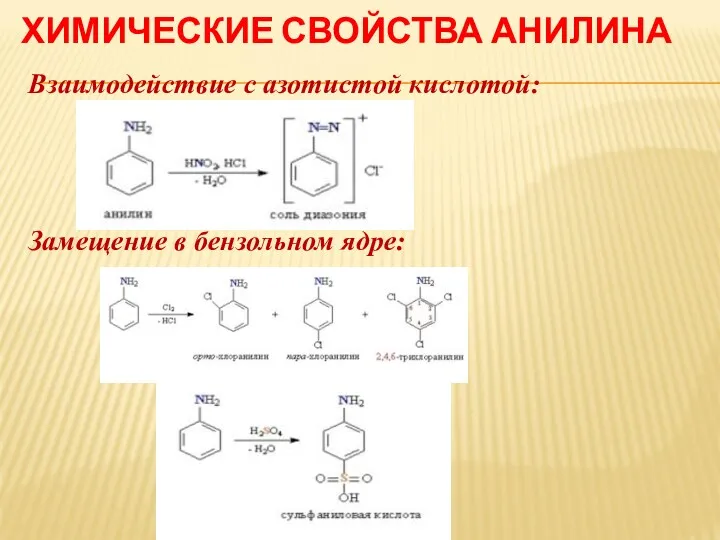
ХИМИЧЕСКИЕ СВОЙСТВА АНИЛИНА
Взаимодействие с азотистой кислотой:
Замещение в бензольном ядре:
Слайд 28
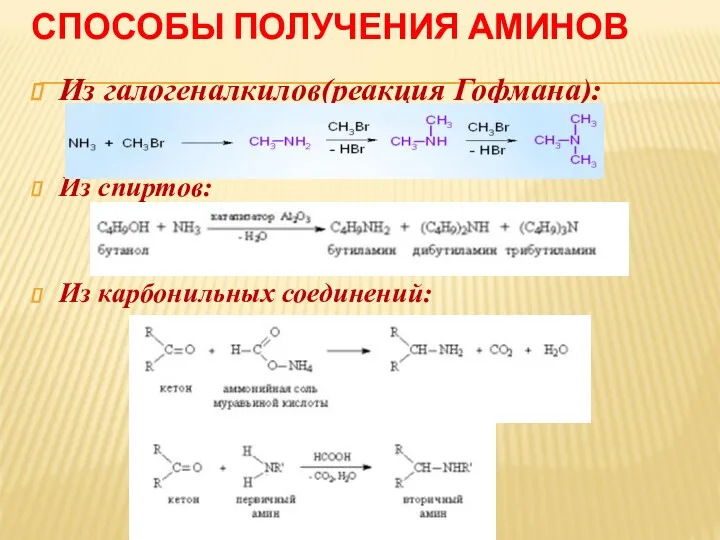
СПОСОБЫ ПОЛУЧЕНИЯ АМИНОВ
Из галогеналкилов(реакция Гофмана):
Из спиртов:
Из карбонильных соединений:
Слайд 29
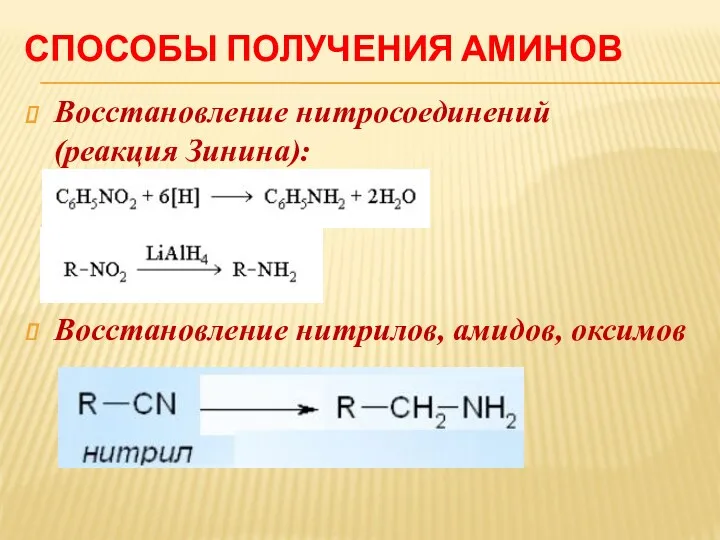
СПОСОБЫ ПОЛУЧЕНИЯ АМИНОВ
Восстановление нитросоединений (реакция Зинина):
Восстановление нитрилов, амидов, оксимов




























 Металлы. Общие свойства металлов
Металлы. Общие свойства металлов Химия и живопись
Химия и живопись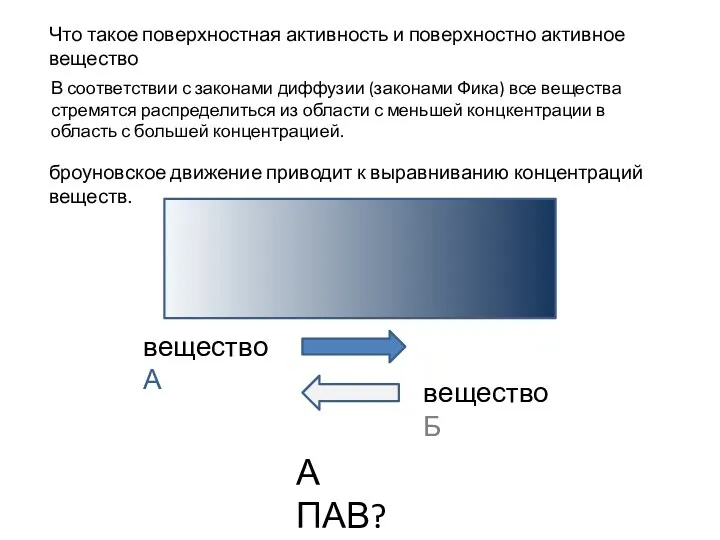 Поверхностная активность и поверхностно активное вещество
Поверхностная активность и поверхностно активное вещество Изменения, происходящие с липидами в процессах технологической переработки сырья и параметры, характеризующие их
Изменения, происходящие с липидами в процессах технологической переработки сырья и параметры, характеризующие их Монокристаллы InSb. Свойства, выращивание, применение
Монокристаллы InSb. Свойства, выращивание, применение Химические элементы. Строение вещества. Химическая связь
Химические элементы. Строение вещества. Химическая связь Мінерали та гірські породи
Мінерали та гірські породи Сульфиды. Лекция 6
Сульфиды. Лекция 6 Тепловой эффект химической реакции. 11 класс
Тепловой эффект химической реакции. 11 класс Новое направление в бизнесе компании – катализаторы синтеза метанола
Новое направление в бизнесе компании – катализаторы синтеза метанола Состав, строение и свойства сырья для производства строительных материалов
Состав, строение и свойства сырья для производства строительных материалов Жесткость воды
Жесткость воды Алюминий и его соединения
Алюминий и его соединения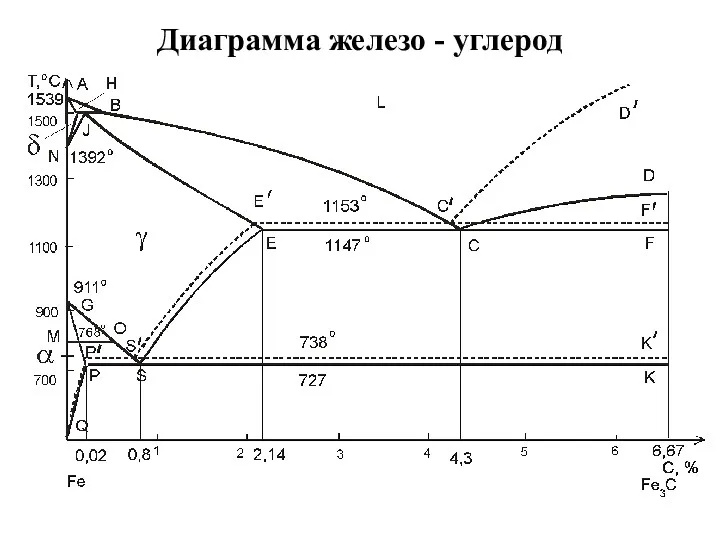 Диаграмма железо - углерод
Диаграмма железо - углерод Предмет физической и коллоидной химии. Термодинамика
Предмет физической и коллоидной химии. Термодинамика Одноосновные карбоновые кислоты. Строение, физические свойства, номенклатура
Одноосновные карбоновые кислоты. Строение, физические свойства, номенклатура Общая характеристика липидов. Строение. Классификация. Функции. Переваривание и всасывание липидов в ЖКТ Роль желчи
Общая характеристика липидов. Строение. Классификация. Функции. Переваривание и всасывание липидов в ЖКТ Роль желчи Средние породы. Типичный андезитовый вулкан
Средние породы. Типичный андезитовый вулкан Хром. Определение химического элемента “хром”
Хром. Определение химического элемента “хром” Хімія в побуті
Хімія в побуті Аминокислоты – структурные единицы белков
Аминокислоты – структурные единицы белков Күкірт оксидтері
Күкірт оксидтері Топливо. Виды топлива. Химический состав топлива. Основные характеристики топлива. Марки топлива
Топливо. Виды топлива. Химический состав топлива. Основные характеристики топлива. Марки топлива Биохимия
Биохимия Бензол. Чикишев С. (2)
Бензол. Чикишев С. (2) Матеріальний баланс процесу горіння
Матеріальний баланс процесу горіння Кинетика. Базовые понятия
Кинетика. Базовые понятия Гигиена особенности при использовании средств бытовой химии и полимеров
Гигиена особенности при использовании средств бытовой химии и полимеров