Содержание
- 2. Химия – наука о превращениях веществ, связанных с изменением электронного окружения атомных ядер
- 3. Д.И.Менделеев*: "Ближайший предмет химии составляет изучениt однородных веществ, из сложения которых составлены все тела мира, превращений
- 4. Вещество – вид материи, которая обладает массой покоя. Состоит из элементарных частиц: электронов, протонов, нейтронов, мезонов
- 5. Тело и вещество. Что мы сажаем, Сажая Леса? Легкие крылья — Лететь в небеса. Стол, за
- 6. Простые вещества Образованы атомами одного химического элемента и потому являются формой его существования в свободном состоянии,
- 7. Сложные вещества Образованы разными элементами и могут иметь состав постоянный (стехиометрические соединения или дальтониды) или меняющийся
- 8. Смеси веществ Смеси – системы, состоящие из двух или более веществ, свойства которых сохраняются, а сами
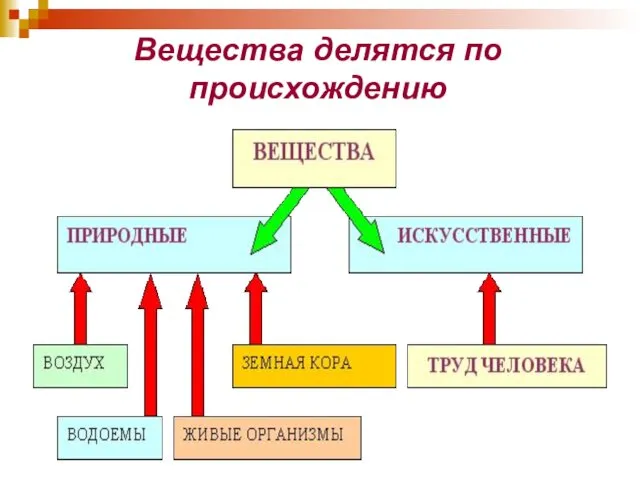
- 9. Вещества делятся по происхождению
- 10. Химические явления Явления, в резуль-тате которых образуются новые вещества, облада-ющие новыми хими-ческими свойства-ми, например:из углекислого газа
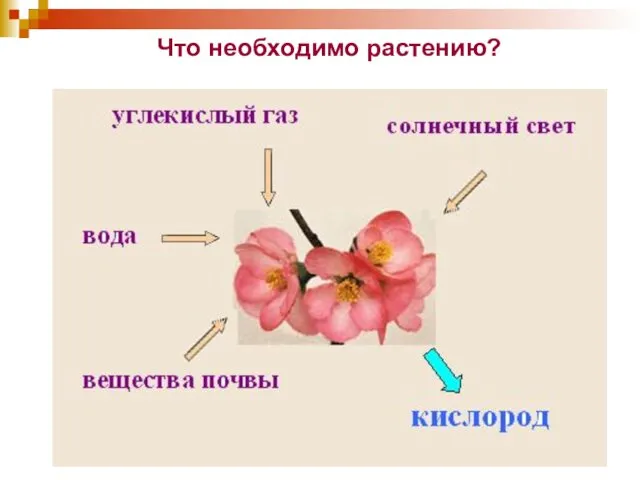
- 11. Что необходимо растению?
- 12. Физические явления Явления, при кото-рых изменяются агрегатное состояние, форма тела, например: замерзание воды (иней) или кипячение
- 13. Уравнение химической реакции Уравнение – условная запись химического процесса, в которой используются химические символы, математические знаки
- 14. Атом (от греч. atomos – неделимый), наименьшая частица химического элемента, носитель его свойств. Элементы химические- совокупности
- 15. Молекула (новолат. molecula, уменьшит. от лат. moles – масса), микрочастица, образованная из двух или большего числа
- 16. Ионы (от греч. ion – идущий), одноатомные или многоатомные частицы, несущие электрический заряд. Положительные ионы называют
- 17. Валентность (от лат. valentia – сила),способность атома присоединять или замещать определенное число других атомов или атомных
- 18. Нанотехнология перед вами – DVD CD DVD
- 20. Скачать презентацию















 Атомно-кристаллическое строение материалов
Атомно-кристаллическое строение материалов Основания. Классификация оснований
Основания. Классификация оснований Карбонові кислоти
Карбонові кислоти Химический состав красителей и препаратов для завивки. Лекция 8. Индустрия красоты
Химический состав красителей и препаратов для завивки. Лекция 8. Индустрия красоты Породообразующие минералы
Породообразующие минералы Классификация химических реакций
Классификация химических реакций Адсорбция. Физическая и химическая адсорбция
Адсорбция. Физическая и химическая адсорбция Природні гази
Природні гази Произведение растворимости. Строение комплексных соединений
Произведение растворимости. Строение комплексных соединений Пространственное строение молекул органических соединений
Пространственное строение молекул органических соединений Углеводы (особенности строения, реакционной способности и методы синтеза альдегидо- и кетоспиртов)
Углеводы (особенности строения, реакционной способности и методы синтеза альдегидо- и кетоспиртов) Фосфор и его соединения
Фосфор и его соединения Зелёная химия
Зелёная химия Алкены. Этилен
Алкены. Этилен Переработка угля
Переработка угля Возобновляемое сырье органической химии
Возобновляемое сырье органической химии Органічні сполуки: ліпіди
Органічні сполуки: ліпіди Штучні і синтетичні волокна
Штучні і синтетичні волокна Растворы. Способы выражения концентрации растворенного вещества
Растворы. Способы выражения концентрации растворенного вещества Обобщение по типам химических реакций
Обобщение по типам химических реакций Щелочные металлы
Щелочные металлы Сульфиды. Занятие 7
Сульфиды. Занятие 7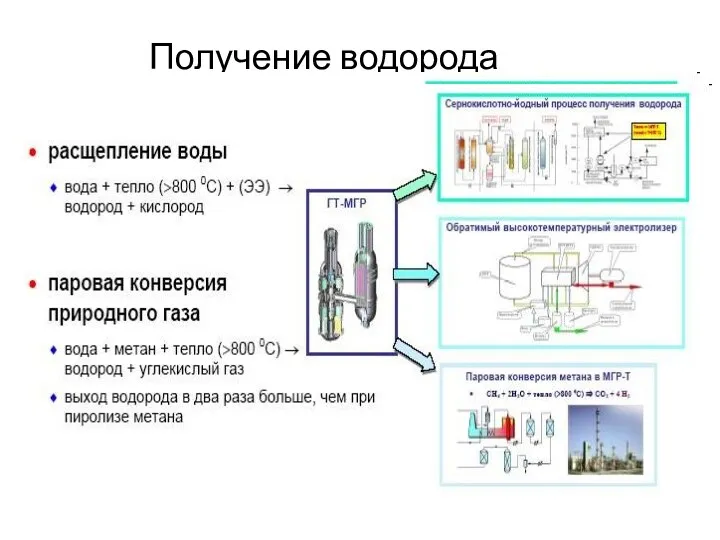 Получение водорода
Получение водорода Сырьевая база промышленной органической химии. Области применения органических веществ. (Лекция 1)
Сырьевая база промышленной органической химии. Области применения органических веществ. (Лекция 1) Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Лекция 6. Алициклические углеводороды (циклоалканы, нафтены)
Лекция 6. Алициклические углеводороды (циклоалканы, нафтены) Производство низших олефинов
Производство низших олефинов Виды топлива
Виды топлива