Содержание
- 2. УМК «ХИМИЯ» Тема лекции: Строение атома Лектор – Иванов М.Г. Разработчик – Данилова Д.А.
- 3. Цель лекции: изложение строения атомов в рамках современной химической теории Компетенции, формируемые у студента: Умения: прогнозировать
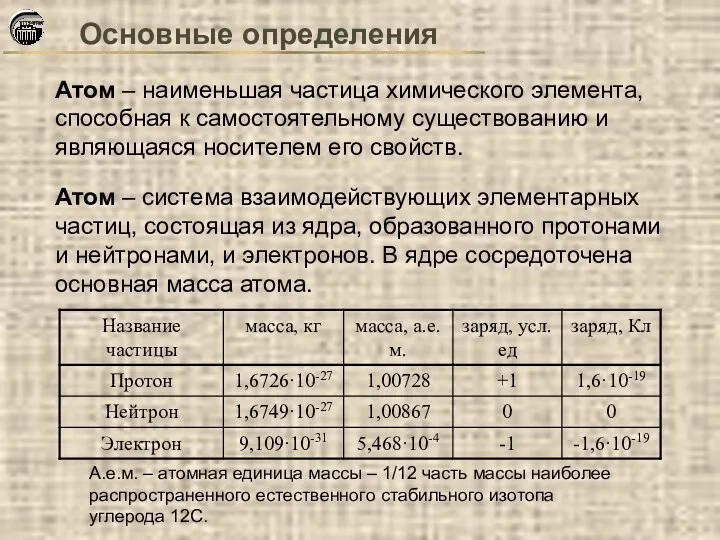
- 4. Основные определения Атом – наименьшая частица химического элемента, способная к самостоятельному существованию и являющаяся носителем его
- 5. Основные определения Химический элемент – совокупность атомов с одинаковым зарядом ядра. А – массовое число Z
- 6. Модель атома Бора Постулаты Бора Электрон может вращаться вокруг ядра не по любым орбитам, а только
- 7. Модель атома Бора Достоинства модели Бор вычислил уровни энергии электрона в атоме водорода. En = -13,6/n2,
- 8. Модель атома Бора Недостатки модели Модель не может объяснить, почему происходит квантование и почему электрон на
- 9. Квантово-механическая модель атома Энергия в микромире поглощается или излучается дискретно в виде квантов (М. Планк) Все
- 10. Квантово-механическая модель атома Уравнение Шредингера: Ψ – волновая функция (пси-функция), m – масса частицы, U –
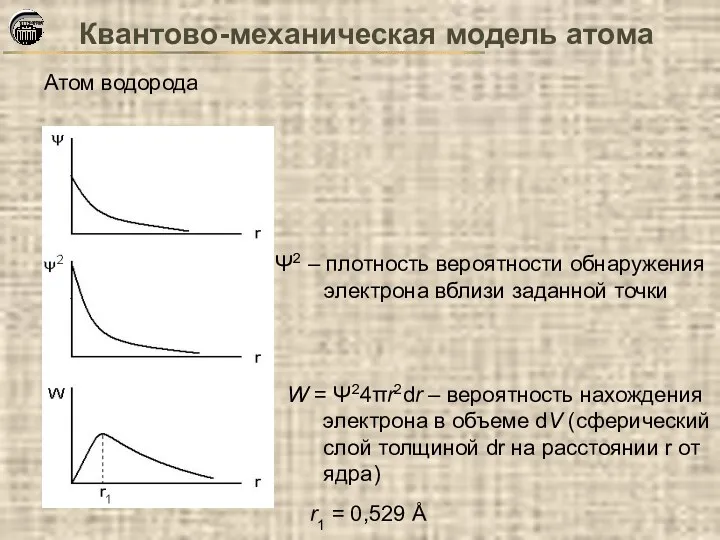
- 11. Квантово-механическая модель атома Атом водорода Ψ2 – плотность вероятности обнаружения электрона вблизи заданной точки W =
- 12. Квантово-механическая модель атома Выводы из решения уравнения Шредингера Из решения уравнения Шредингера автоматически вытекает существование дискретных
- 13. Квантовые числа n – главное квантовое число l – орбитальное квантовое число ml – магнитное квантовое
- 14. Квантовые числа Принимает целочисленные значения: n = 1, 2, 3… . Характеризует основной уровень энергии электрона
- 15. Квантовые числа Орбитальное квантовое число принимеат целочисленные значения от 0 до (n – 1): l =
- 16. Квантовые числа Орбитальное квантовое число Определяет форму атомной орбитали l=0 s-орбиталь l=1 р-орбиталь l=2 d-орбиталь
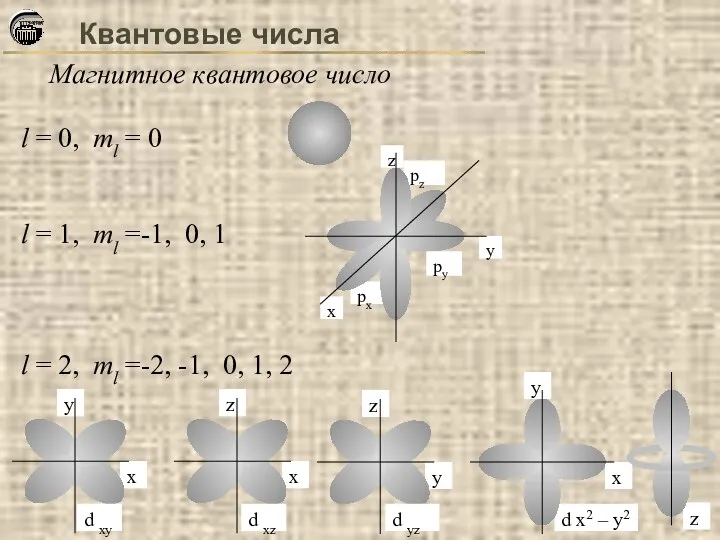
- 17. Квантовые числа Магнитное квантовое число Характеризует результат взаимодействия магнитного поля движущегося электрона с наложенным внешним магнитным
- 18. Квантовые числа Магнитное квантовое число l = 0, ml = 0 l = 1, ml =-1,
- 19. Квантовые числа Спиновое квантовое число Характеризует собственный момент количества движения электрона ms = +1/2 Если направление
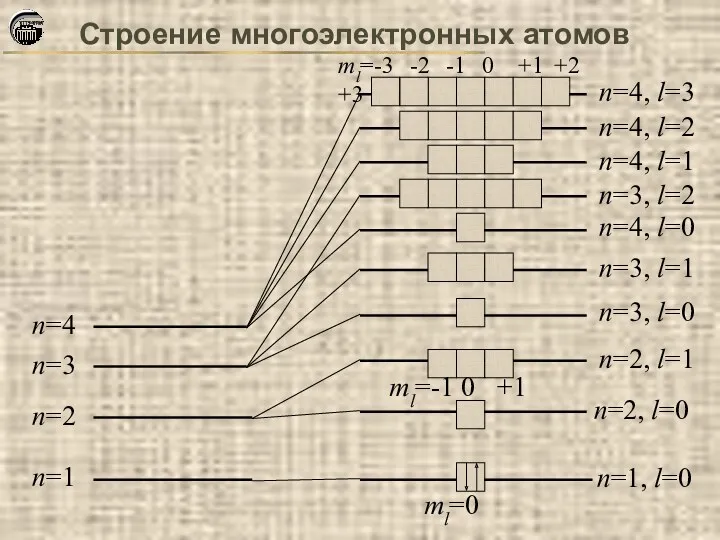
- 20. Строение многоэлектронных атомов 1. Принцип минимума энергии Правило Клечковского: Увеличение энергии и соответственно заполнение орбиталей происходит
- 21. Строение многоэлектронных атомов 1. Правило Гунда Электроны в пределах одного подуровня распределяются таким образом, чтобы их
- 22. Строение многоэлектронных атомов n=1 n=2 n=3 n=4 n=1, l=0 n=2, l=0 n=3, l=0 n=4, l=0 n=2,
- 23. Строение многоэлектронных атомов I период H 1s1 He 1s2 s-элементы II период Li 1s22s1 Be 1s22s2
- 24. III период Na 1s22s22p63s1 Mg 1s22s22p63s2 Al 1s22s22p63s23p1 ……………………… Ar 1s22s22p63s23p6 Строение многоэлектронных атомов s-элементы p-элементы
- 25. IV период K …..4s1 Ca …..4s2 Sc ….3s23p63d14s2 ………………………. Cr ….3s23p63d54s1 Mn ….3s23p63d54s2 ………………………. Cu ….3s23p63d104s1
- 26. Строение многоэлектронных атомов VI период Cs ….4d105s25p66s1 Ba ….4d105s25p66s2 La ….4d105s25p65d16s2 Сe ….4d104f25s25p65d06s2 Pr ….4d104f35s25p65d06s2 ………………………………
- 27. Строение многоэлектронных атомов Каждый новый период начинается с заполнения нового слоя. Каждый период начинается с s-элементов,
- 28. Строение многоэлектронных атомов У s- и p- элементов заполняется внешний слой. Число электронов на внешнем слое
- 29. Изменение свойств элементов в свете Периодического закона Современная формулировка периодического закона: Свойства элементов, а так же
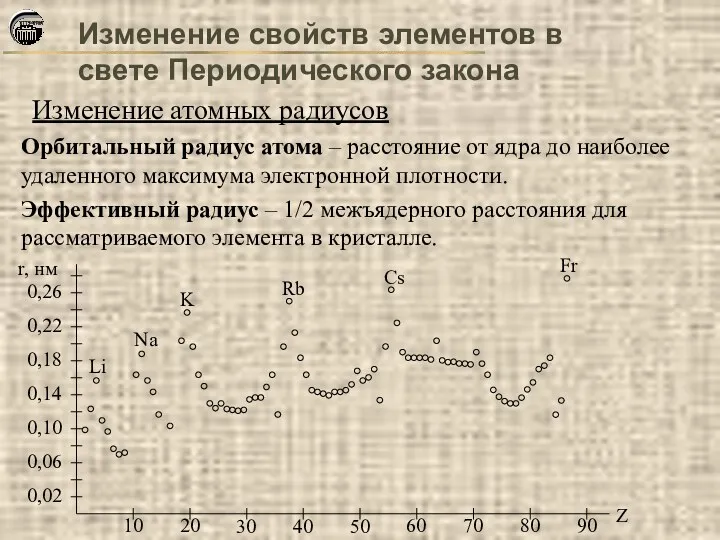
- 30. Изменение атомных радиусов Изменение свойств элементов в свете Периодического закона Орбитальный радиус атома – расстояние от
- 31. Изменение свойств элементов в свете Периодического закона Изменение энергии ионизации Энергия ионизации (I) – это та
- 32. Изменение свойств элементов в свете Периодического закона Изменение энергии сродства к электрону Энергия сродства к электрону
- 33. Изменение свойств элементов в свете Периодического закона Изменение электроотрицательности Электроотрицательность позволяет оценить способность атома данного элемента
- 34. Изменение свойств элементов в свете Периодического закона Изменение химических свойств F 2s22p5 Cl 2s22p63s23p5 Br 3s23p63d104s24p5
- 35. Изменение свойств элементов в свете Периодического закона Изменение химических свойств Нарастание неметаллических свойств
- 36. Литература Глинка Н.Л. Общая химия: учеб. пособие для вузов / Н. Л. Глинка ; под ред.
- 38. Скачать презентацию






























 Начало нанотехнологической эры. Фуллерены
Начало нанотехнологической эры. Фуллерены Закон триад. Открытие периодического закона
Закон триад. Открытие периодического закона Металлическая связь. Агрегатные состояния вещества
Металлическая связь. Агрегатные состояния вещества Основания. Получение и химические свойства
Основания. Получение и химические свойства Азот. Соединения азота
Азот. Соединения азота Окисно-відновні реакції у природі і промисловості
Окисно-відновні реакції у природі і промисловості Обмен липидов
Обмен липидов Типы химических соединений, номенклатура, свойства
Типы химических соединений, номенклатура, свойства Застосування алканів
Застосування алканів ЕГЭ 2017. Подготовка к вопросу № 26
ЕГЭ 2017. Подготовка к вопросу № 26 Структурная химия и кристаллохимия
Структурная химия и кристаллохимия Жиры и мыло
Жиры и мыло Ароматты комирсутектер Бензол
Ароматты комирсутектер Бензол Основания и кислоты. Химические и физические свойства
Основания и кислоты. Химические и физические свойства Гетероциклические соединения. Шестичленные гетероциклы с одним гетероатомом
Гетероциклические соединения. Шестичленные гетероциклы с одним гетероатомом Превращения веществ. Роль химии в жизни человека
Превращения веществ. Роль химии в жизни человека Минеральные вещества
Минеральные вещества Химия и производство
Химия и производство Theories of acids and bases. Ionic equilibria in electrolyte solutions. Buffer solutions (topic 3.4)
Theories of acids and bases. Ionic equilibria in electrolyte solutions. Buffer solutions (topic 3.4) Материаловедение. Атомно-кристаллическое строение металлов и сплавов. (Тема 3)
Материаловедение. Атомно-кристаллическое строение металлов и сплавов. (Тема 3) Синтетические топлива
Синтетические топлива Классификация химических реакций, протекающих с изменением состава веществ
Классификация химических реакций, протекающих с изменением состава веществ Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей
Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей Энергетика химических процессов
Энергетика химических процессов Какими свойствами обладает воздух. Исследовательская работа
Какими свойствами обладает воздух. Исследовательская работа Хімічні властивості карбонових кислот
Хімічні властивості карбонових кислот Полівінілхлорид
Полівінілхлорид Реакции окисления и восстановления органических соединений
Реакции окисления и восстановления органических соединений