Содержание
- 2. Положение в периодической системе
- 3. Строение атома
- 4. История открытия Выделение горючего газа при взаимодействии кислот и металлов наблюдали в заре становления химии как
- 5. Нахождение в природе составляет 0,88% от массы всех трёх оболочек земной коры (атмосферы, гидросферы и литосферы),
- 6. Физические свойства Водород — самый лёгкий газ, он легче воздуха в 14,5 раз. Поэтому, например, мыльные
- 7. Получение Конверсия с водяным паром при 1000 °C: CH4+H2O = CO+3H2 Пропускание паров воды над раскалённым
- 8. Химические свойства 1)взаимодействие с металлами: Ca+H2=CaH2 CaH2+2H2O=Ca(OH)2+2H2 2)взаимодействие с неметаллами: H2+F2=2HF 2H2+C=CH4 2H2+O2=2H2O Восстановление металлов из
- 9. Применение Много водорода уходит на производство аммиака (NH3). Далее из аммиака получают азотные удобрения, синтетические волокна
- 11. Скачать презентацию
Слайд 2
Положение в периодической системе
Положение в периодической системе
Слайд 3
Строение атома
Строение атома
Слайд 4
История открытия
Выделение горючего газа при взаимодействии кислот и металлов наблюдали в заре
История открытия
Выделение горючего газа при взаимодействии кислот и металлов наблюдали в заре
становления химии как науки. Прямо указывал на выделение его и МXVI и XVII веках на Михаил Васильевич Ломоносов, но уже определённо сознавая, что это не флогистон. Английский физик и химик Генри Кавендиш в 1766 году исследовал этот газ и назвал его «горючим воздухом». При сжигании «горючий воздух» давал воду, но приверженность Кавендиша теории флогистона помешала ему сделать правильные выводы. Французский химик Антуан Лавуазье совместно с инженером Жаном Мёнье, используя специальные газометры, в 1783 г. осуществил синтез воды, а затем и её анализ, разложив водяной пар раскалённым железом. Так он установил, что «горючий воздух» входит в состав воды и может быть из неё получен.
Слайд 5
Нахождение в природе
составляет 0,88% от массы всех трёх оболочек земной коры
Нахождение в природе
составляет 0,88% от массы всех трёх оболочек земной коры
(атмосферы, гидросферы и литосферы), что при пересчёте на атомные проценты даёт цифру 15,5. Основное количество этого элемента находится в связанном состоянии. Так, вода содержит его около 11 вес. %, глина - около 1,5% и т. д. В виде соединений с углеродом водород входит в состав нефти, горючих природных газов и всех организмов.
Свободный водород состоит из молекул Н2. Он часто содержится в вулканических газах. Частично он образуется также при разложении некоторых органических остатков. Небольшие его количества выделяются зелёными растениями. Атмосфера содержит около 10-5 объёмн. % водорода.
В природе водород образуется главным образом при разложении органических веществ, например целлюлозы или белков, некоторыми видами бактерий. Большие его количества освобождаются при коксовании угля; поэтому светильный и коксовый газы в среднем состоят на 50 объёмн. % из свободного водорода. В последнее время коксовый газ стали технически перерабатывать на водород, сжижая его и выделяя водород как трудно конденсирующийся газ.
Свободный водород состоит из молекул Н2. Он часто содержится в вулканических газах. Частично он образуется также при разложении некоторых органических остатков. Небольшие его количества выделяются зелёными растениями. Атмосфера содержит около 10-5 объёмн. % водорода.
В природе водород образуется главным образом при разложении органических веществ, например целлюлозы или белков, некоторыми видами бактерий. Большие его количества освобождаются при коксовании угля; поэтому светильный и коксовый газы в среднем состоят на 50 объёмн. % из свободного водорода. В последнее время коксовый газ стали технически перерабатывать на водород, сжижая его и выделяя водород как трудно конденсирующийся газ.
Слайд 6
Физические свойства
Водород — самый лёгкий газ, он легче воздуха в 14,5 раз. Поэтому,
Физические свойства
Водород — самый лёгкий газ, он легче воздуха в 14,5 раз. Поэтому,
например, мыльные пузыри, наполненные водородом, на воздухе стремятся вверх. Чем меньше масса молекул, тем выше их скорость при одной и той же температуре. Как самые лёгкие, молекулы водорода движутся быстрее молекул любого другого газа и тем самым быстрее могут передавать теплоту от одного тела к другому. Отсюда следует, что водород обладает самой высокой теплопроводностью среди газообразных веществ. Его теплопроводность примерно в семь раз выше теплопроводности воздуха.
Молекула водорода двухатомна — Н2. При нормальных условиях — это газ без цвета, запаха и вкуса. Плотность 0,08987 г/л (н. у.), температура кипения −252,76 °C, удельная теплота сгорания 120,9·106 Дж/кг, малорастворим в воде — 18,8 мл/л.
Водород хорошо растворим во многих металлах (Ni, Pt, Pd и др.), особенно в палладии (850 объёмов H2 на 1 объём Pd). С растворимостью водорода в металлах связана его способность диффундировать через них; диффузия через углеродистый сплав (например, сталь) иногда сопровождается разрушением сплава вследствие взаимодействия водорода с углеродом (так называемая декарбонизация). Практически не растворим в серебре.
Молекула водорода двухатомна — Н2. При нормальных условиях — это газ без цвета, запаха и вкуса. Плотность 0,08987 г/л (н. у.), температура кипения −252,76 °C, удельная теплота сгорания 120,9·106 Дж/кг, малорастворим в воде — 18,8 мл/л.
Водород хорошо растворим во многих металлах (Ni, Pt, Pd и др.), особенно в палладии (850 объёмов H2 на 1 объём Pd). С растворимостью водорода в металлах связана его способность диффундировать через них; диффузия через углеродистый сплав (например, сталь) иногда сопровождается разрушением сплава вследствие взаимодействия водорода с углеродом (так называемая декарбонизация). Практически не растворим в серебре.
Слайд 7
Получение
Конверсия с водяным паром при 1000 °C:
CH4+H2O = CO+3H2
Пропускание паров воды над
Получение
Конверсия с водяным паром при 1000 °C:
CH4+H2O = CO+3H2
Пропускание паров воды над
раскалённым коксом при температуре около 1000 °C:
H2O+C=CO+H2
Электролиз водных растворов солей:
2NaCl+2H2O=2NaOH+Cl2+H2
Каталитическое окисление кислородом:
2CH4+O2=2CO+4H2
Взаимодействие кальция с водой:
Ca+2H2O = Ca (OH)2+H2
Гидролиз гидридов:
NaH+H2O=NaOH+H2
H2O+C=CO+H2
Электролиз водных растворов солей:
2NaCl+2H2O=2NaOH+Cl2+H2
Каталитическое окисление кислородом:
2CH4+O2=2CO+4H2
Взаимодействие кальция с водой:
Ca+2H2O = Ca (OH)2+H2
Гидролиз гидридов:
NaH+H2O=NaOH+H2
Слайд 8
Химические свойства
1)взаимодействие с металлами:
Ca+H2=CaH2
CaH2+2H2O=Ca(OH)2+2H2
2)взаимодействие с неметаллами:
H2+F2=2HF
2H2+C=CH4
2H2+O2=2H2O
Восстановление металлов из оксида:
Fe2O3+3H2=2Fe+3H2O
Химические свойства
1)взаимодействие с металлами:
Ca+H2=CaH2
CaH2+2H2O=Ca(OH)2+2H2
2)взаимодействие с неметаллами:
H2+F2=2HF
2H2+C=CH4
2H2+O2=2H2O
Восстановление металлов из оксида:
Fe2O3+3H2=2Fe+3H2O
Слайд 9
Применение
Много водорода уходит на производство аммиака (NH3). Далее из аммиака получают
Применение
Много водорода уходит на производство аммиака (NH3). Далее из аммиака получают
азотные удобрения, синтетические волокна и пластмассы, лекарства.
Из водорода и хлора производят хлороводород (HCl) и соляную кислоту (водный раствор HCl).
Водород используют при производстве различных органических веществ. Например, для производства метилового спирта используют смесь водорода с угарным газом (CO) — синтез-газ.
В пищевой промышленности водород используют при производстве маргарина, в состав которого входят твердые растительные жиры. Чтобы их получить из жидких жиров, над ними пропускают водород.
С помощью водорода в промышленных масштабах восстанавливают некоторые металлы из их оксидов. Так получают, например, вольфрам.
Когда водород горит в кислороде, то поднимается температура около 3000 °C. При такой температуре можно плавить и сваривать тугоплавкие металлы. Таким образом водород используется при сварке.
Сжиженный водород применяют как ракетное горючее.
Раньше водородом заполняли воздушные шары и аэростаты, так как он намного легче воздуха.
Из водорода и хлора производят хлороводород (HCl) и соляную кислоту (водный раствор HCl).
Водород используют при производстве различных органических веществ. Например, для производства метилового спирта используют смесь водорода с угарным газом (CO) — синтез-газ.
В пищевой промышленности водород используют при производстве маргарина, в состав которого входят твердые растительные жиры. Чтобы их получить из жидких жиров, над ними пропускают водород.
С помощью водорода в промышленных масштабах восстанавливают некоторые металлы из их оксидов. Так получают, например, вольфрам.
Когда водород горит в кислороде, то поднимается температура около 3000 °C. При такой температуре можно плавить и сваривать тугоплавкие металлы. Таким образом водород используется при сварке.
Сжиженный водород применяют как ракетное горючее.
Раньше водородом заполняли воздушные шары и аэростаты, так как он намного легче воздуха.
Следующая -
Величины 1 класс







 Оттекті органикалық қосылыстар тақырыбын пәнаралық байланыс арқылы оқыту әдістемесі
Оттекті органикалық қосылыстар тақырыбын пәнаралық байланыс арқылы оқыту әдістемесі Отрицательное влияние азотных минеральных удобрений на почву
Отрицательное влияние азотных минеральных удобрений на почву Предмет органической химии. Основные положения теории химического строения органических соединений
Предмет органической химии. Основные положения теории химического строения органических соединений Бета-окисление жирных кислот
Бета-окисление жирных кислот Аммиак
Аммиак Представники d-елементів (перехідних елементів) періодичної системи елементів
Представники d-елементів (перехідних елементів) періодичної системи елементів Характеристика элементов VIII-В группы. Семейство железа
Характеристика элементов VIII-В группы. Семейство железа Химические реакции
Химические реакции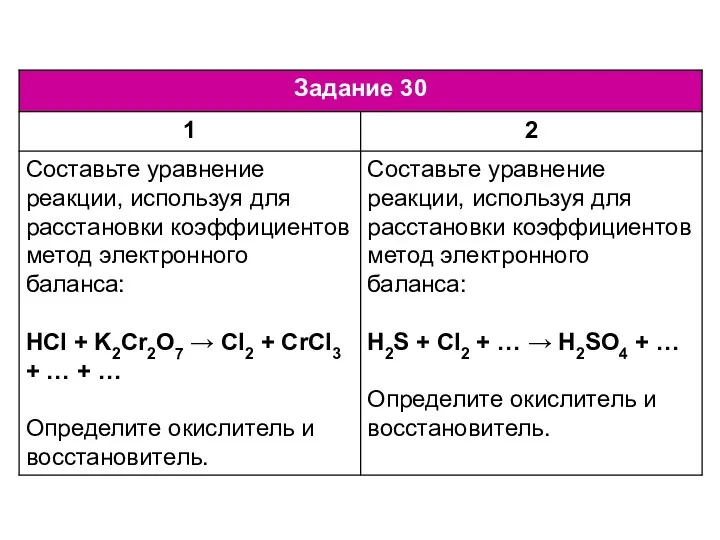 ЕГЭ по химии. Задание 30-34
ЕГЭ по химии. Задание 30-34 Железо, его физические и химические свойства. Урок химии в 9 классе
Железо, его физические и химические свойства. Урок химии в 9 классе Природный и искусственный камень
Природный и искусственный камень Использование потенциостата-гальваностата Elins p-20x в электрохимических исследованиях
Использование потенциостата-гальваностата Elins p-20x в электрохимических исследованиях Электролитическая диссоциация
Электролитическая диссоциация Пестициды. Применение пестицидов
Пестициды. Применение пестицидов Хлорид натрия (NaCI)
Хлорид натрия (NaCI) Молекулалық орбиталдың негіздері ТФП 315
Молекулалық орбиталдың негіздері ТФП 315 АТФ Аденозинтрифосфат
АТФ Аденозинтрифосфат Растворы
Растворы Фенолы. Классификация и изомерия
Фенолы. Классификация и изомерия Properties of Atoms and the Periodic Table
Properties of Atoms and the Periodic Table Кевлар. Структура кевлара
Кевлар. Структура кевлара XXI ғасыр көшбасшысы
XXI ғасыр көшбасшысы Первичная переработка нефти
Первичная переработка нефти 20230306_vodorod_ego_fizicheskie_svoystva
20230306_vodorod_ego_fizicheskie_svoystva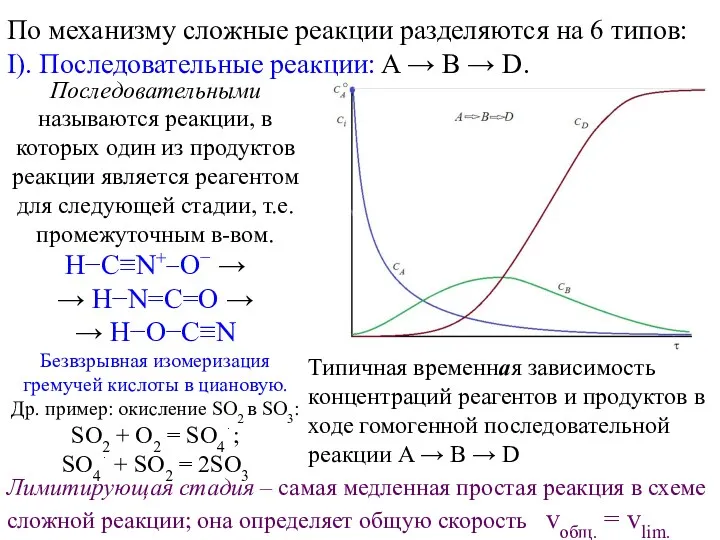 Сложные реакции по механизму
Сложные реакции по механизму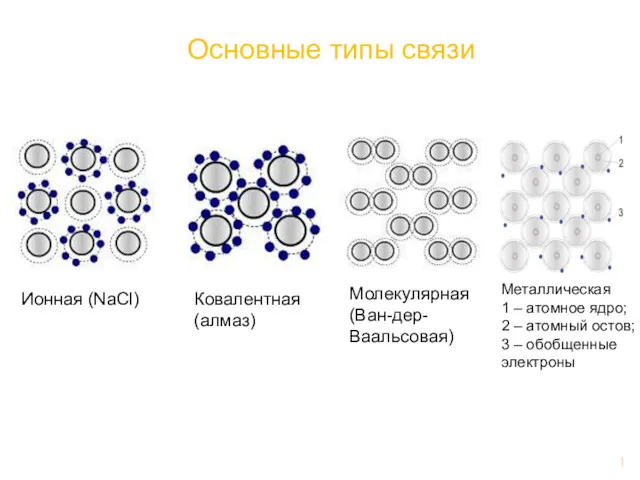 Основные типы связи
Основные типы связи Метал конструкциялық материалдар
Метал конструкциялық материалдар Химическая термодинамика
Химическая термодинамика