Содержание
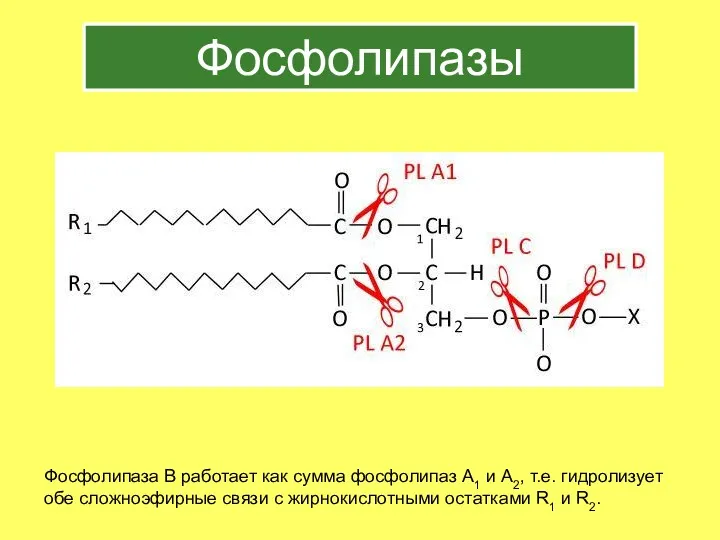
- 2. Фосфолипазы Фосфолипаза В работает как сумма фосфолипаз А1 и А2, т.е. гидролизует обе сложноэфирные связи с
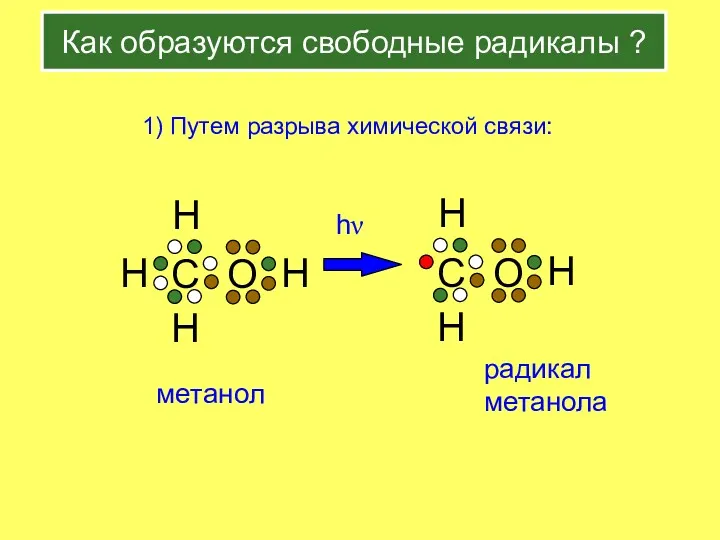
- 3. Как образуются свободные радикалы ? 1) Путем разрыва химической связи: hν
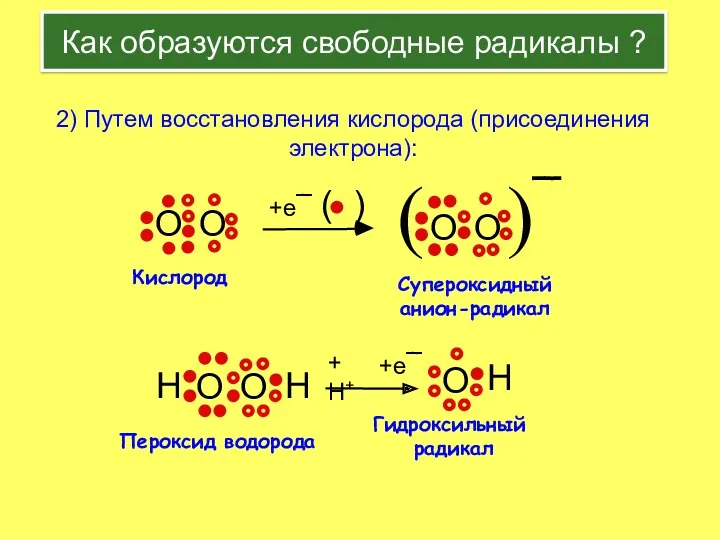
- 4. Кислород Супероксидный анион-радикал +e¯ ( ) Пероксид водорода Гидроксильный радикал + H+ +e¯ 2) Путем восстановления
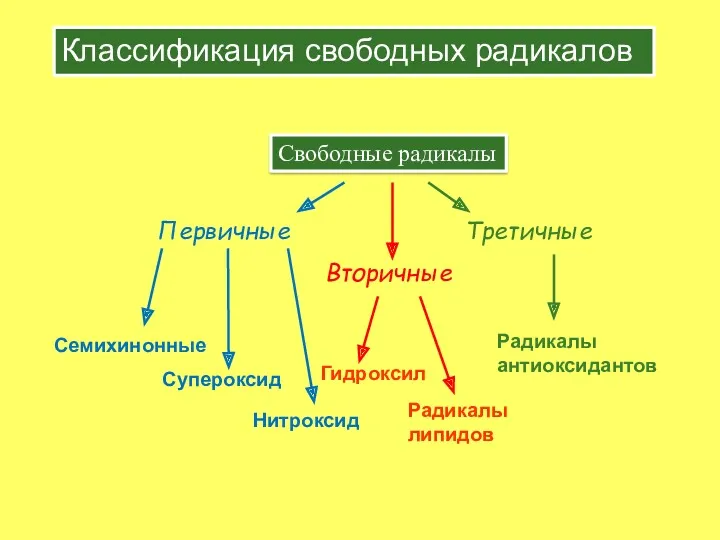
- 5. Классификация свободных радикалов Первичные Вторичные Третичные Супероксид Нитроксид Семихинонные Гидроксил Радикалы липидов Радикалы антиоксидантов Свободные радикалы
- 6. Активные формы кислорода (Reactive oxygen species, ROS)
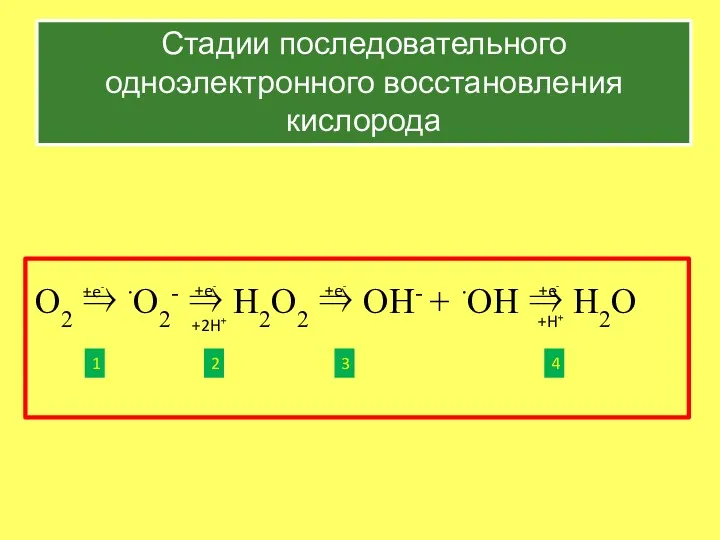
- 7. O2 ⇒ ∙O2- ⇒ H2O2 ⇒ OH- + ∙OH ⇒ H2O Стадии последовательного одноэлектронного восстановления кислорода
- 8. Какие частицы относят к активным формам кислорода? ●O2─ супероксидный радикал H2O2 пероксид водорода ●OH гидроксильный радикал
- 9. Метаболизм супероксидного радикала и пероксида водорода в водной среде NADPH – оксидаза: O2 + e¯ →
- 10. Супероксидный радикал
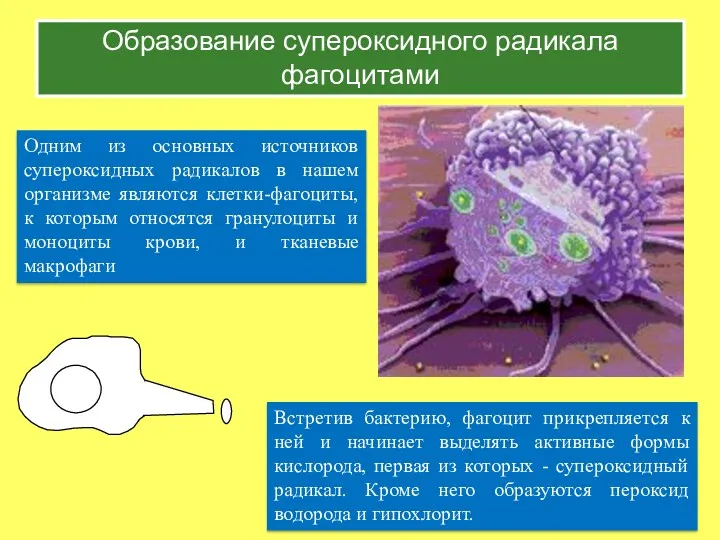
- 11. Образование супероксидного радикала фагоцитами Одним из основных источников супероксидных радикалов в нашем организме являются клетки-фагоциты, к
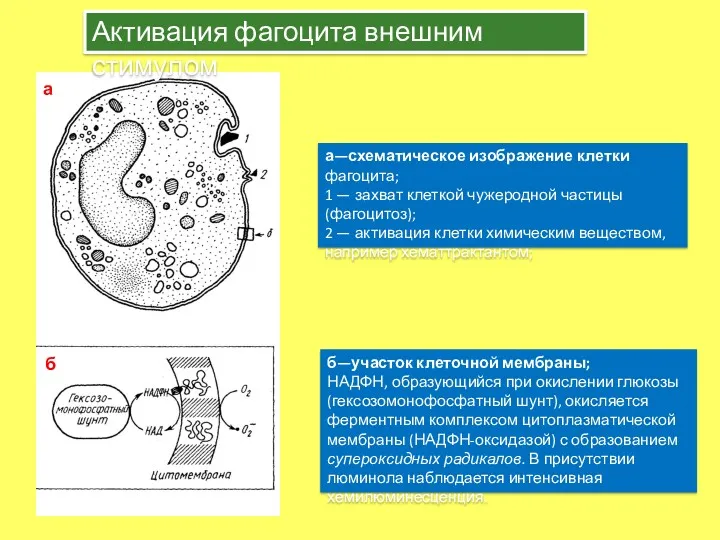
- 12. а—схематическое изображение клетки фагоцита; 1 — захват клеткой чужеродной частицы (фагоцитоз); 2 — активация клетки химическим
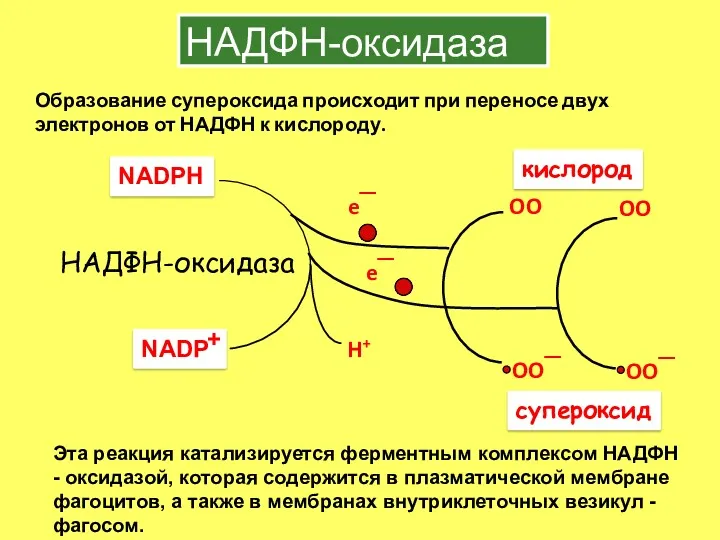
- 13. НАДФН-оксидаза Образование супероксида происходит при переносе двух электронов от НАДФН к кислороду. Эта реакция катализируется ферментным
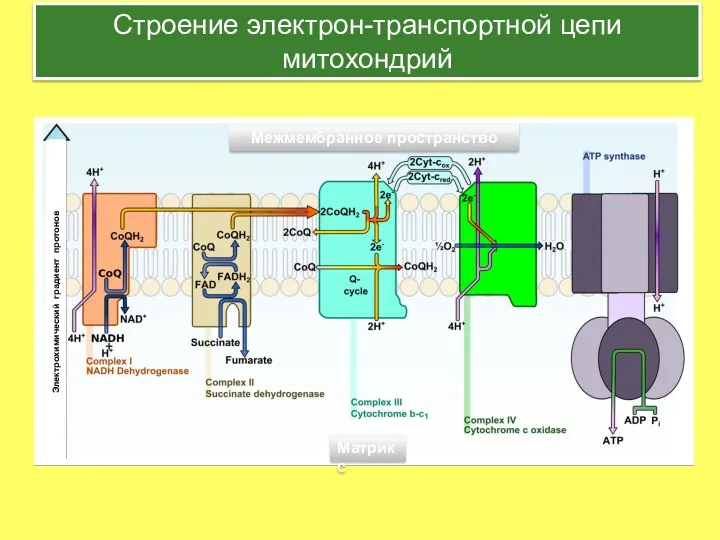
- 14. Строение электрон-транспортной цепи митохондрий Межмембранное пространство Матрикс Электрохимический градиент протонов
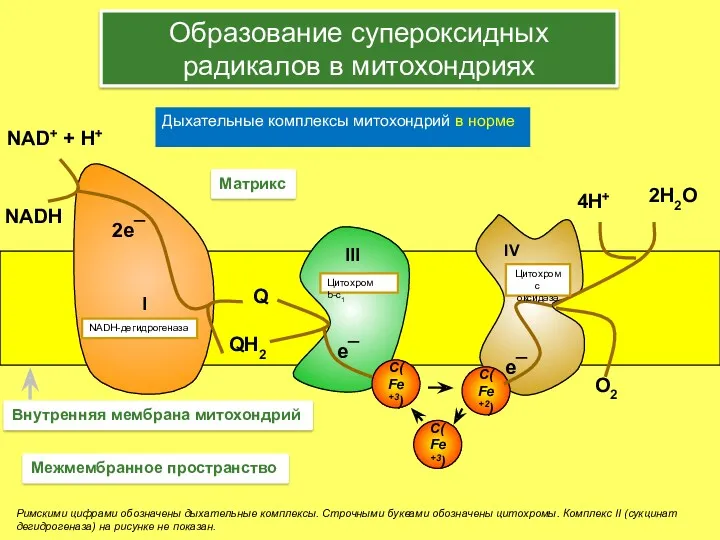
- 15. Дыхательные комплексы митохондрий в норме Римскими цифрами обозначены дыхательные комплексы. Строчными буквами обозначены цитохромы. Комплекс II
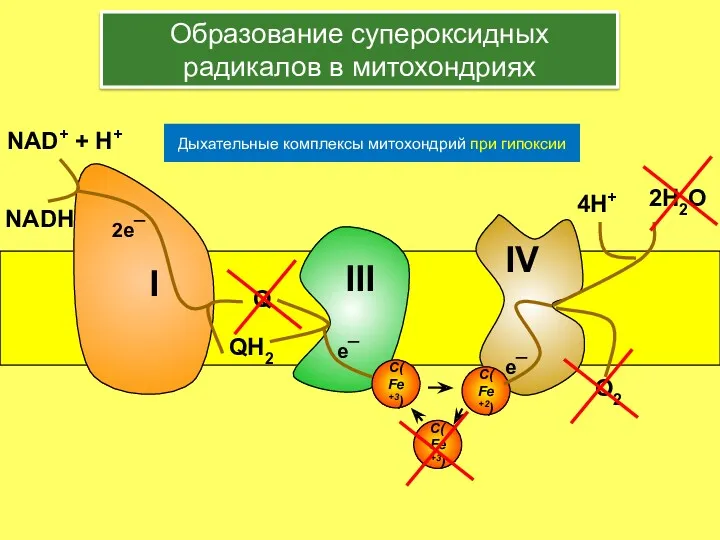
- 16. C(Fe+3) e¯ Образование супероксидных радикалов в митохондриях Дыхательные комплексы митохондрий при гипоксии
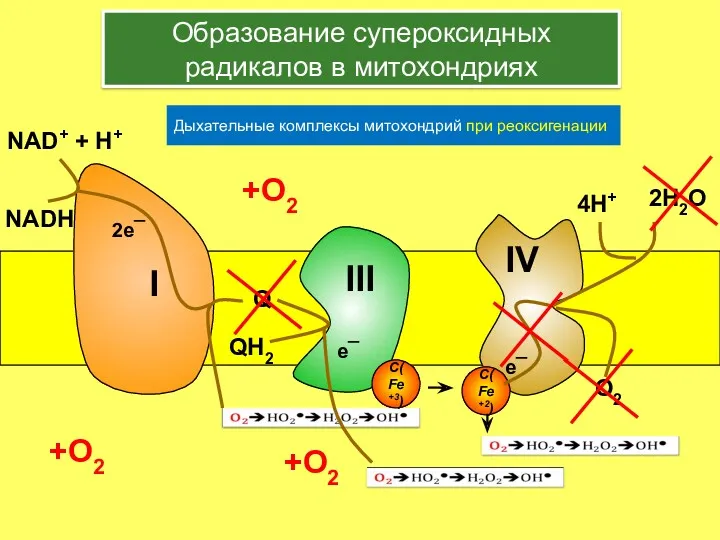
- 17. e¯ +О2 +О2 +О2 Образование супероксидных радикалов в митохондриях Дыхательные комплексы митохондрий при реоксигенации
- 18. Факторы, способствующие образованию супероксида митохондриями Гипоксия и последующая реоксигенация Отравление дыхательной цепи (например цианидом) Ингибирование цитохромоксидазы
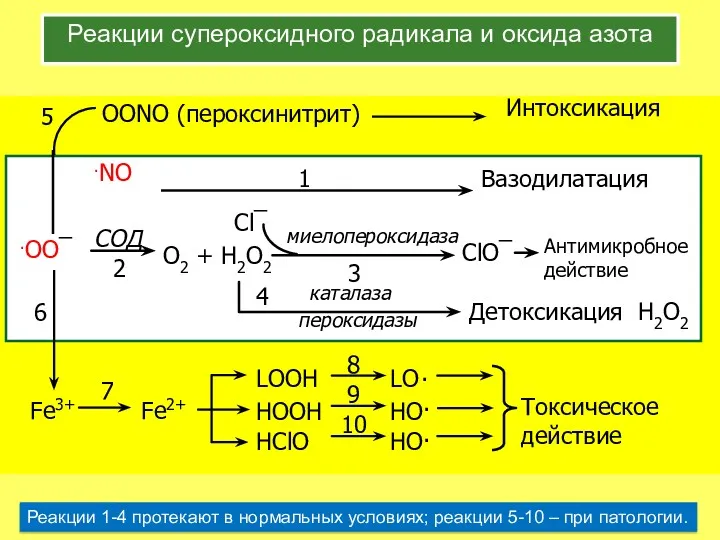
- 19. Реакции супероксидного радикала и оксида азота Реакции 1-4 протекают в нормальных условиях; реакции 5-10 – при
- 20. Синглетный кислород 1О2
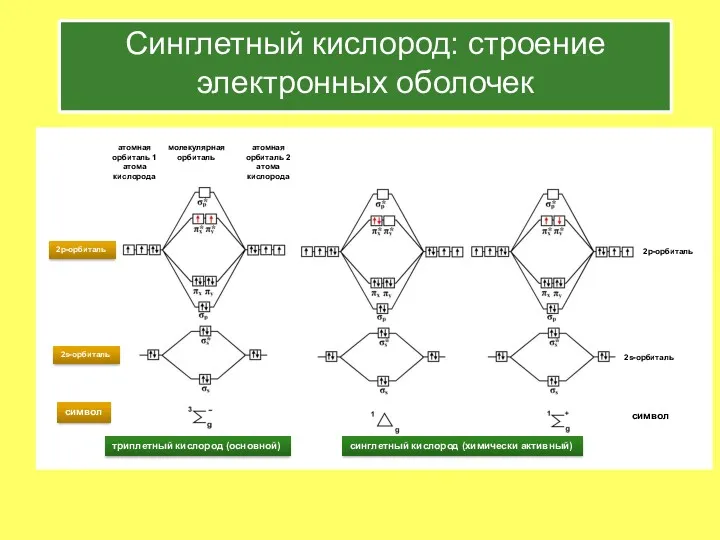
- 21. Синглетный кислород: строение электронных оболочек
- 22. Синглетный кислород: строение электронных оболочек 1О2 – является возбужденным состоянием обычного 3О2 Обычно образуется при фотохимических
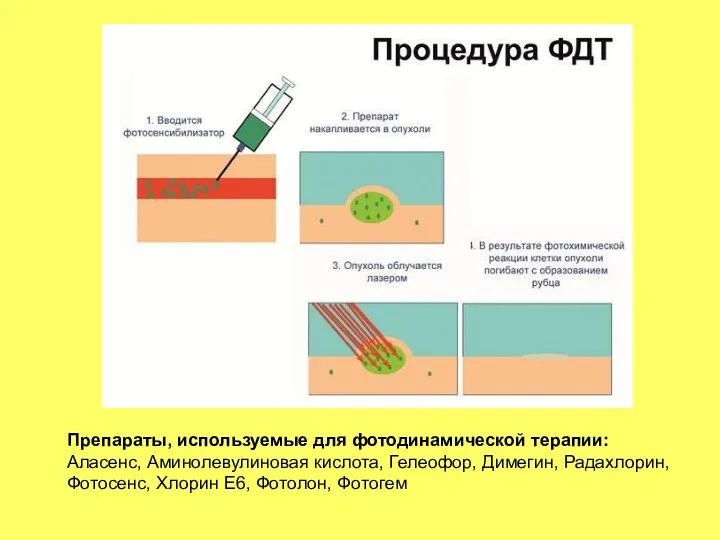
- 23. Препараты, используемые для фотодинамической терапии: Аласенс, Аминолевулиновая кислота, Гелеофор, Димегин, Радахлорин, Фотосенс, Хлорин Е6, Фотолон, Фотогем
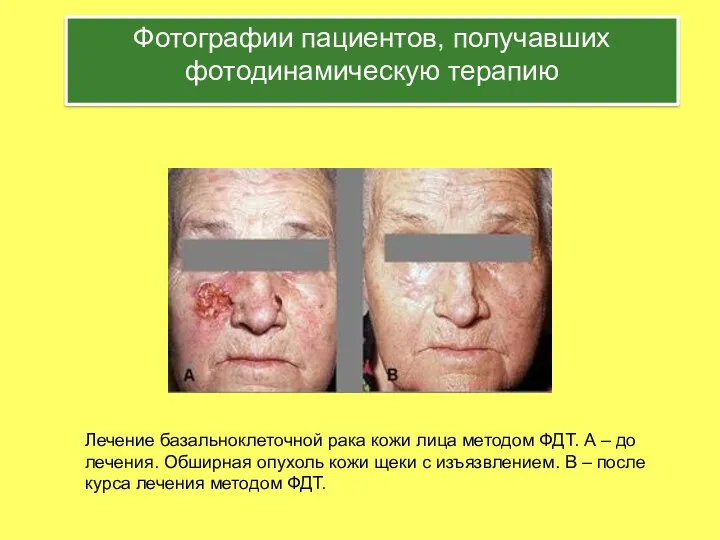
- 24. Фотографии пациентов, получавших фотодинамическую терапию Лечение базальноклеточной рака кожи лица методом ФДТ. А – до лечения.
- 25. Гипохлорит OCl-/HOCl
- 26. Гипохлорит Образуется миелопероксидазой нейтрофилов из H2O2 и Cl- H2O2 + Cl- ? OCl-/HOCl pK (OCl-/HOCl) =
- 27. Пероксинитрит ONOO-
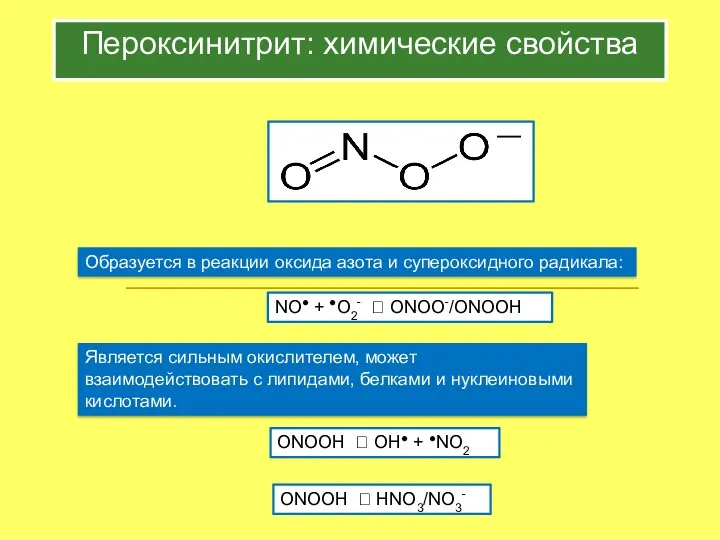
- 28. Пероксинитрит: химические свойства Образуется в реакции оксида азота и супероксидного радикала: NO● + ●O2- ? ONOO-/ONOOH
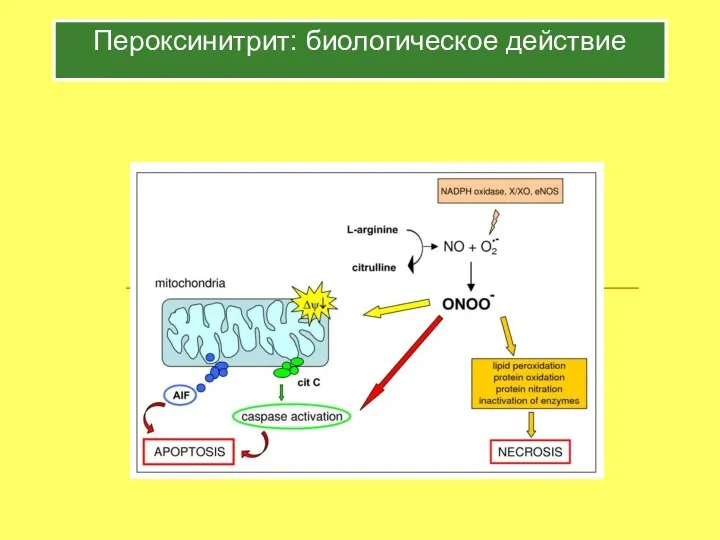
- 29. Пероксинитрит: биологическое действие
- 30. Оксид азота
- 31. участвует в процессе внутриклеточной передачи сигналов у млекопитающих, включая человека. Он играет ключевую роль в неврологии,
- 32. Химические свойства NO 1. Реакция с кислородом: 2NO∙ + O2 ⇒ 2NO2∙ 2. Реакция с супероксидным
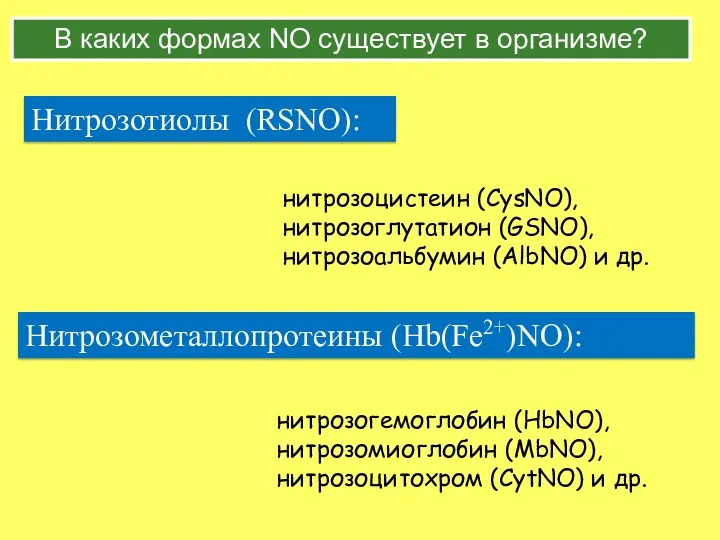
- 33. В каких формах NO существует в организме? Нитрозотиолы (RSNO): нитрозоцистеин (CysNO), нитрозоглутатион (GSNO), нитрозоальбумин (AlbNO) и
- 34. Оксид азота синтезируется в организме из L-аргинина ферментом NO-синтазой. В организме есть 3 типа NO-синтаз (NOS):
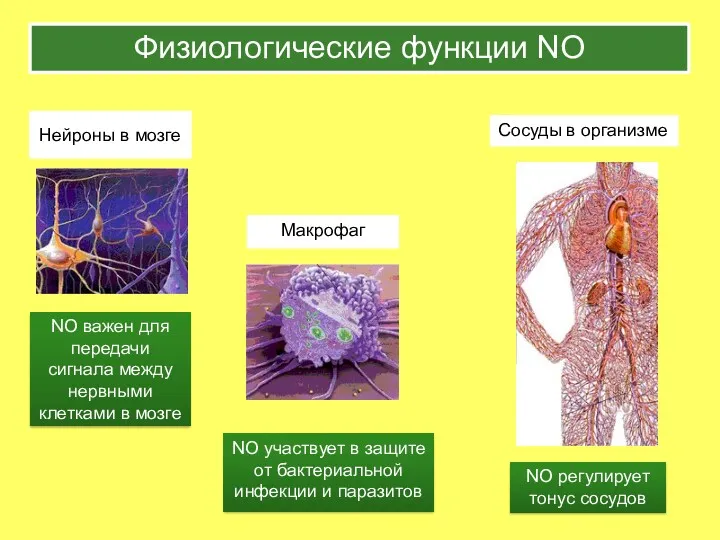
- 35. Физиологические функции NO NO важен для передачи сигнала между нервными клетками в мозге NO участвует в
- 36. тормозит агрегацию тромбоцитов и адгезию лейкоцитов к эндотелию. может вызывать повреждения при гипокии-реперфузии: при гипоксии синтезируется
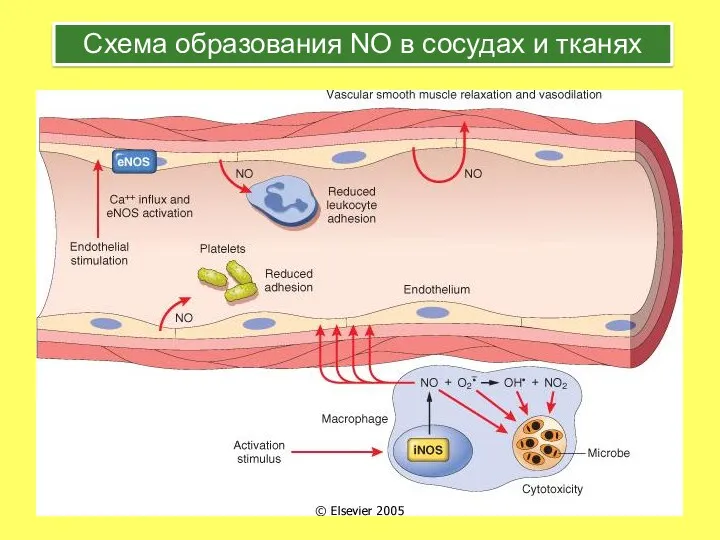
- 37. Схема образования NO в сосудах и тканях
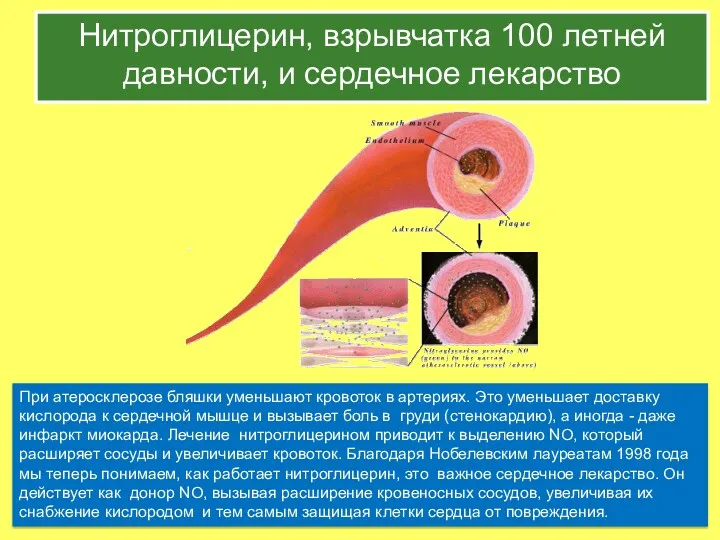
- 38. Нитроглицерин, взрывчатка 100 летней давности, и сердечное лекарство При атеросклерозе бляшки уменьшают кровоток в артериях. Это
- 39. Роберт Фуршготт, Родился в 1916. Работает в Отд. Фармакологии, SUNY Health Science Center New York Луис
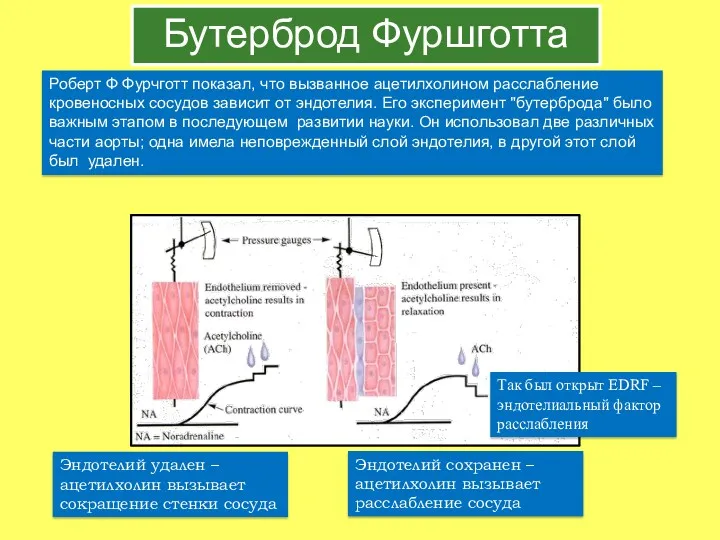
- 40. Бутерброд Фуршготта Роберт Ф Фурчготт показал, что вызванное ацетилхолином расслабление кровеносных сосудов зависит от эндотелия. Его
- 41. Спектральный анализ Иньярро Луи Иньярро сообщил, что EDRF расслабляет кровеносные сосуды. Он также идентифицировал EDRF как
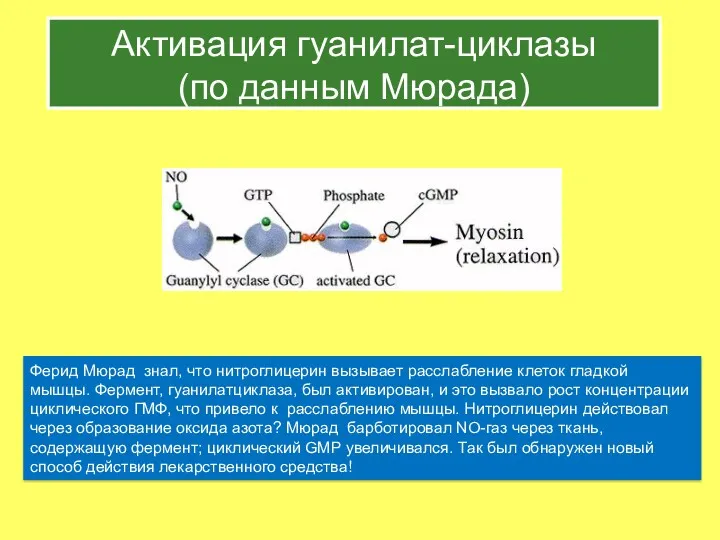
- 42. Активация гуанилат-циклазы (по данным Мюрада) Ферид Мюрад знал, что нитроглицерин вызывает расслабление клеток гладкой мышцы. Фермент,
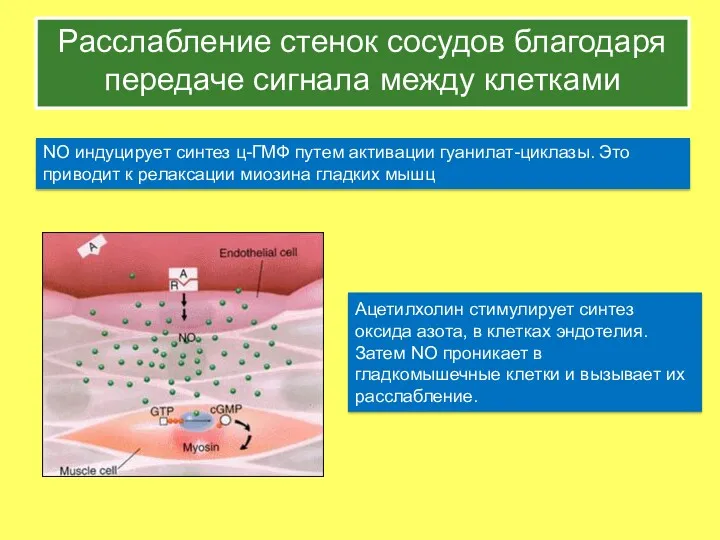
- 43. Расслабление стенок сосудов благодаря передаче сигнала между клетками NO индуцирует синтез ц-ГМФ путем активации гуанилат-циклазы. Это
- 45. Скачать презентацию

















 Нарушения речи и особенности их коррекции у детей с интеллектуальной недостаточностью
Нарушения речи и особенности их коррекции у детей с интеллектуальной недостаточностью Лікарські засоби, що впливають на серцево-судинну систему та функцію нирок
Лікарські засоби, що впливають на серцево-судинну систему та функцію нирок Геморрагические лихорадки
Геморрагические лихорадки Гемолитическая болезнь плода и новорожденного. Повышение непрямого билирубина
Гемолитическая болезнь плода и новорожденного. Повышение непрямого билирубина Особенности фармакокинетики лекарственных веществ, вводимых роженице в родах и их влияние на плод
Особенности фармакокинетики лекарственных веществ, вводимых роженице в родах и их влияние на плод Инвазия. Формы инвазии
Инвазия. Формы инвазии Расспрос больных с заболеваниями органов дыхания. Общий осмотр. Осмотр и пальпация грудной клетки. Перкуссия легких
Расспрос больных с заболеваниями органов дыхания. Общий осмотр. Осмотр и пальпация грудной клетки. Перкуссия легких Әлеуметтік диагностика
Әлеуметтік диагностика Энергетическая ценность пищевых продуктов
Энергетическая ценность пищевых продуктов Функционирование учреждения здравоохранения в условиях чрезвычайных ситуаций
Функционирование учреждения здравоохранения в условиях чрезвычайных ситуаций Клиническая психология
Клиническая психология Предупреждение желудочно-кишечных болезней
Предупреждение желудочно-кишечных болезней Пролиферативное воспаление
Пролиферативное воспаление Переломи і опіки
Переломи і опіки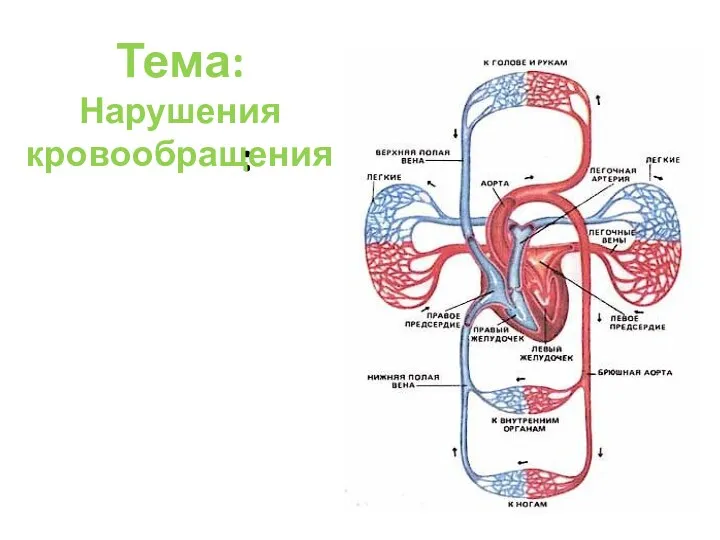 ОП нарушения кровообращения
ОП нарушения кровообращения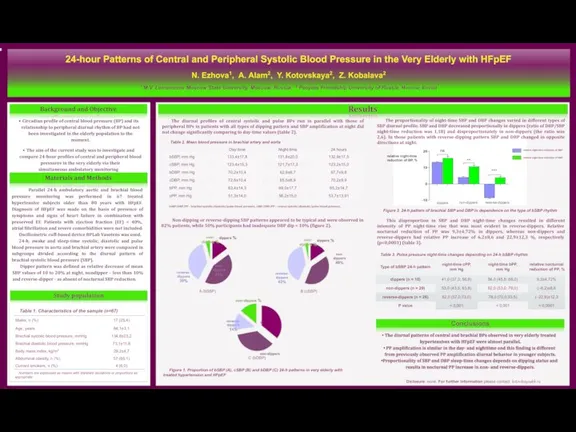 24-hour patterns of central and peripheral systolic blood pressure in the very elderly with HFpEF
24-hour patterns of central and peripheral systolic blood pressure in the very elderly with HFpEF Периферическая нервная система. Спинномозговые нервы
Периферическая нервная система. Спинномозговые нервы Медицинская служба Вооруженных сил РФ в ЧС
Медицинская служба Вооруженных сил РФ в ЧС Рожистое воспаление
Рожистое воспаление Гипогликемия и гипергликемия у новорожденных
Гипогликемия и гипергликемия у новорожденных Первая помощь при термотравмах и электротравмах
Первая помощь при термотравмах и электротравмах Переливание крови. История. Изогемагглютинация, группы крови. Механизм действия перелитой крови
Переливание крови. История. Изогемагглютинация, группы крови. Механизм действия перелитой крови Проблема инвалидности
Проблема инвалидности Эффект применения Флуфеназина в лечении синдрома Туретта
Эффект применения Флуфеназина в лечении синдрома Туретта Синдром пангипопитуитаризма
Синдром пангипопитуитаризма Вторичный метаболизм
Вторичный метаболизм Клинико-психологическое сопровождение пожилых людей страдающих инволлюционным паранойдом
Клинико-психологическое сопровождение пожилых людей страдающих инволлюционным паранойдом Ультразвуковые маркеры хромосомной патологии
Ультразвуковые маркеры хромосомной патологии