Содержание
- 2. Понятие об алкинах Алкины – углеводороды, содержащие в молекуле одну тройную связь между атомами углерода, а
- 3. Характеристика тройной связи Вид гибридизации – sp Валентный угол – 180 Длина связи С = С
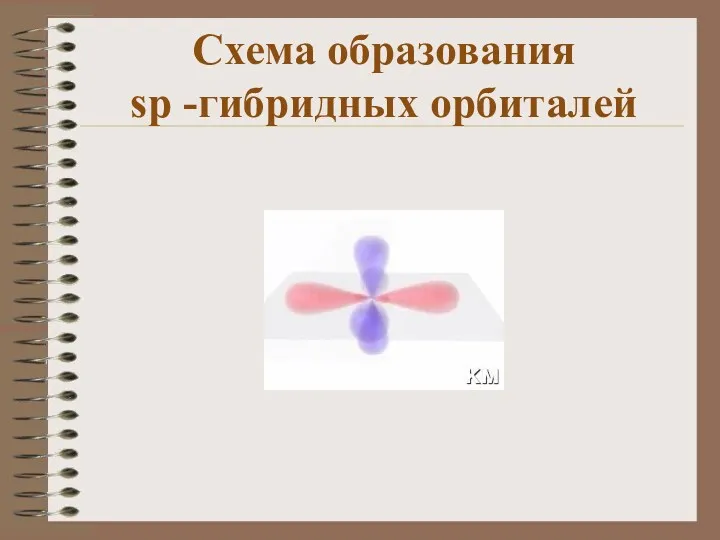
- 4. Схема образования sp -гибридных орбиталей
- 5. Схема образования sp -гибридных орбиталей
- 6. Гомологический ряд алкинов C2H2 C3H4 C4H6 C5H8 C6H10 C7H12 Этин Пропин Бутин Пентин Гексин Гептин
- 7. Изомерия алкинов Структурная изомерия 1. Изомерия положения тройной связи (начиная с С4Н6): СН ≡С−СН2−СН3 СН3−С≡С−СН3 бутин-1
- 8. Физические свойства Температуры кипения и плавления алкинов, так же как и алкенов, закономерно повышаются при увеличении
- 9. Ацетилен получают в промышленности двумя способами: 1. Термический крекинг метана: 1500°С 2СН4 ⎯⎯→ С2Н2 + 3Н2
- 10. Химические свойства алкинов Химические свойства ацетилена и его гомологов в основном определяются наличием в их молекулах
- 11. Реакции присоединения 1. Галогенирование Обесцвечивание бромной воды является качественной реакцией на все непредельные углеводороды
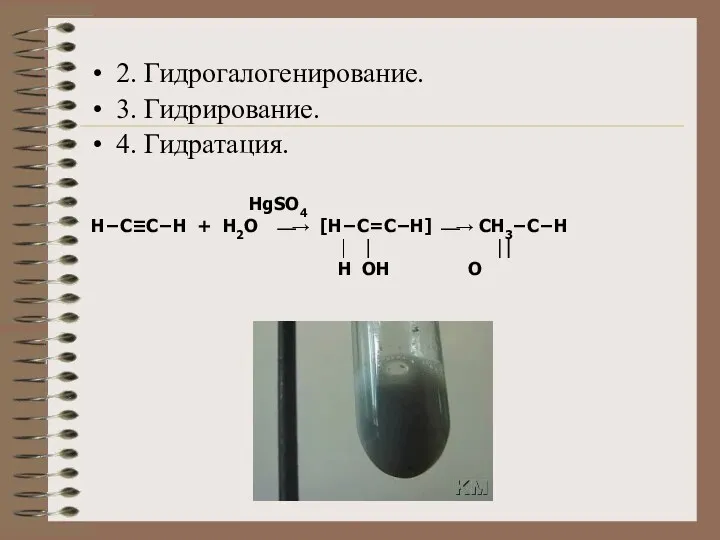
- 12. 2. Гидрогалогенирование. 3. Гидрирование. 4. Гидратация. HgSO4 Н−C≡C−H + H2O ⎯→ [H−C=C−H] ⎯→ CH3−C−H ⏐ ⏐
- 13. Окисление Ацетилен и его гомологи окисляются перманганатом калия с расщеплением тройной связи и образованием карбоновых кислот:
- 14. Горение ацетилена При сгорании (полном окислении) ацетилена выделяется большое количества тепла: HC≡CH + 2О2 ⎯→ 2СО2
- 15. Реакции замещения При взаимодействии ацетилена (или R−C≡C−H) с аммиачными растворами оксида серебра выпадают осадки нерастворимых ацетиленидов:
- 16. Реакция полимеризации 1. Димеризация под действием водного раствора CuCl и NH4Cl: НC≡CH + НC≡CH ⎯→ Н2C=CH−C≡CH
- 18. Скачать презентацию













 Сложение и вычитание десятичных дробей
Сложение и вычитание десятичных дробей Определение экономической точности отклонения по размеру и классу точности обрабатываемой поверхности
Определение экономической точности отклонения по размеру и классу точности обрабатываемой поверхности Теории происхождения искусства
Теории происхождения искусства Возникновение речи у ребенка и ее развитие в дошкольном и школьном возрасте
Возникновение речи у ребенка и ее развитие в дошкольном и школьном возрасте Зимующие птицы
Зимующие птицы Основные группы лекарственных препаратов при лечении ОРЗ и ОРВИ
Основные группы лекарственных препаратов при лечении ОРЗ и ОРВИ Влияние вредных привычек на человека
Влияние вредных привычек на человека Австралия - страна, где всё наоборот Интегрированный урок географии и английского языка в 7 классе Австралия - страна, где всё наоборот
Австралия - страна, где всё наоборот Интегрированный урок географии и английского языка в 7 классе Австралия - страна, где всё наоборот Портфоліо вчителя початкових класів Тимофій Наталії Іванівни. Фотоальбом
Портфоліо вчителя початкових класів Тимофій Наталії Іванівни. Фотоальбом Технология и оборудование для сварки профильных балок
Технология и оборудование для сварки профильных балок Air transport
Air transport Аускультация сердца и фонокардиография
Аускультация сердца и фонокардиография Окислительно-восстановительные реакции
Окислительно-восстановительные реакции График заселения иногородних студентов в общежития Университета
График заселения иногородних студентов в общежития Университета Атмосферное давление. Ветер.
Атмосферное давление. Ветер. Проект по географии Геослово
Проект по географии Геослово Маркировка товаров
Маркировка товаров О некоторых фамилиях Любытинского района
О некоторых фамилиях Любытинского района Вычитание вида 11-
Вычитание вида 11- Молекулярная биология
Молекулярная биология Презентация деятельности детских организаций и органов ученического самоуправления
Презентация деятельности детских организаций и органов ученического самоуправления Организация, вооружение и боевая техника подразделений армии США. Разведывательная подготовка
Организация, вооружение и боевая техника подразделений армии США. Разведывательная подготовка Озеро Баскунчак
Озеро Баскунчак Правовые системы современности
Правовые системы современности Основы ландшафтной колористики
Основы ландшафтной колористики Николай Бруни. Штрихи к портрету.
Николай Бруни. Штрихи к портрету. Развитие воображения и фантазии у дошкольников
Развитие воображения и фантазии у дошкольников Западноевропейское искусство. Искусство стиля барокко
Западноевропейское искусство. Искусство стиля барокко