Содержание
- 2. ВИДЕОФРАГМЕНТ
- 3. Заполняем первую графу таблицы в карточке
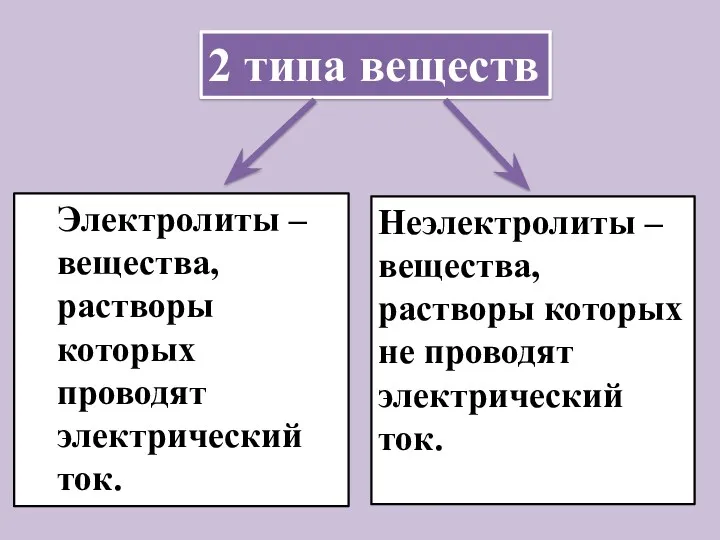
- 4. Электролиты – вещества, растворы которых проводят электрический ток. Неэлектролиты – вещества, растворы которых не проводят электрический
- 5. ИОНЫ СВЯЗАННЫЕ СВОБОДНЫЕ Ионы – это одна из форм существования химического элемента
- 6. Процесс распада электролита на ионы называется электролитической диссоциацией.
- 7. Почему сахар не проводит электрический ток? состоит из молекул у сахара ковалентная химическая связь
- 8. Заполняем вторую графу таблицы в карточке
- 9. К электролитам относятся только растворимые соли и основания Определить это можно по таблице растворимости
- 10. карбонат кальция Са СО3 Из каких ионов состоит это вещество? из ионов кальция Са2+ и карбонат-ионов
- 14. Механизм электролитической диссоциации Вещества с ионной химической связью Вспомним строение молекулы воды
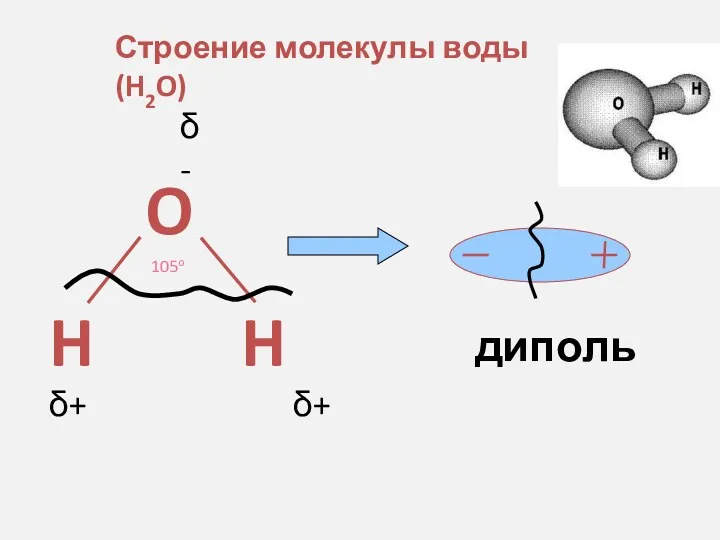
- 15. Строение молекулы воды (H2O) δ- δ+ δ+
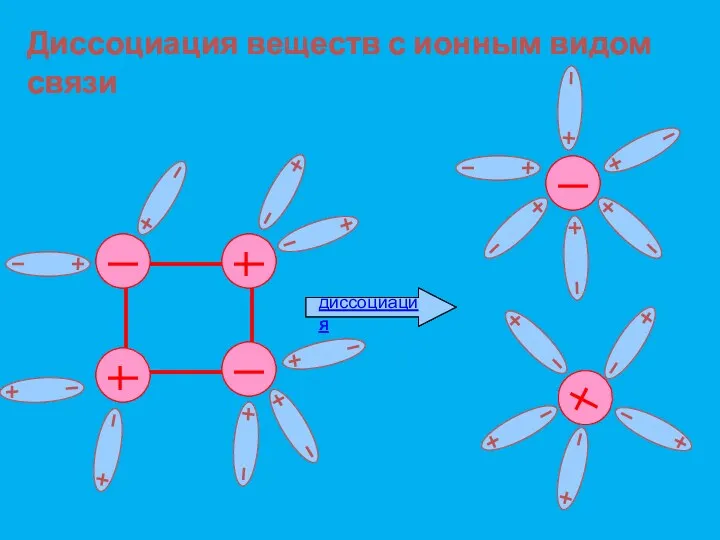
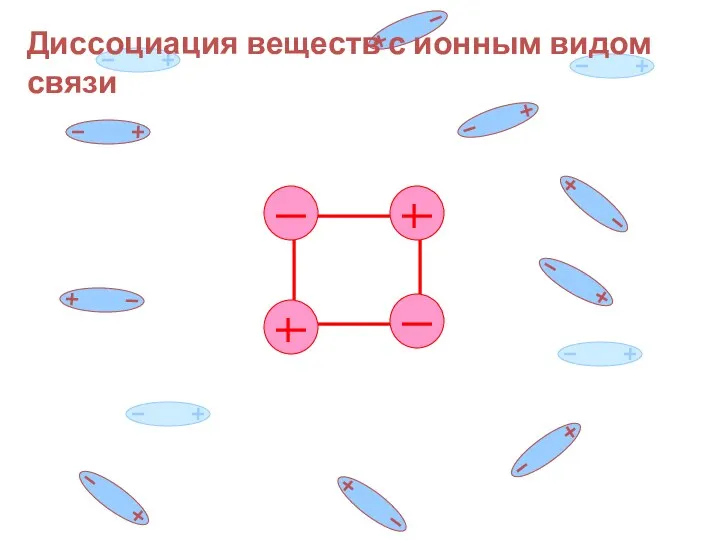
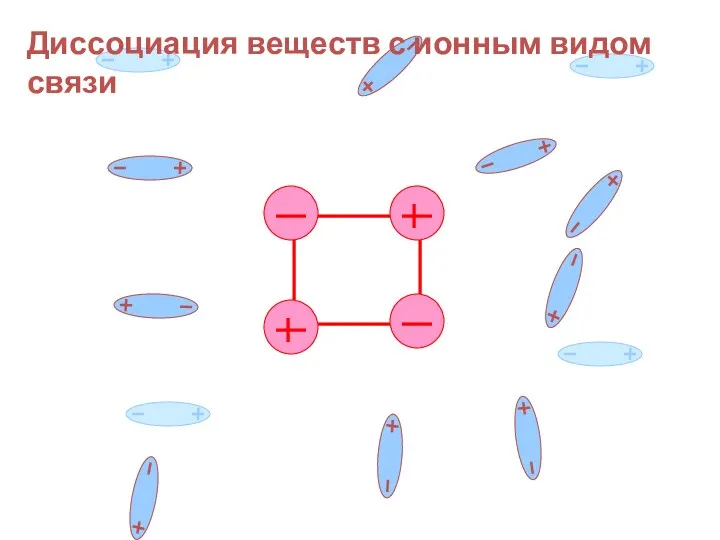
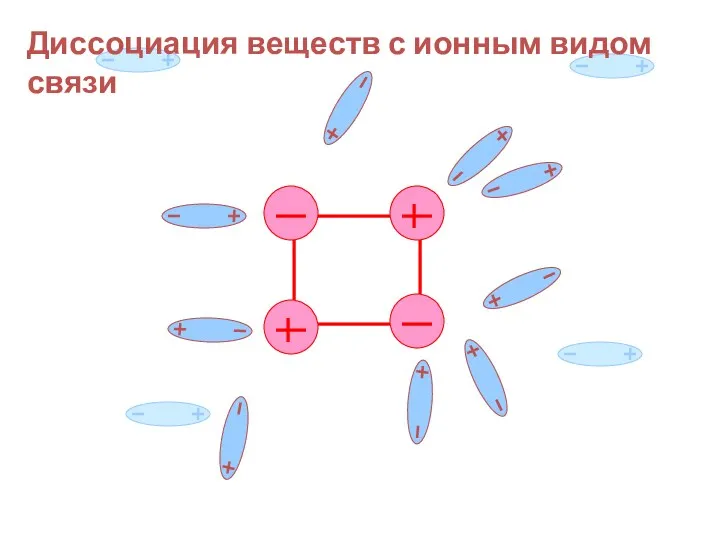
- 16. Давайте рассмотрим схему растворения и электролитической диссоциации соединений с ионной связью
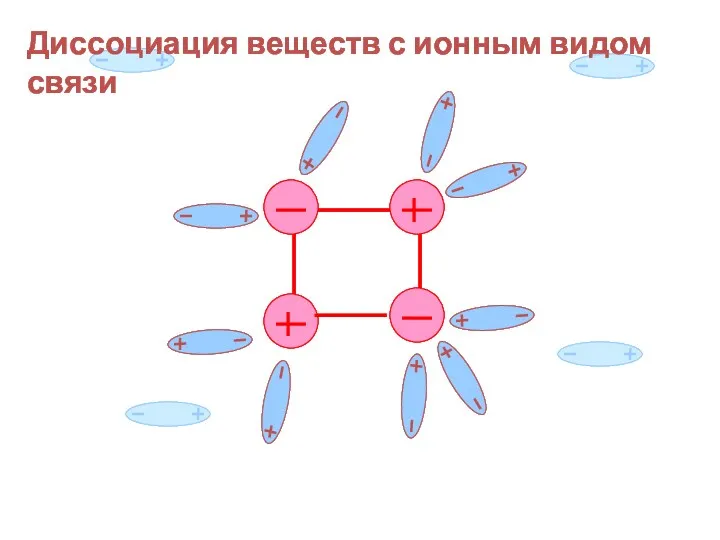
- 17. Диссоциация веществ с ионным видом связи диссоциация
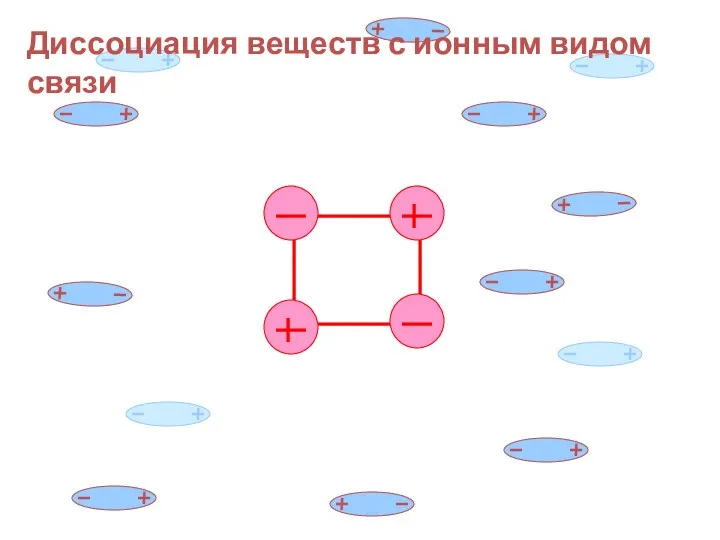
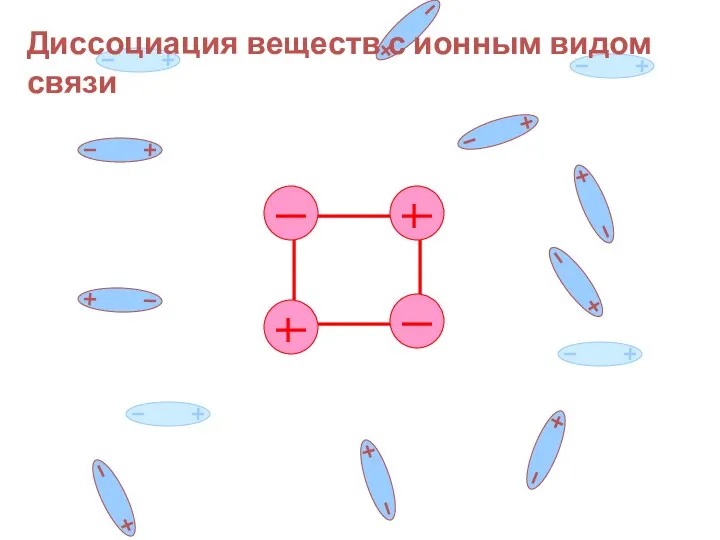
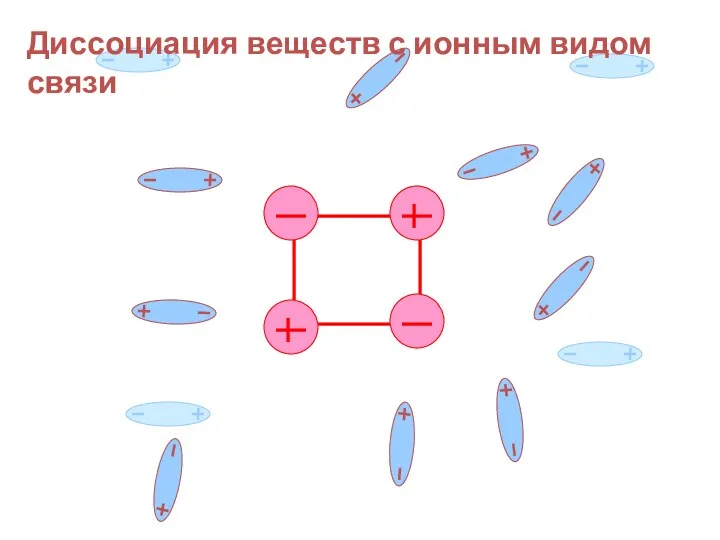
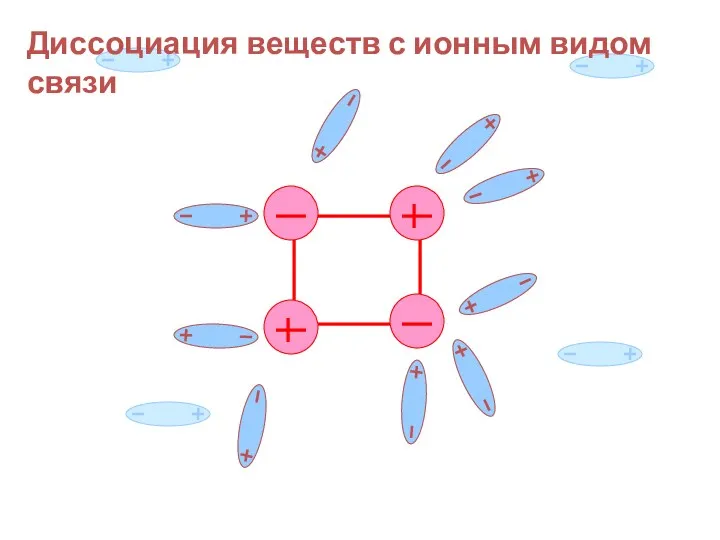
- 18. Диссоциация веществ с ионным видом связи
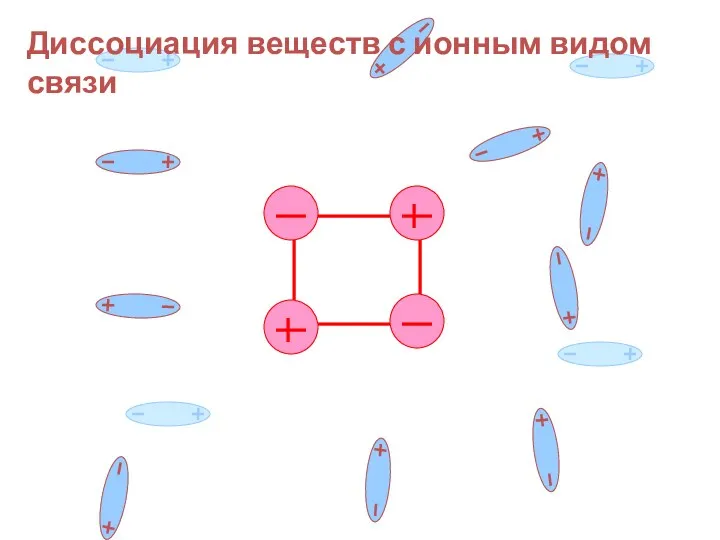
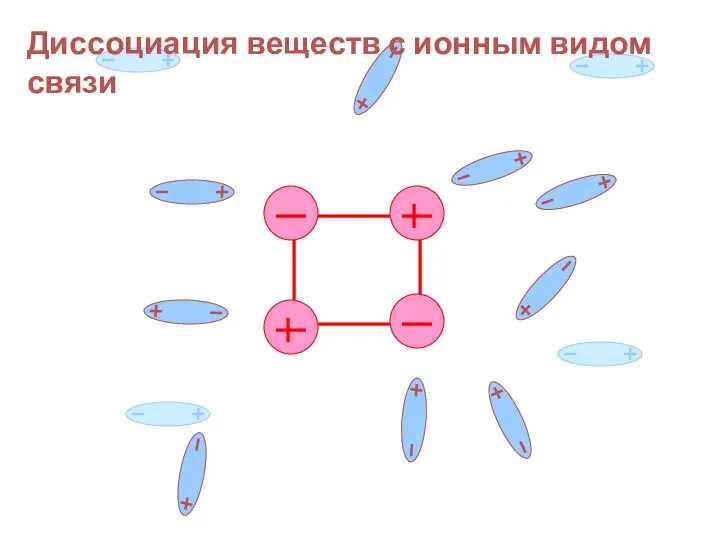
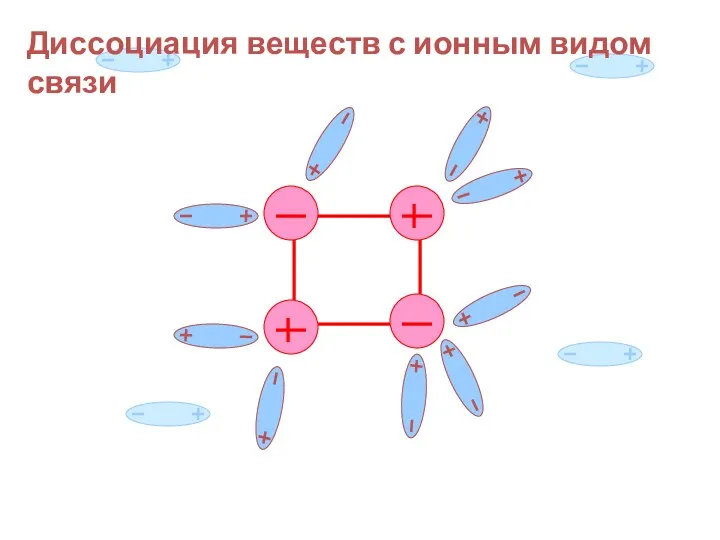
- 19. Диссоциация веществ с ионным видом связи
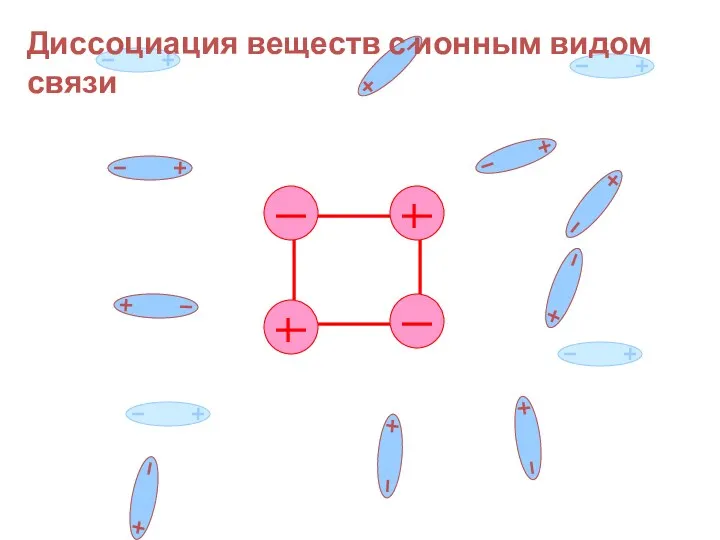
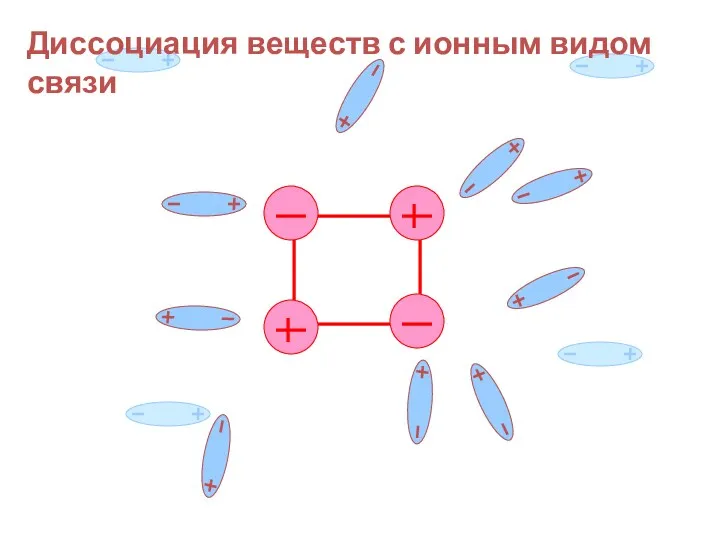
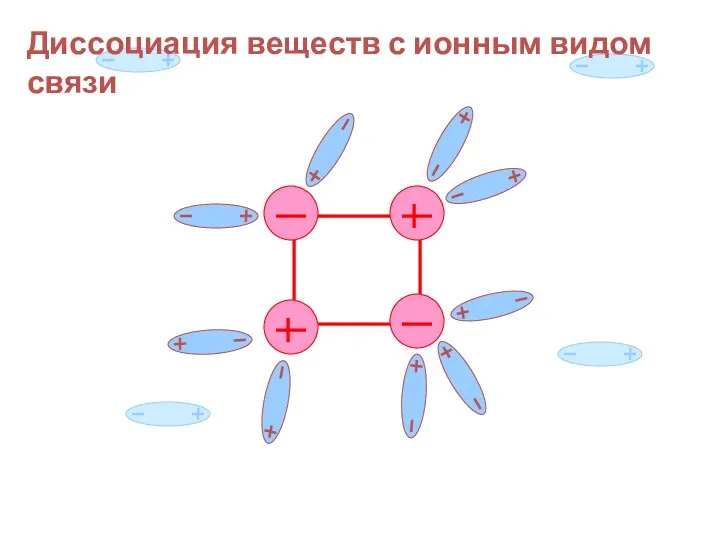
- 20. Диссоциация веществ с ионным видом связи
- 21. Диссоциация веществ с ионным видом связи
- 22. Диссоциация веществ с ионным видом связи
- 23. Диссоциация веществ с ионным видом связи
- 24. Диссоциация веществ с ионным видом связи
- 25. Диссоциация веществ с ионным видом связи
- 26. Диссоциация веществ с ионным видом связи
- 27. Диссоциация веществ с ионным видом связи
- 28. Диссоциация веществ с ионным видом связи
- 29. Диссоциация веществ с ионным видом связи
- 30. Диссоциация веществ с ионным видом связи
- 31. Диссоциация веществ с ионным видом связи
- 32. Диссоциация веществ с ионным видом связи
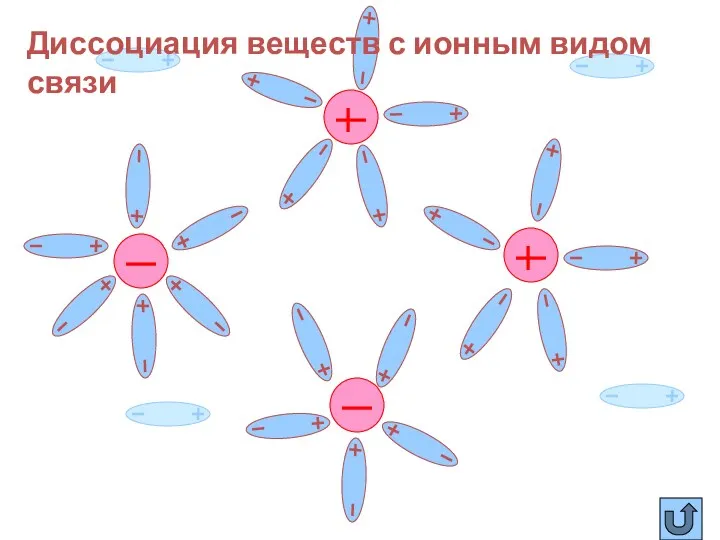
- 33. Этапы диссоциации веществ с ионной связью Ориентация Гидратация Диссоциация
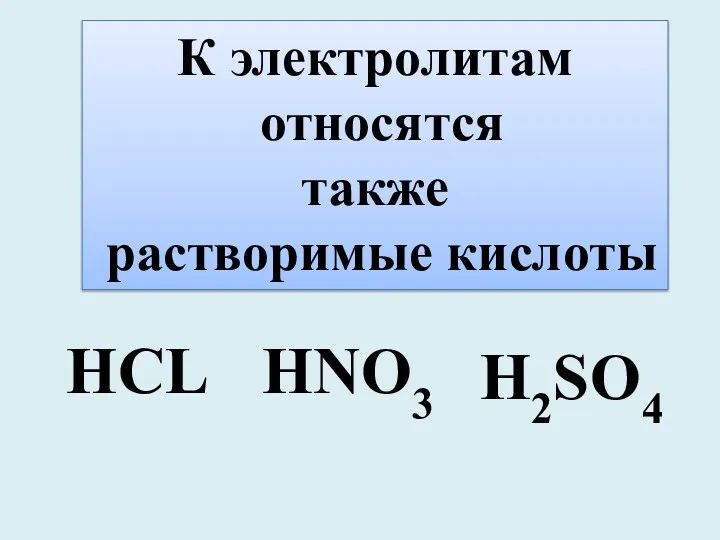
- 34. К электролитам относятся также растворимые кислоты HCL HNO3 H2SO4
- 35. Механизм электролитической диссоциации веществ с ковалентной сильнополярной связью. На примере хлороводородной кислоты
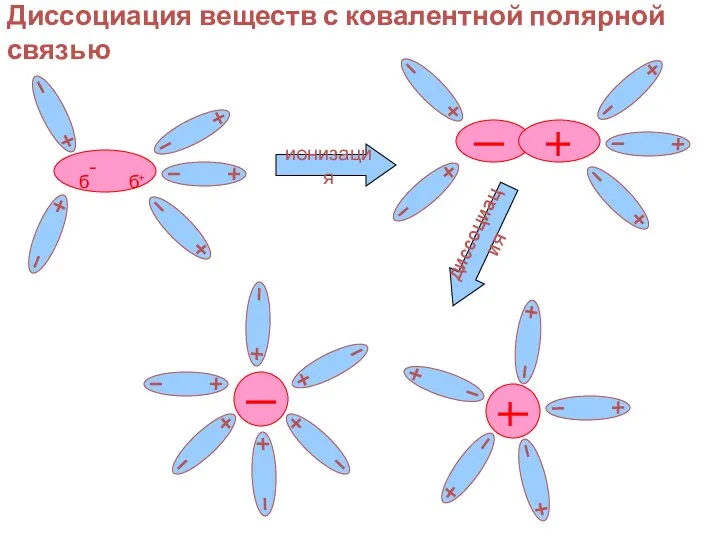
- 36. ионизация диссоциация Диссоциация веществ с ковалентной полярной связью
- 37. Этапы диссоциации веществ с ковалентной сильнополярной связью Ориентация Гидратация Ионизация Диссоциация
- 38. Вещества по разному распадаются на ионы. А как это происходит и почему вы узнаете на следующем
- 39. Оценим полученные знания Правильный ответ «+» Неправильный ответ «-» Критерии оценивания: колличество правильных ответов от 14
- 41. ОЦЕНКИ ЗА УРОК
- 43. Скачать презентацию




















 ПрезентацияМужские архетипы
ПрезентацияМужские архетипы презентация к уроку Основания 8 класс
презентация к уроку Основания 8 класс Разделы науки о языке
Разделы науки о языке Новое царство
Новое царство Растения в интерьере жилого дома
Растения в интерьере жилого дома Р. Сеф Весёлые стихи, 3класс
Р. Сеф Весёлые стихи, 3класс презентация группового занятия по патриотическому воспитанию
презентация группового занятия по патриотическому воспитанию Программа кормления животных ветеринарных врачей на территории дилера ИП Коробов
Программа кормления животных ветеринарных врачей на территории дилера ИП Коробов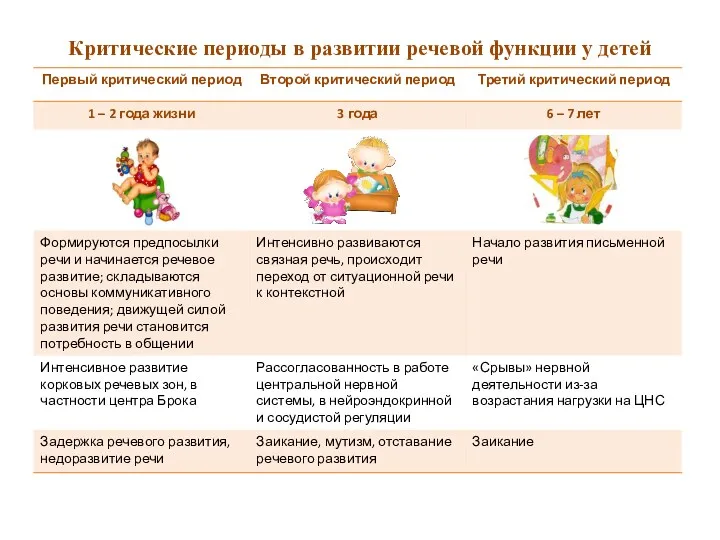 Информация для родителей. Критические периоды в развитии речевой функции у детей.
Информация для родителей. Критические периоды в развитии речевой функции у детей. Алгоритм сочинения загадок по опорным таблицам
Алгоритм сочинения загадок по опорным таблицам Презентация по химии для 9 класса по теме: Органические вещества.
Презентация по химии для 9 класса по теме: Органические вещества. Бойове застосування КЗА 86Ж6. Алгоритми обробки радiолокацiйної iнформацiї, виявлення та захоплення цiлей. (Тема 8.4)
Бойове застосування КЗА 86Ж6. Алгоритми обробки радiолокацiйної iнформацiї, виявлення та захоплення цiлей. (Тема 8.4) Презентация к статье Образовательное путешествие. Новые возможности
Презентация к статье Образовательное путешествие. Новые возможности Экологические проблемы Берингова моря
Экологические проблемы Берингова моря Портфолио педагога дополнительного образования (Презентация)
Портфолио педагога дополнительного образования (Презентация) Мастер-класс Народная кукла Кувадка
Мастер-класс Народная кукла Кувадка Сумматоры. Виды
Сумматоры. Виды DSM Food Specialties
DSM Food Specialties Wodospady iguazú - park narodowy Аrgentyny i Вrazylii
Wodospady iguazú - park narodowy Аrgentyny i Вrazylii 20230916_videoprezentatsiya_k_obobshchayushchemu_uroku_po_prirodovedeniyu_dlya_6_kl
20230916_videoprezentatsiya_k_obobshchayushchemu_uroku_po_prirodovedeniyu_dlya_6_kl Презентация. Климат Австралии, 7 класс.
Презентация. Климат Австралии, 7 класс. Устный счёт
Устный счёт Мастер - класс по фелтингу Осенние листья
Мастер - класс по фелтингу Осенние листья Мы - граждане России
Мы - граждане России Презентация Весёлый гномик
Презентация Весёлый гномик Устройство и эксплуатация солнечных батарей
Устройство и эксплуатация солнечных батарей Поэтапное рисование кошки
Поэтапное рисование кошки Кузнецкая крепость Диск
Кузнецкая крепость Диск