Содержание
- 2. Згадай 1. Що таке хімічна реакція? 2.Що відбувається з молекулами при перебігу реакції? 3. Які ознаки
- 3. Концентрація Величина, що показує вміст кількості речовини в одиниці об’єму називається концентрацією. С=v/ V де c
- 4. Отже, швидкість реакції - це зміна концентрації одного з реагентів чи одного з продуктів реакції за
- 5. Вчені, що зробили внесок в розвиток хімічної кінетики Якоб Вант – Гофф – голландський вчений, перший
- 6. Вчені, що зробили внесок в розвиток хімічної кінетики Сванте Арреніус (лауреат Нобелівської премії за відкриття в
- 7. Фактори, що впливають на швидкість реакції. Природа реагуючих речовин Ступінь подрібнення Площа поверхні контакту Концентрація Температура
- 8. Лабораторний дослід №5. Вплив площі поверхні контакту реагентів, концентрації й температури на швидкість хімічної реакції. Група
- 9. Закон діючих мас 1867 рік Математична залежність швидкості від концентрації для реакції : А + Б
- 10. Думай самостійно У скільки разів збільшиться швидкість реакції, якщо збільшити концентрації речовин в 2 рази? Рівняння
- 11. Додумався? Молодець! Швидкість реакції збільшиться у 16 разів
- 12. Правило Вант - Гоффа При збільшенні температури на кожні 100 швидкість реакции зростає у 2-4 рази.Величина,
- 13. Математичний вираз правила Вант- Гоффа V2/ V1 = Υt2- t 1/10
- 14. Думай самостійно У скільки разів збільшиться швидкість реакції при підвищенні температури з 60◦С до 80 ◦
- 15. Додумався? Молодець! Швидкість реакції збільшиться у 9 разів
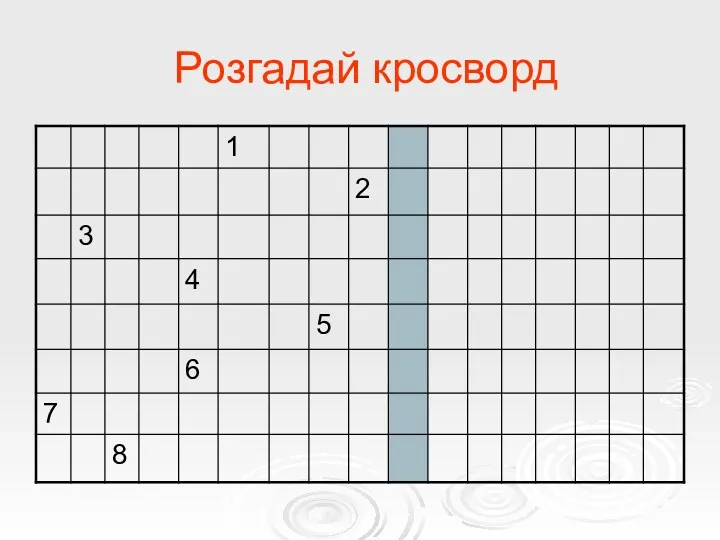
- 16. Розгадай кросворд
- 18. Скачать презентацию














 Подростковый кризис
Подростковый кризис Аппаратура измерения температуры газов двигателей (урок 15)
Аппаратура измерения температуры газов двигателей (урок 15) Презентация Внутренние воды северной Америки
Презентация Внутренние воды северной Америки Типовые системы управления режимами работы и регулирования авиационных ГТД
Типовые системы управления режимами работы и регулирования авиационных ГТД Какая бывает промышленность?
Какая бывает промышленность? Психология, как наука
Психология, как наука Лікувальне застосування магнітних полів. Механізм дії, показання та протипоказання
Лікувальне застосування магнітних полів. Механізм дії, показання та протипоказання Носовые кровотечения при лейкозах
Носовые кровотечения при лейкозах Икона Пресвятой Богородицы Одигитрия Устюженская
Икона Пресвятой Богородицы Одигитрия Устюженская Индустриальная революция: достижения и проблемы
Индустриальная революция: достижения и проблемы Острая дыхательная недостаточность
Острая дыхательная недостаточность воспитательная программа - Ступень познания
воспитательная программа - Ступень познания Агрокультура. Факт 2018
Агрокультура. Факт 2018 Религия и общественно-политическая мысль в США
Религия и общественно-политическая мысль в США Основы специальной теории относительности
Основы специальной теории относительности Марафон Техника, с которой мы победили. Танк Т-34 “Челябинские колхозники”
Марафон Техника, с которой мы победили. Танк Т-34 “Челябинские колхозники” Кадровое обеспечение системы управления персоналом
Кадровое обеспечение системы управления персоналом Фармакология - наука о лекарствах
Фармакология - наука о лекарствах Модерн в архитектуре
Модерн в архитектуре Военнослужащие и взаимоотношения между ними. Размещение военнослужащих. Распределение времени и повседневный порядок
Военнослужащие и взаимоотношения между ними. Размещение военнослужащих. Распределение времени и повседневный порядок Транспортирование строительных грузов
Транспортирование строительных грузов Христофор Колумб
Христофор Колумб Перевод с платного обучения на бюджет
Перевод с платного обучения на бюджет Математиканың иллюзиямен байланысы
Математиканың иллюзиямен байланысы иваньков
иваньков Креативное программирование. Погружение в мир программирования и создание креативных проектов
Креативное программирование. Погружение в мир программирования и создание креативных проектов Бинарные соединения – оксиды и летучие водородные соединения
Бинарные соединения – оксиды и летучие водородные соединения Основное оборудование сварочно-монтажного цеха
Основное оборудование сварочно-монтажного цеха