Содержание
- 2. Задание для первой группы М. В.Ломоносов в статье, опубликованной в 1745 г., писал : «При растворении
- 3. Задание для второй группы Семен Исаакович Вольфкович (1896 – 1980) в одной из лабораторий Московского университета
- 4. Задание для третьей группы Шведский химик так описал один свой опыт, выполненный в 1774 г.: «Я
- 5. Задание для четвертой группы У Куртуа был любимый кот, который во время обеда сидел обычно на
- 6. Какой неметалл ценится дороже золота, и когда платят деньги за то, чтобы от него избавиться? Задание
- 7. « Я слушаю - и забываю Я вижу - и запоминаю Я делаю - и понимаю»
- 8. Кислоты с точки зрения ТЭД – это электролиты, которые при диссоциации образуют катионы водорода и анионы
- 9. ОРГАНИЧЕСКИЕ – ЛИМОННАЯ, ЯБЛОЧНАЯ, УКСУСНАЯ, ЩАВЕЛЕВАЯ, МУРАВЬИНАЯ. По происхождению
- 10. НЕОРГАНИЧЕСКИЕ- СЕРНАЯ, СОЛЯНАЯ, ПЛАВИКОВАЯ, ФОСФОРНАЯ, АЗОТНАЯ.
- 11. Соляная кислота, находящаяся в желудке, помогает переваривать пищу. Молочная кислота образуется в мышцах при физической нагрузке.
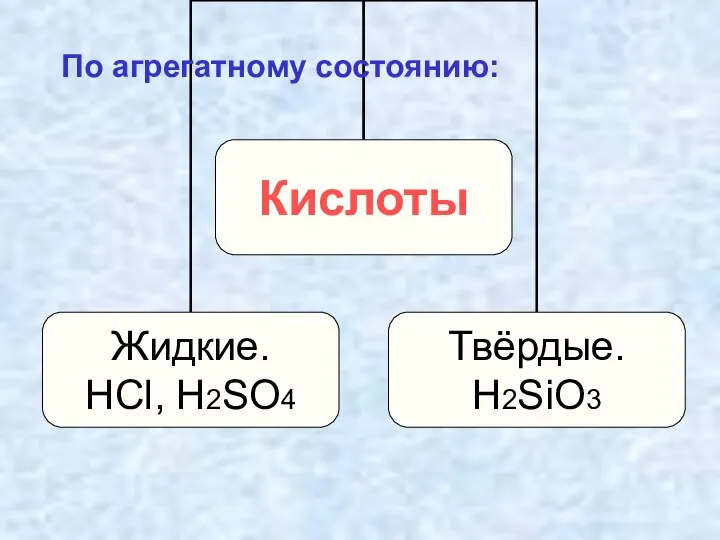
- 12. По агрегатному состоянию:
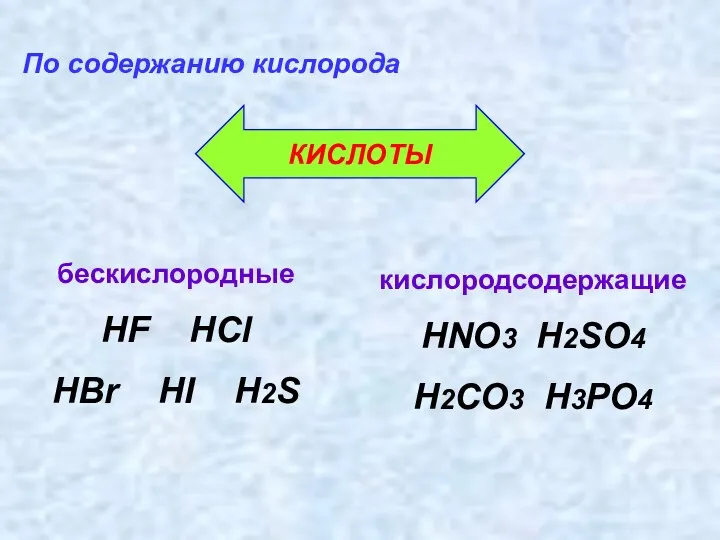
- 13. бескислородные HF HCl HBr HI H2S По содержанию кислорода кислородсодержащие HNO3 H2SO4 H2CO3 H3PO4 КИСЛОТЫ
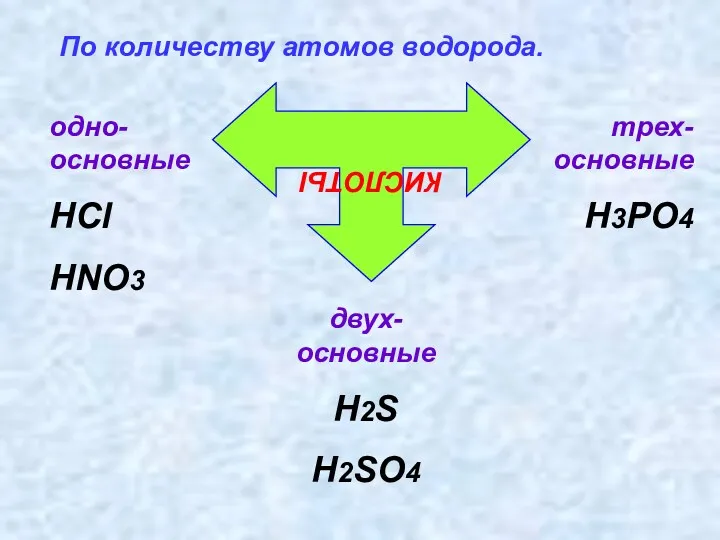
- 14. По количеству атомов водорода. КИСЛОТЫ одно-основные HCl HNO3 двух-основные H2S H2SO4 трех-основные H3PO4
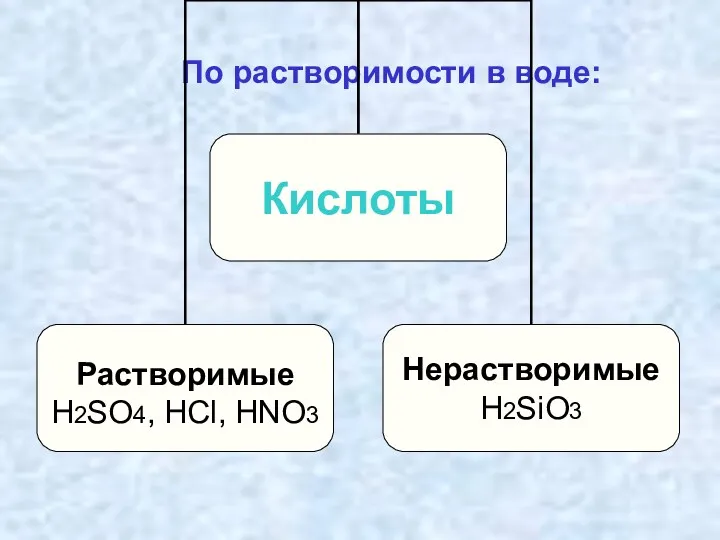
- 15. По растворимости в воде:
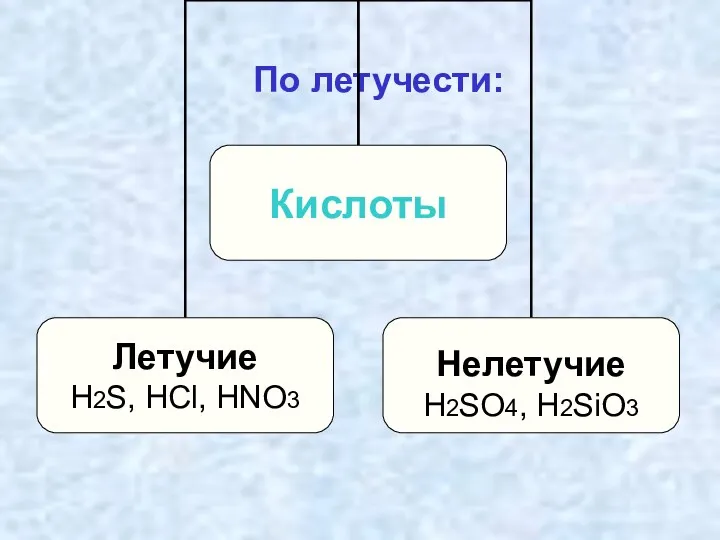
- 16. По летучести:
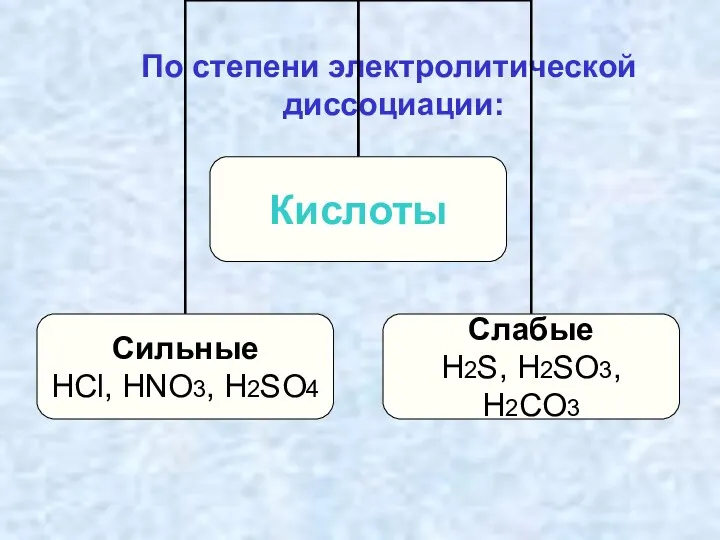
- 17. По степени электролитической диссоциации:
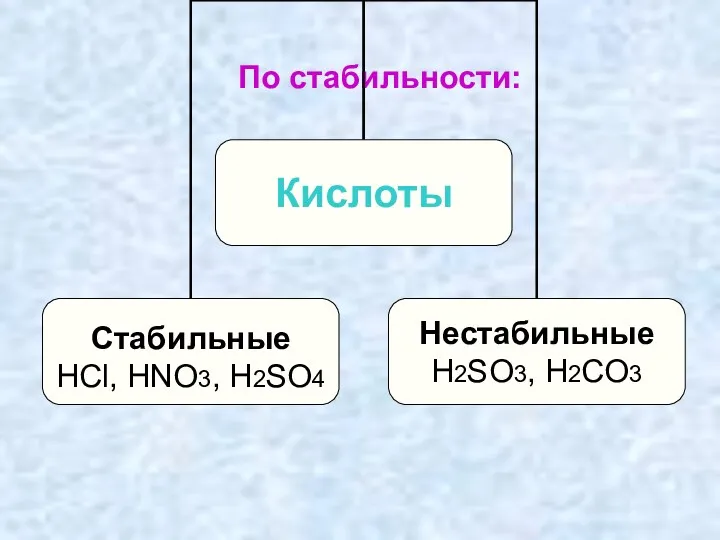
- 18. По стабильности:
- 19. КИСЛОТЫ ПРИМЕНЯЮТСЯ В МЕДИЦИНЕ. Аскорбиновая, фолиевая, липоевая, ацетилсалициловая
- 20. КИСЛОТЫ ПРИМЕНЯЮТСЯ В КУЛИНАРИИ . Уксусная и лимонная кислоты
- 21. Составить портрет Дайте классификацию уксусной кислоте(1В), серной кислоте(2В) по всем известным признакам классификации. Напишите уравнение диссоциации
- 22. Содержится в желудочном соке, в соленых огурцах. Применяется при дублении кожи, для подкисления безалкогольных напитков, ее
- 23. Правильный ответ №3
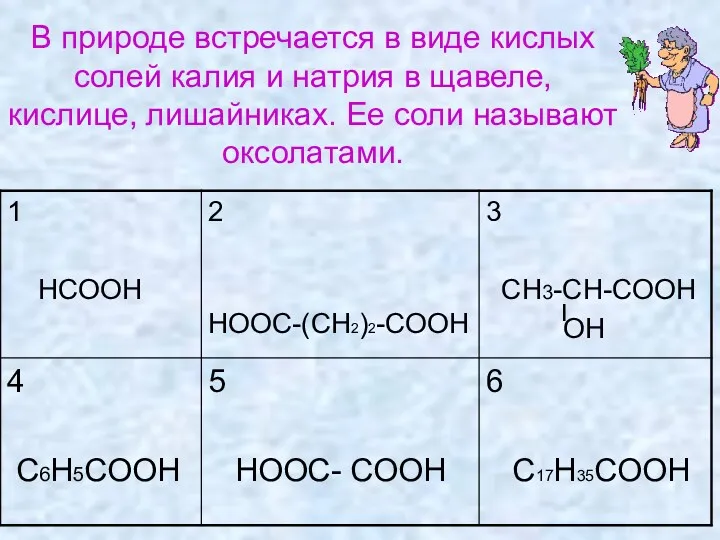
- 24. В природе встречается в виде кислых солей калия и натрия в щавеле, кислице, лишайниках. Ее соли
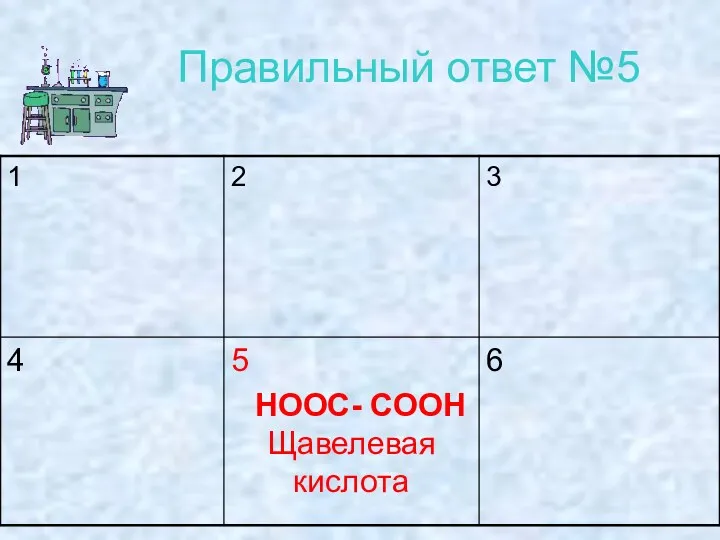
- 25. Правильный ответ №5
- 26. Находится в выделениях желез муравьев, в иглах ели, в ворсинках жгучей крапивы и в поте животных.
- 27. Правильный ответ №1
- 28. Лабораторная работа№1 На кусочек лимона капните 1-2 капли лакмуса. Что наблюдаете?
- 29. Лабораторная работа №2 В каждую из трёх пробирок, где находятся металлы – цинк, железо, медь прилейте
- 30. Лабораторная работа №3 В каждую из двух пробирок, где находятся оксид кальция и оксид меди, добавьте
- 31. Лабораторная работа №4 В пробирку с гидроксидом натрия добавьте 1-2 мл. соляной кислоты(1в)и уксусную кислоту (2в).
- 32. Лабораторная работа №5 В пробирку с раствором соляной кислоты(1в) добавьте 1-2 мл. нитрата серебра. Что наблюдаете?
- 33. Общие химические свойства у неорганических и неорганических кислот Диссоциация Взаимодействие с индикаторами Взаимодействие с металлами Взаимодействие
- 34. Закрепление Выбери правильный ответ. А-1 С какими из приведённых веществ не будет взаимодействовать соляная кислота: а)
- 35. А -4 В результате взаимодействия соляной кислоты с нитратом серебра выпадает : а) чёрный осадок б)
- 36. Ответы 1б 2в 3б 4в 5а
- 37. 1. С какими веществами реагирует уксусная кислота: А) оксид магния б) углекислый газ в) соляная кислота
- 39. Домашнее задание: П. 20 упр.1-5 1.Подготовьте интересные сообщения о кислотах 2.Сделайте свою презентацию о кислотах
- 41. Скачать презентацию





























 Anthropogenic factors of occurrence instability in the biosphere
Anthropogenic factors of occurrence instability in the biosphere Выключатели. Требования к выключателям
Выключатели. Требования к выключателям Введение в Автоматизацию. Лекция 7
Введение в Автоматизацию. Лекция 7 Дальность видимости горизонта и ориентиров в море
Дальность видимости горизонта и ориентиров в море Зарядка для пальчиков
Зарядка для пальчиков Тыва чоннуң аян-чорук чорууру-биле холбашкан ёзулалдары
Тыва чоннуң аян-чорук чорууру-биле холбашкан ёзулалдары Алкоголь және оның сурогаттары
Алкоголь және оның сурогаттары Непрерывность функции. Метод интервалов
Непрерывность функции. Метод интервалов Презентация Развитие мелкой моторики руки
Презентация Развитие мелкой моторики руки Затраты на производстве
Затраты на производстве Блиц-опрос по теме: Сущность и функции процесса обучения. Система целей
Блиц-опрос по теме: Сущность и функции процесса обучения. Система целей Холодильное оборудование
Холодильное оборудование Приборы радиационной и химической разведки
Приборы радиационной и химической разведки Приборы определения скорости корабля и пройденного им расстояния. (Тема 6)
Приборы определения скорости корабля и пройденного им расстояния. (Тема 6) Нейросифилис
Нейросифилис Покорение космоса.
Покорение космоса. Аксиомы стереометрии
Аксиомы стереометрии Чувствительность
Чувствительность Православные монастыри. Ипатьевский монастырь
Православные монастыри. Ипатьевский монастырь Эргономика рабочего места
Эргономика рабочего места Андрей Валерьевич Геласимов
Андрей Валерьевич Геласимов Кинематика. Равномерное движение
Кинематика. Равномерное движение 20230924_41319_1
20230924_41319_1 Жизнь древнейших людей. Древнейшие собиратели и охотники. Появление древнейших людей
Жизнь древнейших людей. Древнейшие собиратели и охотники. Появление древнейших людей Отчет о работе актива в Совете Старшеклассников
Отчет о работе актива в Совете Старшеклассников Автоматическое регулирование технологических процессов. Системы автоматического регулирования
Автоматическое регулирование технологических процессов. Системы автоматического регулирования Збудники дифтерії та мікобактеріозів (туберкульоз, лепра)
Збудники дифтерії та мікобактеріозів (туберкульоз, лепра) c5-bfaf8e79
c5-bfaf8e79