Содержание
- 2. Термодинамика исторически возникла как эмпирическая наука об основных способах преобразования внутренней энергии тел для совершения механической
- 3. Термодинамика – наука о закономерностях превращения энергии. В термодинамике широко используется понятие термодинамической системы. Термодинамической системой
- 4. Соотношение для перехода от градусов Цельсия к градусам Кельвина: T [K] = t [°C] + 273.15
- 5. Если в термодинамической системе меняется хотя бы один из параметров любого входящего в систему тела, то
- 6. Изохорный Рассмотрим термодинамическую систему, состоящую из одного тела – какого либо газа в сосуде с поршнем,
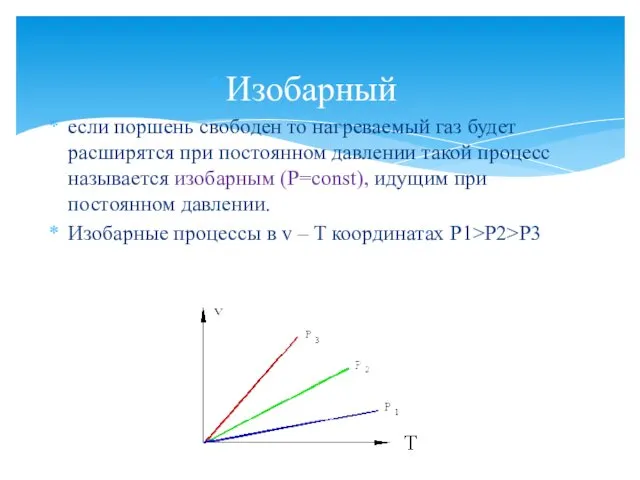
- 7. Изобарный eсли поршень свободен то нагреваемый газ будет расширятся при постоянном давлении такой процесс называется изобарным
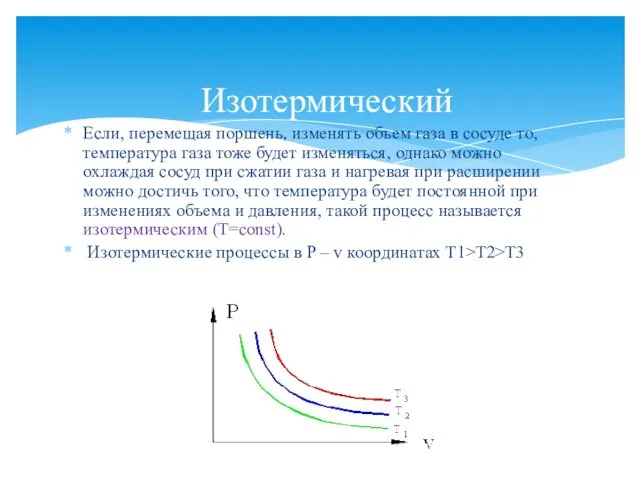
- 8. Изотермический Если, перемещая поршень, изменять объем газа в сосуде то, температура газа тоже будет изменяться, однако
- 9. Адиабатический Процесс, при котором отсутствует теплообмен между системой и окружающей средой, называется адиабатным, при этом количество
- 10. Внутренняя энергия Сумма кинетических энергий хаотического движения всех частиц тела относительно центра масс тела (молекул, атомов)
- 11. Внутренняя энергия одноатомного идеального газа Для идеального газа: U=U(T), т.к. взаимодействием на расстоянии пренебрегаем или Внутренняя
- 12. Способы изменения внутренней энергии Совершение работы (А) над телом ( U увелич.) самим телом (U уменьш.)
- 13. Работа в термодинамике По третьему закону Ньютона: Работа внешних сил над газом: Работа газа:
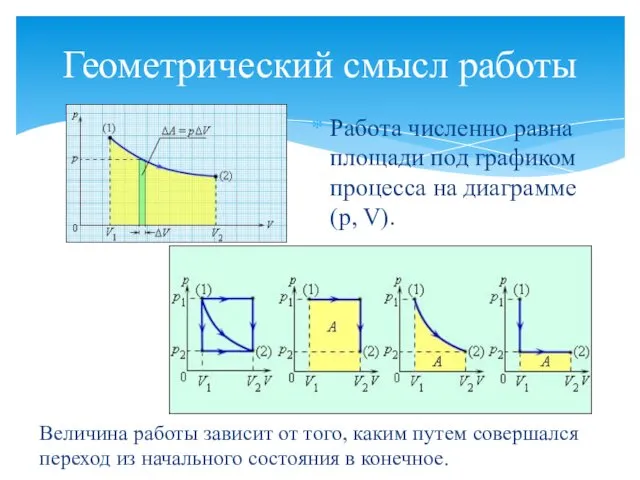
- 14. Геометрический смысл работы Работа численно равна площади под графиком процесса на диаграмме (p, V). Величина работы
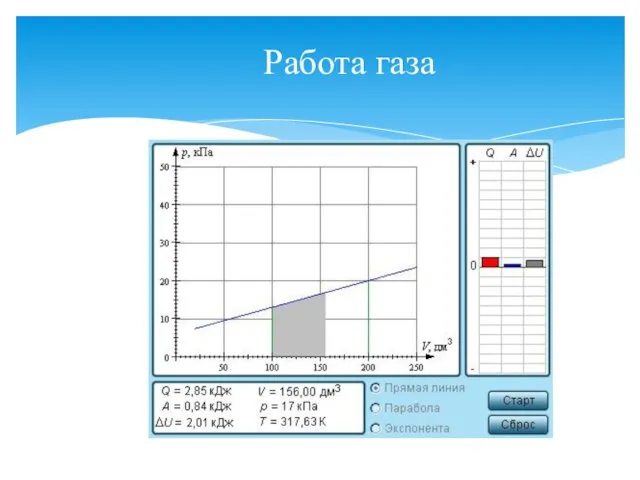
- 15. Работа газа
- 16. Q = cm(t02-t01) – нагревание (охлаждение) Q=±λm - плавление (отвердевание) Q = ±Lm - парообразование (конденсация)
- 17. Первый закон термодинамики Обмен энергией между термодинамической системой и окружающими телами в результате теплообмена и совершаемой
- 18. Первый закон термодинамики Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно
- 19. Энтальпия это сумма внутренней энергии тела и произведения давления на объем. I = U + PV
- 20. Теплота q не является функцией состояния, количество теплоты выделившейся или поглотившейся в процессе зависит от самого
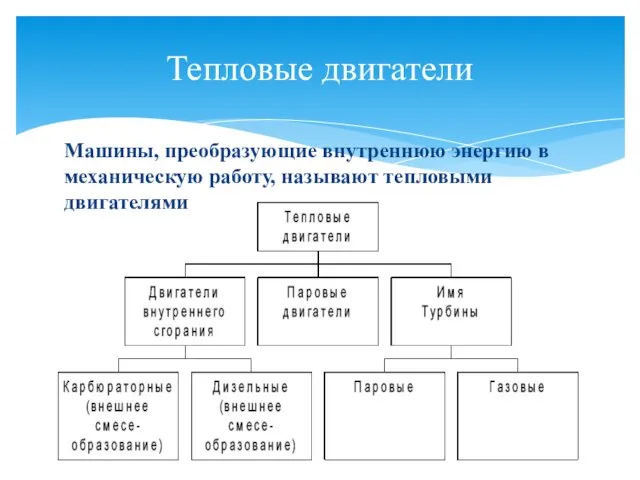
- 21. Тепловые двигатели Машины, преобразующие внутреннюю энергию в механическую работу, называют тепловыми двигателями
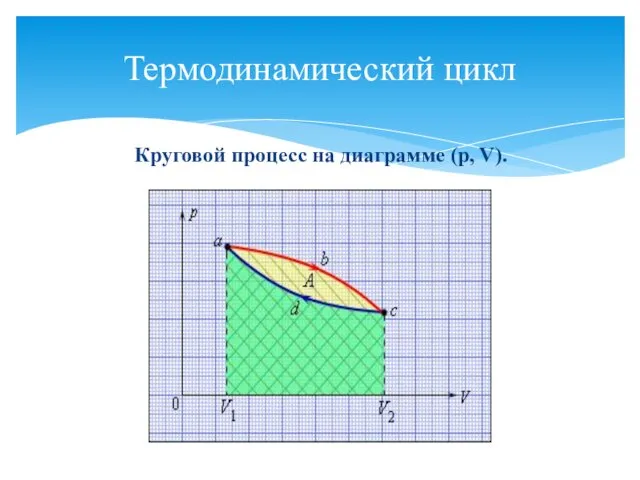
- 22. Термодинамический цикл Круговой процесс на диаграмме (p, V).
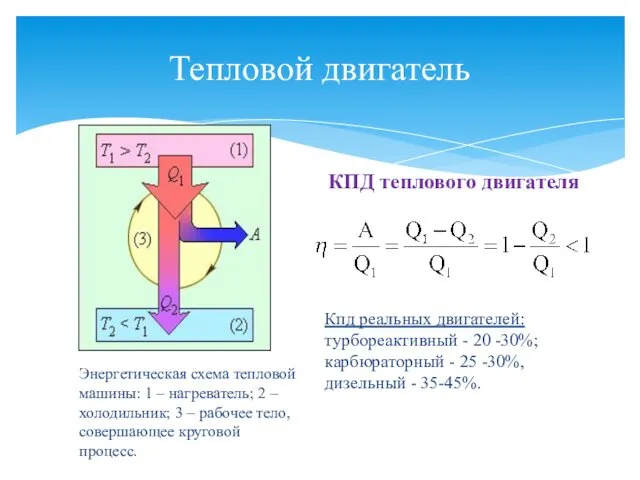
- 23. Тепловой двигатель КПД теплового двигателя Кпд реальных двигателей: турбореактивный - 20 -30%; карбюраторный - 25 -30%,
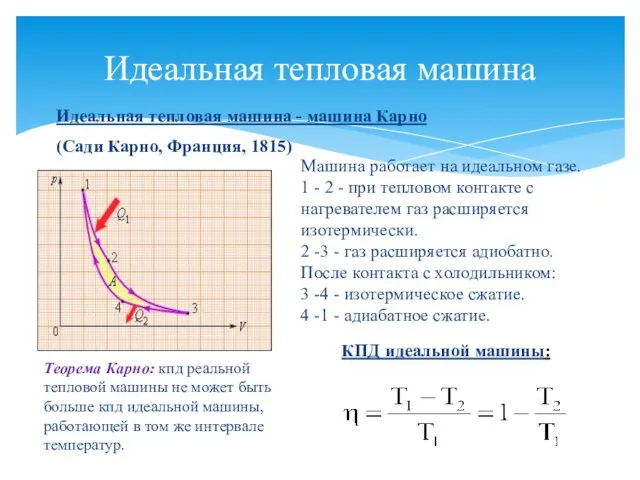
- 24. Идеальная тепловая машина Идеальная тепловая машина - машина Карно (Сади Карно, Франция, 1815) Машина работает на
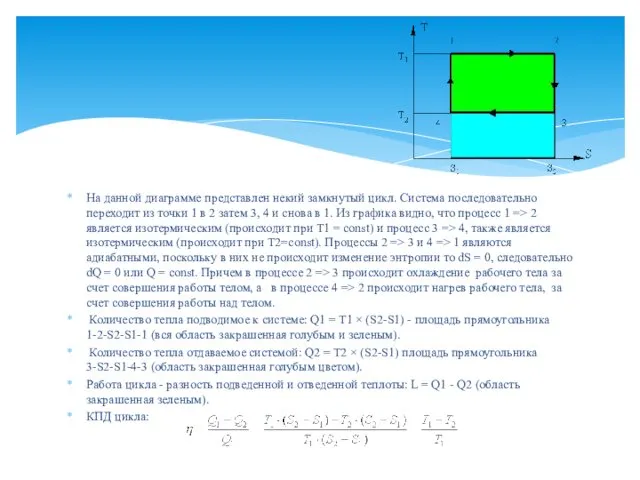
- 25. Цикл Карно Удельную энтропию можно применять совместно с одним из основных параметров для графического изображения процессов.
- 26. На данной диаграмме представлен некий замкнутый цикл. Система последовательно переходит из точки 1 в 2 затем
- 27. Второй закон термодинамики Второй з-н термодинамики указывает направление возможных энергетических превращений и тем самым выражает необратимость
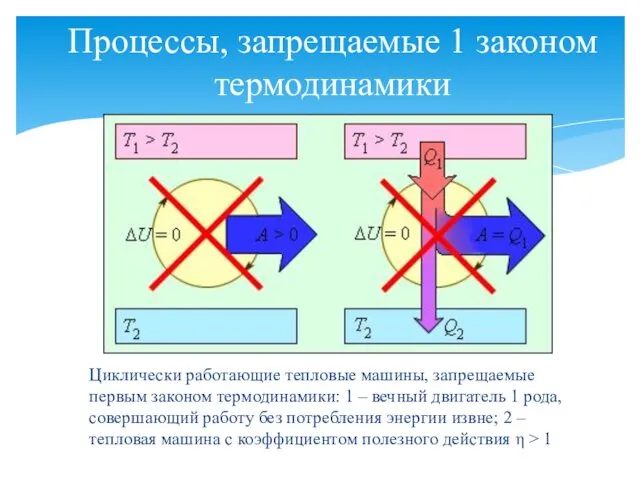
- 28. Процессы, запрещаемые 1 законом термодинамики Циклически работающие тепловые машины, запрещаемые первым законом термодинамики: 1 – вечный
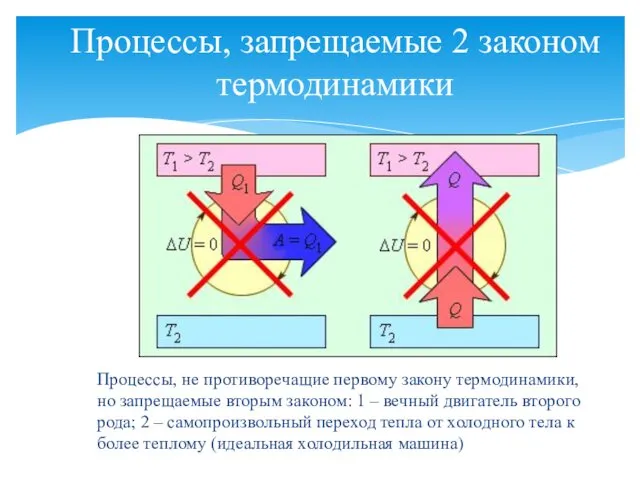
- 29. Процессы, запрещаемые 2 законом термодинамики Процессы, не противоречащие первому закону термодинамики, но запрещаемые вторым законом: 1
- 30. Закон Дюлонга-Пти (Закон постоянства теплоёмкости) — эмпирический закон, согласно которому молярная теплоёмкость твёрдых тел при комнатной
- 32. Скачать презентацию


















 Влияние электромагнитных излучений на живые организмы
Влияние электромагнитных излучений на живые организмы Турбомашиналардың паралель жұмыс істеуі бір
Турбомашиналардың паралель жұмыс істеуі бір Инерция
Инерция Валы, оси, шпоночные и зубчатые соединения
Валы, оси, шпоночные и зубчатые соединения Отделка поверхностей на токарном станке
Отделка поверхностей на токарном станке Теоретические основы радиолокации. Теория обнаружения радиолокационных сигналов. Функции рассогласования в радиолокации
Теоретические основы радиолокации. Теория обнаружения радиолокационных сигналов. Функции рассогласования в радиолокации Технология деятельностного подхода как средство реализации ФГОС ООО при проектировании уроков физики и подготовке учащихся к ОГЭ
Технология деятельностного подхода как средство реализации ФГОС ООО при проектировании уроков физики и подготовке учащихся к ОГЭ Стандарт механической обработки детали 5910-9305268 Кольцо
Стандарт механической обработки детали 5910-9305268 Кольцо МКТ.Своя игра
МКТ.Своя игра История тепловых двигателей
История тепловых двигателей Рамы конструкции и виды
Рамы конструкции и виды урок физики в 8 классе Мир сквозь очки
урок физики в 8 классе Мир сквозь очки Криволінійний рух під дією незмінної сили тяжіння. Урок 12. Фізика. 10 клас
Криволінійний рух під дією незмінної сили тяжіння. Урок 12. Фізика. 10 клас Презентация о Потенциальной и Кинетической энергии
Презентация о Потенциальной и Кинетической энергии Механические свойства твердых тел
Механические свойства твердых тел Основы аэродинамики и динамики полёта. Занятие 1
Основы аэродинамики и динамики полёта. Занятие 1 L09 - Torques
L09 - Torques Выбор и обоснование узлов приводов робота - манипулятора для загрузочных операций
Выбор и обоснование узлов приводов робота - манипулятора для загрузочных операций Траекторные измерения
Траекторные измерения Презентация Использование Использование Excel
Презентация Использование Использование Excel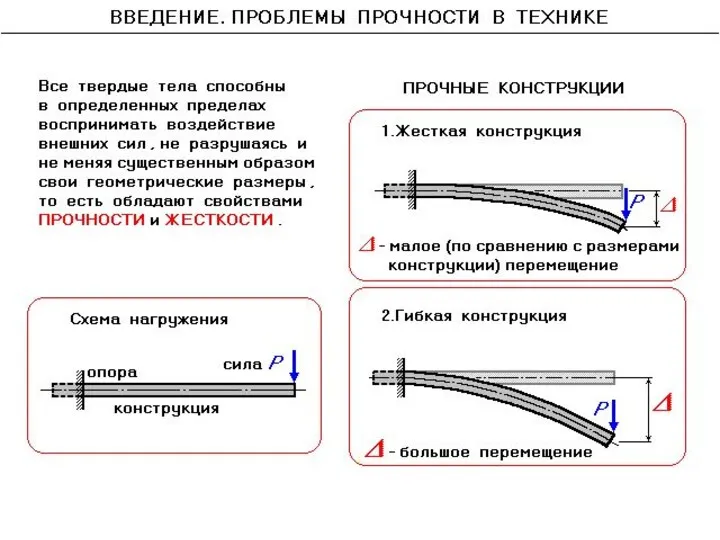 Проблемы прочности в технике
Проблемы прочности в технике Теория судна. Статика. Лекция № 1. Геометрия корпуса судна
Теория судна. Статика. Лекция № 1. Геометрия корпуса судна Методическая разработка урока в 7 классе по теме Механическое движение
Методическая разработка урока в 7 классе по теме Механическое движение Машини та обладнання для тваринництва механізація підготовки кормів до згодовування
Машини та обладнання для тваринництва механізація підготовки кормів до згодовування Решение задач. Сила Архимеда. 7 класс
Решение задач. Сила Архимеда. 7 класс Разработка установки для измерения магнитострикции
Разработка установки для измерения магнитострикции Брэйн-ринг по физике
Брэйн-ринг по физике Тракт генерирования и излучения. Общие сведения о радиопередающих устройствах. (Тема 4.1)
Тракт генерирования и излучения. Общие сведения о радиопередающих устройствах. (Тема 4.1)