Содержание
- 2. Лекция № 1 1. Состояние термодинамического равно- весия. Температура. 2. Модель идеального газа. Давление. Абсолютная температура.
- 3. СТАТИСТИЧЕСКИЙ И ТЕРМО- ДИНАМИЧЕСКИЙ МЕТОДЫ Существуют два способа описания процессов, происхо- дящих в макроскопических телах (телах,
- 5. ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМА. ПАРАМЕТРЫ СОСТОЯНИЯ Термодинамической системой называется совокупность макроскопических тел, которые могут обмениваться энер- гией между
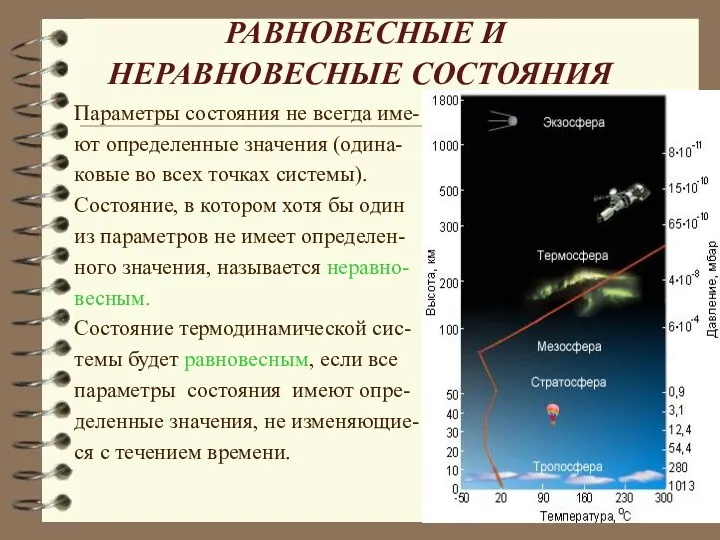
- 6. РАВНОВЕСНЫЕ И НЕРАВНОВЕСНЫЕ СОСТОЯНИЯ Параметры состояния не всегда име- ют определенные значения (одина- ковые во всех
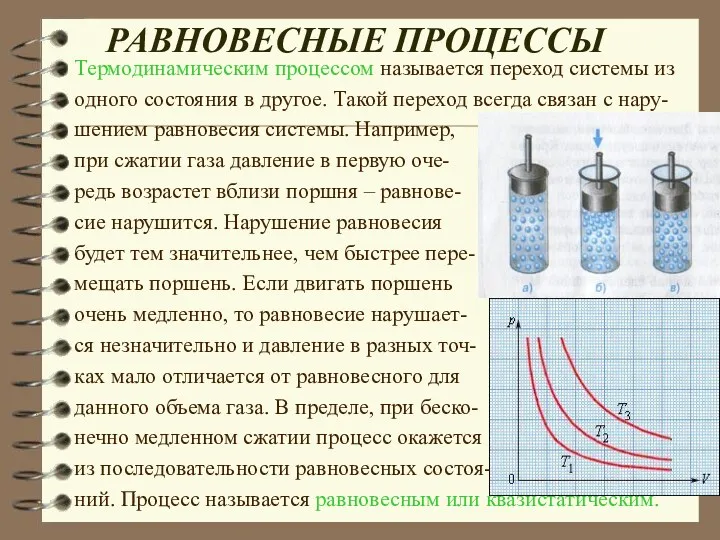
- 7. РАВНОВЕСНЫЕ ПРОЦЕССЫ Термодинамическим процессом называется переход системы из одного состояния в другое. Такой переход всегда связан
- 8. Состояние термодинамической системы, не изменяющееся во времени и не сопровожда-ющееся переносом через систему вещества или энергии,
- 9. ТЕМПЕРАТУРА Если два тела находятся в состоянии термодина- мического равновесия, то есть не обмениваются энергией путем
- 10. В физике и технике за абсолютную шкалу температур принята шкала Кельвина, названная в честь знаменитого английского
- 11. Абсолютная температура Т не может быть отрицательной величиной. Своеобразие температуры заключается в том, что она не
- 12. Модель идеального газа Абстрактная модель, отражающая существенные черты явления, аналогичная материальной точке. 1. Молекулы (или атомы)
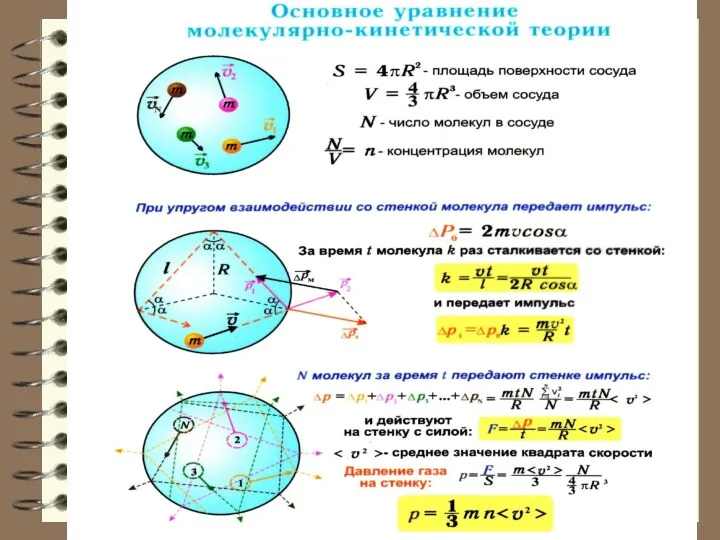
- 13. Давление. Основное уравнение молекулярно-кинетической теории Рассмотрим подробнее, что представляет собой один из основных параметров состояния –
- 14. Находящиеся под давлением газ или жидкость действуют с некоторой силой на любую поверхность, ограничивающую их объем.
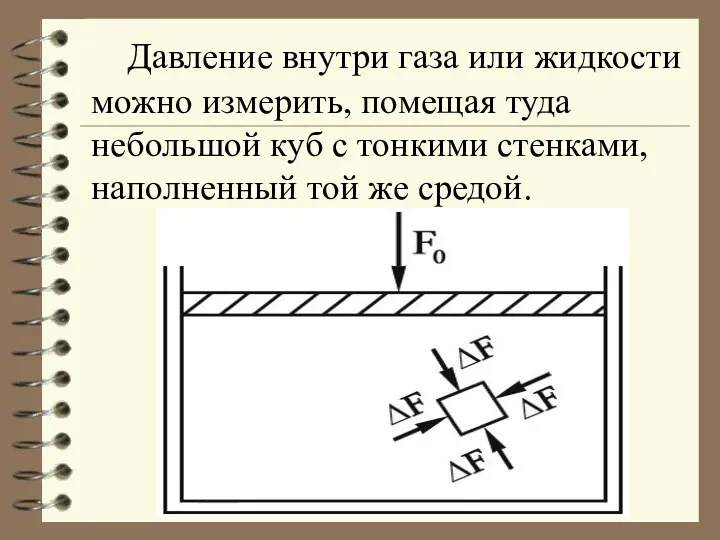
- 15. Давление внутри газа или жидкости можно измерить, помещая туда небольшой куб с тонкими стенками, наполненный той
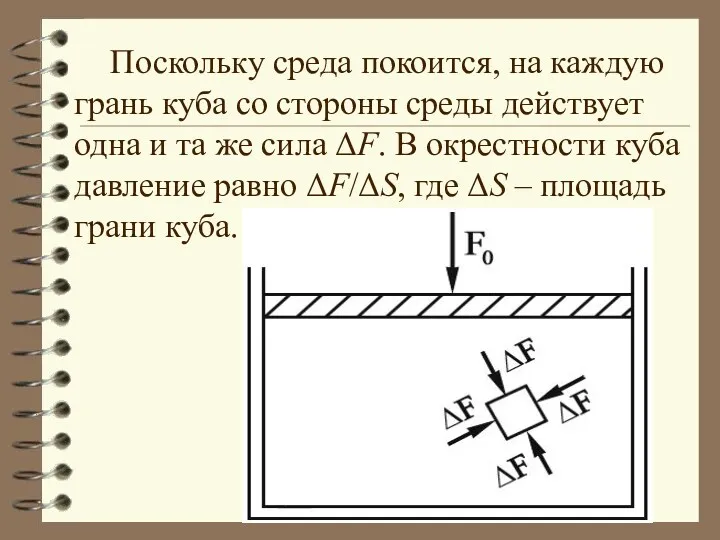
- 16. Поскольку среда покоится, на каждую грань куба со стороны среды действует одна и та же сила
- 17. Внутреннее давление является одним и тем же во всех направлениях, и, во всем объеме независимо от
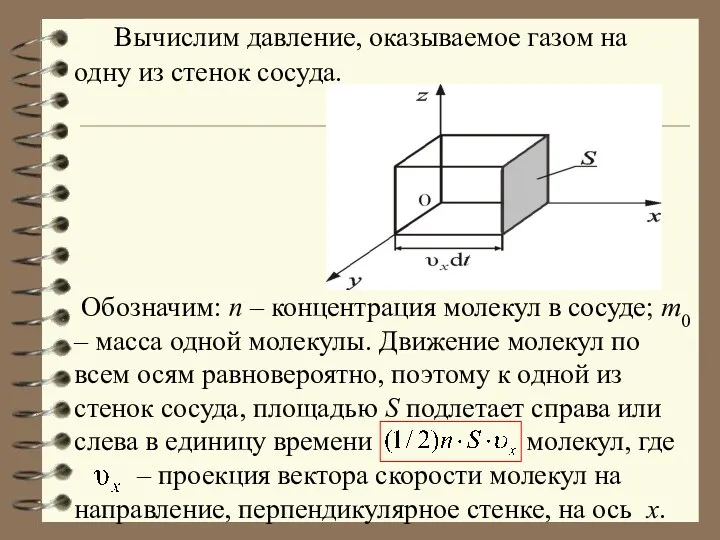
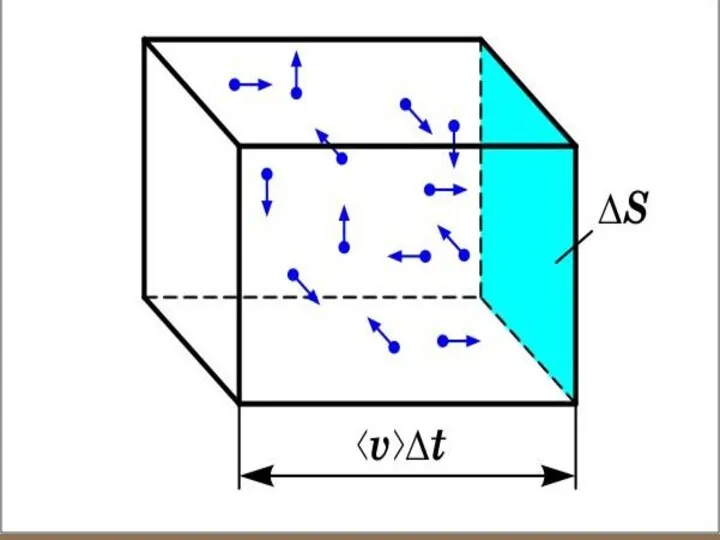
- 18. Вычислим давление, оказываемое газом на одну из стенок сосуда. Обозначим: n – концентрация молекул в сосуде;
- 20. Каждая молекула обладает импульсом m0υx, но стенка получает импульс (при абсолютно-упругом ударе ). За время dt
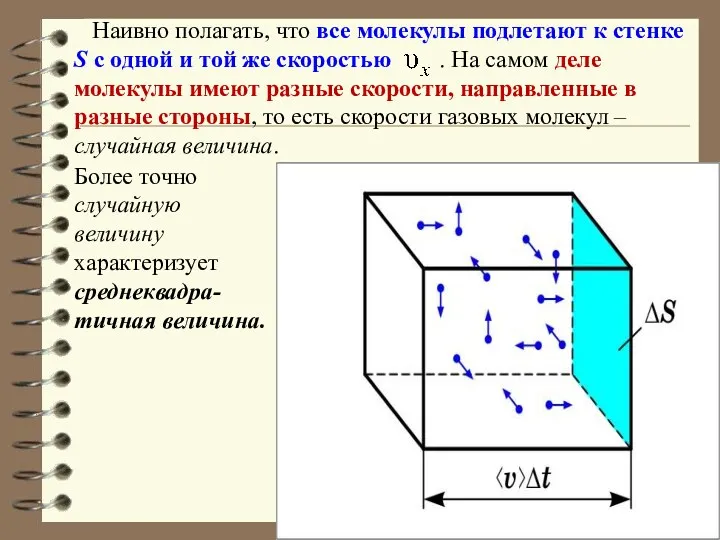
- 21. Наивно полагать, что все молекулы подлетают к стенке S с одной и той же скоростью .
- 22. Под скоростью понимаем среднеквадратичную скорость Вектор скорости, направленный произвольно в пространстве, можно разделить на три составляющих:
- 23. Следовательно, на другие стенки будет точно такое же давление. Тогда можно записать в общем случае, заменяя
- 25. Единицы измерения давления. По определению, поэтому размерность давления 1 Н/м2 = 1 Па; 1 атм.=760 мм
- 26. Чтобы связать энергию с температурой, Больцман ввел коэффициент пропорциональ-ности k, который впоследствии был назван его именем:
- 27. Величину T называют абсолютной температурой и измеряют в градусах Кельвина (К). Она служит мерой кинети-ческой энергии
- 28. Тогдa для NA частиц идеального газа: следовательно, – это формула кинетической энергии для молярной массы газа.
- 29. Основное уравнение молекулярно-кинетической теории можно записать по другом Т.к. Отсюда: В таком виде основное уравнение молекулярно-кинетической
- 30. Из уравнения , зная, что в объёме V содержится N частиц и концен- трация их n
- 31. Основные законы идеального газа В XVII – XIX веках были сформулированы опытные законы идеальных газов, которые
- 32. 1.Изохорический процесс. V = const. Изохорическим процессом называется процесс, протекающий при постоянном объёме V. Поведение газа
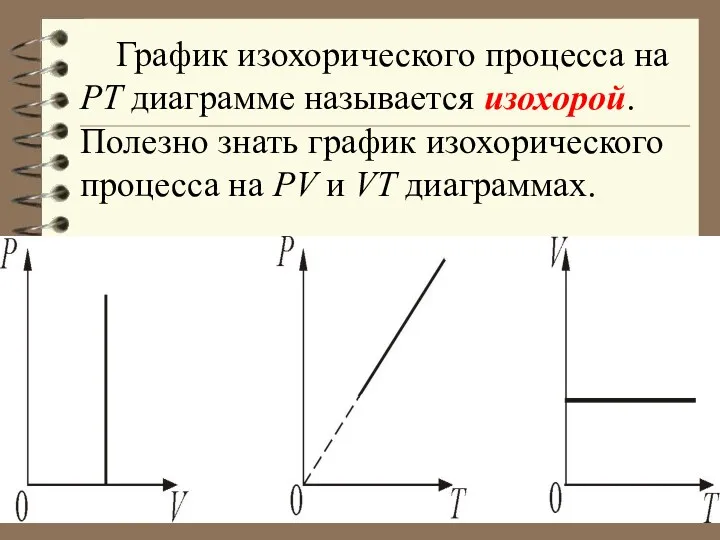
- 33. График изохорического процесса на РТ диаграмме называется изохорой. Полезно знать график изохорического процесса на РV и
- 34. 2. Изобарический процесс. Р = const. Изобарическим процессом называется процесс, протекающий при постоянном давлении Р. Поведение
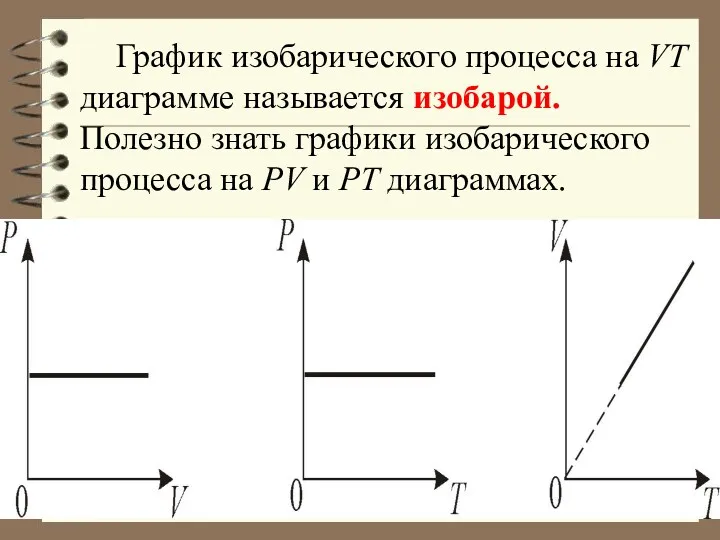
- 35. График изобарического процесса на VT диаграмме называется изобарой. Полезно знать графики изобарического процесса на РV и
- 36. 3. Изотермический процесс. T = const. Изотермическим процессом называется процесс, протекающий при постоянной температуре Т. Поведение
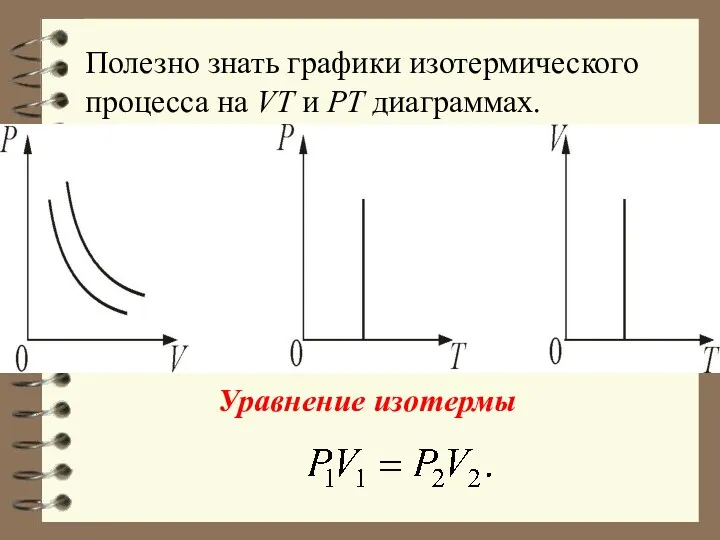
- 37. Полезно знать графики изотермического процесса на VT и РT диаграммах. Уравнение изотермы
- 38. 4. Адиабатический процесс (изоэнтропийный). Процесс, происходящий без теплообмена с окружающей средой. 5. Политропический процесс. Процесс, при
- 39. 6. Закон Авогадро. При одинаковых давлениях и одинаковых температурах, в равных объёмах различных идеальных газов содержится
- 40. 7. Закон Дальтона. Давление смеси идеальных газов равно сумме парциальных давлений Р, входящих в неё газов
- 41. 8. Объединённый газовый закон (Закон Клапейрона). В соответствии с законами Бойля - Мариотта и Гей-Люссака можно
- 42. Менделеев объединил известные нам законы Бойля-Мариотта, Гей-Люссака и Шарля с законом Авогадро. Уравнение, связывающее все эти
- 43. Если обозначим – плотность газа, то Если рассматривать смесь газов, заполняющих объём V при температуре Т,
- 45. Скачать презентацию































 Двигатели внутреннего сгорания
Двигатели внутреннего сгорания Отделка изделий из металла
Отделка изделий из металла Презентация к уроку развивающего обучения Простые механизмы часть 2
Презентация к уроку развивающего обучения Простые механизмы часть 2 Технология слесарных и слесарно-сборочных работ
Технология слесарных и слесарно-сборочных работ Рост наноструктур и микроскопия. Методы выращивания наноструктур
Рост наноструктур и микроскопия. Методы выращивания наноструктур Динамика кулисного механизма
Динамика кулисного механизма Alternating current. (Lecture 3)
Alternating current. (Lecture 3) Intelligent energy storage
Intelligent energy storage Электростатическое поле в вакууме
Электростатическое поле в вакууме Реальный газ и его работа. (лекция 5в)
Реальный газ и его работа. (лекция 5в) Роботизированная коробка передач DSG
Роботизированная коробка передач DSG Аккумуляторы для крупномасштабного хранения энергии. Лекция 8
Аккумуляторы для крупномасштабного хранения энергии. Лекция 8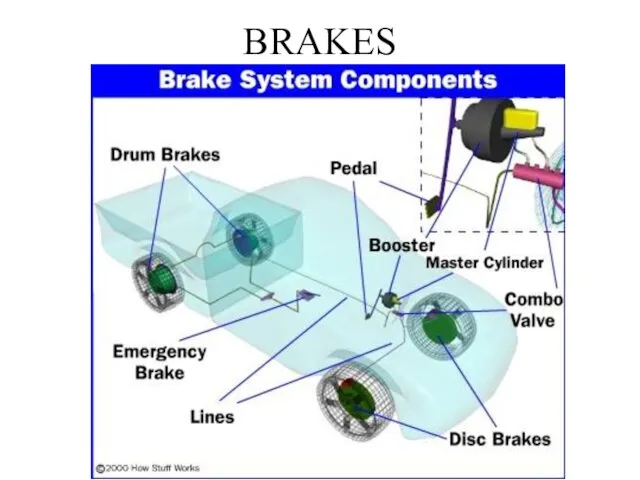 Brakes. Brake System Components
Brakes. Brake System Components разработка технологического процесса на механическую обработку детали фланец
разработка технологического процесса на механическую обработку детали фланец Подшипники. Смазочные материалы
Подшипники. Смазочные материалы Как можно обрабатывать заготовки из древесины, имеющие цилиндрическую форму. Устройство токарного станка по дереву
Как можно обрабатывать заготовки из древесины, имеющие цилиндрическую форму. Устройство токарного станка по дереву Всероссийский турнир юных физиков. Катание на диске
Всероссийский турнир юных физиков. Катание на диске Макросистема (термодинамическая система)
Макросистема (термодинамическая система)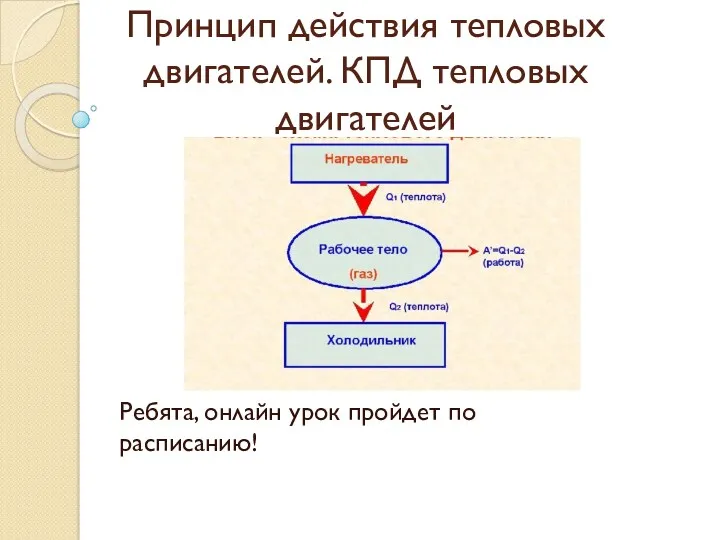 Принцип действия тепловых двигателей. КПД тепловых двигателей
Принцип действия тепловых двигателей. КПД тепловых двигателей Притяжение Земли
Притяжение Земли Шкала электромагнитных волн.
Шкала электромагнитных волн. Теории прочности
Теории прочности Виды эксплуатационных разрушений и причины их возникновения
Виды эксплуатационных разрушений и причины их возникновения Электрический ток в электролитах
Электрический ток в электролитах Урок с презентацией Рентгеновские лучи
Урок с презентацией Рентгеновские лучи Спектроскопические методы анализа. Методы атомной и молекулярной спектроскопии
Спектроскопические методы анализа. Методы атомной и молекулярной спектроскопии Проект урока по теме Звуковые волны 9 класс
Проект урока по теме Звуковые волны 9 класс Решение нестандартных задач по физике
Решение нестандартных задач по физике