Содержание
- 2. Изучить закон сохранения энергии, распространённый на тепловые явления – первый закон термодинамики. Рассмотреть изопроцессы в газах
- 3. Фронтальный опрос 1. Дать определение внутренней энергии. 2.Что называют количеством теплоты? Повторение 3 .Что называют вечным
- 4. Содержание 1-ого закона термодинамики Применение 1-ого закона термодинамики к изопроцессам в газах Адиабатический процесс Необратимость процессов
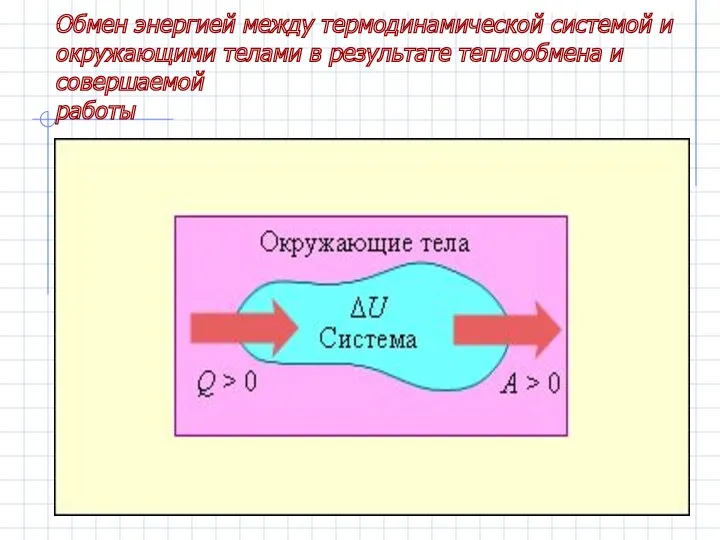
- 5. Обмен энергией между термодинамической системой и окружающими телами в результате теплообмена и совершаемой работы
- 6. Изменение Δ U внутренней энергии системы при переходе ее из одного состояния в другое равно сумме
- 7. Q = ΔU + A’ Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и
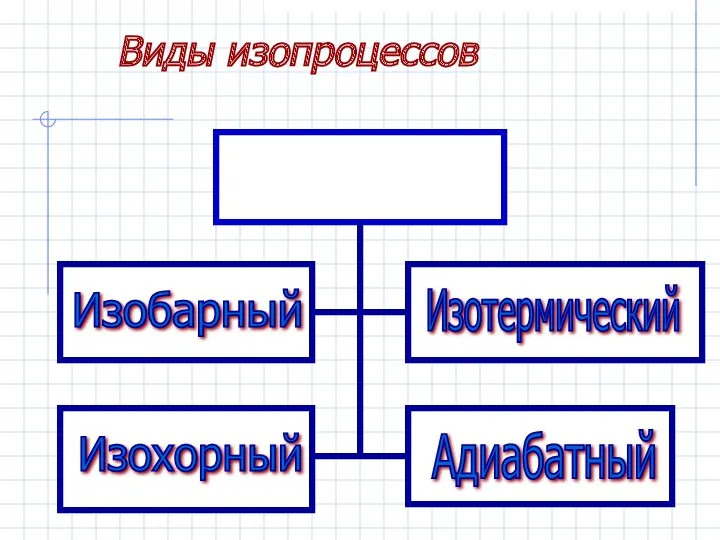
- 8. Виды изопроцессов Изопроцессы Изобарный Изохорный Изотермический Адиабатный
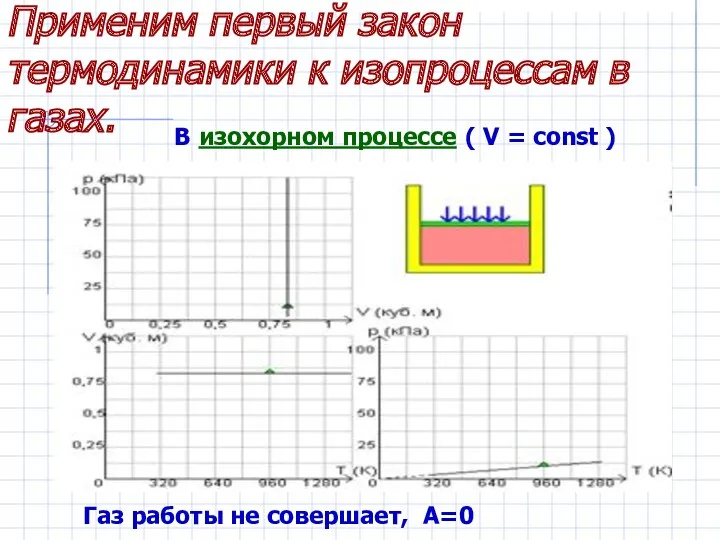
- 9. Применим первый закон термодинамики к изопроцессам в газах. В изохорном процессе ( V = const )
- 10. Здесь U (T1) и U (T2) – внутренние энергии газа в начальном и конечном состояниях. Q
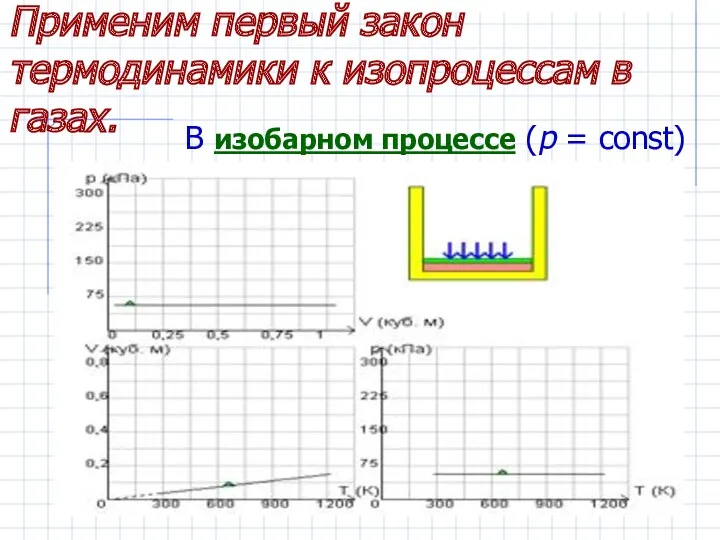
- 11. Применим первый закон термодинамики к изопроцессам в газах. В изобарном процессе (p = const)
- 12. Работа, совершаемая газом, выражается соотношением A=p(V2 – V1)=pΔV p-давление V1,V2- объем в начальном и конечном состояниях
- 13. Применим первый закон термодинамики к изопроцессам в газах. Первый закон термодинамики для изобарного процесса : Q
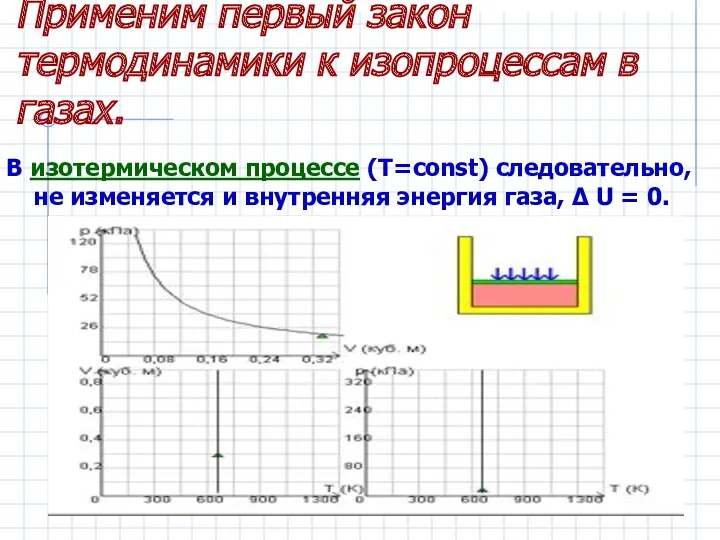
- 14. Применим первый закон термодинамики к изопроцессам в газах. В изотермическом процессе (T=const) следовательно, не изменяется и
- 15. Первый закон термодинамики для изотермического процесса выражается соотношением Q = A’ Количество теплоты Q, полученной газом
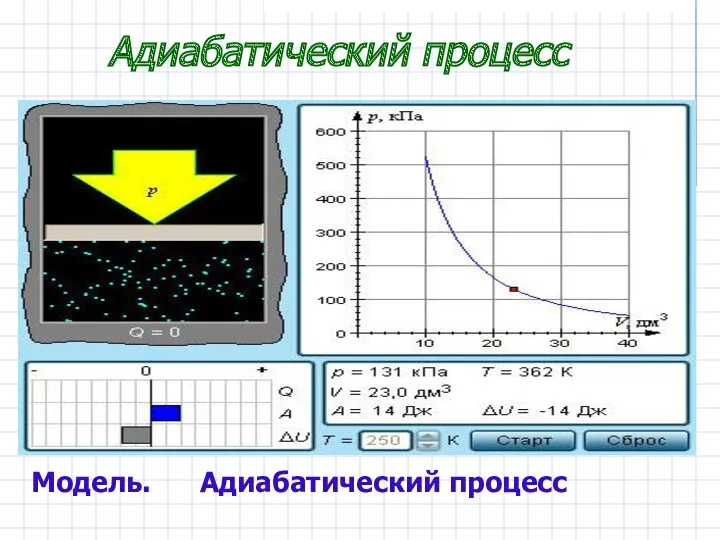
- 16. Адиабатический процесс Модель. Адиабатический процесс
- 17. В адиабатическом процессе Q = 0; поэтому первый закон термодинамики принимает вид газ совершает работу за
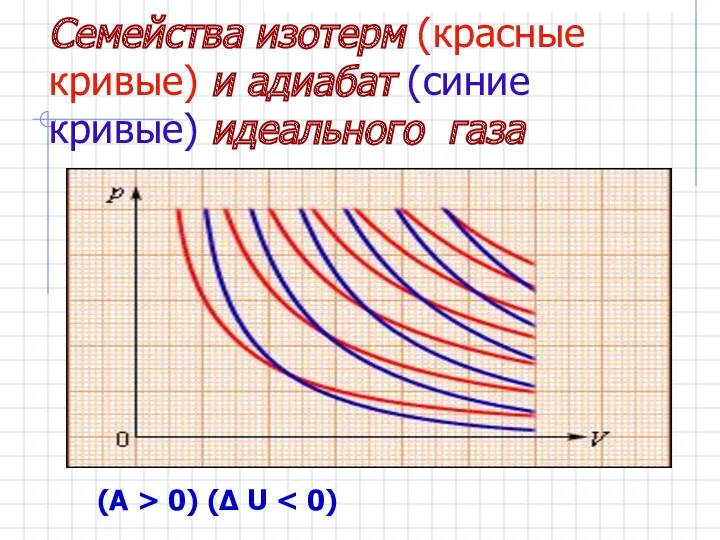
- 18. Семейства изотерм (красные кривые) и адиабат (синие кривые) идеального газа (A > 0) (Δ U
- 19. Работа газа в адиабатическом процессе просто выражается через температуры T 1 и T 2 начального и
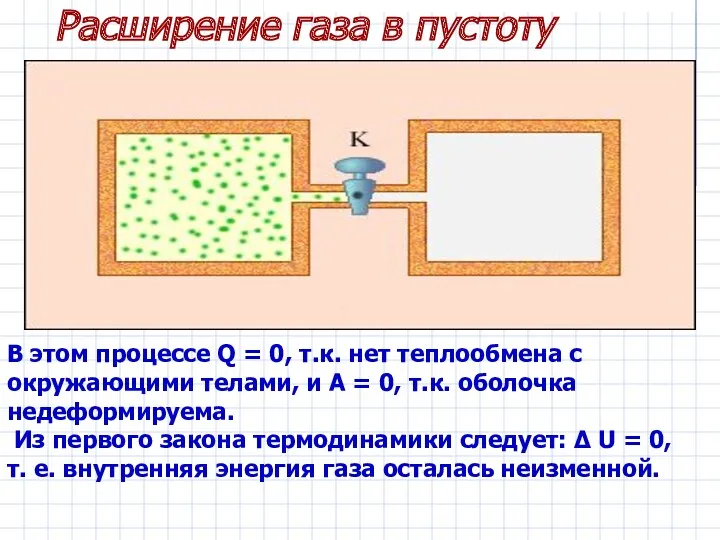
- 20. Расширение газа в пустоту В этом процессе Q = 0, т.к. нет теплообмена с окружающими телами,
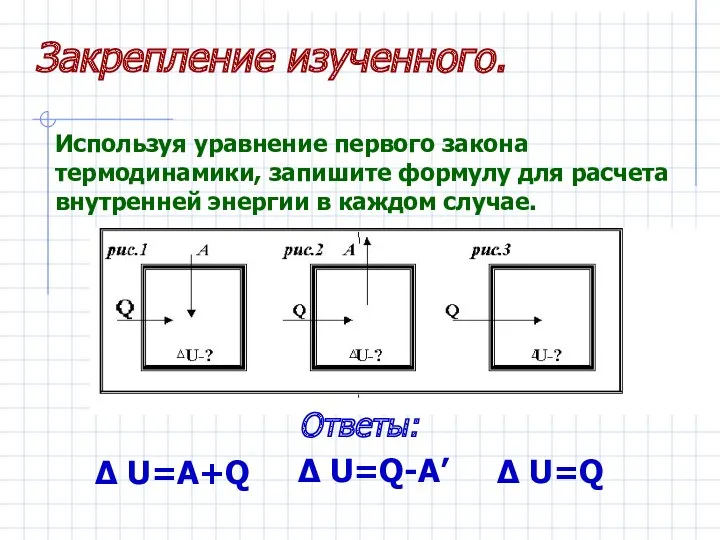
- 21. Δ U=A+Q Δ U=Q Δ U=Q-A’ Используя уравнение первого закона термодинамики, запишите формулу для расчета внутренней
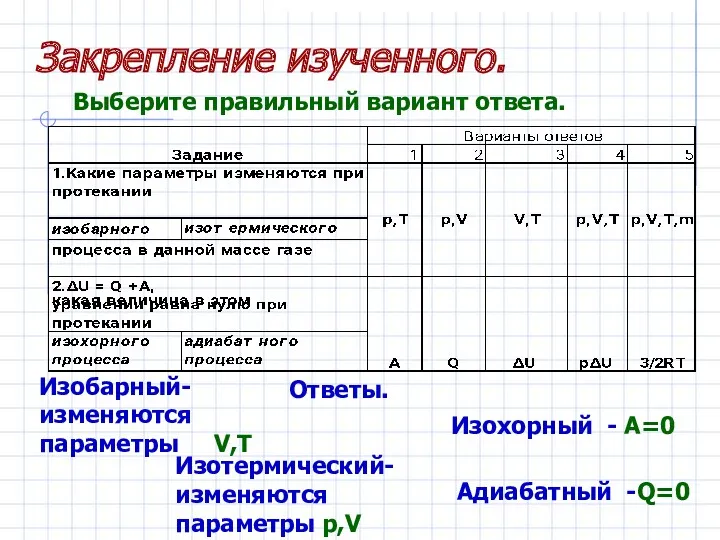
- 22. Ответы. Изобарный- изменяются параметры V,T Изотермический-изменяются параметры p,V Изохорный - A=0 Адиабатный -Q=0 Выберите правильный вариант
- 23. Обратимые и необратимые процессы. Необратимость тепловых процессов. Второй закон термодинамики
- 25. Домашнее задание Параграф 81, вопросы
- 26. Закон сохранения энергии утверждает, что количество энергии при любых ее превращениях остается неизменным. Между тем многие
- 27. Из первого закона термодинамики направленность и тем самым необратимость тепловых процессов не вытекает. Первый закон термодинамики
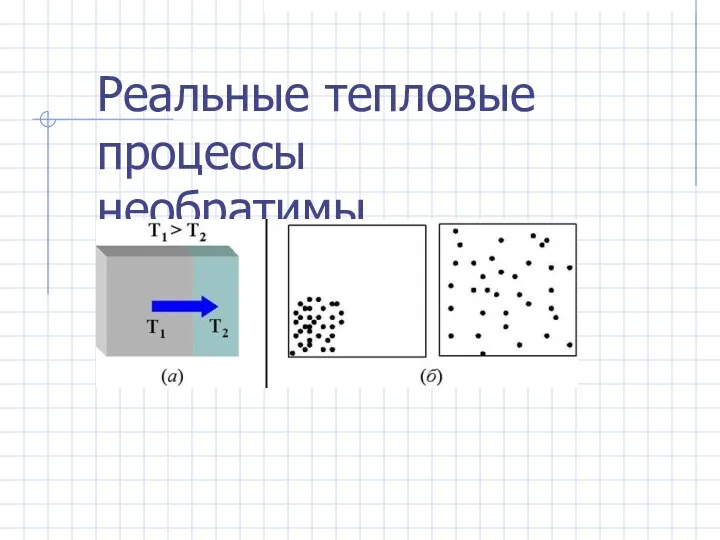
- 28. Реальные тепловые процессы необратимы.
- 30. Примеры: При диффузии выравнивание концентраций происходит самопроизвольно. Обратный же процесс сам по себе никогда не пойдет:
- 31. Теплообмен, как показывает опыт, также является односторонне направленным процессом. В результате теплообмена энергия передается сама по
- 32. Необратимым является также процесс превращения механической энергии во внутреннюю при неупругом ударе или при трении.
- 34. Существуют несколько формулировок второго закона термодинамики. Одна из них принадлежит немецкому учёному Р. Клаузису – «Невозможен
- 36. Вечный двигатель первого рода — непрерывно или периодически действующая машина, которая совершала бы работу, большую подводимой
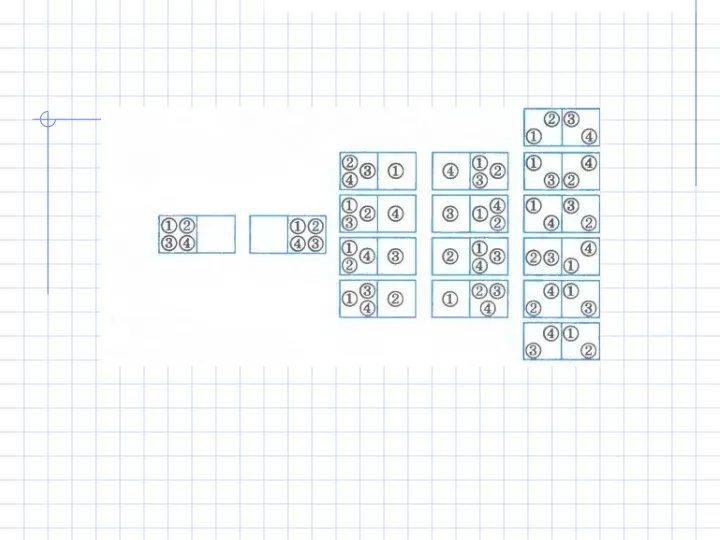
- 37. Статистическое истолкование необратимости процессов в природе Пронумеруем молекулы цифрами 1, 2, 3, 4. Возможны 16 различных
- 39. Молекулы идеального газа движутся практически независимо друг от друга. Для одной молекулы вероятность того, что она
- 40. Но если взять реальное число молекул газа в 1 см3 при нормальных условиях (n=3•1019), то вероятность
- 41. Необратимость процессов в природе связана со стремлением систем к переходу в наиболее вероятное состояние, которому отвечает
- 42. Принципы действия тепловых двигателей. КПД тепловых двигателей
- 43. ЦЕЛИ УРОКА: 1.Сформировать понятие о физических принципах действия тепловых двигателей. 2.Познакомить учащихся с важнейшими направлениями применения
- 44. Вращайтесь, мощные колеса, Свистите, длинные ремни, Горите свыше, впрямь и косо, Над взмахами валов, огни! Пуды,
- 45. ЧТО ТАКОЕ ТЕПЛОВОЙ ДВИГАТЕЛЬ? Тепловой двигатель – это устройство, преобразующее внутреннюю энергию топлива в механическую энергию.
- 46. ВИДЫ ТЕПЛОВЫХ ДВИГАТЕЛЕЙ:
- 47. ИСТОРИЯ СОЗДАНИЯ ТЕПЛОВОГО ДВИГАТЕЛЯ. 1690 – пароатмосферная машина Д.Папена 1705 - пароатмосферная машина Т.Ньюкомена для подъема
- 48. В апреле 1763 г. Ползунов демонстрировал работу огнедействующей машины «для заводских нужд»
- 49. В 1781 г. Джеймс Уатт получил патент на изобретение второй модели своей машины. В 1782 г.
- 50. К 1863 году был готов первый образец атмосферного газового двигателя с поршнем от авиационного мотора и
- 51. 1878 – 1888 гг. Рудольф Дизель работает над созданием двигателя принципиально новой конструкции. В голову ему
- 52. УСТРОЙСТВО ТЕПЛОВОГО ДВИГАТЕЛЯ Три основных элемента любого теплового двигателя: 1.Нагреватель, сообщающий энергию рабочему телу. 2. Рабочее
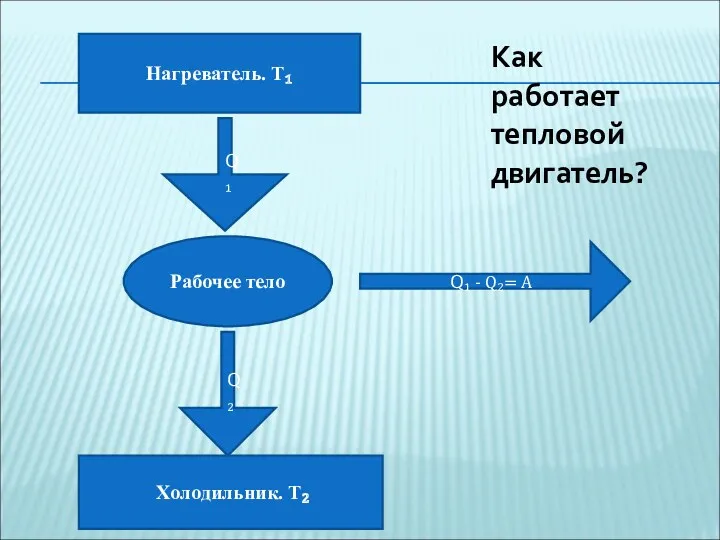
- 53. ПРИНЦИП ДЕЙСТВИЯ ТЕПЛОВОГО ДВИГАТЕЛЯ Принцип действия теплового двигателя основан на свойстве газа или пара при расширении
- 54. Нагреватель. T₁ Холодильник. T₂ Рабочее тело Q₁ Q₂ Q₁ - Q₂= A Как работает тепловой двигатель?
- 55. КПД ТЕПЛОВОГО ДВИГАТЕЛЯ. Коэффициент полезного действия теплового двигателя (КПД) – отношение работы, совершаемой двигателем за цикл,
- 56. КПД ТЕПЛОВЫХ ДВИГАТЕЛЕЙ
- 57. Карно Никола Леонард Сади (1796-1832 г.)- французский физик и инженер. Свои исследования он изложил в сочинении
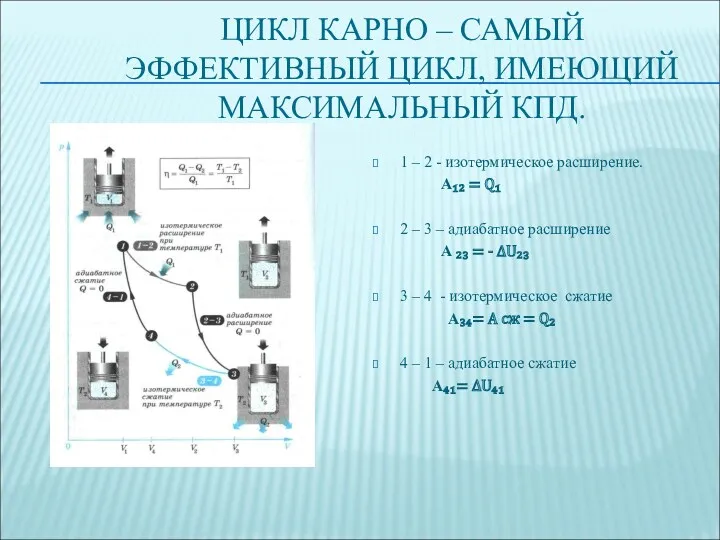
- 58. ЦИКЛ КАРНО – САМЫЙ ЭФФЕКТИВНЫЙ ЦИКЛ, ИМЕЮЩИЙ МАКСИМАЛЬНЫЙ КПД. 1 – 2 - изотермическое расширение. А₁₂
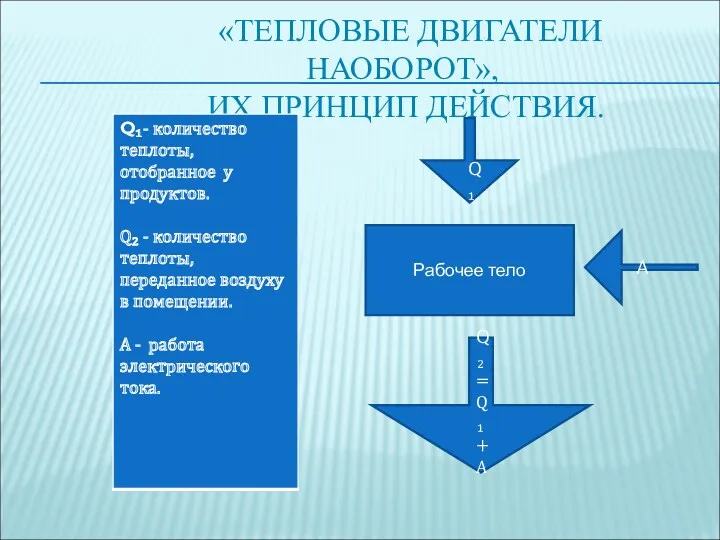
- 59. «ТЕПЛОВЫЕ ДВИГАТЕЛИ НАОБОРОТ». «Тепловые двигатели наоборот» это : холодильник, кондиционер и тепловой насос. В них происходит
- 60. «ТЕПЛОВЫЕ ДВИГАТЕЛИ НАОБОРОТ», ИХ ПРИНЦИП ДЕЙСТВИЯ. Рабочее тело Q₁ A Q₂=Q₁+A
- 61. ТЕПЛОВЫЕ ДВИГАТЕЛИ В НАРОДНОМ ХОЗЯЙСТВЕ. Тепловые двигатели – необходимый атрибут современной цивилизации. С их помощью вырабатывается
- 62. ВОДНЫЙ ТРАНСПОРТ. Первый практически пригодный пароход построен в 1807 году Фультоном. (амер) Первый российский пароход «Елизавета»
- 63. ЖЕЛЕЗНОДОРОЖНЫЙ ТРАНСПОРТ. В 1829 году инженер Дж. Стефенсон построил лучший для того времени паровоз «Ракета». Первый
- 64. АВТОМОБИЛЬНЫЙ ТРАНСПОРТ. Прообразом современного автомобиля считают самодвижущуюся повозку немецких механиков Г.Даймлера и Бенца. В 1883 году
- 65. АВИАЦИОННЫЙ ТРАНСПОРТ. 17 декабря 1903 года американские изобретатели Орвил и Уилбур Райт провели испытание первого в
- 66. КОСМИЧЕСКИЙ ТРАНСПОРТ. 17 августа 1933 года в воздух поднялась на высоту около 400 м первая советская
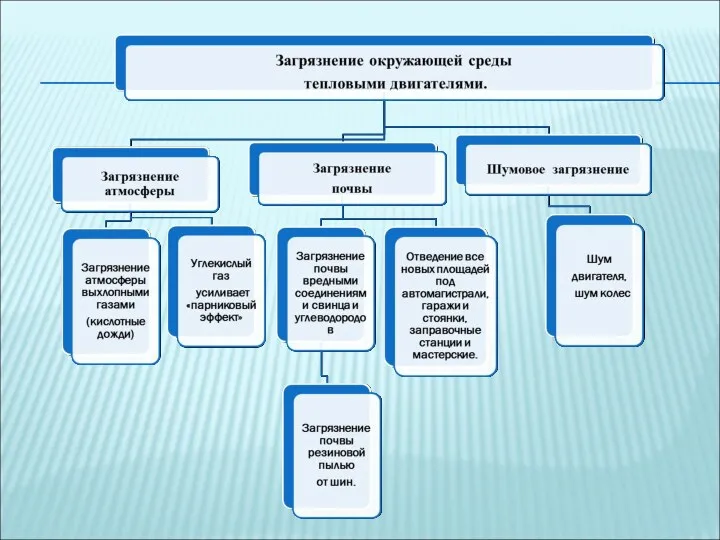
- 67. ВЛИЯНИЕ ТЕПЛОВЫХ ДВИГАТЕЛЕЙ НА ОКРУЖАЮЩУЮ СРЕДУ.
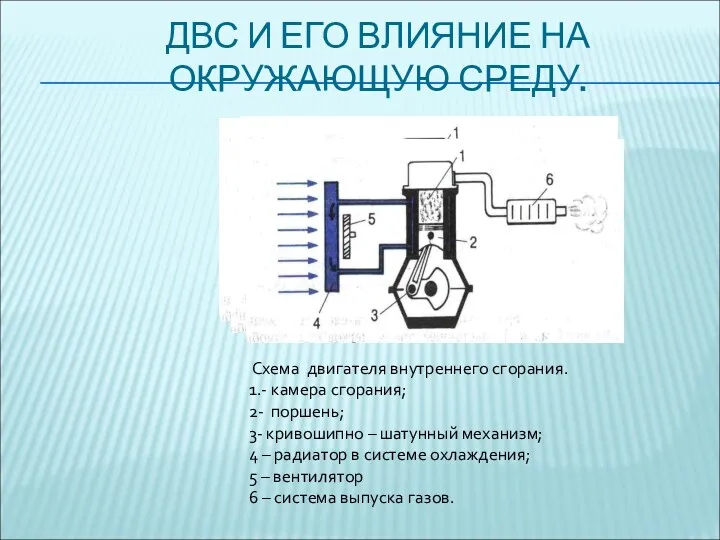
- 68. ДВС И ЕГО ВЛИЯНИЕ НА ОКРУЖАЮЩУЮ СРЕДУ. Схема двигателя внутреннего сгорания. 1.- камера сгорания; 2- поршень;
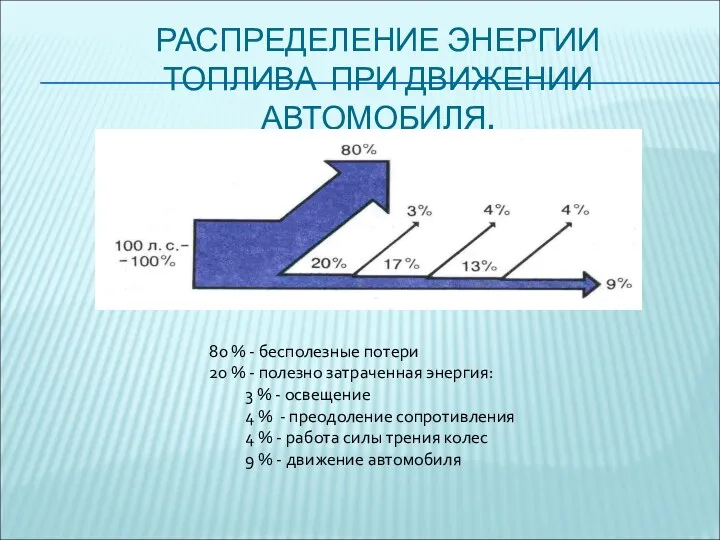
- 69. РАСПРЕДЕЛЕНИЕ ЭНЕРГИИ ТОПЛИВА ПРИ ДВИЖЕНИИ АВТОМОБИЛЯ. 80 % - бесполезные потери 20 % - полезно затраченная
- 70. «НЕЛЬЗЯ ДОПУСТИТЬ, ЧТОБЫ ЛЮДИ НАПРАВЛЯЛИ НА СОБСТВЕННОЕ УНИЧТОЖЕНИЕ ТЕ СИЛЫ ПРИРОДЫ, КОТОРЫЕ СУМЕЛИ ОТКРЫТЬ И ПОКОРИТЬ»
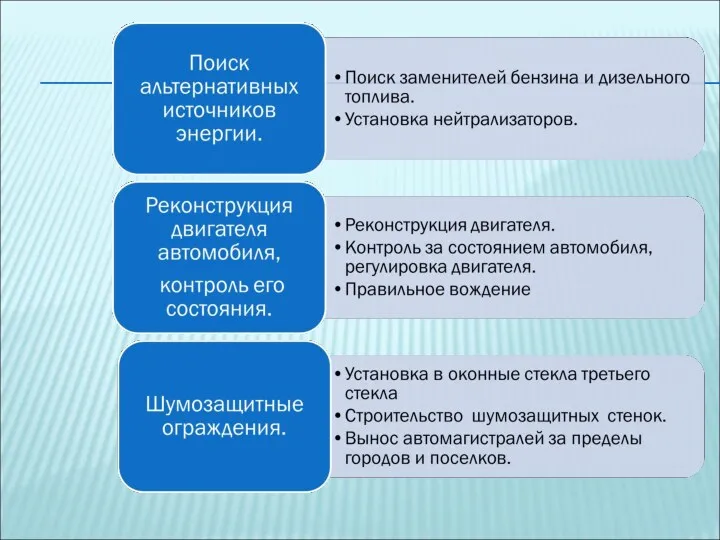
- 72. ПОВЫШЕНИЕ КПД ТЕПЛОВОГО ДВИГАТЕЛЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ.
- 74. Использование тепловых двигателей дает человеку огромные возможности и одновременно является наиболее сильным фактором разрушения природы.
- 75. ТЕСТ «ТЕРМОДИНАМИКА» 1.Тело, состоящее из атомов или молекул, обладает: 1) Кинетической энергией беспорядочного теплового движения частиц.
- 76. ТЕСТ «ТЕРМОДИНАМИКА» 2.Осуществлены три процесса теплообмена. В первом процессе тело М получило количество теплоты Q от
- 77. ТЕСТ «ТЕРМОДИНАМИКА» 3. При постоянном давлении Р объем газа увеличился на Какая величина равна произведению А.
- 78. ТЕСТ «ТЕРМОДИНАМИКА» 4. Первый закон термодинамики утверждает, что построить «вечный двигатель» невозможно. Каков смысл этого утверждения?
- 79. ТЕСТ «ТЕРМОДИНАМИКА» 5. При постоянном давлении 105 Па объем воздуха, находившегося в квартире, увеличился на 20
- 80. ТЕСТ «ТЕРМОДИНАМИКА» 6. В результате получения количества теплоты 20Дж и совершения работы внутренняя энергия идеального газа
- 81. ТЕСТ «ТЕРМОДИНАМИКА» 7. Что служит рабочим телом в двигателе автомобиля? А. Воздух. Б. Вода. В. Пары
- 82. ТЕСТ «ТЕРМОДИНАМИКА» 8. Каково максимально возможное значение КПД тепловой машины, использующей нагреватель с температурой 4270С и
- 83. «Могущество страны не только в одном материальном богатстве, но и в духе народа. Чем шире, свободнее
- 84. ОТВЕТЫ НА ТЕСТ ТЕСТ «ТЕРМОДИНАМИКА» 1-Г 2-Г 3-А 4-Б 5-Д 6-В 7-В 8-В. 1-Д 2-А 3-В
- 85. ДОМАШНЕЕ ЗАДАНИЕ Параграф 82, 83 задачи 1,3,5
- 87. Скачать презентацию

































































 Электрическая лампа накаливания. (6 класс)
Электрическая лампа накаливания. (6 класс) Термодинамика биологических процессов
Термодинамика биологических процессов “Движение тел. Материальная точка”
“Движение тел. Материальная точка” Iсторiя розвитку машин та механiзмiв
Iсторiя розвитку машин та механiзмiв Интерактивный урок Эксплуатация и ремонт. Возможные неисправности топливораздаточных колонок и способы их устранения
Интерактивный урок Эксплуатация и ремонт. Возможные неисправности топливораздаточных колонок и способы их устранения Механические волны. Виды волн
Механические волны. Виды волн Принцип действия циклона
Принцип действия циклона Путь к звездам
Путь к звездам Тракт приема радиолокационной информации. Сведения о радиоприемных устройствах. (Тема 5.1)
Тракт приема радиолокационной информации. Сведения о радиоприемных устройствах. (Тема 5.1) презентация на тему: Строение атома
презентация на тему: Строение атома Строительные машины. Контрольная работа
Строительные машины. Контрольная работа Опоры валов и осей
Опоры валов и осей Особенности получения метапредметных результатов на уроках физики и внеурочной деятельности
Особенности получения метапредметных результатов на уроках физики и внеурочной деятельности Элементы машиноведения. Машины
Элементы машиноведения. Машины Колесные пары тепловозов
Колесные пары тепловозов Физико-химические методы анализа
Физико-химические методы анализа Скорость движения жидкости как сплошной среды
Скорость движения жидкости как сплошной среды Общие сведения о колебаниях. Тема 1
Общие сведения о колебаниях. Тема 1 Потенциал и работа электростатического поля. Связь напряженности с потенциалом
Потенциал и работа электростатического поля. Связь напряженности с потенциалом Монтаж гидрогенератора
Монтаж гидрогенератора Перемещение при прямолинейном движении
Перемещение при прямолинейном движении Экологические проблемы теплоэнергетики
Экологические проблемы теплоэнергетики Опыт Резерфорда
Опыт Резерфорда Зонная теория твёрдых тел
Зонная теория твёрдых тел Линзы. Ход лучей в линзе
Линзы. Ход лучей в линзе Сварные и паяные соединения
Сварные и паяные соединения Линейные цепи при несинусоидальных периодических токах
Линейные цепи при несинусоидальных периодических токах Ядерная модель атома. Квантовые постулаты Бора
Ядерная модель атома. Квантовые постулаты Бора