Содержание
- 2. Электрохимической коррозией называется самопроизвольный процесс разрушения металлов под действием электролитов , при котором окисление металла и
- 3. ЭРаспространеннррррр Электролит – любая электропроводящая жидкость. В строительной практике это вода и любые водные растворы и
- 4. Электрохимическая коррозия встречается повсеместно (атмосферная, подводная, грунтовая коррозии). Возникает вопрос: как возникают на поверхности металле две
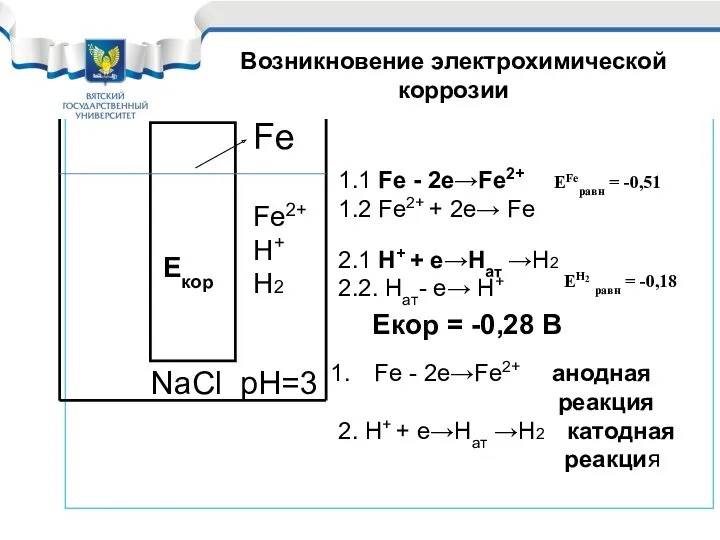
- 5. Fe - 2e→Fe2+ анодная реакция 2. H+ + e→Haт →Н2 катодная реакция NaCl рН=3 Fe Fe2+
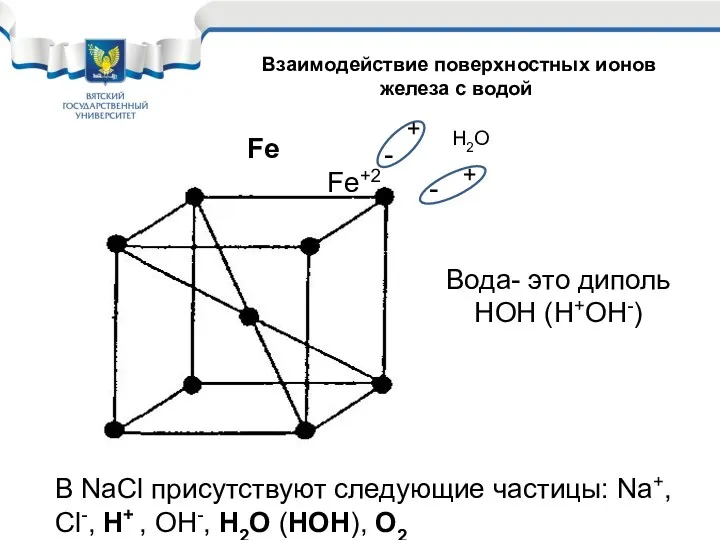
- 6. - + Fe Fe+2 Взаимодействие поверхностных ионов железа с водой Вода- это диполь НОН (Н+ОН-) -
- 7. Екор – потенциал коррозии, образующийся за счёт одновременного протекания на нём двух электрохимических реакций очень важное
- 8. Коррозионный потенциал возникает всегда когда выполняется термодинамическое условие электрохимической коррозии Термодинамическое условие: потенциал корродирующего металла должен
- 9. Насколько часто выполняется термодинамическое условие электрохимической коррозии? ЕMeравн В обычной воде есть следующие виды молекул и
- 10. Al Zn Fe Ni H2 Cu Ag O2 -1,5 -0,79 -0,44 -0,23 0 +0,34 1,23 Ряд
- 11. Растворенный в электролите кислород самый распространенный окислитель О2 + 4Н+ + 4е 2Н2О (кислая среда) или
- 12. Ион водорода или вода также могут вызывать электрохимическую коррозию 2Н+ + 2е 2Нат Н2 (кислая среда)
- 13. Me - ne Катионы Меne+ Комплексные соединения [Ме(Кn)]m+, [Ме(Кn)]m- Оксиды и гидроксиды МеО, Ме(ОН)2 Сложные анионы
- 14. Наиболее опасен для практики случай, когда получаются растворимые продукты коррозии Гидратированные катионы Сложные анионы металла Комплексные
- 15. Если в результате анодной реакции коррозионного процесса получаются нерастворимые продукты коррозии: оксиды, гидроксиды, трудностворимые соли, то
- 16. Если продукты коррозии получаются рыхлые не упорядоченные (например, ржавчина на железе), то такие продукты мало тормозят
- 17. Состояние повышенной коррозионной стойкости металла, вызванное торможением анодного процесса за счет образования упорядоченных оксидных, гидроксидных и
- 18. Электрохимическая коррозия чаще всего протекает локально, т.е. анодная и катодная реакции коррозионного процесса протекают на разных
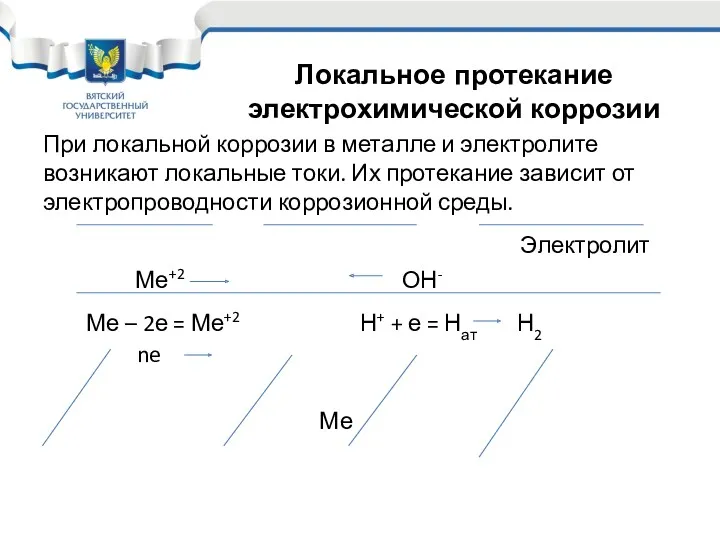
- 19. При локальной коррозии в металле и электролите возникают локальные токи. Их протекание зависит от электропроводности коррозионной
- 20. Возникает всегда, когда на поверхности металла появляется электролит; Протекает в виде двух сопряженных электрохимических реакций; На
- 21. В строительной практике электрохимическая коррозия чаще всего протекает по действием двух окислителей иона водорода или воды:
- 22. Особенности коррозии с водородной деполяризацией Сопровождается выделением атомарного водорода Нат , который проникая вглубь металла, вызывает
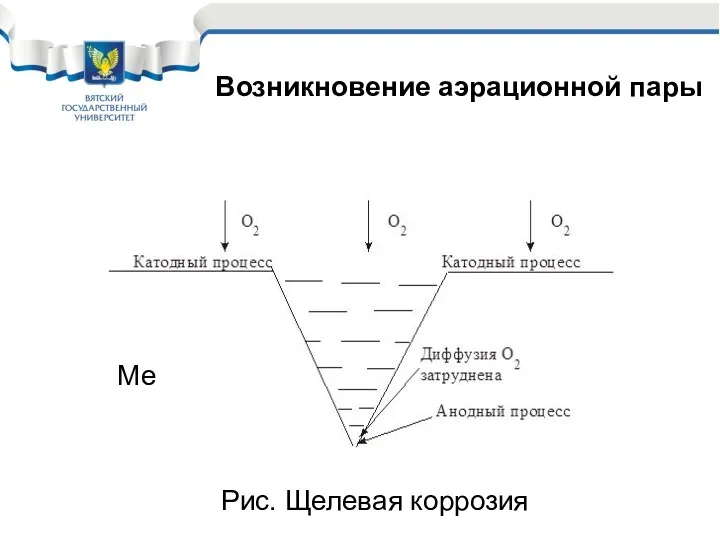
- 23. Особенности коррозии с кислородной деполяризацией Растворимость кислорода в электролитах не велика, поэтому диффузия его к корродирующему
- 24. Возникновение аэрационной пары Рис. Щелевая коррозия Ме
- 25. Чтобы проанализировать коррозионную ситуацию и оценить опасность коррозии необходимо выяснить: Какие катодные реакции идут на поверхности
- 26. Исходя из состава коррозионной среды прежде всего определяется, какие окислители в ней присутствуют. Их как минимум
- 27. Далее необходимо сравнить стационарный потенциал коррозии (Екор) с равновесными потенциалами этих окислителей (Еохравн). Если выполняется соотношение
- 28. Равновесные потенциалы окислителей (Н+ и О2) при известном рН коррозионной среды рассчитываются по уравнениям: ЕН2равн= -
- 29. Пример: Если потенциал коррозии Екор равен - 0,2 В, а рН среды разная (2, 7,12) то
- 30. Для определения пути реакции коррозионного процесса нужно знать состав коррозионной среды. Если в составе коррозионной среды
- 31. Если в коррозионной среде нет комплексообразователей, и анионов, способных образовывать с корродирующим металлом труднорастворимую соль, то
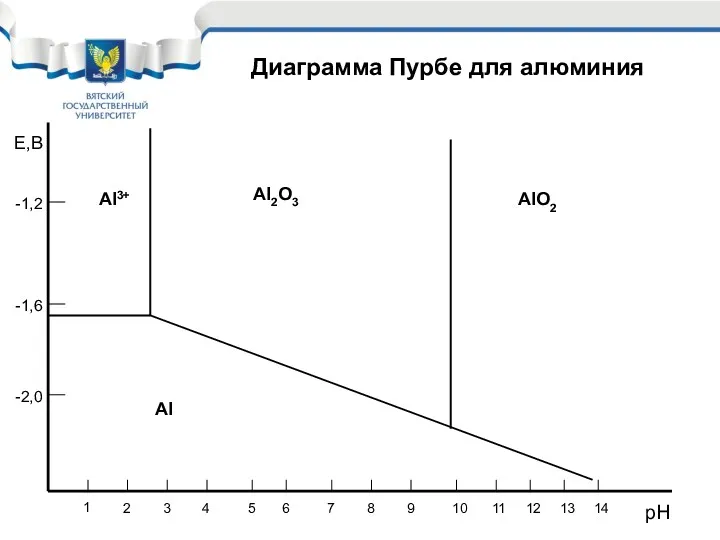
- 32. 7 2 3 4 1 6 5 9 8 11 10 13 12 рН 14 Е,В
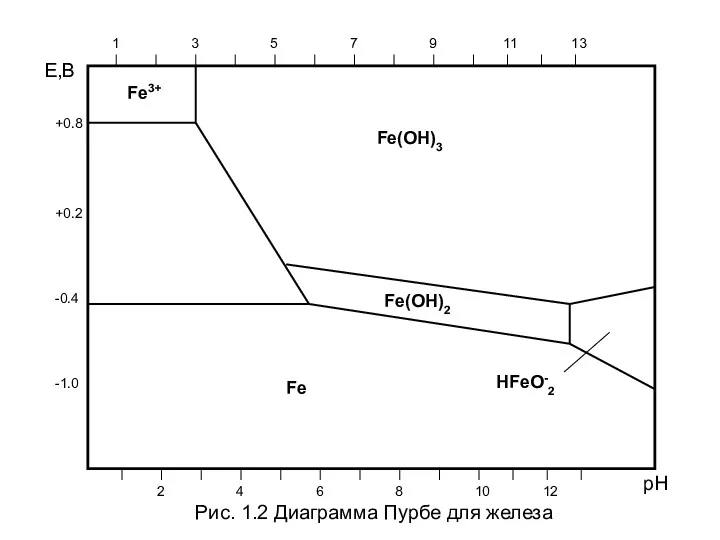
- 33. 1 3 5 7 9 11 13 2 12 10 8 4 6 +0.2 +0.8 -1.0
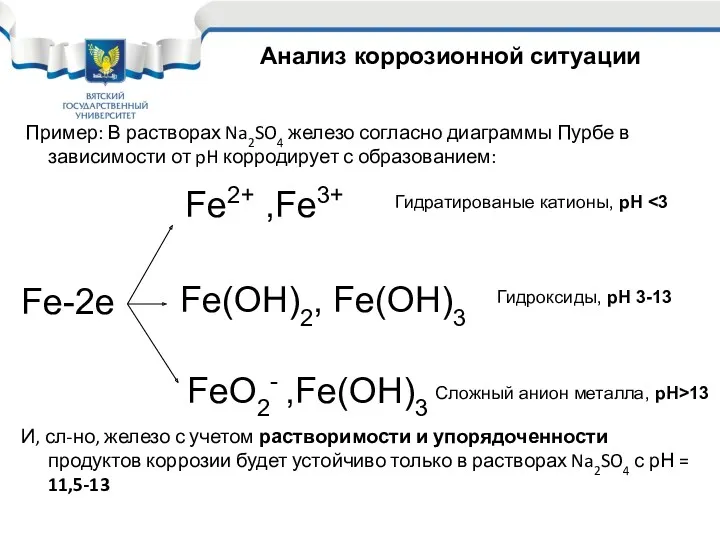
- 34. Пример: В растворах Na2SO4 железо согласно диаграммы Пурбе в зависимости от pH корродирует с образованием: И,
- 35. Анализ коррозионного процесса для углеродистых и низколегированных сталей в средах с различным рН показывает: При рН
- 36. В диапазоне рН 11,5-13 железо корродирует под действием только О2, продуктами коррозии также являются смесь гидроксидов
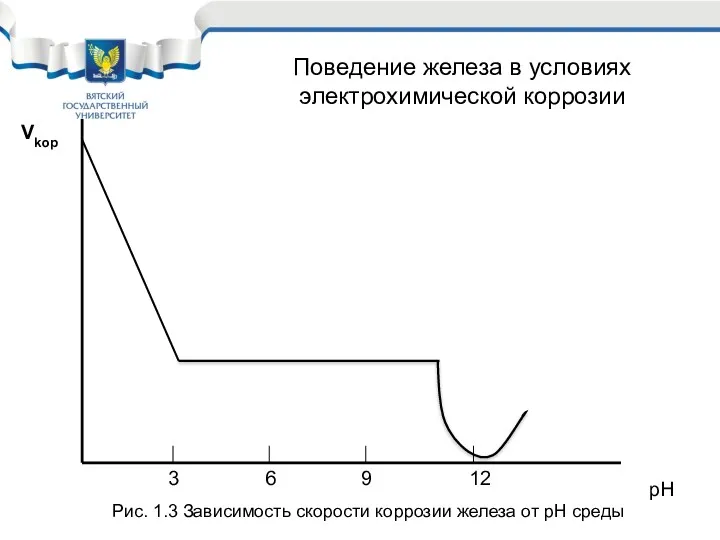
- 37. Vkop рH 3 6 9 12 Рис. 1.3 Зависимость скорости коррозии железа от рН среды Поведение
- 38. Вывод: Железо, углеродистые и низколегированные стали в условиях электрохимической коррозии необходимо защищать во всех средах, кроме
- 39. Коррозия металлов в контакте (Контактная коррозия) В реальной практике конструкции часто выполняются из двух или нескольких
- 40. Т.е. при контактной коррозии потенциал более отрицательного металла сдвигается в положительном направлении и скорость коррозии его
- 42. Скачать презентацию









![Me - ne Катионы Меne+ Комплексные соединения [Ме(Кn)]m+, [Ме(Кn)]m- Оксиды](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/212856/slide-12.jpg)





















 Соединения водорода
Соединения водорода Химическая промышленность
Химическая промышленность Химические свойства неорганических соединений
Химические свойства неорганических соединений Алкины — углеводороды, содержащие тройную связь между атомами углерода
Алкины — углеводороды, содержащие тройную связь между атомами углерода Арены. Бензол
Арены. Бензол Практическая работа №2. Наблюдение за горящей свечой
Практическая работа №2. Наблюдение за горящей свечой Флотационные реагенты. Активаторы
Флотационные реагенты. Активаторы Основания. Химические свойства оснований. Сильные и слабые основания
Основания. Химические свойства оснований. Сильные и слабые основания Получение, собирание и распознавание газов. Практическая работа
Получение, собирание и распознавание газов. Практическая работа Сапалық талдау. Сапалық аналитикалық реакциялар
Сапалық талдау. Сапалық аналитикалық реакциялар Окислительно-восстановительные процессы
Окислительно-восстановительные процессы Химическая посуда
Химическая посуда Количество вещества. Молярная масса. Молярный объем
Количество вещества. Молярная масса. Молярный объем Производство серной кислоты
Производство серной кислоты Химические свойста воды
Химические свойста воды Масса и формулы. Химия 8 класс
Масса и формулы. Химия 8 класс Гидросульфит натрия (пищевая добавка Е222)
Гидросульфит натрия (пищевая добавка Е222) Гетерофункциональные производные бензольного ряда как лекарственные средства. Гетероциклические соединения. Алкалоиды
Гетерофункциональные производные бензольного ряда как лекарственные средства. Гетероциклические соединения. Алкалоиды Бром. Общие сведения
Бром. Общие сведения Эко-упаковка
Эко-упаковка Проект Получение пресной и чистой воды
Проект Получение пресной и чистой воды Строение атома
Строение атома Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Изомерия. (11 класс)
Изомерия. (11 класс) Оксиды. Номенклатура, классификация, физические свойства
Оксиды. Номенклатура, классификация, физические свойства Алмазы. Бриллианты
Алмазы. Бриллианты Использование горюче-смазочных материалов в автотранспорте
Использование горюче-смазочных материалов в автотранспорте Химический потенциал. Фазовые равновесия
Химический потенциал. Фазовые равновесия