Содержание
- 2. Содержание : 1. Определение сущности процесса электролиза 2. Электролиз в расплавах: а) процессы на катоде б)
- 3. Электролиз – это окислительно-восстановительный процесс, протекающий на электродах в растворах или расплавах электролитов при пропускании электрического
- 4. Электролиз в расплавах На катоде происходит процесс восстановления • В расплавах катионы металла восстанавливаются до свободного
- 5. Электролиз в расплавах На аноде происходит процесс окисления • В расплавах анионы бескислородных кислот (кроме фторидов)
- 6. ЭЛЕКТРОЛИЗ – окислительно-восстановительный процесс, протекающий на электродах при прохождении электрического тока через расплав или раствор электролита
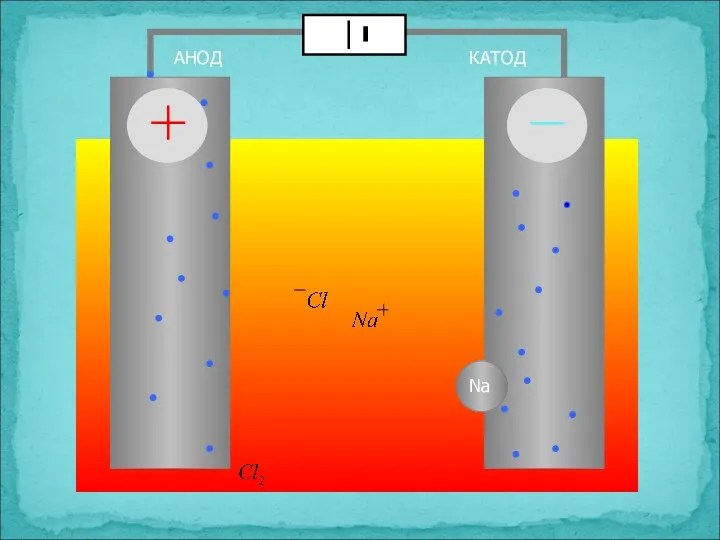
- 7. АНОД КАТОД
- 8. Электролиз расплава NaCl К(-) NaCl А(+) ↓ ← Na+ + Cl- → Na+ + 1ē =
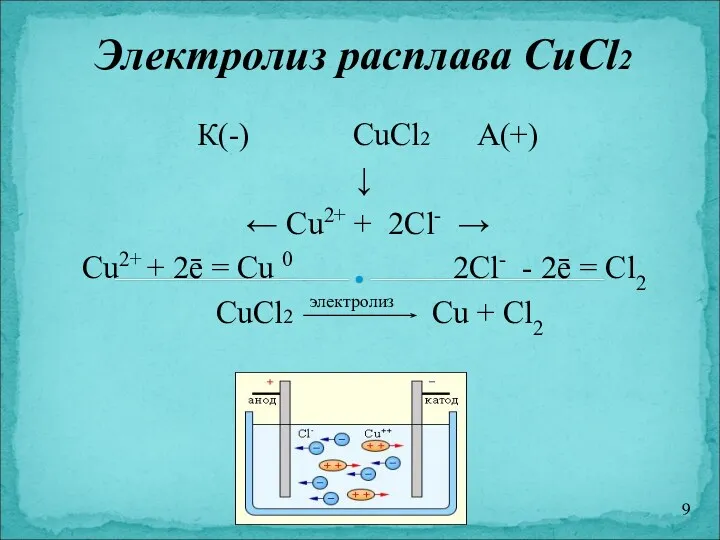
- 9. К(-) CuCl2 А(+) ↓ ← Cu2+ + 2Cl- → Cu2+ + 2ē = Cu 0 2Cl-
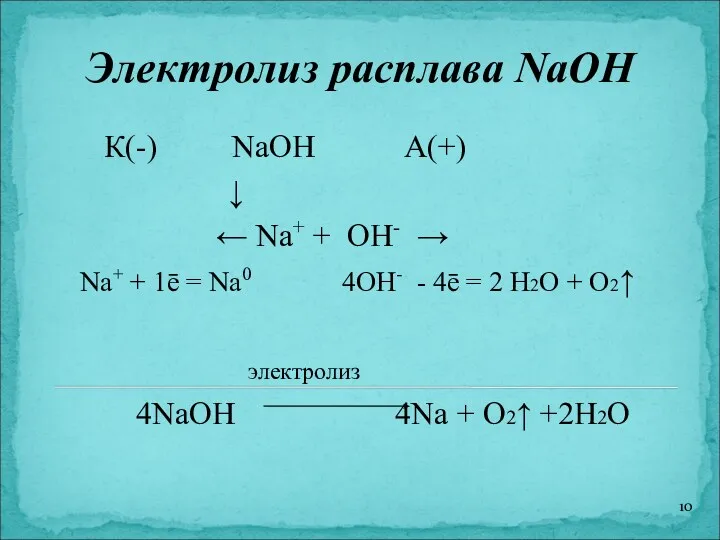
- 10. Электролиз расплава NaOH К(-) NaOH А(+) ↓ ← Na+ + OH- → Na+ + 1ē =
- 11. Электролиз в растворах (процесс на катоде) В растворах процесс на катоде не зависит от материала катода,
- 12. Электролиз в растворах (процесс на катоде) б) Если металл расположен в ряду напряжений между Al и
- 13. Процессы на КАТОДЕ
- 14. Процессы на АНОДЕ
- 15. Процесс на аноде В растворах процесс на аноде зависит от материала анода и от природы аниона.
- 16. Процесс на аноде б) Если анод инертный, то в случае бескислородных анионов (кроме фторидов) идет окисление
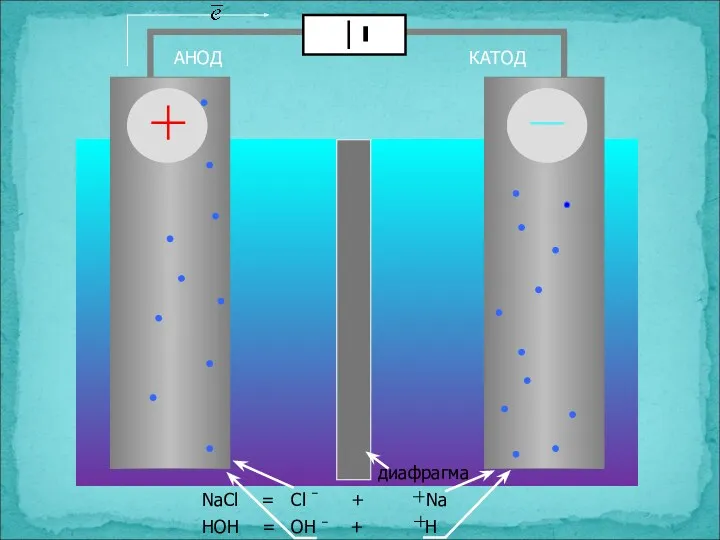
- 17. Схема электролизера на примере электролиза NaCl
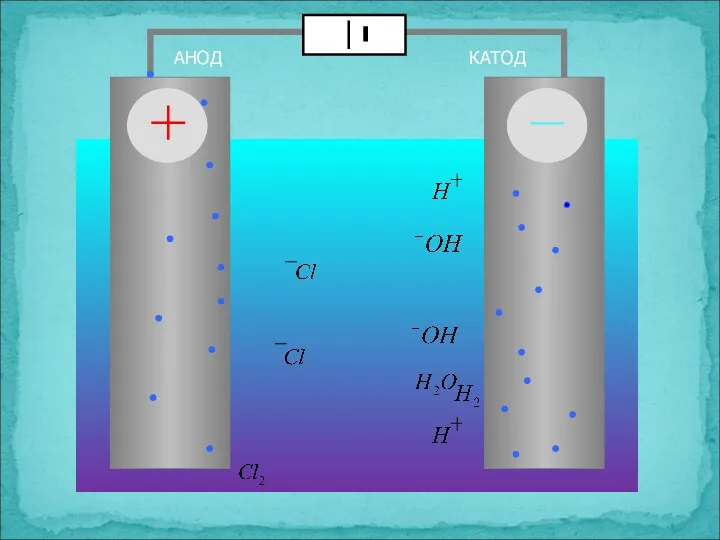
- 18. АНОД КАТОД диафрагма NaCl = Cl + Na HOH = OH + H
- 19. АНОД КАТОД
- 20. Электролиз раствора NaCl на инертном аноде К(-) NaCl А(+) ↓ ← Na+ + Cl- → 2Н2О
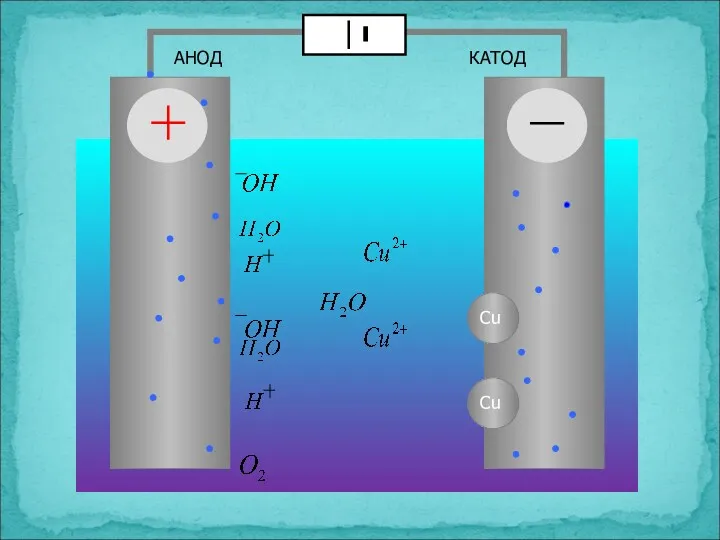
- 21. Схема электролиза раствора CuSO4
- 22. АНОД КАТОД
- 23. Электролиз раствора CuSO4 на инертном аноде К(-) CuSO4 А(+) ↓ ← Cu2+ + SO42- → Cu2+
- 24. Электролиз раствора NaCl на растворимом аноде К(-) NaCl А(+) ↓ (Cu) ← Na+ + Cl- →
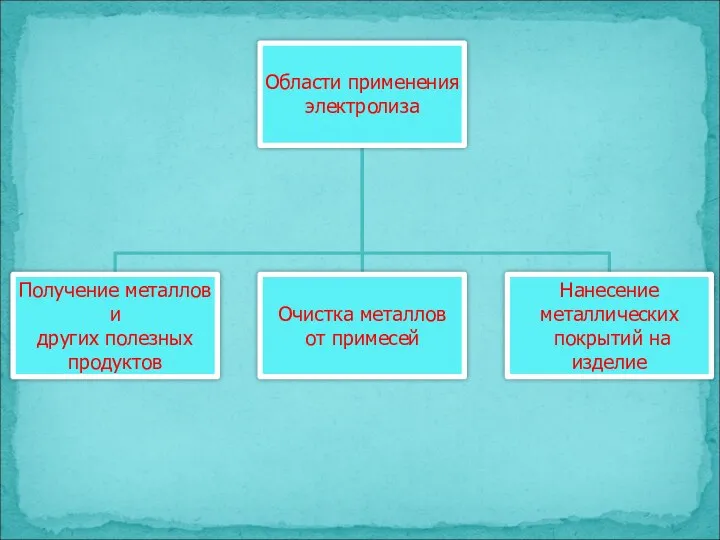
- 26. Области применения электролиза В основной химической промышленности – получение H2, O2, S, галогенов, щелочей и др.
- 27. Применение электролиза: получение чистых металлов (Алюминий, магний, натрий, кадмий получают только электролизом)
- 28. очистка металлов получение щелочей, хлора, водорода, кислорода
- 29. защита металлов от коррозии (При этом на поверхности металлических изделий электрохимическим методом наносят тонкий слой другого
- 30. копирование рельефных изделий из металлов и других материалов. Гальванопластика позволяет создавать документально точные копии барельефов, монет,
- 31. применение электролиза в косметологии для электроэпиляции (при удалении волос этим методом используются очень тонкие иголочки, которыми
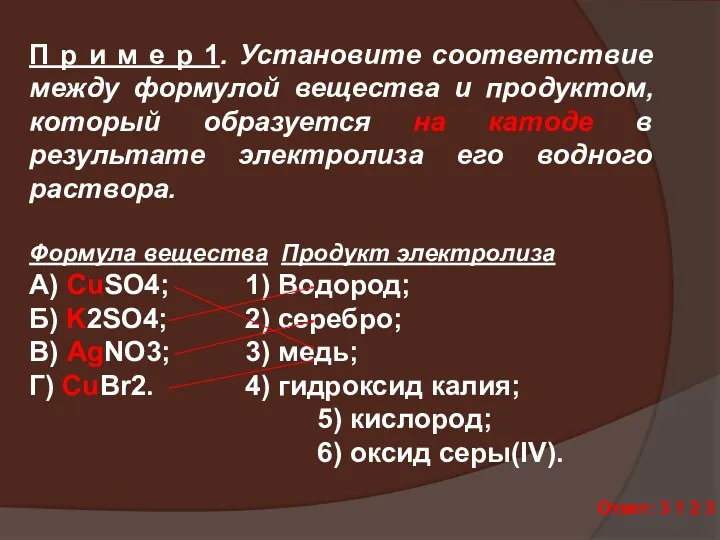
- 32. П р и м е р 1. Установите соответствие между формулой вещества и продуктом, который образуется
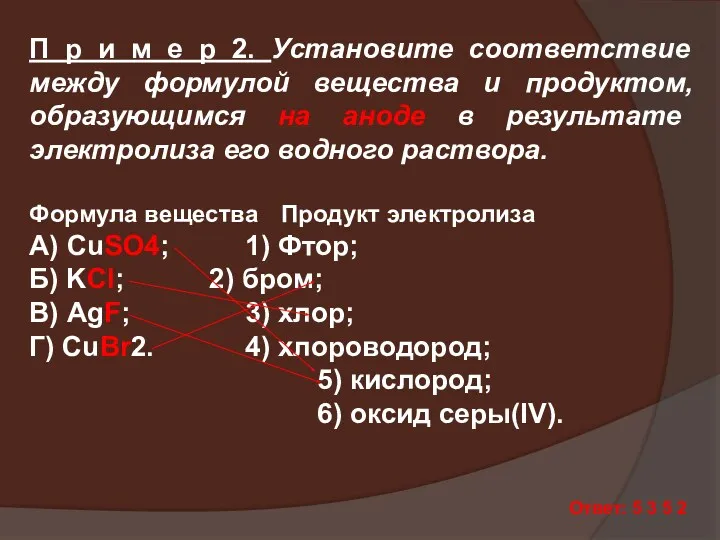
- 33. П р и м е р 2. Установите соответствие между формулой вещества и продуктом, образующимся на
- 34. П р и м е р 8. Установите соответствие между названием вещества и продуктами электролиза на
- 35. П р и м е р 3. Установите соответствие между формулой вещества и итоговым уравнением электролиза
- 36. П р и м е р 4. Установите соответствие между формулой соли и схемой процесса, протекающего
- 37. Тест по теме "Электролиз" 1. При электролизе раствора сульфата цинка с инертными электродами на аноде выделяется:
- 38. 3. При электролизе расплава гидроксида натрия на аноде выделяется: а) натрий; б) водород; в) кислород; г)
- 39. 5. Процесс на катоде при электролизе растворов солей зависит от: а) природы катода; б) активности металла;
- 40. 7. При электролизе 240 г 15%-го раствора гидроксида натрия на аноде выделилось 89,6 л (н.у.) кислорода.
- 41. А теперь проверим ваши ответы! 1-б 2-б 3-в, г 4-а, г 5-б 6- в 7- в
- 42. Список использованной литературы: 1. О.С.Габриелян Учебник химии для 11 класса, М., Дрофа, 2004г. 2. Г.П.Хомченко, К.И.Севастьянова
- 44. Скачать презентацию































 Електролітична дисоціація. Гідроліз солей
Електролітична дисоціація. Гідроліз солей Группа веществ, изолируемых из биологического материала дистилляцией
Группа веществ, изолируемых из биологического материала дистилляцией Виды присадок к моторным топливам. Бензин
Виды присадок к моторным топливам. Бензин Созвездие талантов. Игра-зачет по теме Основные классы неорганической химии 8 класс
Созвездие талантов. Игра-зачет по теме Основные классы неорганической химии 8 класс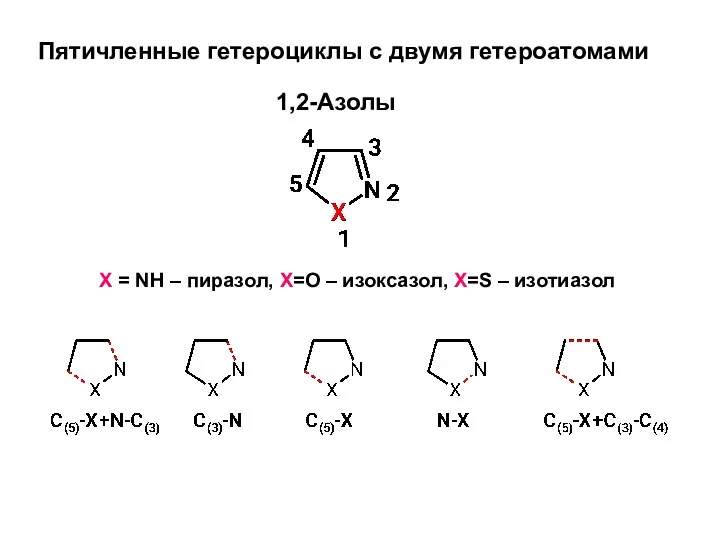 Пятичленные гетероциклы с двумя гетероатомами
Пятичленные гетероциклы с двумя гетероатомами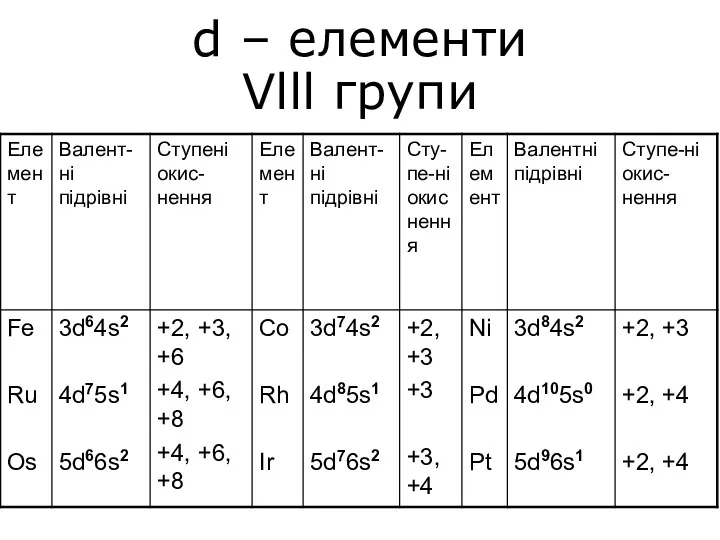 d – елементи Vlll групи
d – елементи Vlll групи Влияние спирта на здоровье человека
Влияние спирта на здоровье человека Сероводород и сульфиды
Сероводород и сульфиды Понятие о солях (8 класс)
Понятие о солях (8 класс) Природный газ и его свойства. Раздел 1
Природный газ и его свойства. Раздел 1 Тотығу-тотықсыздану титрлеу әдісі
Тотығу-тотықсыздану титрлеу әдісі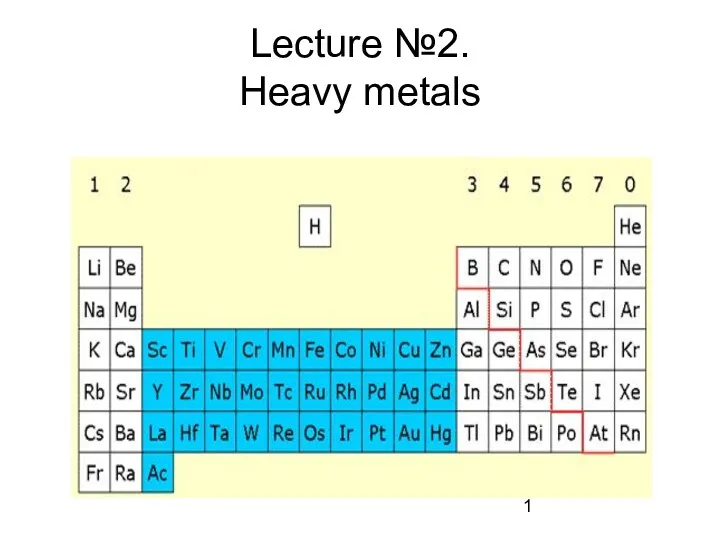 Heavy metals
Heavy metals Валентность и степень окисления
Валентность и степень окисления Теоретические основы органической химии
Теоретические основы органической химии Научные основы и технологии зеленой химии
Научные основы и технологии зеленой химии Қанықпаған майлар және соның негізіндегі БАЗ
Қанықпаған майлар және соның негізіндегі БАЗ Алмастырылмайтын аминқышқылды алу биотехнологиясы
Алмастырылмайтын аминқышқылды алу биотехнологиясы Молярный объем газов
Молярный объем газов Наноалотропи карбону: класифікація, одержання та застосування
Наноалотропи карбону: класифікація, одержання та застосування Фенолы
Фенолы Состав, строение и свойства натурального каучука
Состав, строение и свойства натурального каучука Химиялық элементтердің табиғи топтары
Химиялық элементтердің табиғи топтары Вода. Растворимость, растворы
Вода. Растворимость, растворы Пищевые добавки
Пищевые добавки Хімічні властивості кисню. Реакції сполучення
Хімічні властивості кисню. Реакції сполучення Биологически важные вещества жиры
Биологически важные вещества жиры Полимеры и пластические массы
Полимеры и пластические массы Щелочные металлы
Щелочные металлы