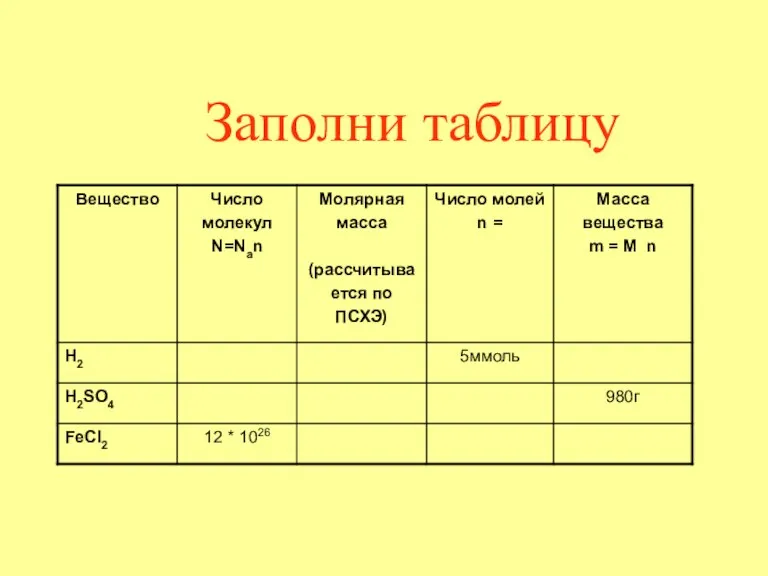
Слайд 2

Цель урока: Сформировать понятие о молярном объеме газов. Научиться производить расчеты, используя
закон Авогадро и следствие из него
Слайд 3

М (н2о) = 18г/моль
1) n (н2о) = 5 моль
m(н2о) = ? 2) n (н2о) = 10 моль
m(н2о) = ?
Слайд 4

М (н2о) = 18г/моль
1) n (н2о) = 5 моль
m(н2о) = 90г
2) n (н2о) = 10 моль
m(н2о) = 180г
Слайд 5

V (н2о) = 18 /1 = 18 мл/моль
Слайд 6

М (CuO) = 80 г/моль
М (KCl) = 74,5 г/моль
Слайд 7

Закон Авогадро
(Амедео Авогадро, итал. в 1811г )
В равных объемах различных
газов содержится одинаковое число молекул (при н. у.)
Слайд 8

нормальные условия:
(t = 0 °С, P = 1 атм)
Слайд 9

Объем можно вычислить, если известна масса 1 л газа.
Например,
при н.у. :
I. масса 1 л водорода равна 0,09 г,
(плотность 0,09 г/л); М(Н2) = 2,016 г/моль.
II. масса 1 л кислорода равна 1,429 г,
(плотность 1,429 г/л); М(О2) = 32 г/моль
Слайд 10

Слайд 11

Слайд 12

Слайд 13

= n * NА
Слайд 14

Решите задачи
Iвариант: Задача 1. Рассчитайте, какой объем занимают 5 моль
аммиака (н. у.).
Задача 2. Рассчитайте, какой объем при нормальных условиях займет оксид углерода (IV) массой 5,6 г.
IIвариант: Задача 1. Какое количество вещества оксида азота (II) заключено в объеме 448 л? Задача 2. Определите массу 5 л аммиака (н.у.)
Слайд 15














 Хімічні формули речовин
Хімічні формули речовин Водород
Водород Химиялық қауіптілер. Нитраттар
Химиялық қауіптілер. Нитраттар Кислоты в свете теории электролитической диссоциации (ТЭД)
Кислоты в свете теории электролитической диссоциации (ТЭД) Кристаллическое строение и свойства металлов
Кристаллическое строение и свойства металлов Материаловедение промышленного производства. Особенности строения твердых тел
Материаловедение промышленного производства. Особенности строения твердых тел Неметаллы: общая характеристика. 9 класс
Неметаллы: общая характеристика. 9 класс Понятия про синтетические лекарственные средства
Понятия про синтетические лекарственные средства Основи. Властивості, застосування гідроксидів Натрію і Калію
Основи. Властивості, застосування гідроксидів Натрію і Калію Акцепторы катионов и анионов. Краун-эфиры и близкие структурные аналоги: поданды, лариатэфиры. Супрамолекулярная фотоника
Акцепторы катионов и анионов. Краун-эфиры и близкие структурные аналоги: поданды, лариатэфиры. Супрамолекулярная фотоника Химия в Великую Отечественную войну
Химия в Великую Отечественную войну Массовая доля вещества в растворе
Массовая доля вещества в растворе Строение атома. Периодический закон и периодическая система элементов
Строение атома. Периодический закон и периодическая система элементов Современные химические технологии
Современные химические технологии Каталитический риформинг
Каталитический риформинг Получение, собирание, распознавание газов. (Практическая работа 2)
Получение, собирание, распознавание газов. (Практическая работа 2) Углеводороды. Предельные нециклические (ациклические) углеводороды. Алканы
Углеводороды. Предельные нециклические (ациклические) углеводороды. Алканы Простые вещества
Простые вещества Незвичайна вода
Незвичайна вода Фазовое равновесие
Фазовое равновесие Химия в повседневной жизни человека
Химия в повседневной жизни человека Химическая очистка сточных вод. Окисление и восстановление
Химическая очистка сточных вод. Окисление и восстановление Растворы: состав и их коллигативные свойства
Растворы: состав и их коллигативные свойства Щелочные и щелочноземельные металлы
Щелочные и щелочноземельные металлы Относительная молекулярная масса вещества. Задачи
Относительная молекулярная масса вещества. Задачи Химические свойства карбокатионов
Химические свойства карбокатионов Тіршілік процесіне қатысатын гетерофункционалды қосылыстар
Тіршілік процесіне қатысатын гетерофункционалды қосылыстар Скорость химических реакций
Скорость химических реакций