Електронні і графічні електронні формули атомів s-, р-, d- елементів. Принцип мінімальної енергії презентация
Содержание
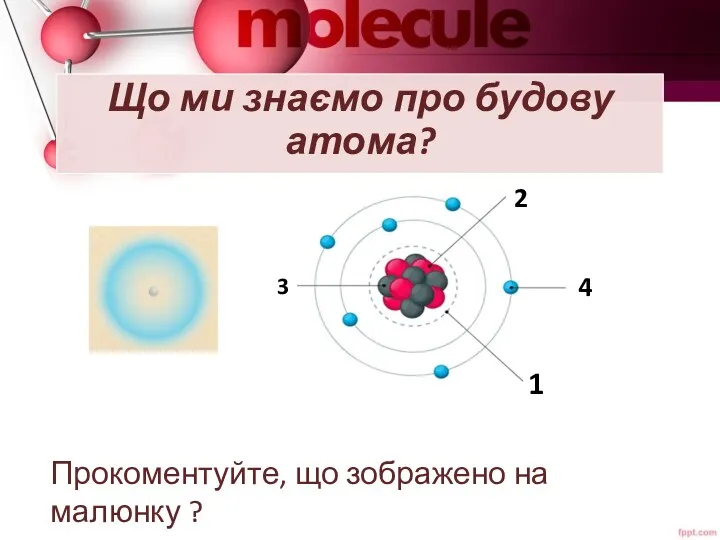
- 2. Що ми знаємо про будову атома? Прокоментуйте, що зображено на малюнку ? 3 2 4 1
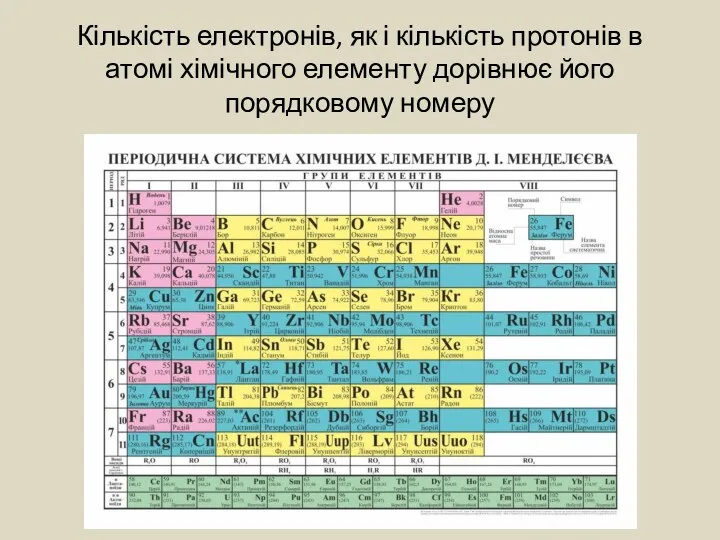
- 3. Кількість електронів, як і кількість протонів в атомі хімічного елементу дорівнює його порядковому номеру
- 4. Електрони розміщуються навколо ядра за певними правилами: 1) Електрони розподіляються по енергетичним рівням. Кількість енергетичних рівнів
- 5. 2) Електрон в атомі перебуває не в одній конкретній точці, а утворює під час руху електронну
- 6. Місткість орбіталей 3) На кожній орбіталі максимально можуть розміститися два електрони, що мають однакову енергію, але
- 7. Зазвичай електронну оболонку атомів утворює не один електрон, їх може бути до декількох десятків і навіть
- 8. Орбіталі різної форми позначають різними буквами: s, р, d і f. s-Орбіталі мають форму кулі (а),
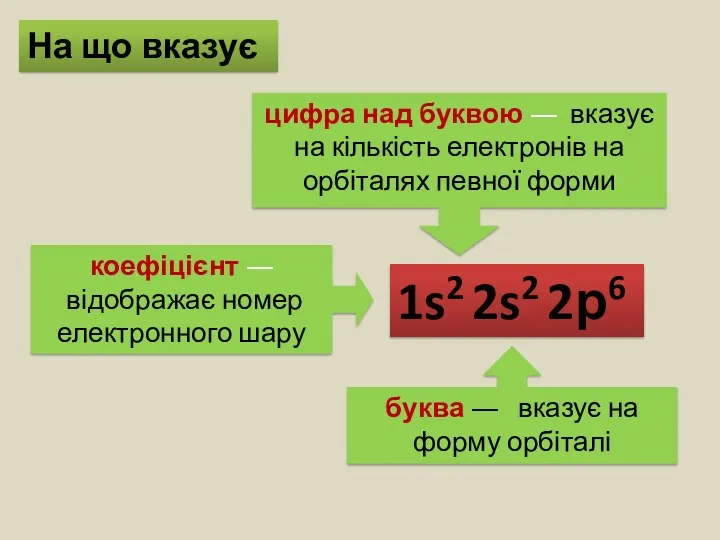
- 9. Електронна формула атома — це запис розподілу електронів в електронній оболонці атома, де коефіцієнтами позначають енергетичні
- 10. 1s2 2s2 2р6 буква ― вказує на форму орбіталі цифра над буквою ― вказує на кількість
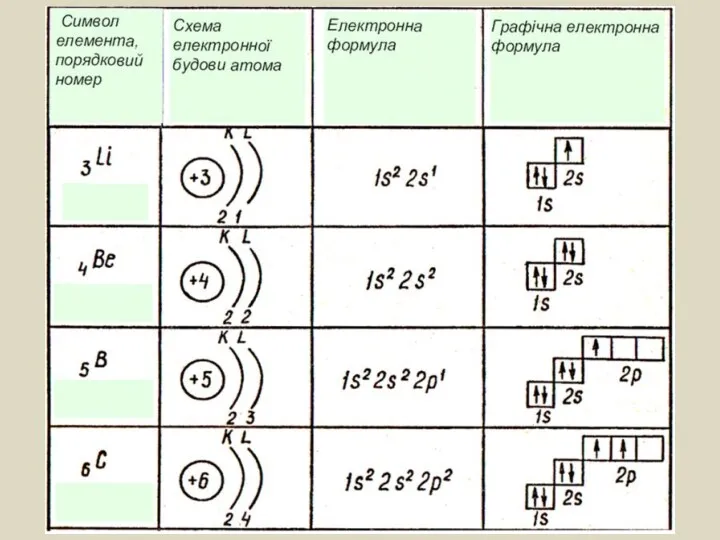
- 11. Графічне зображення (електронні графічні формули): Графічно електрони зображують у вигляді стрілок, спрямованих догори або донизу, що
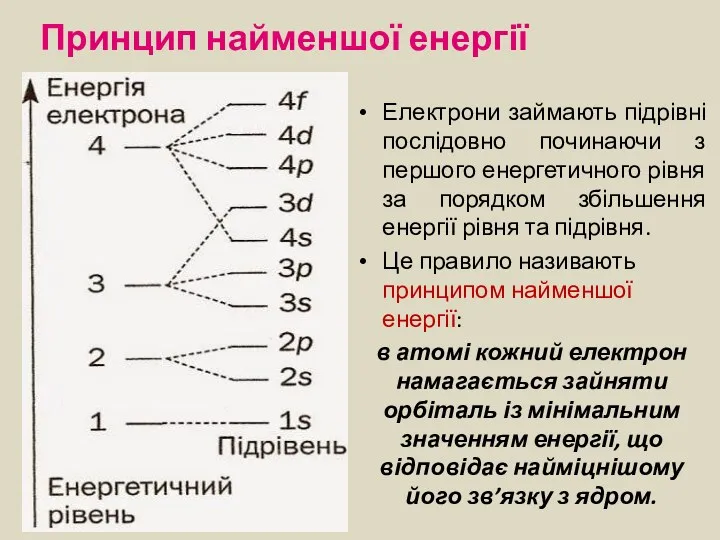
- 13. Принцип найменшої енергії Електрони займають підрівні послідовно починаючи з першого енергетичного рівня за порядком збільшення енергії
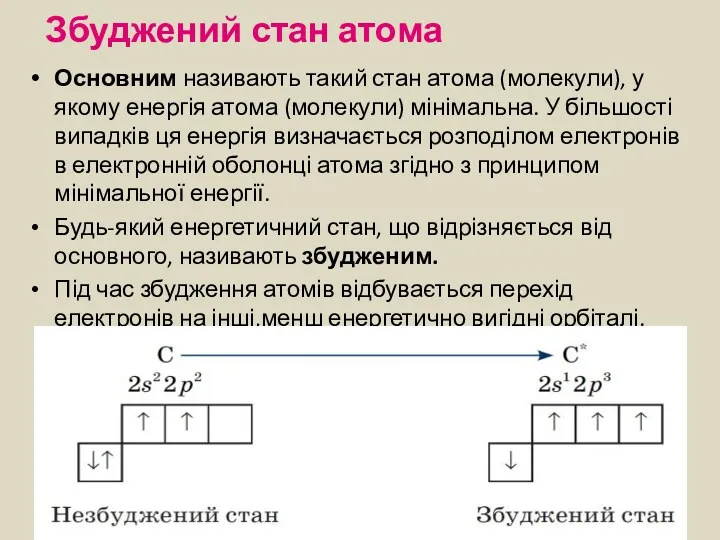
- 14. Збуджений стан атома Основним називають такий стан атома (молекули), у якому енергія атома (молекули) мінімальна. У
- 16. Скачать презентацию







 Методика преподавания химии
Методика преподавания химии Многоатомные и одноатомные спирты
Многоатомные и одноатомные спирты Конструкционные материалы. Пластмассы
Конструкционные материалы. Пластмассы Строение атома. Строение электронных оболочек атомов
Строение атома. Строение электронных оболочек атомов Основания. 8 класс
Основания. 8 класс Химические свойства солей
Химические свойства солей Соли
Соли Biochemistry. What is biochemistry?
Biochemistry. What is biochemistry? Классификация органических реакций
Классификация органических реакций Галогены. Физические свойства галогенов
Галогены. Физические свойства галогенов Тепловой эффект химических реакций. 8 класс
Тепловой эффект химических реакций. 8 класс Периодическая система химических элементов. Периоды
Периодическая система химических элементов. Периоды Оксид серы(4). Сернистая кислота и её соли
Оксид серы(4). Сернистая кислота и её соли Алмазы. Бриллианты
Алмазы. Бриллианты Геохимическая классификация элементов
Геохимическая классификация элементов Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Хлориды. Химические свойства
Хлориды. Химические свойства Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Учения о растворах. Коллигативные свойства растворов. Лекция 33
Учения о растворах. Коллигативные свойства растворов. Лекция 33 Понятия о металлических сплавах. Лекция 4
Понятия о металлических сплавах. Лекция 4 Окислительно-восстановительные реакции. Лабораторная работа
Окислительно-восстановительные реакции. Лабораторная работа Лекция 15. Аминокислоты
Лекция 15. Аминокислоты Обмен простых белков. Дезаминирование и трансаминирование аминокислот
Обмен простых белков. Дезаминирование и трансаминирование аминокислот Химические свойства основных классов неорганических соединений
Химические свойства основных классов неорганических соединений Оксид фосфора
Оксид фосфора Набор № 3 ВС Щелочи
Набор № 3 ВС Щелочи Оксиды серы. Сернистая кислота
Оксиды серы. Сернистая кислота Молярный объем газов
Молярный объем газов