Содержание
- 2. Общие сведения Галогены (от греч. ἁλός — соль и γένος — рождение, происхождение; иногда употребляется устаревшее
- 3. Общие сведения Реагируют почти со всеми простыми веществами, кроме некоторых неметаллов. Все галогены — энергичные окислители,
- 4. Общие сведения С увеличением порядкового номера химическая активность галогенов уменьшается, химическая активность галогенид-ионов F−, Cl−, Br−,
- 5. Общие сведения К галогенам относятся фтор F, хлор Cl, бром Br, иод I, астат At, а
- 6. Общие сведения При взаимодействии с металлами возникает ионная связь, и образуются соли. Галогены, (кроме F) при
- 7. Физические свойства галогенов www.power-slide.ru Фтор является трудносжижаемым, а хлор легкосжижаемым газом с удушливым резким запахом. Фтор
- 8. Физические свойства галогенов Энергия связи галогенов сверху вниз по ряду изменяется не равномерно. Фтор имеет аномально
- 9. Физические свойства галогенов От хлора к астату энергия связи постепенно ослабевает, что связано с увеличением атомного
- 10. Химические свойства галогенов Все галогены проявляют высокую окислительную активность, которая уменьшается при переходе от фтора к
- 11. Фтор — самый активный из галогенов, реагирует со всеми металлами без исключения, многие из них в
- 12. Без нагревания фтор реагирует и со многими неметаллами (H2, S, С, Si, Р) — все реакции
- 13. Свободный хлор также очень реакционноспособен, хотя его активность и меньше, чем у фтора. Он непосредственно реагирует
- 14. Особый интерес представляет реакция с водородом. Так, при комнатной температуре, без освещения хлор практически не реагирует
- 15. Хлор вступает в реакцию со многими сложными веществами, например замещения и присоединения с углеводородами: СН3-СН3 +
- 16. Хлор способен при нагревании вытеснять бром или йод из их соединений с водородом или металлами: Cl2
- 17. Химическая активность брома меньше, чем у фтора и хлора, но все же достаточно велика в связи
- 18. Йод существенно отличается по химической активности от остальных галогенов. Он не реагирует с большинством неметаллов, а
- 19. Взаимодействие же йода с водородом происходит только при сильном нагревании, реакция является эндотермической и сильно обратимой:
- 20. Таким образом, химическая активность галогенов последовательно уменьшается от фтора к астату. Каждый галоген в ряду F
- 21. Астат ещё менее реакционноспособен, чем иод. Но и он реагирует с металлами (например с литием): 2Li
- 23. Скачать презентацию




















 Вещества молекулярного и немолекулярного строения. Типы кристаллических решеток
Вещества молекулярного и немолекулярного строения. Типы кристаллических решеток Гетерогенді химиялық реакциялар
Гетерогенді химиялық реакциялар Рафинирование металлических расплавов
Рафинирование металлических расплавов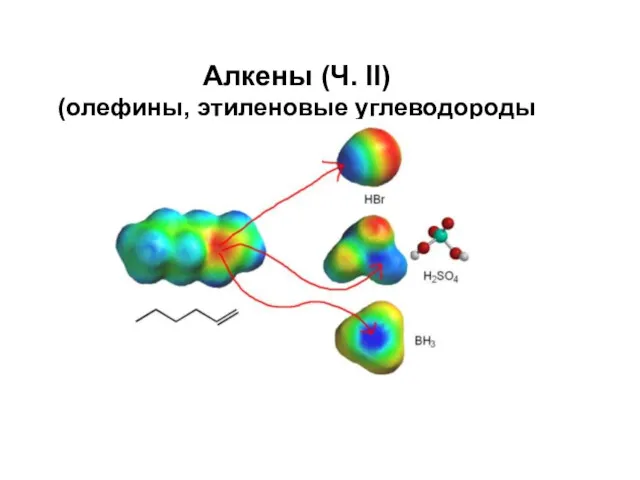 Алкены (олефины, этиленовые углеводороды)
Алкены (олефины, этиленовые углеводороды) Металлы в природе. Общие способы их получения
Металлы в природе. Общие способы их получения Общая характеристика металлов
Общая характеристика металлов Алкандар. Метан молекуласының құрылысы Метан және оның гомологтарының қасиеттері
Алкандар. Метан молекуласының құрылысы Метан және оның гомологтарының қасиеттері Химия сабағындағы өздік жұмыстар
Химия сабағындағы өздік жұмыстар Ископаемые углеводороды
Ископаемые углеводороды Времена алхимиков
Времена алхимиков Буферные растворы. Граф структуры. Теория электрической диссоциации. Химическое равновесие
Буферные растворы. Граф структуры. Теория электрической диссоциации. Химическое равновесие Оксид серы (IV) и серы (VI)
Оксид серы (IV) и серы (VI) Минералы для ИЗБ
Минералы для ИЗБ Химия: классификация химических реакций
Химия: классификация химических реакций Химический элемент углерод
Химический элемент углерод Реакції йонного обміну між електролітами у водних розчинах. Практична робота №1
Реакції йонного обміну між електролітами у водних розчинах. Практична робота №1 Бытовая химия. Правила безопасного обращения со средствами бытовой химии
Бытовая химия. Правила безопасного обращения со средствами бытовой химии Значення хімії у розв’ язанні енергетичної проблеми
Значення хімії у розв’ язанні енергетичної проблеми Термодинамика химических процессов
Термодинамика химических процессов Theories of acids and bases. Ionic equilibria in electrolyte solutions. Buffer solutions (topic 3.4)
Theories of acids and bases. Ionic equilibria in electrolyte solutions. Buffer solutions (topic 3.4) Осмос. Онкотикалық қысым. Изотоникалық коэффицент. Гипо, гипер изотоникалық ерітінділер
Осмос. Онкотикалық қысым. Изотоникалық коэффицент. Гипо, гипер изотоникалық ерітінділер Химическая кинетика. Тема 2.2
Химическая кинетика. Тема 2.2 Атомы и молекулы. Простые и сложные вещества (8 класс)
Атомы и молекулы. Простые и сложные вещества (8 класс) Растворы. Лекция 7
Растворы. Лекция 7 Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Алкадиены (диены)
Алкадиены (диены) Гидролиз солей
Гидролиз солей Галогены
Галогены