Содержание
- 2. Нахождение металлов в природе Самородные металлы Минералы и руды Таблица «Свойства руд железа» Металлургия Основные способы
- 3. Остальные металлы – меньше 2% Прежде чем считать звезды – внимательно посмотри под ноги. восточное изречение
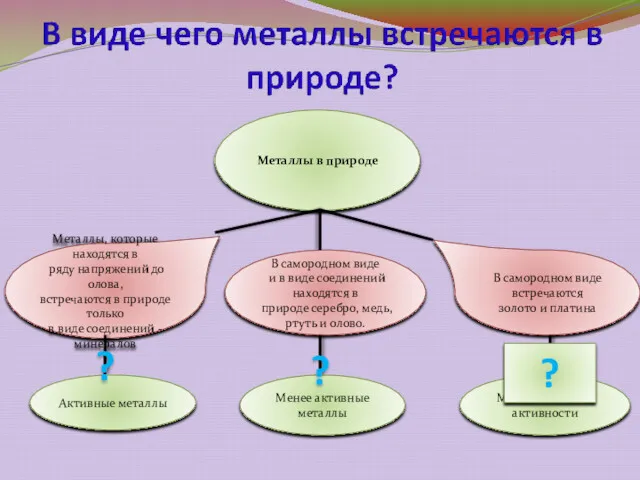
- 4. Металлы в природе В самородном виде встречаются золото и платина В самородном виде и в виде
- 5. Золото в природе чрезвычайно рассеяно. По распространенности в земной коре оно занимает 74 место. Но оно
- 6. Платина относится к наименее распространенным в природе элементам. Земная кора содержит 5×10−7% платины. В самородном состоянии
- 7. По распространенности в земной коре занимает 67 место, но запасы его в 20 раз больше, чем
- 8. Иду на мелкую монету, В колоколах люблю звенеть, Мне ставят памятник за это И знают: имя
- 9. По распространенности занимает 66 место. В самородном виде встречается редко, причем чаще её находят в виде
- 10. Минералы – природные химические соединения металлов. В настоящее время известно более 4000 тысяч минералов. Только 70
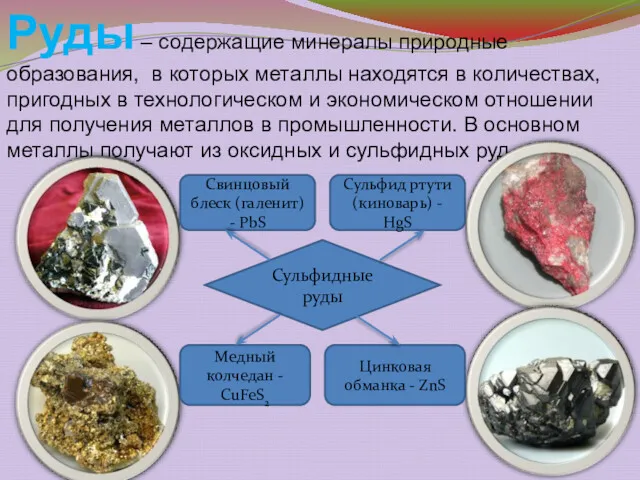
- 11. Руды – содержащие минералы природные образования, в которых металлы находятся в количествах, пригодных в технологическом и
- 12. Бурый железняк (лимонит) – 2Fe2O3·3H2O Среди металлов самый славный, важнейший в мире элемент. Железо Магнитный железняк
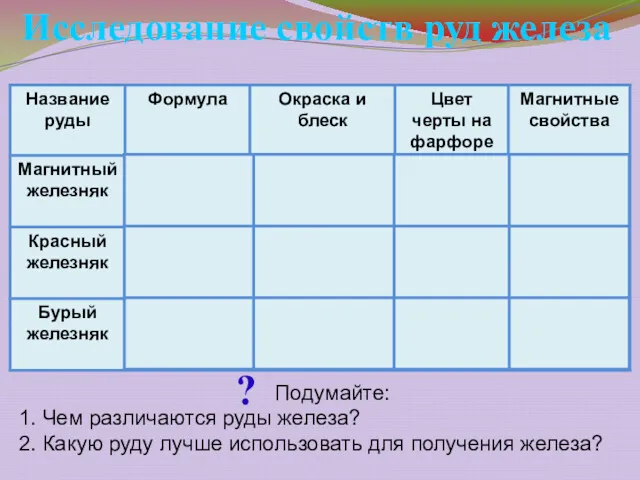
- 13. Подумайте: 1. Чем различаются руды железа? 2. Какую руду лучше использовать для получения железа? Исследование свойств
- 14. Подумайте: Какой основной химический процесс лежит в основе получения металлов? Процесс восстановления Mn+ + nē =
- 15. Основателем науки о металлах в России считается великий русский ученый М. В. Ломоносов. Ему принадлежит первый
- 16. Разработал способ получения булатной стали. Он впервые использовал микроскоп для исследования внутреннего строения металлов. Труды Аносова
- 17. Является основоположником современного металловедения и металлографии – науки о строении металлов и сплавов. Его научные открытия
- 18. Открыл процесс вытеснения металлов из растворов солей под действием других металлов и металлотермический метод. Показал, что
- 19. «Металлург», Л. Татьяничева Я в космос не летал... Но эта сталь — Моя. А это значит,
- 20. Указом Президиума Верховного Совета СССР в 1957 году был утвержден День металлурга , с тех пор
- 21. Пирометаллургия – методы переработки руд, основанные на химических реакциях, происходящих при высоких температурах (греч. пирос –
- 22. Природное соединение растворяют в подходящем реагенте с целью получения раствора соли этого металла CuO + 2HCl
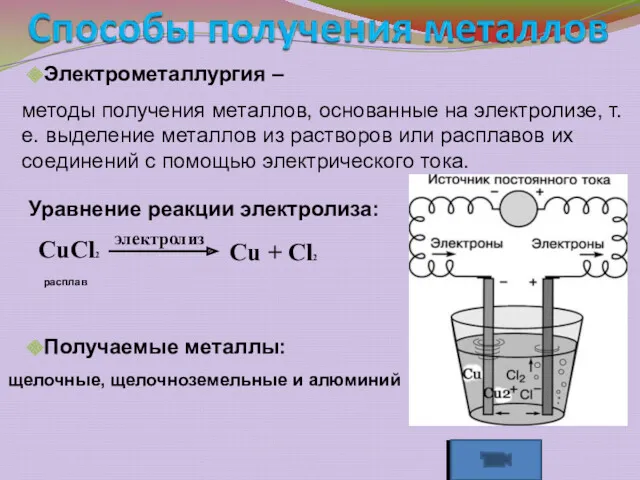
- 23. методы получения металлов, основанные на электролизе, т.е. выделение металлов из растворов или расплавов их соединений с
- 24. Негативное воздействие на окружающую среду: 1.Загрязнение почвы по причине массового складирования отходов. Для выработки 1 т
- 25. Предприятия черной металлургии выбрасывают в атмосферу 25% металлосодержащей пыли и оксида углерода (II) от общего количества
- 26. Металлургия использует 25% от всей потребляемой российской промышленностью воды. Например, для получения 1 т. алюминия используется
- 27. Пути решения Переработка и использование отходов Строительство очистных сооружений и замкнутых систем водоснабжения Разработка новых технологий
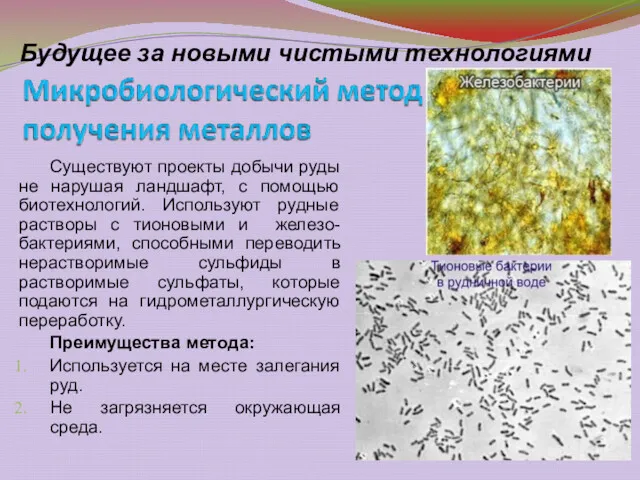
- 28. Будущее за новыми чистыми технологиями Существуют проекты добычи руды не нарушая ландшафт, с помощью биотехнологий. Используют
- 29. Проверь себя Fe2O3 + Al O2 FeO Fe Al2O3 Fe2O3 + H2 Fe H2O H2O2 Fe(OH)3
- 31. Скачать презентацию




















 Соединения кальция. Жесткость воды и способы её устранения
Соединения кальция. Жесткость воды и способы её устранения Азотсодержащие гетероциклические соединения
Азотсодержащие гетероциклические соединения Хімічні властивості оксидів
Хімічні властивості оксидів Кристаллические и аморфные тела
Кристаллические и аморфные тела Пегматитовые месторождения
Пегматитовые месторождения Хлороводород и соляная кислота
Хлороводород и соляная кислота Электролитическая диссоциация
Электролитическая диссоциация Металлическая связь
Металлическая связь Химия и здоровье
Химия и здоровье Жескость воды
Жескость воды Ювелирная работа – изысканный шедевр
Ювелирная работа – изысканный шедевр Процессы и аппараты химических производств
Процессы и аппараты химических производств Химический элемент цинк
Химический элемент цинк Аналитическая химия и химический анализ. (Лекция 1)
Аналитическая химия и химический анализ. (Лекция 1) Щелочноземельные металлы
Щелочноземельные металлы Синтетические моющие средства. Механизм моющего действия
Синтетические моющие средства. Механизм моющего действия Геохимия природных процессов. Геохимическая типизация гранитоидов Л.В. Таусона
Геохимия природных процессов. Геохимическая типизация гранитоидов Л.В. Таусона Нанохимия
Нанохимия Экспериментально исследовательский проект Соль волшебница
Экспериментально исследовательский проект Соль волшебница Воздух, его состав и значение
Воздух, его состав и значение Химическая лаборатрия. Химический состав растений
Химическая лаборатрия. Химический состав растений Розділ 3. Теорія комплексних сполук. Комплексні сполуки
Розділ 3. Теорія комплексних сполук. Комплексні сполуки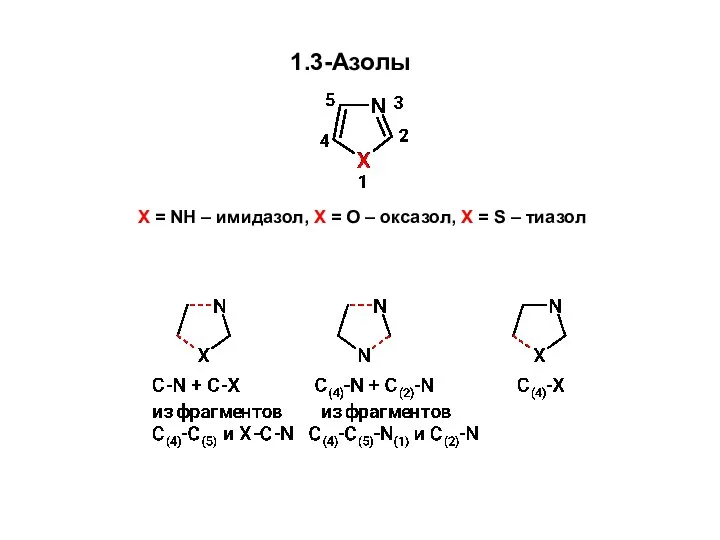 Образование связей C-N и C-X Синтез 1,3-азолов из углеродного фрагмента С(4)-С(5) и фрагмента X-C-N
Образование связей C-N и C-X Синтез 1,3-азолов из углеродного фрагмента С(4)-С(5) и фрагмента X-C-N The structure and properties of the nitrogen and ammonia molecules. Industrial production of nitrogen fertilizers (topic 4.4)
The structure and properties of the nitrogen and ammonia molecules. Industrial production of nitrogen fertilizers (topic 4.4) Номенклатура органических соединений
Номенклатура органических соединений Використання натуральних та штучних добавок при виготовленні харчових продукцій
Використання натуральних та штучних добавок при виготовленні харчових продукцій Учение об агрегатных состояниях вещества. Газообразное состояние
Учение об агрегатных состояниях вещества. Газообразное состояние Железо и его соединения
Железо и его соединения