Содержание
- 2. Девиз урока
- 3. Цель урока Повторить химические свойства оксидов, кислот, оснований , солей. Рассмотреть уравнения реакций в свете окислительной-восстановительной
- 4. Химические свойства оксидов Вспомните, с какими веществами взаимодействуют оксиды? Основные оксиды С кислотами С водой С
- 5. Химические свойства основных оксидов Взаимодействуют с кислотами +2 -2 +1 +6 -2 t +2 +6 -2
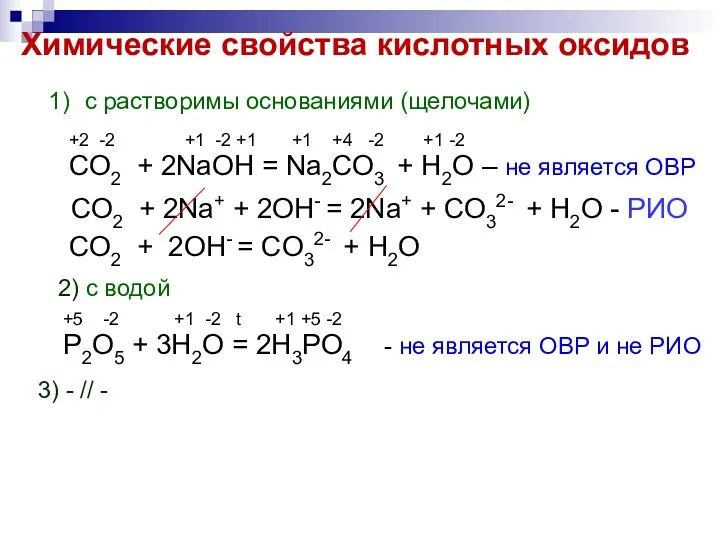
- 6. Химические свойства кислотных оксидов с растворимы основаниями (щелочами) +2 -2 +1 -2 +1 +1 +4 -2
- 7. Химические свойства кислот Вспомните, с какими веществами взаимодействуют кислоты ? с металлами с основными оксидами с
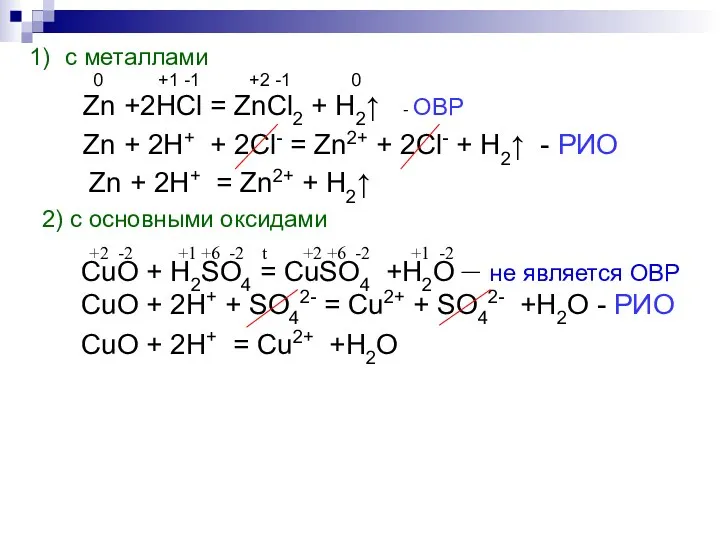
- 8. с металлами 0 +1 -1 +2 -1 0 Zn +2HCl = ZnCl2 + H2↑ - ОВР
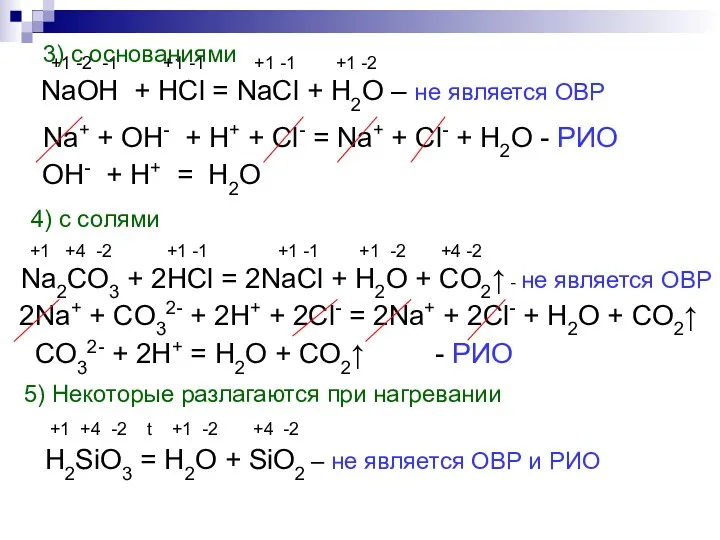
- 9. +1 -2 -1 +1 -1 +1 -1 +1 -2 NaOH + HCl = NaCl + H2O
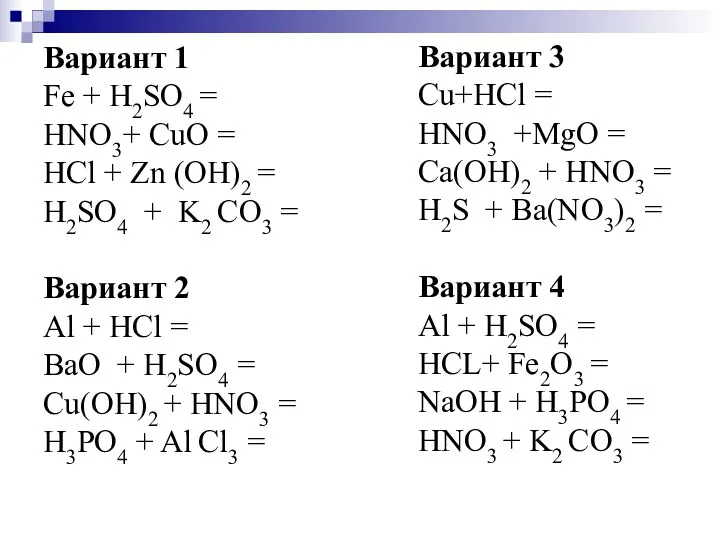
- 10. Вариант 1 Fe + H2SO4 = HNO3+ CuO = HCl + Zn (OH)2 = H2SO4 +
- 11. Вариант 1 Fe + H2SO4 = FeSO4 + H2 HNO3+ CuO = Cu(NO3)2 + H2O HCl
- 12. Химические свойства оснований
- 13. Цель урока Повторить химические свойства оснований. Рассмотреть уравнения реакций в свете электролитической диссоциации; Уметь писать полные
- 14. Химические свойства оснований Вспомните, с какими веществами взаимодействуют основания? с кислотами растворимые основания (щелочи) с солями
- 15. Химические свойства оснований с кислотами +1 -2 +1 +1 +6 -2 +1 +6 -2 +1 -2
- 16. Химические свойства оснований 3) Растворимые основания (щелочи) с кислотными оксидами +1 -2 +1 +6 -2 +1
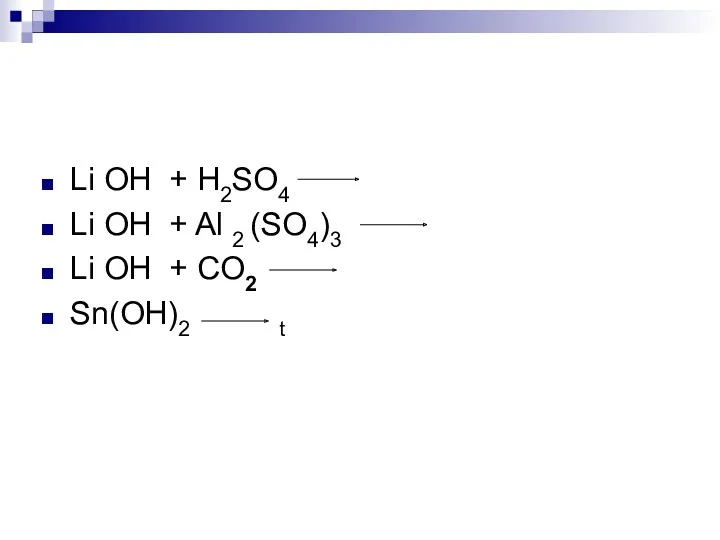
- 17. Li OH + H2SO4 Li OH + Al 2 (SO4)3 Li OH + CO2 Sn(OH)2 t
- 18. Химическая свойства солей Вспомните, с какими веществами взаимодействуют соли? с металлами с кислотами с растворимыми основаниями
- 19. Химические свойства солей с металлами 0 +2 +6 -2 +2 +6 -2 0 Fe + CuSO4
- 20. Химические свойства солей 3) с растворимыми основаниями (щелочами) +2 -1 +1 -2 +1 +1 -1 +2
- 21. Химические свойства солей 5) с кислотными оксидами +2 +4 -2 +4 -2 t +2 +4 -2
- 22. ГИА-9 (№22) Даны вещества: Mg, HNO3, Ba(NO3)2, HCl, AgNO3 . Используя воду и необходимые вещества только
- 23. Самопроверка 1) Mg + 2HCl = MgCl2 + H2↑ 2) MgCl2 + 2 AgNO3 = Mg(NO3)2
- 24. ГИА (№21) Какая масса осадка образуется при взаимодействии избытка раствора хлорида бария с 200 г раствора
- 25. Самопроверка Дано: mр-ра(Al2(SO4)3)= 200г ω (Al2(SO4)3) =10,4% m( BaSO4 ) - ? Решение: Al2(SO4)3 + 3BaCl2
- 26. Домашнее задание Повторить химические свойства неорганических соединений, §9, зад.6 Дополнительно для желающих (раздать карточки)
- 27. МОЛОДЦЫ! Вы успешно справились с работой!
- 28. Дополнительное д/з 1) Бесцветный прозрачный раствор способен изменить окраску фенолфталеина на малиновую. И пропускание через раствор
- 29. Дополнительное задание (ОГЭ-2020, №23) В трех колбах находятся растворы веществ: хлорида железа (II), хлорида магния и
- 31. Скачать презентацию























 Ерітінділер туралы ілім. Буферлік ерітінділер
Ерітінділер туралы ілім. Буферлік ерітінділер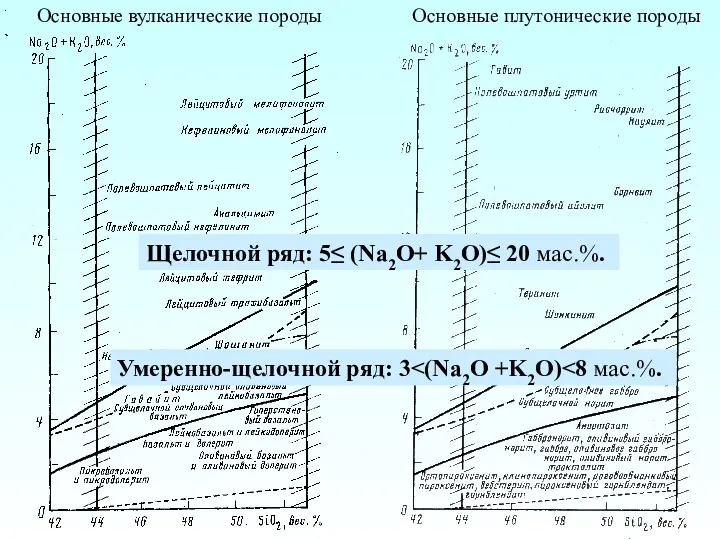 Основные вулканические породы. Основные плутонические породы
Основные вулканические породы. Основные плутонические породы Классификация химических реакций
Классификация химических реакций Металлы. Классификация металлов
Металлы. Классификация металлов Полиэтилен - термопластичный полимер этилена
Полиэтилен - термопластичный полимер этилена Периодическая система химических элементов. Знаки химических элементов
Периодическая система химических элементов. Знаки химических элементов Введение в органическую химию
Введение в органическую химию Йод. Химические свойства
Йод. Химические свойства Химиялық элемент оттегі
Химиялық элемент оттегі Эквивалент. Лекция 1
Эквивалент. Лекция 1 Строение атома
Строение атома Химические реакции
Химические реакции Воздух, его состав и значение
Воздух, его состав и значение Массовая доля растворенного вещества в растворе
Массовая доля растворенного вещества в растворе Химическая кинетика и катализ
Химическая кинетика и катализ Оксид серы (IV). Сернистая кислота и её соли
Оксид серы (IV). Сернистая кислота и её соли Минеральные удобрения
Минеральные удобрения Современные конструкционные материалы
Современные конструкционные материалы Катионная полимеризация (Лекция 6)
Катионная полимеризация (Лекция 6) Оксиды. Классификация. Получение. Свойства
Оксиды. Классификация. Получение. Свойства Поверхневі явища в дисперсних системах. Поверхнева енергія
Поверхневі явища в дисперсних системах. Поверхнева енергія Аналитические химические реакции. Классификация аналитических химических реакций
Аналитические химические реакции. Классификация аналитических химических реакций Термодинамика химических процессов
Термодинамика химических процессов Фтор (Fluorum), F
Фтор (Fluorum), F Понятие о СМС и моющем процессе
Понятие о СМС и моющем процессе Кислоты, содержащие серу (S)
Кислоты, содержащие серу (S) Количественный учет влияния заместителя на реакционную способность и его использование для интерпретации механизмов реакций
Количественный учет влияния заместителя на реакционную способность и его использование для интерпретации механизмов реакций Предельные одноатомные спирты
Предельные одноатомные спирты