Содержание
- 2. 1 Эквивалентом называют реальную или условную частицу вещества, которая может замещать, присоединять, высвобождать или быть каким-либо
- 3. 2 Эквивалентная масса кислоты (Мэк) равна отношению молярной массы кислоты к ее основности, которая определяется как
- 4. 3 Рассмотрим пример реакции: H3PO4 + 2NaOH = Na2HPO4 + 2H2O, где в молекуле ортофосфорной кислоты
- 5. 4 Эквивалентная масса основания (Мэосн) равна отношению молярной массы основания к числу замещенных гидроксильных групп: Определение
- 6. 5 Эквивалентная масса соли (Мэсоли) равна отношению молярной массы соли к произведению числа атомов металла на
- 7. 6 Эквивалентная масса оксида (Мэок) равна отношению молярной массы оксида к произведению числа атомов кислорода на
- 8. Закон эквивалентов 7 Вещества реагируют друг с другом в эквивалентных количествах. Если реакцию выразить схемой: А
- 9. 8 где: m1 – масса твердого вещества, г; Мэ1 – эквивалентная масса твердого вещества, г; V2
- 10. Примеры решения задач Задача: При окислении 5,0 г металла образуется 9,44 г оксида металла. Определить эквивалентную
- 11. 10 Известны массы оксида и металла, найдем массу кислорода: mO= mок – mме = 9,44 –
- 13. Скачать презентацию










 Атомный и ионный радиусы. Принципы шаровых упаковок
Атомный и ионный радиусы. Принципы шаровых упаковок Азот және он қосылыстары
Азот және он қосылыстары Приёмы обращения с лабораторным оборудованием
Приёмы обращения с лабораторным оборудованием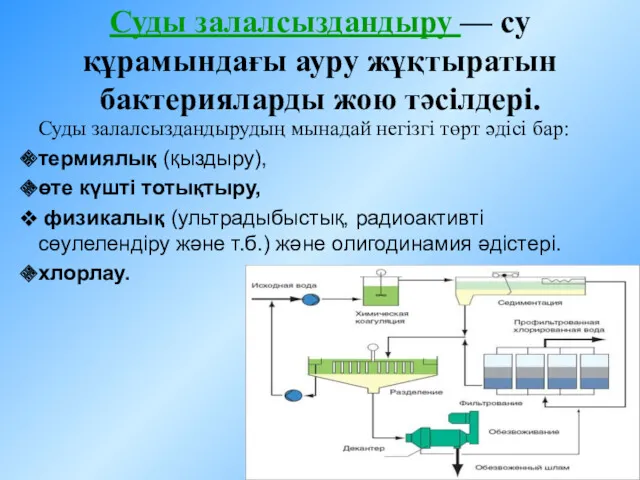 Суды залалсыздандыру - су құрамындағы ауру жұқтыратын бактерияларды жою тәсілдері
Суды залалсыздандыру - су құрамындағы ауру жұқтыратын бактерияларды жою тәсілдері Детонаційна стійкість бензину
Детонаційна стійкість бензину Одноатомные спирты
Одноатомные спирты Минералы. Классификация
Минералы. Классификация Загадки минералов. 7 класс
Загадки минералов. 7 класс Карбоновые кислоты
Карбоновые кислоты Химия в решении сырьевой проблемы
Химия в решении сырьевой проблемы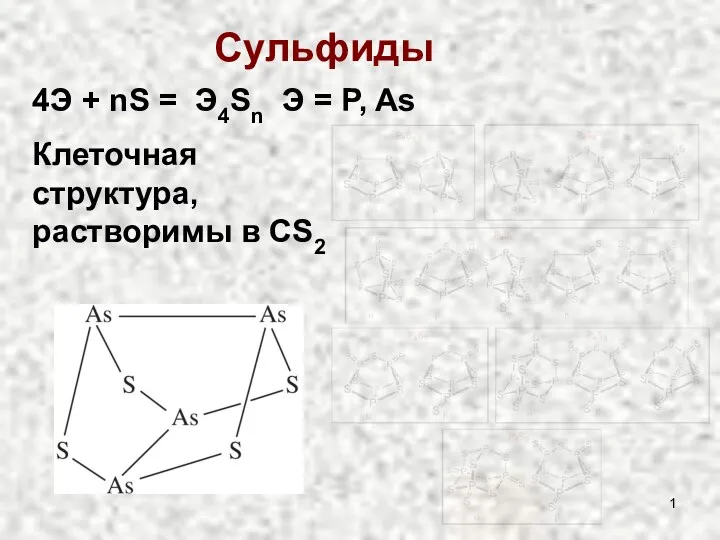 Сульфиды и оксиды
Сульфиды и оксиды Углеводы: классификация, строение и физико-химические свойства
Углеводы: классификация, строение и физико-химические свойства 6-я группа элементов. 9 класс
6-я группа элементов. 9 класс Алмаз. Алмаз дегеніміз не
Алмаз. Алмаз дегеніміз не Производные хинолина и хинуклидина, производные 4-замещенных хинолина
Производные хинолина и хинуклидина, производные 4-замещенных хинолина Научно-исследовательская работа Вся правда о продуктах с сахарозаменителями
Научно-исследовательская работа Вся правда о продуктах с сахарозаменителями Вода. Растворимость, растворы
Вода. Растворимость, растворы Кислородные соединения азота
Кислородные соединения азота Соли, их классификация и свойства в свете ТЭД
Соли, их классификация и свойства в свете ТЭД Основы химмотологии моторных топлив. Тема 3
Основы химмотологии моторных топлив. Тема 3 Камни и Козерог
Камни и Козерог АЛКАНЫ 9 класс
АЛКАНЫ 9 класс Біріншілік алкилсульфаттар және алкилэтоксисульфаттар немесе біріншілік спирттегі сульфоэфирдің тұздары. 4 Лекция
Біріншілік алкилсульфаттар және алкилэтоксисульфаттар немесе біріншілік спирттегі сульфоэфирдің тұздары. 4 Лекция Объемная доля компонента газовой смеси
Объемная доля компонента газовой смеси Строение и переваривание липидов. Классификация и роль жирных кислот. Нутриомика. Липофильных соединений
Строение и переваривание липидов. Классификация и роль жирных кислот. Нутриомика. Липофильных соединений Иccледовательская работа по химии красное, желтое ,зеленое, какое полезнее?
Иccледовательская работа по химии красное, желтое ,зеленое, какое полезнее? КОВАЛЕНТНАЯ СВЯЗЬ
КОВАЛЕНТНАЯ СВЯЗЬ Chemistry of life
Chemistry of life