Содержание
- 2. Адам термодинамикалық жүйе ретінде. Тірі ағзаның термодинамикалық жүйе ретіндегі ерекшеліктері. Пригожин принципі Жоспар Химиялық термодинамиканың негізгі
- 3. Химия – түрлі жүйелердегі, соның ішінде тірі ағзадағы да процестерді зерттеу мен түсіну үшін қажетті инструмент
- 4. Термодинамикалық жүйе – қоршаған ортадан шынайы не шартты түрде бөлінген, бір немесе өзара әрекеттесуші бірнеше денелер
- 5. Жүйе күйі: Термодинамикалық тепе-теңдік күйі – уақыт аралығындағы жүйе қасиеттерінің кез-келген нүктедегі тұрақтылығы, энергия және зат
- 6. Термодинамикалық тұрғыдан тірі ағза: стационарлық күйде болатын ашық гетерогенді термодинамикалық жүйе Тірі ағзаға тән: Жүйе параметрлерінің
- 7. Ішкі энергия (U) –жүйенің жалпы энергия қоры, жүйе бөлшектерінің өзара әрекеттесуі мен қозғалыстарының барлық түрін құрайды
- 8. Энтальпия (Н) –изобарлы-изотермиялық жағдайдағы жүйенің энергиясын сипаттайтын жүйе күйінің функциясы. Ол ішкі энергия мен жұмыстың қосындысына
- 9. Химиялық реакция қай бағытта өздігінен жүру керек? Өздігінен жүретін процесс – сыртқы факторлардың әсерінсіз жүретін термодинамикалық
- 10. Егер процесс кезінде ретсіздік өзгермесе (ΔS = 0), онда процестің бағыты энтальпияның өзгерісімен анықталады және процесс
- 11. Дж. Гиббс (1839-1903) Процестердің өздігінен жүру шарты ретінде екі фактордың да (энтальпия және энтропия) әсерін ескеретін
- 12. Процестің өздігінен жүру мүмкіндігінің шарттары: Процесс өздігінен жүреді dG 0) Процесс өздігінен жүрмейді dG>0 (dH>0, dS
- 13. Пригожин принципі: Стационарлық күйдегі термодинамикалық ашық жүйеде қайтымсыз процестердің жүру барысындағы энтропияның пайда болу жылдамдығының мәні
- 14. Энергетикалық қабысу принципі: АТФ + Н2О → АДФ + H3PO4 (а) Глюкоза + фруктоза → сахароза
- 15. Химиялық кинетика химиялық реакциялардың жылдамдығын; химиялық реакциялардың жүру механизмін; реакция жылдамдығының түрлі факторларға тәуелділігін зерттейтін ғылыми
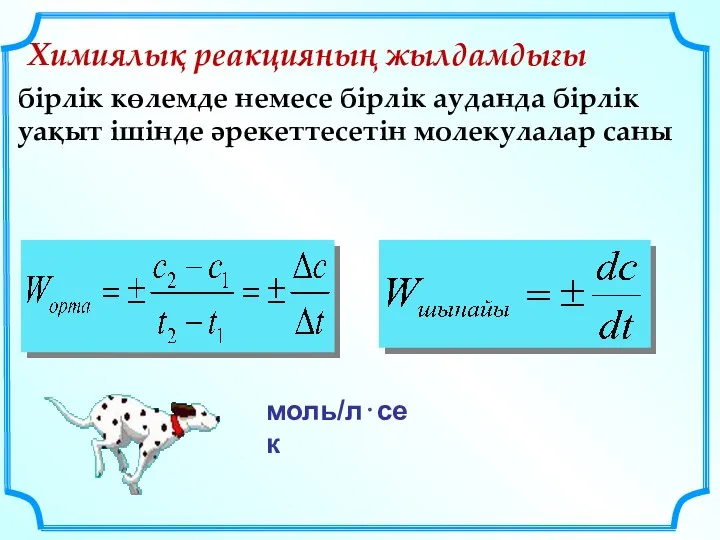
- 16. Химиялық реакцияның жылдамдығы бірлік көлемде немесе бірлік ауданда бірлік уақыт ішінде әрекеттесетін молекулалар саны моль/л⋅сек
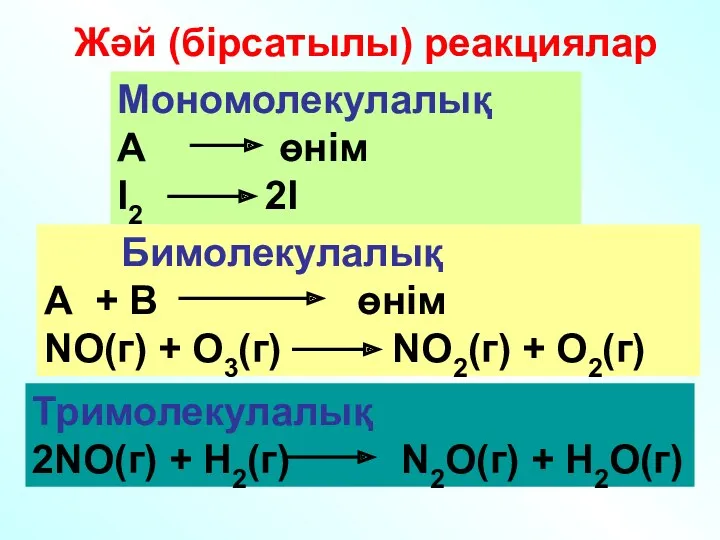
- 17. Жәй (бірсатылы) реакциялар Мономолекулалық А өнім I2 2I Тримолекулалық 2NO(г) + H2(г) N2O(г) + H2O(г) Бимолекулалық
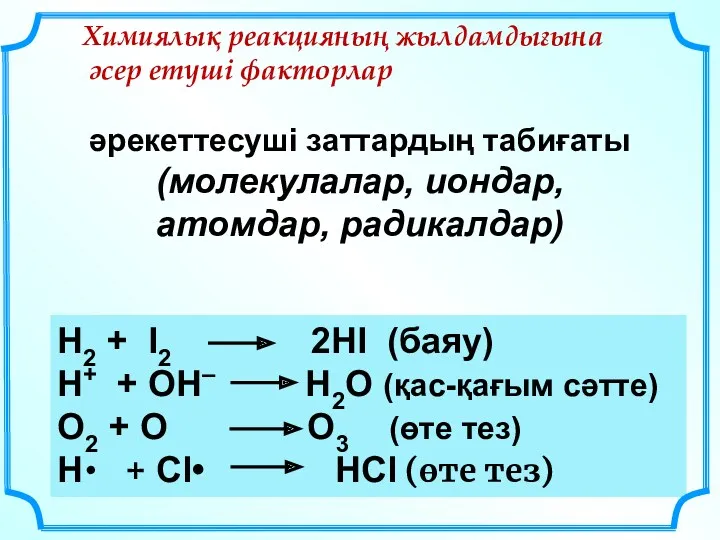
- 18. Химиялық реакцияның жылдамдығына әсер етуші факторлар: әрекеттесуші заттардың табиғаты; әрекеттесуші заттардың концентрациясы; температура; катализатордың қатысы
- 19. әрекеттесуші заттардың табиғаты (молекулалар, иондар, атомдар, радикалдар) Н2 + I2 2НI (баяу) Н+ + ОН– Н2О
- 20. Концентрация: Әрекеттесуші заттар концентрациясының артуымен реакция жылдамдығы артады Берілген температурада, химиялық реакцияның жылдамдығы, стехиометриялық коэффициенттері дәреже
- 21. Массалар әрекеттесуші заңы n = a + b + d – реакцияның жалпы реті aA +
- 22. Вант-Гофф теңдеуі Температураны әрбір 10 градусқа көтергенде реакция жылдамдығы 2-4 есе артады Биореакциялар үшін қолданылмайды γ
- 23. КАТАЛИЗ Оң катализ Теріс катализ Катализдің негізгі заңдылықтары Каt тек қана ТД мүмкін реакцияларды ғана жылдамдатады
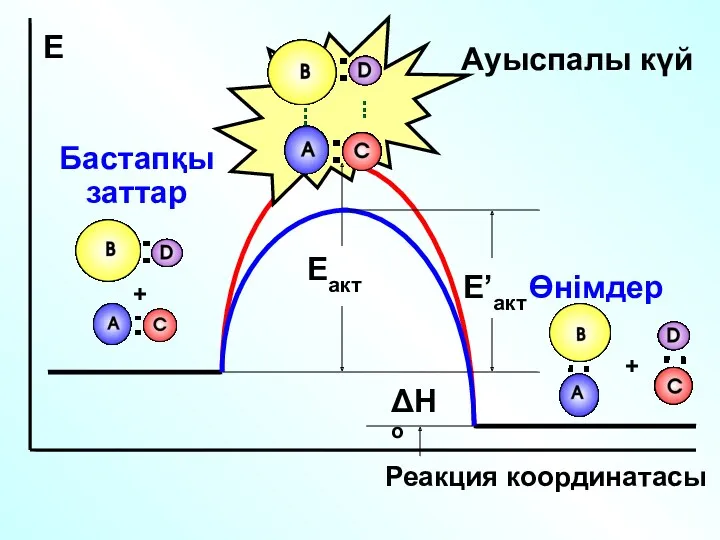
- 24. + + ΔHo Eакт Е Реакция координатасы Өнімдер Бастапқы заттар Ауыспалы күй E’акт
- 25. Ферментативті катализ Катализдіің жалпы заңдылықтары сақталынады! Ферменттердің катализатор ретіндегі негізгі ерекшеліктері: өте жоғары каталитикалық активтілігі; субстратқа
- 26. Ферменттердің каталитикалық активтілік көрсету шарттары Температураның жоғары болмауы; рН мәндерінің шағын аумағы; Қысымның тұрақты болуы.
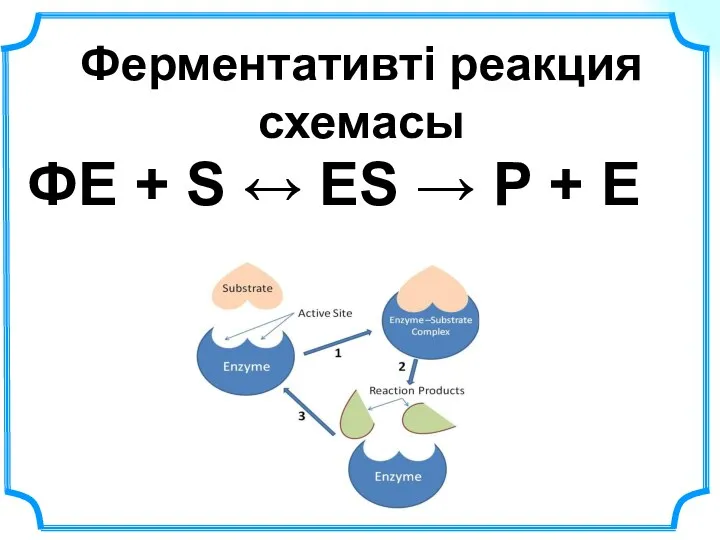
- 27. Ферментативті реакция схемасы ФЕ + S ↔ ЕS → Р + Е
- 28. Михаэлис-Ментен теңдеуі
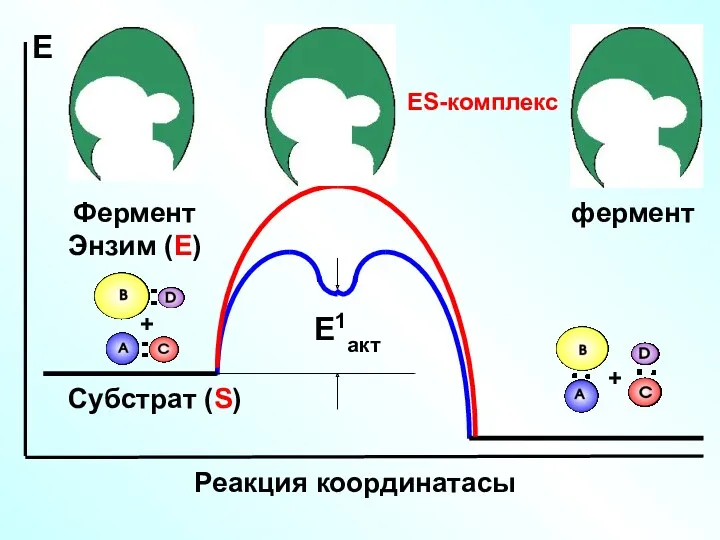
- 29. + + E1акт Е Реакция координатасы Фермент Энзим (Е) фермент ES-комплекс Субстрат (S)
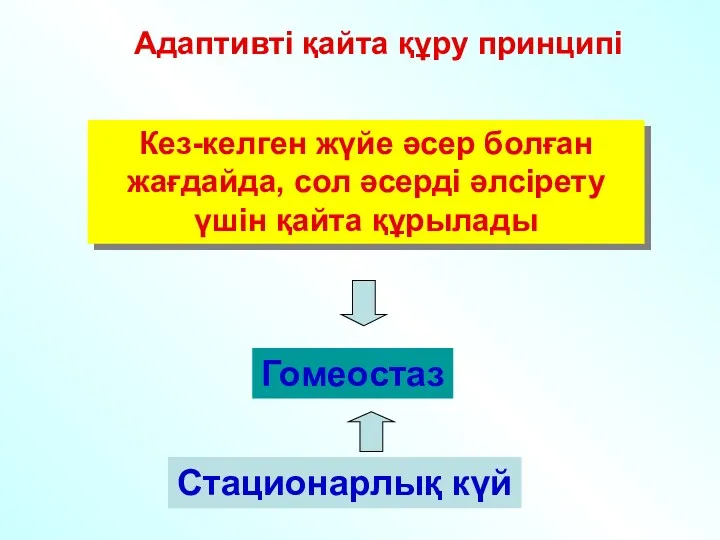
- 30. Адаптивті қайта құру принципі Кез-келген жүйе әсер болған жағдайда, сол әсерді әлсірету үшін қайта құрылады Гомеостаз
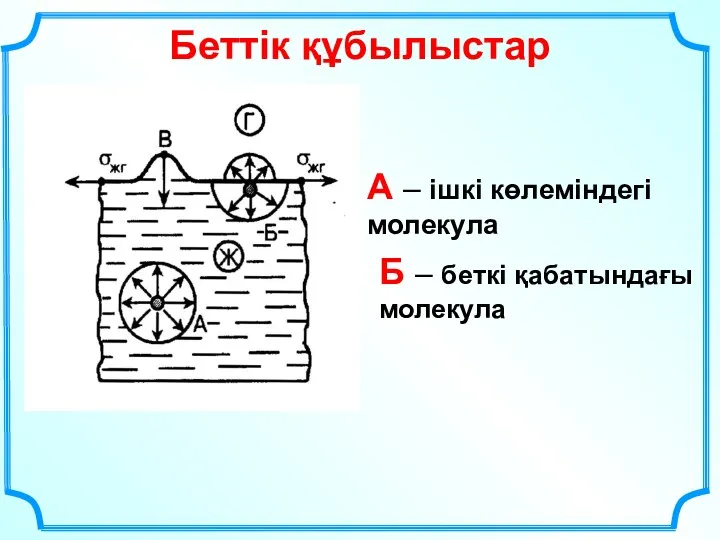
- 31. Беттік құбылыстар А – ішкі көлеміндегі молекула Б – беткі қабатындағы молекула
- 32. Адсорбция –еріген зат концентрациясының фазалардың бөліну бетінде өздігінен өзгере жүретін процесс Адсорбент – бет қабатында адсорбция
- 33. Хроматография Біреуі – қозғалмайтын, ал екіншісі – қозғалатын өзара араласпайтын екі фаза арасында заттардың таралуына негізделген,
- 34. Қоспаларды бөлу процесінің механизмі бойынша хроматография әдістерінің жіктелуі Адсорбциялық хроматография бөлінетін заттардың адсорбциялық қасиеттеріндегі айырмашылыққа негізделген
- 35. Қоспаларды бөлу процесінің механизмі бойынша хроматография әдістерінің жіктелуі Ион алмасу хроматографиясы ионит (қоршаған ортамен иондарымен алмасуға
- 36. Тәжірибені жүргізу техникасы бойынша хроматографиялық әдістердің жіктелуі Бағаналы хроматография Капиллярлы хроматография Қағаз хроматографиясы Жұқа қабатты Фазалардың
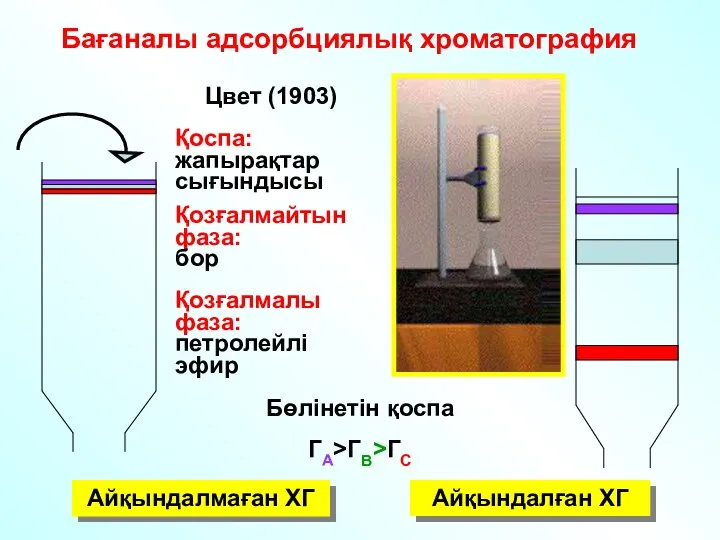
- 37. Бөлінетін қоспа ГА>ГB>ГС Айқындалмаған ХГ Айқындалған ХГ Бағаналы адсорбциялық хроматография Цвет (1903) Қоспа: жапырақтар сығындысы Қозғалмайтын
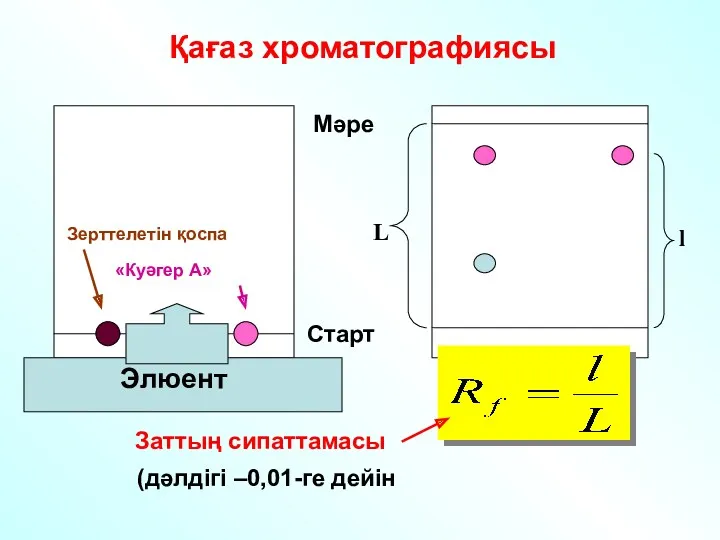
- 38. Зерттелетін қоспа «Куәгер A» Элюент Қағаз хроматографиясы Мәре Старт L l Заттың сипаттамасы (дәлдігі –0,01-ге дейін
- 39. Жұқа қабатты хроматография дейін старт кейін Тасымалдаушы: фольга, полимер Адсорбент: алюминий оксиді, силикагель
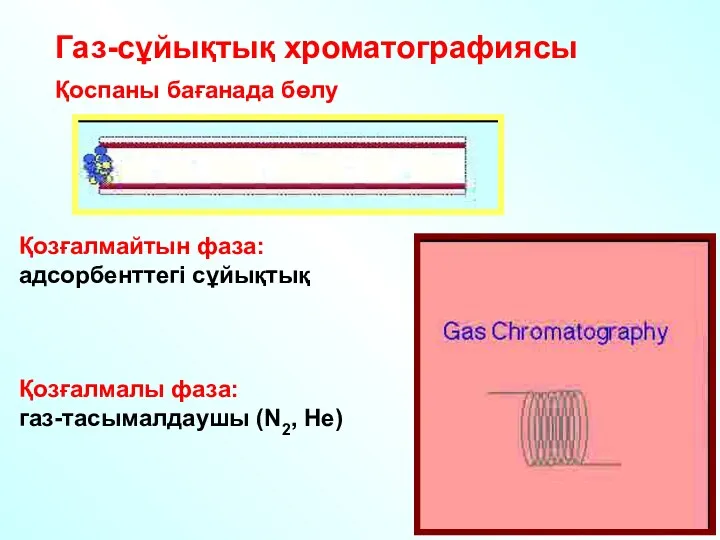
- 40. Қозғалмайтын фаза: адсорбенттегі сұйықтық Қозғалмалы фаза: газ-тасымалдаушы (N2, He) Газ-сұйықтық хроматографиясы Қоспаны бағанада бөлу
- 41. Хроматографияның артықшылықтары Талдауды орындау жылдамдығы Жоғары сезімталдығы (10-8 %-ға дейін) Талданатын заттың химиялық өзгеріске ұшырап кетпеуі
- 42. Хроматографиялық әдістердің биология және медицинада қолданылуы: кейбір патологияларда, биологиялық сұйықтықтарда пайда болатын микрокомпоненттерді анықтау; допинг-бақылауды жүргізу;
- 44. Скачать презентацию





























 Rhodium
Rhodium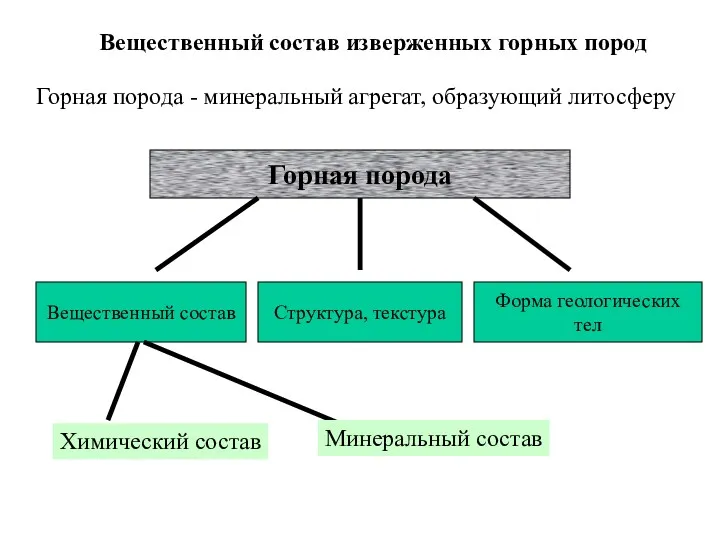 Вещественный состав изверженных горных пород
Вещественный состав изверженных горных пород Химический факультет
Химический факультет Жорсткість води і методи її усунення. 11 клас
Жорсткість води і методи її усунення. 11 клас Полисахариды: крахмал и целлюлоза
Полисахариды: крахмал и целлюлоза Сплавы металлов. 11 класс
Сплавы металлов. 11 класс Ароматические углеводороды (арены)
Ароматические углеводороды (арены) Камни и Телец
Камни и Телец Основы кристаллографии
Основы кристаллографии Мир кристаллов
Мир кристаллов Значение периодического закона
Значение периодического закона Кремний. Применение кремния
Кремний. Применение кремния Циклические углеводороды. Циклоалканы
Циклические углеводороды. Циклоалканы Биологически активные вещества и их содержание в лекарственных растениях
Биологически активные вещества и их содержание в лекарственных растениях Закономерность изменений в строении электронных оболочек атома
Закономерность изменений в строении электронных оболочек атома Основания. 8 класс
Основания. 8 класс Железо и его соединения
Железо и его соединения Кинетическое уравнение математическая запись закона действующих масс
Кинетическое уравнение математическая запись закона действующих масс Катионная полимеризация (Лекция 6)
Катионная полимеризация (Лекция 6) Циклоалканы. 10 класс
Циклоалканы. 10 класс Классификация химических реакций в органической и неорганической химии
Классификация химических реакций в органической и неорганической химии Строение атома
Строение атома Роль химии в жизни человека
Роль химии в жизни человека Палладий. История открытия химических веществ
Палладий. История открытия химических веществ Геология полезных ископаемых
Геология полезных ископаемых Типы химических реакций
Типы химических реакций Криминалистическое исследование нефтепродуктов, горючесмазочных материалов, спиртосодержащих жидкостей,
Криминалистическое исследование нефтепродуктов, горючесмазочных материалов, спиртосодержащих жидкостей, Химические реакции
Химические реакции