Содержание
- 2. Физические свойства кремния Кристаллический кремний – вещество темно-серого цвета; обладает стальным блеском; полупроводник (его электропроводность возрастает
- 3. Важнейшие соединения кремния
- 4. Родоначальник гомологического ряда кремневодородов SinH2n+2. Представляет собой очень ядовитый бесцветный газ с запахом, напоминающим AsH3 и
- 5. Встречается главным образом в виде минерала кварца. Загрязненный примесями кварц - обычный песок - является одним
- 6. Кремниевая кислота H2SiO3. Почти нерастворима в воде (в форме истинного раствора). Легко образует коллоидные растворы и
- 7. Стекло Na2CaSi6O14 или Na2O.CaO.6SiO2. Довольно близко к этому составу подходит обычное оконное стекло. Практически нерастворимо, однако
- 8. Карбид кремния (карборунд) SiC. Твердое, тугоплавкое вещество. Его кристаллическая решетка аналогична решетке алмаза. Является полупроводником. Интенсивно
- 9. Нахождение кремния в природе
- 10. Кремний – один из самых распространенных в земной коре элементов (более 25% массы). Если углерод –
- 11. Природные силикаты – это довольно сложные вещества. Их состав обычно изображается как соединение нескольких оксидов. Соединения,
- 12. Многие природные силикаты в чистом виде являются драгоценными камнями, например, аквамарин, изумруд, топаз и др. Значительная
- 13. Оксид кремния (IV), окрашенный различными примесями, образует драгоценные и полудрагоценные камни – агат, аметист, яшма. В
- 14. Химические свойства кремния
- 15. По химическим свойствам кремний, как и углерод, является неметаллом, но его неметалличность выражена слабее, так как
- 16. Кремний при обычных условиях довольно инертен, что следует объяснить прочностью его кристаллической решетки. Непосредственно при комнатной
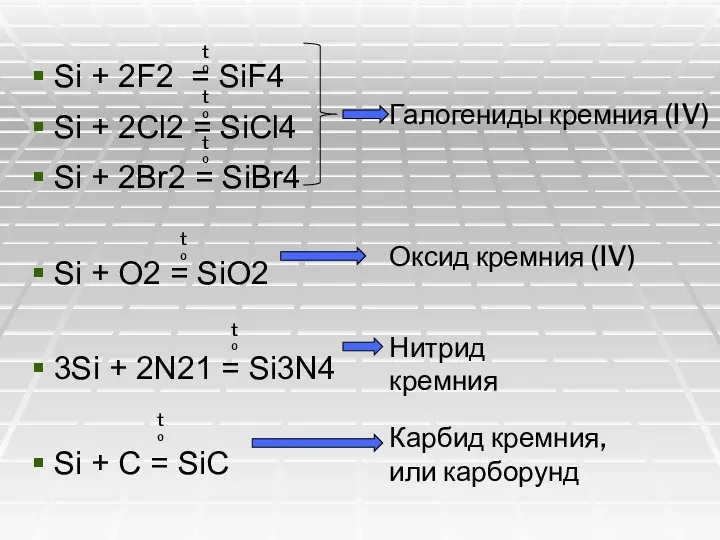
- 17. Si + 2F2 = SiF4 Si + 2Cl2 = SiCl4 Si + 2Br2 = SiBr4 Si
- 18. В технике карборунд получают в электрических печах из смеси песка и кокса: SiO2 + 3C =
- 19. Кремний как восстановитель взаимодействует и с некоторыми сложными веществами, например с фтороводородом: Si + 4HF =
- 20. Кремний не растворяется даже в азотной кислоте, так как на его поверхности образуется плотная оксидная пленка
- 21. Водные растворы щелочей растворяют кремний с образованием растворимых солей кремниевой кислоты – силикатов, при этом происходит
- 22. Виртуальный эксперимент
- 23. При взаимодействии с металлами кремний играет роль окислителя. Соединения кремния с металлами называют силицидами : Si
- 24. Получение кремния
- 25. В промышленности кремний технической чистоты получают, восстанавливая расплав SiO2 коксом при температуре около 1800 °C в
- 26. 1. Очистка в лабораторных условиях может быть проведена путём предварительного получения силицида магния Mg2Si. Далее из
- 27. 2. Очистка кремния в промышленных масштабах осуществляется путём непосредственного хлорирования кремния. При этом образуются соединения состава
- 28. 3. Разрабатываются более дешёвые, чистые и эффективные промышленные технологии очистки кремния. На 2010 г. к таковым
- 29. Получение кремния термитным способом
- 30. Применение кремния
- 31. Кремний используют в качестве полупроводника. Из него изготавливают так называемые солнечные батареи, превращающие световую энергию в
- 32. Соединения кремния служат основой для производства стекла и цемента. Также существует силикатная керамика — кирпич, фарфор,
- 34. Скачать презентацию






























 Простые вещества металлы
Простые вещества металлы Биотыңайтқыштар
Биотыңайтқыштар Цинк
Цинк Тканые армирующие наполнители
Тканые армирующие наполнители Углеводы. Урок по химии для 9 класса
Углеводы. Урок по химии для 9 класса Оксиди нітрогену
Оксиди нітрогену Классы неорганических веществ (лекция № 4/5)
Классы неорганических веществ (лекция № 4/5) Роль хімії у розв`язанні екологічної проблеми
Роль хімії у розв`язанні екологічної проблеми Молекулярна маса речовини
Молекулярна маса речовини Расчеты по химическим уравнениям
Расчеты по химическим уравнениям Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Запалювання нагрітим тілом та електричним розрядом
Запалювання нагрітим тілом та електричним розрядом Интересные факты о химических веществах
Интересные факты о химических веществах Аналитическая химия. Предмет и задачи
Аналитическая химия. Предмет и задачи General, specific properties are common to all matters
General, specific properties are common to all matters Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25)
Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25) Фосфор и его соединения. Урок по химии для 9 класса
Фосфор и его соединения. Урок по химии для 9 класса Химические реакторы
Химические реакторы Физические методы стабилизации масел
Физические методы стабилизации масел Экспериментальным исследованием установить тип данной химической реакции
Экспериментальным исследованием установить тип данной химической реакции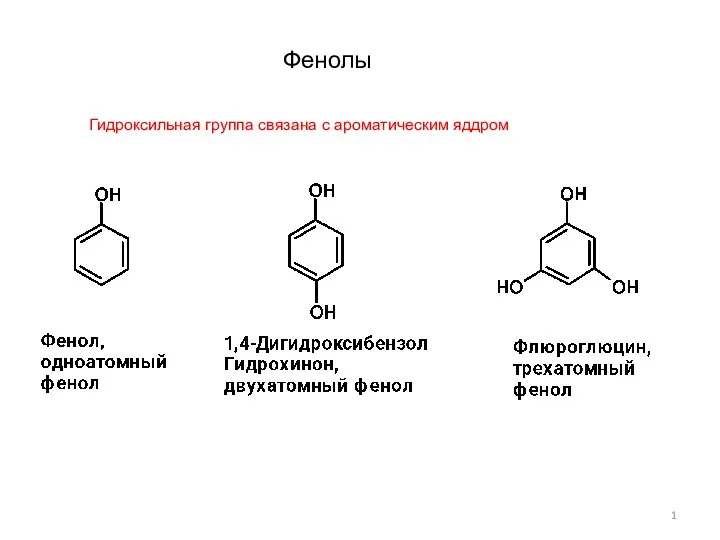 Фенолы-1
Фенолы-1 Химический факультет
Химический факультет Непредельные углеводороды. Алкины
Непредельные углеводороды. Алкины Катиониты. Классификация катионитов
Катиониты. Классификация катионитов Азотная кислота
Азотная кислота Классификация химических реакций
Классификация химических реакций Озон. Применение
Озон. Применение Дисперсные системы
Дисперсные системы