Содержание
- 2. План 1.1. Введение 1.2.Классификация органических соединений 1.3. Номенклатура органических соединений
- 3. 1.1 Введение
- 4. Биоорганическая химия изучает строение и реакционную способность органических веществ, лежащих в основе процессов жизнедеятельности, в непосредственной
- 5. Научную основу биоорганической химии составляют закономерности во взаимосвязи строения и реакционной способности органических соединений
- 6. Целью биоорганической химии как самостоятельной дисциплины является формирование знаний о взаимосвязи строения и химических свойств биологически-
- 7. История развития органической химии Органическая химия в своем развитии прошла несколько этапов: Эмпирический 2. Аналитический 3.
- 8. История развития органической химии Эмпирический -накопление экспериментальных данных
- 9. Теофраст Парацельс (1493–1541) Швейцарский врач -эмпирик, естество-испытатель и ал-химик эпохи Воз-рождения. Он яв-ляется основопо-ложником ятро-химии (меди-цинской
- 10. История развития органической химии 2.Аналитический Основное внимание исследователей направлено на выяснение состава органических соединений и создание
- 11. История развития органической химии 3. Структурный Созданы соединения не существующие в природе, но предсказанные теорией. Именно
- 12. 4. Особенно быстрое раз-витие органическая химия получила в начале 20 века, который получил название современного периода
- 13. Органическая химия- химия углерода и его соединений Определение А.М.Бутлерова (1828-1886)
- 14. Определение К.Шорлеммера Органическая химия – это химия углеводородов и их производных, причем в состав производных могут
- 15. 1.2 Классификация органических соединений Для описания структуры молекул органических соединений используют различные химические формулы: эмпирические, молекулярные
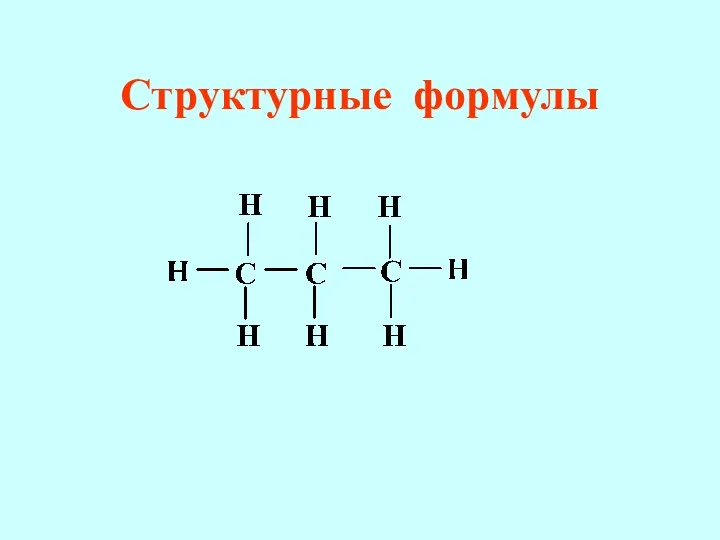
- 16. Наиболее полную информацию о строении молекулы содержит структурная (графическая) фор-мула,которая отражает природу атомов, входящих в состав
- 17. Структурные формулы
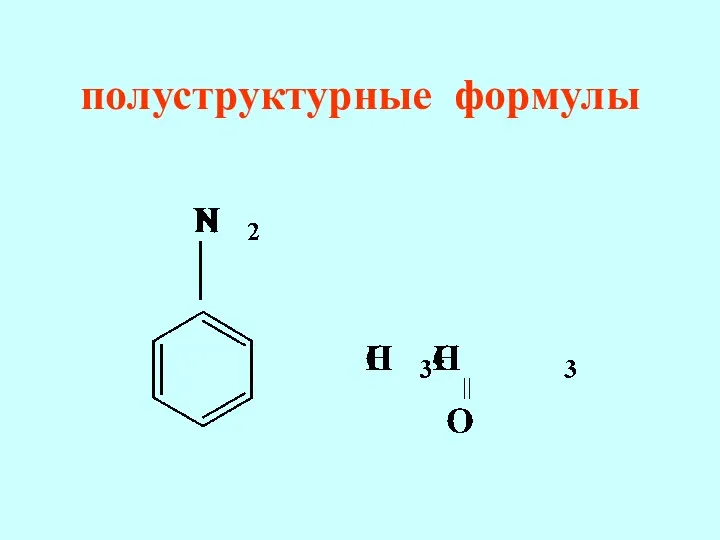
- 18. полуструктурные формулы
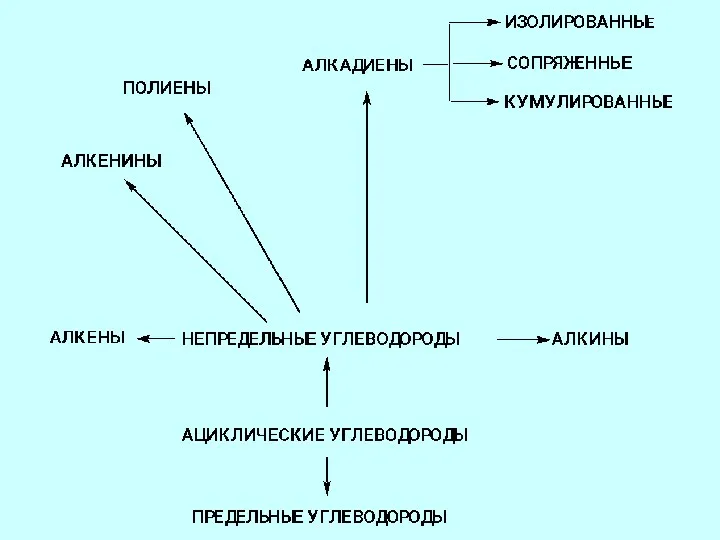
- 19. Классификация органических соединений Органические соединения Ациклические Циклические Карбоциклические Гетероциклические Алициклические Ароматические
- 21. Предельные или насыщенные углеводороды (алканы, парафины) содержат только простые углерод-углеродные связи, все остальные валентности атомов углерода
- 22. Непредельные или ненасыщенные углеводороды Имеют кратные (двойные или тройные) углерод – углеродные связи
- 23. Алкены (олефины, этиленовые углеводороды) Содержат одну двойную связь. Общая формула СnН2n Родоначальник ряда – этилен СН2
- 24. Алкины (ацетиленовые углеводороды) имеют тройную связь Общая формула СnН2n-2 Родоначальник ряда – ацетилен СН≡СН
- 25. Алкадиены (диолефины, диеновые углеводороды) содержат две двойные связи Общая формула как у алкинов СnН2n-2 ;алкины и
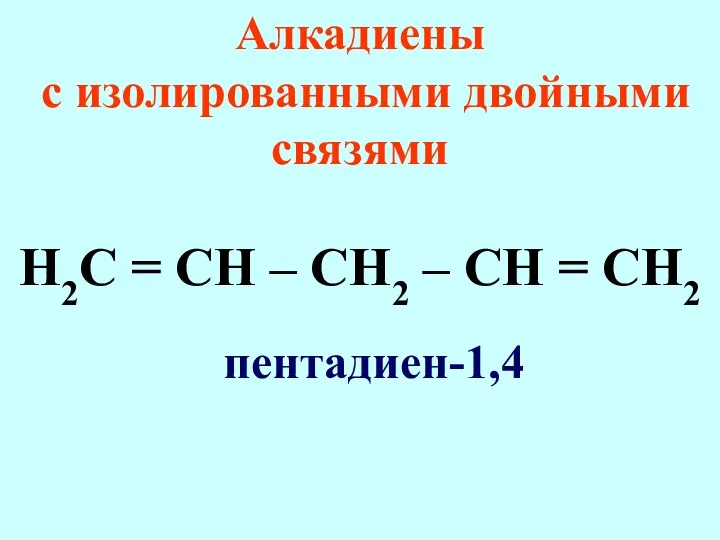
- 26. Алкадиены с изолированными двойными связями Н2С = СН – СН2 – СН = СН2 пентадиен-1,4
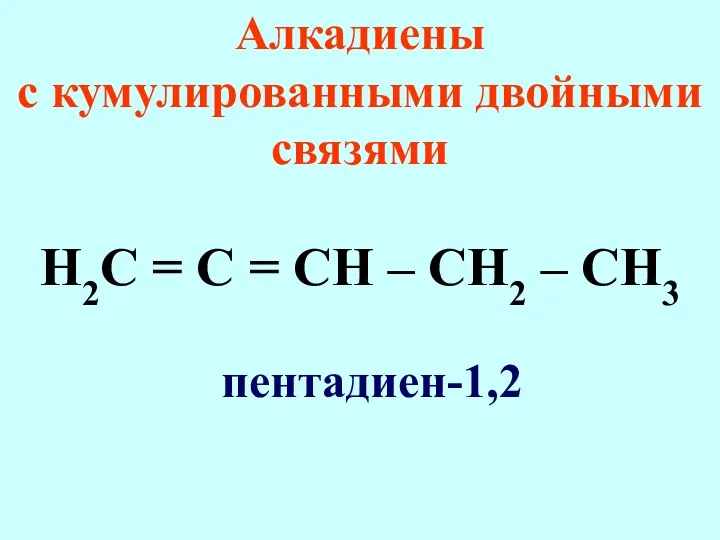
- 27. Алкадиены с кумулированными двойными связями Н2С = С = СН – СН2 – СН3 пентадиен-1,2
- 28. Алкадиены с сопряженными двойными связями Н2С = СН – СН = СН – СН3 пентадиен-1,3
- 29. Алкенины соединения с одной двойной и одной тройной связями Н2С = СН – С ≡ СН
- 30. Алкадиины соединения с двумя тройными связями НС ≡ С – С ≡ СН бутадиин-1,3
- 31. Полиены (полиолефины) соединения со многими двойными связями Н2С = СН – СН = СН – СН
- 32. Алициклические углеводороды (циклоалканы, циклопара-фины, полиметилены, цик-ланы) – циклические соединения содержащие только простые одинарные связи. Общая формула
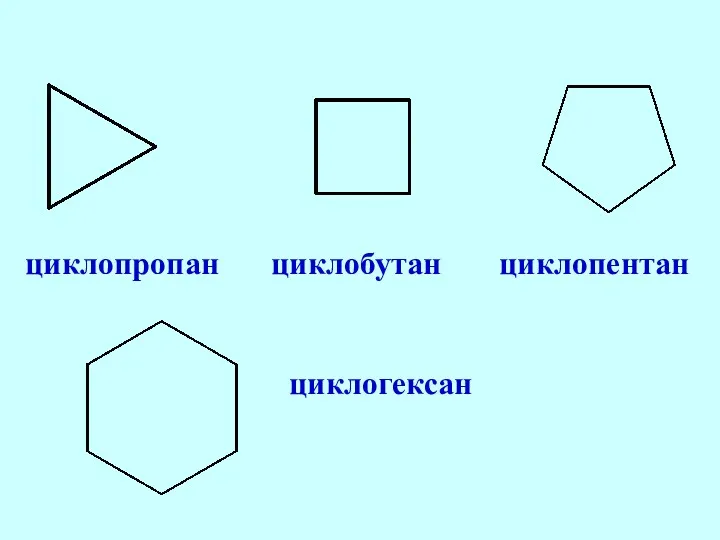
- 33. циклопропан циклобутан циклопентан циклогексан
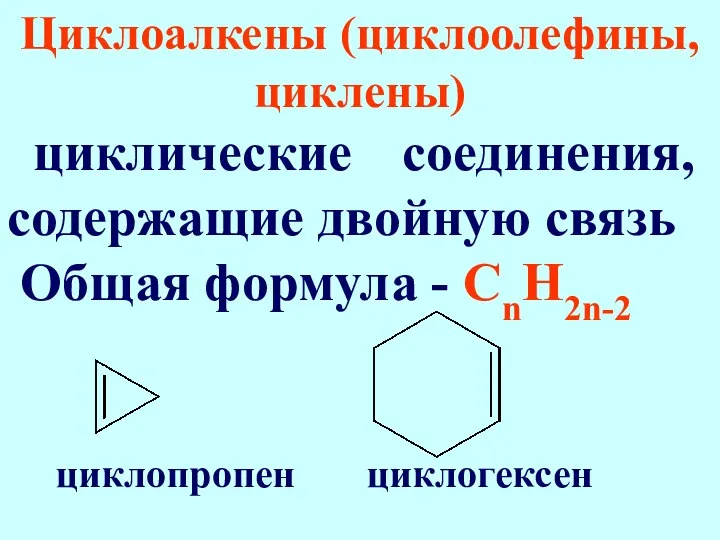
- 34. Циклоалкены (циклоолефины, циклены) циклические соединения, содержащие двойную связь Общая формула - СnН2n-2 циклопропен циклогексен
- 35. Циклоалкадиены циклические соединения, содержащие две двойные связи. Общая формула – СnН2n-4 циклопентадиен-1,3 циклогексадиен-1,4
- 36. Алициклические соединения могут содержать один, два и более циклов. Бициклические соединения в зависимости от способа соединения
- 37. Конденсированные Спирановые Спиро-[2,5]-октан Бицикло-[4,2,0]-октан
- 38. Мостиковые Бицикло-[3,2,1]-октан
- 39. Ароматические соединения (арены) – группа карбоциклов, характеризующихся наличием ароматической системы. Ароматические соединения бывают двух видов:
- 40. Бензоидные ароматические соединения обязательной составной частью молекулы является бензольное ядро
- 41. Небензоидные ароматические соединения структуры, отвечающие требованиям ароматич-ности, но лишенные шестичленных бензольных колец
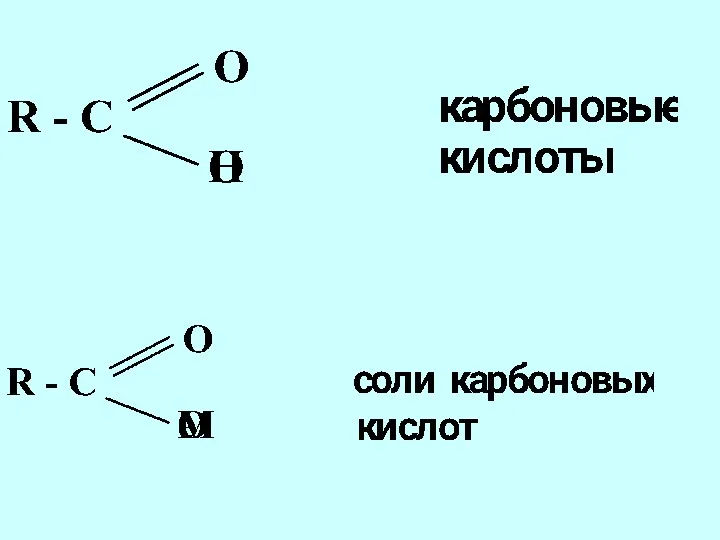
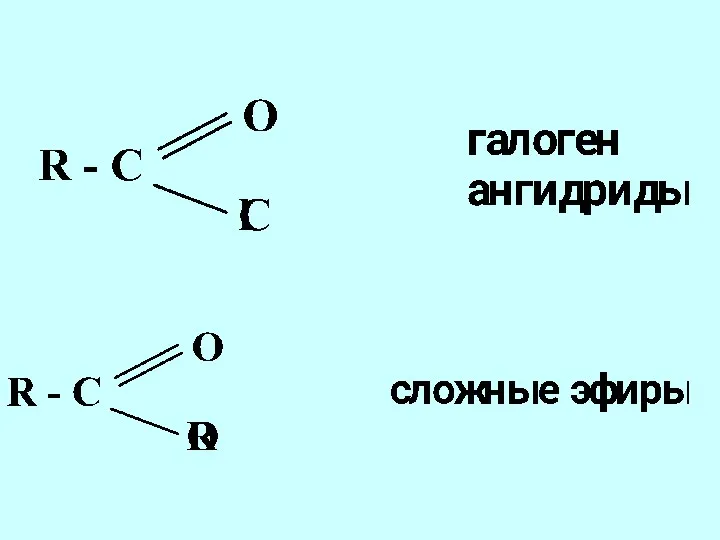
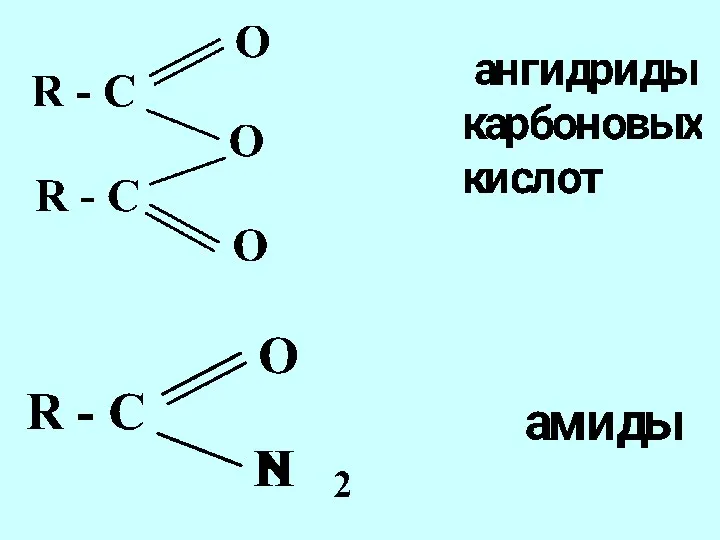
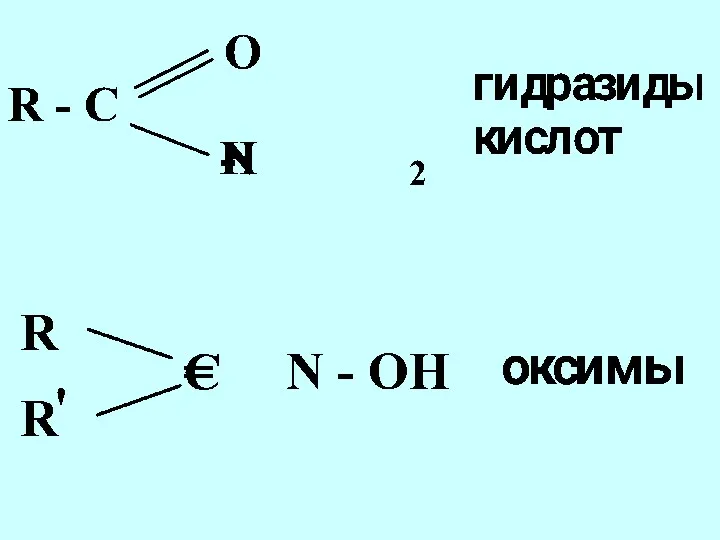
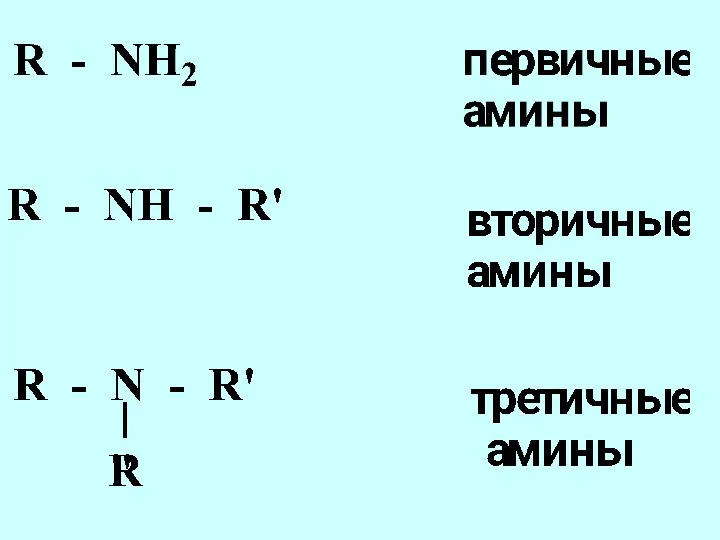
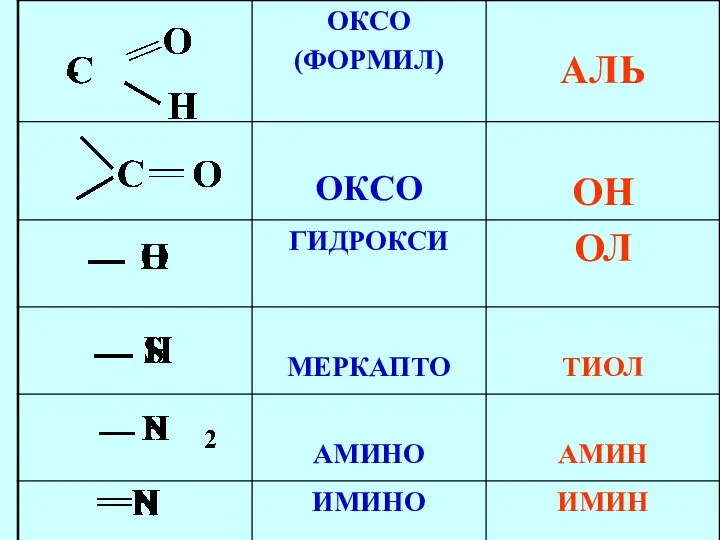
- 42. Функциональная группа структурный фрагмент молекулы, определяющий её химические свойства
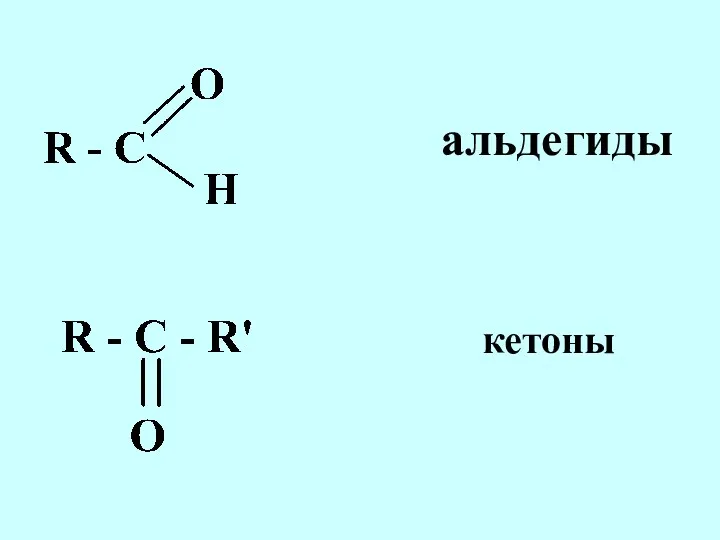
- 44. альдегиды кетоны
- 51. 1.3 Номенклатура органических соединений Номенклатура – это совокуп-ность названий веществ, их групп и классов, а также
- 52. Тривиальная Названия соединений случайные, обусловленные различными обстоятельствами (в основе лежат различные отличительные признаки).
- 53. 1.Источники выделения 2. Отличительные свойства 3. Способы выделения (получения). 4. Область применения.
- 54. Рациональная все соединения в данном гомологическом ряду рассматриваются как производные простейшего соединения для данного гомологического ряда
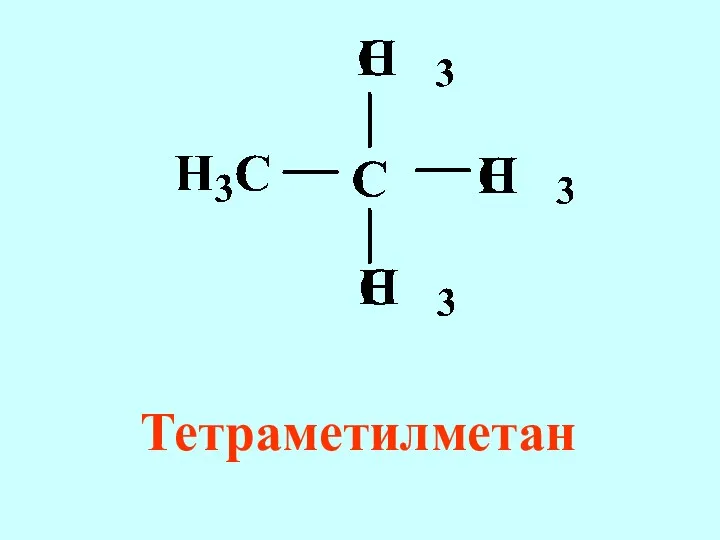
- 55. Тетраметилметан
- 56. Диметилэтилэтилен
- 57. Радикально-функциональная номенклатура Применяется для названий моно- и бифункциональных соединений некоторых классов природных соединений (терпены, стероиды, алкалоиды
- 58. В названии старшей характеристической группы не применяются суффиксы, называется радикал и основной класс соединений
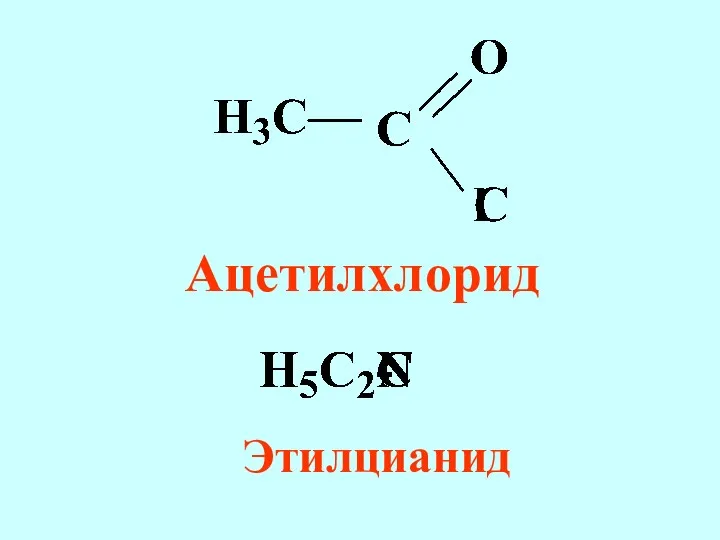
- 59. Ацетилхлорид Этилцианид
- 60. Изобутиловый спирт Винилхлорид
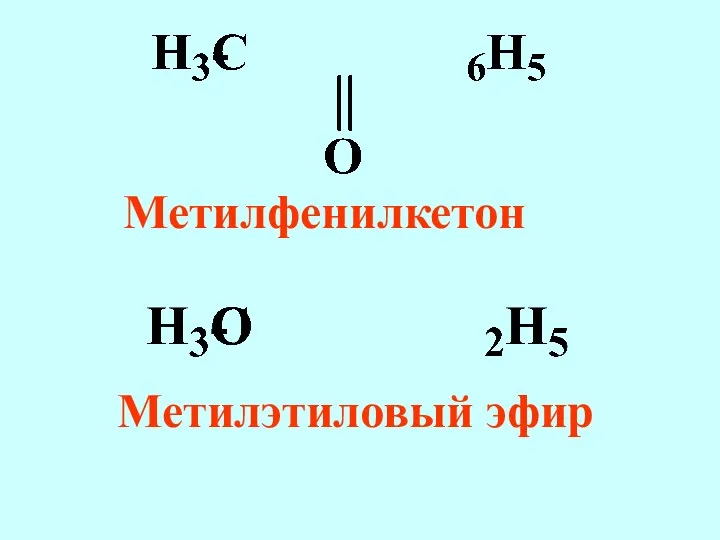
- 61. Метилфенилкетон Метилэтиловый эфир
- 62. В настоящее время признанной во всём мире является номенклатура IUPAC International Union of Pure and Applied
- 63. Её ещё называют международной, систематической, Женевской (т.к. основы заложены в 1892 году на международном конгрессе химиков
- 64. Название IUPAC номенклатура получила на ХIХ конгрессе Международного союза чистой и прикладной химии в 1957 году.
- 65. Общая схема составления названий Префикс + корень + суффикс + окончание Боковые цепи и младшие функцио-нальные
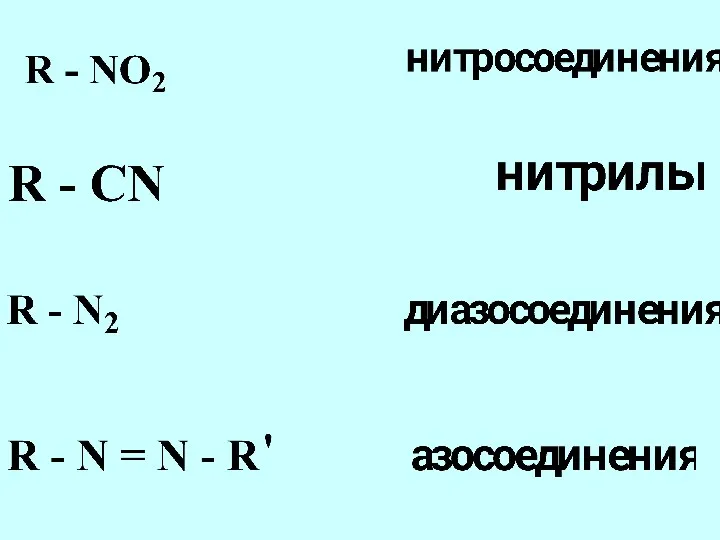
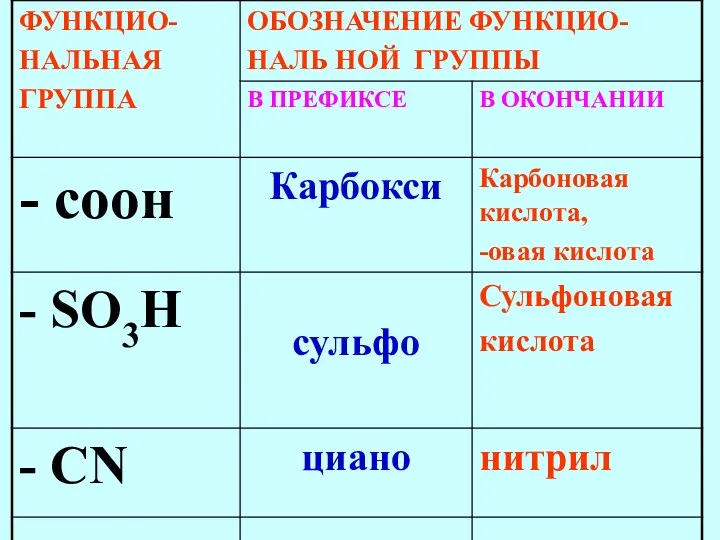
- 66. Только в префиксе Cl, Br, I, F - OR алкокси - SR алкилтио арилтио - NO2
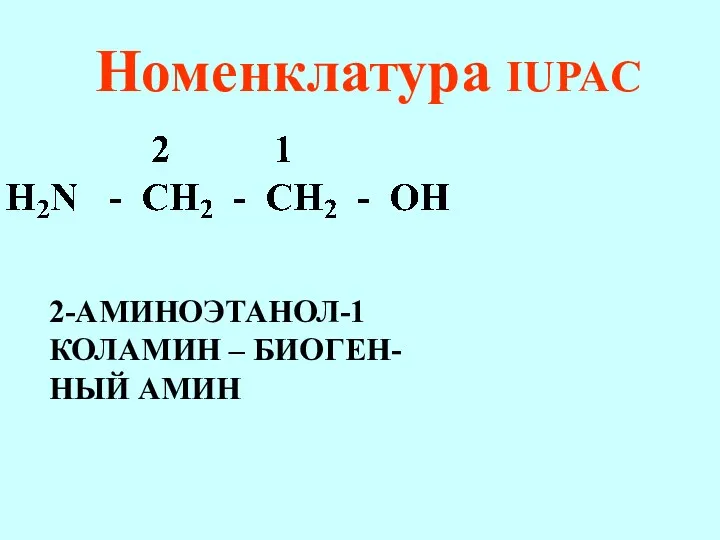
- 67. Номенклатура IUPAC 2-АМИНОЭТАНОЛ-1 КОЛАМИН – БИОГЕН- НЫЙ АМИН
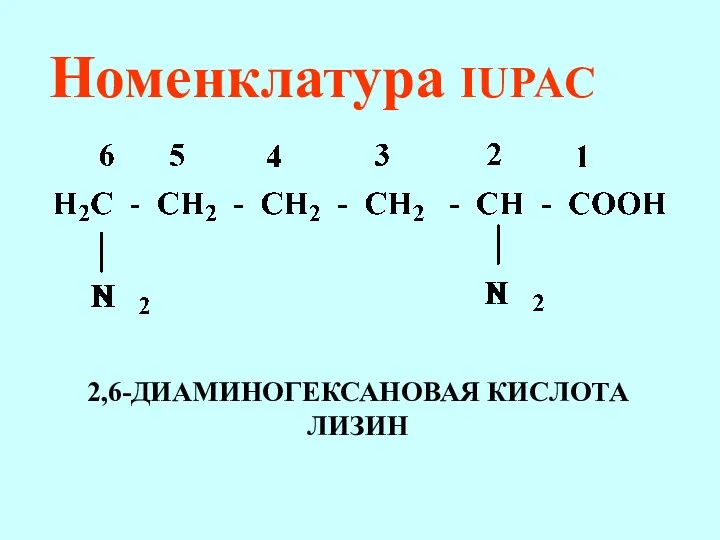
- 68. Номенклатура IUPAC 2,6-ДИАМИНОГЕКСАНОВАЯ КИСЛОТА ЛИЗИН
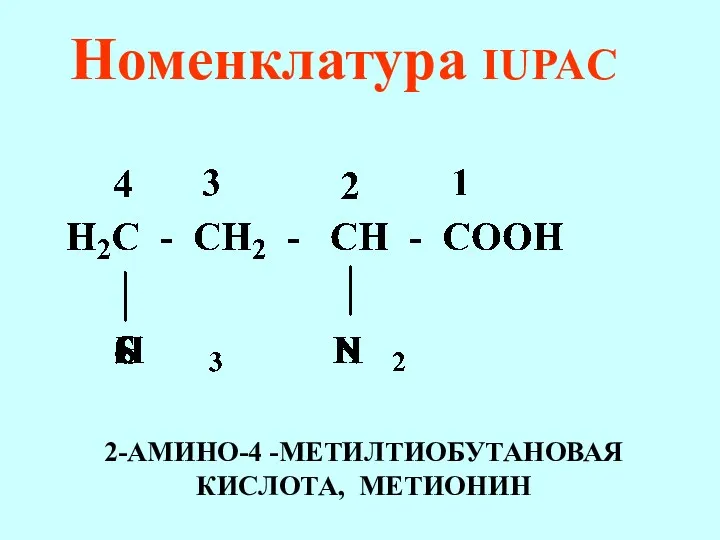
- 69. Номенклатура IUPAC 2-АМИНО-4 -МЕТИЛТИОБУТАНОВАЯ КИСЛОТА, МЕТИОНИН
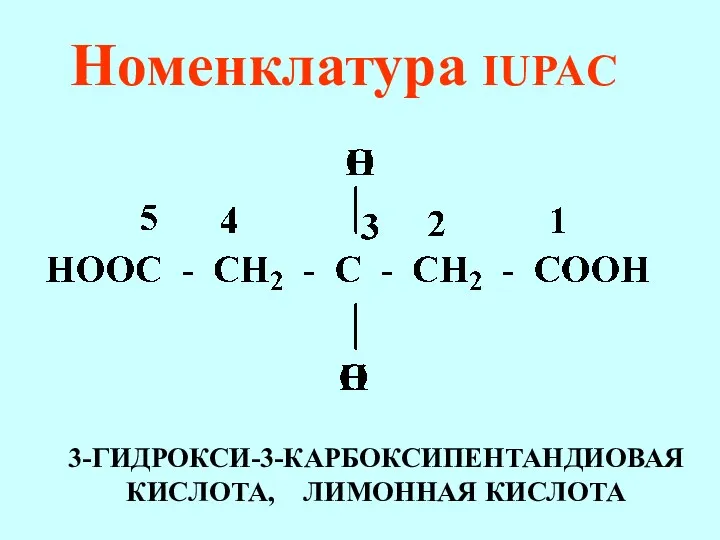
- 70. Номенклатура IUPAC 3-ГИДРОКСИ-3-КАРБОКСИПЕНТАНДИОВАЯ КИСЛОТА, ЛИМОННАЯ КИСЛОТА
- 71. Названия некоторых углеводородных радикалов Метил; этил Изопропил
- 72. Названия некоторых углеводородных радикалов Изобутил Втор. бутил
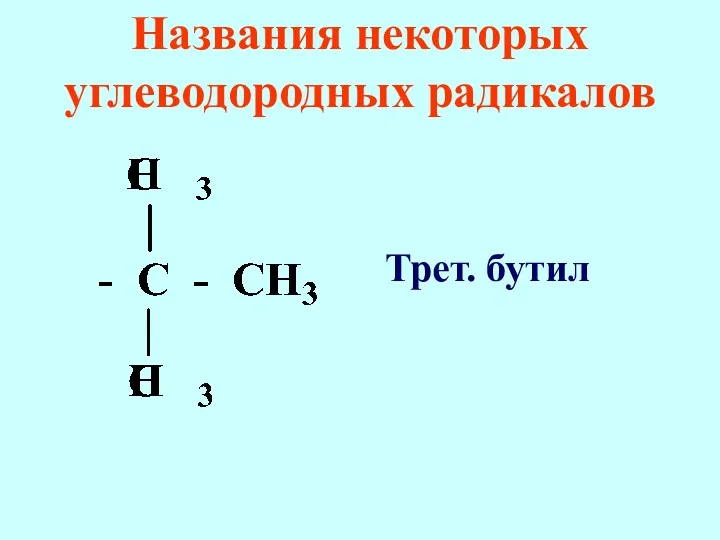
- 73. Названия некоторых углеводородных радикалов Трет. бутил
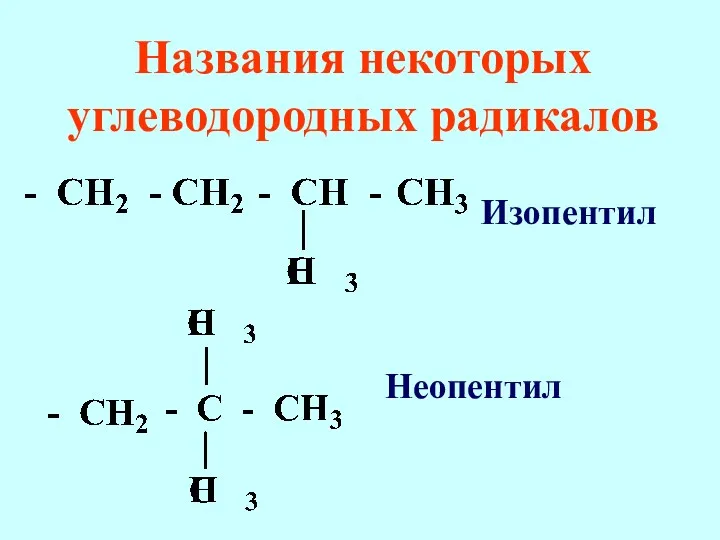
- 74. Названия некоторых углеводородных радикалов Изопентил Неопентил
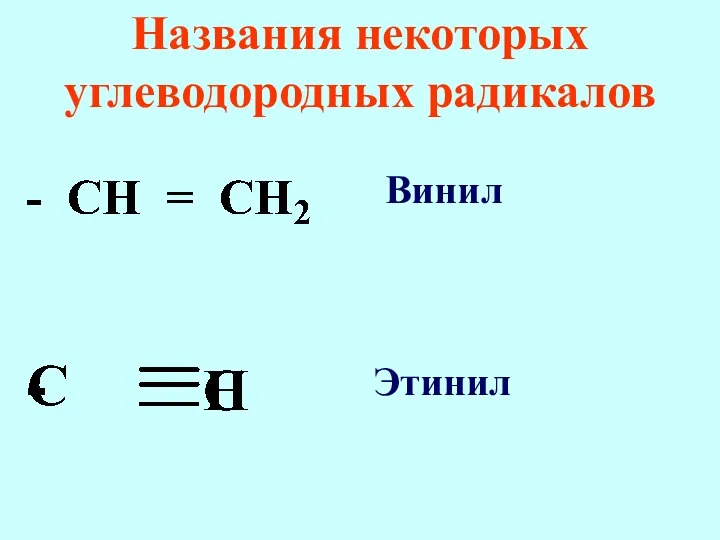
- 75. Названия некоторых углеводородных радикалов Винил Этинил
- 76. Названия некоторых углеводородных радикалов Аллил
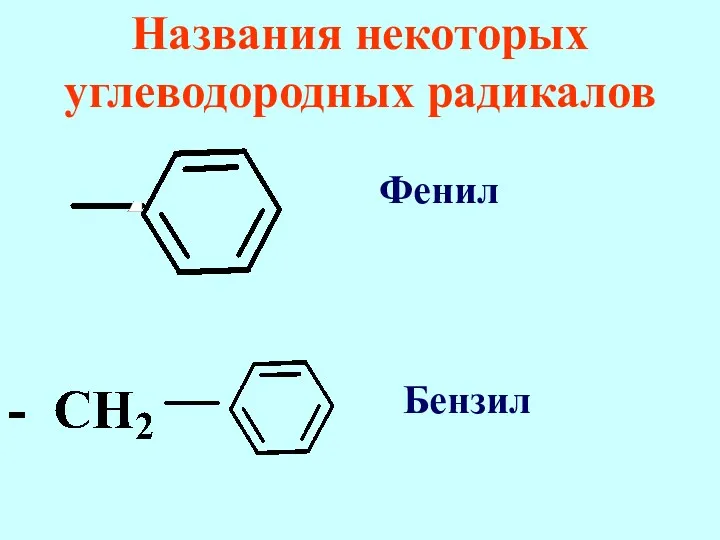
- 77. Названия некоторых углеводородных радикалов Фенил Бензил
- 78. Важнейшие функциональные группы, расположенные в порядке убывания старшинства
- 82. Скачать презентацию




























![Конденсированные Спирановые Спиро-[2,5]-октан Бицикло-[4,2,0]-октан](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/400765/slide-36.jpg)
![Мостиковые Бицикло-[3,2,1]-октан](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/400765/slide-37.jpg)






















 Полифенолды қосылыстар. Флавоноидтар
Полифенолды қосылыстар. Флавоноидтар Фазовое равновесие
Фазовое равновесие Основы термической и химико-термической обработки стали. Теория и технология термической обработки стали. Лекция 3. Тема 7
Основы термической и химико-термической обработки стали. Теория и технология термической обработки стали. Лекция 3. Тема 7 Хром. Физические свойства и применение
Хром. Физические свойства и применение Валентность и степень окисления
Валентность и степень окисления Минералы и горные породы
Минералы и горные породы Алюминий и его соединения
Алюминий и его соединения Закон постоянства состава. Молекулярная формула вещества
Закон постоянства состава. Молекулярная формула вещества Агрегатное состояние веществ и типы химических связей
Агрегатное состояние веществ и типы химических связей Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Азотная кислота и ее соли. 9 класс
Азотная кислота и ее соли. 9 класс Минералы и их основные морфологические характеристики
Минералы и их основные морфологические характеристики Спирты
Спирты Оксиды углерода
Оксиды углерода Коллоидные ПАВ. Мицеллообрaзование в растворах коллоидных ПАВ. Солюбилизация
Коллоидные ПАВ. Мицеллообрaзование в растворах коллоидных ПАВ. Солюбилизация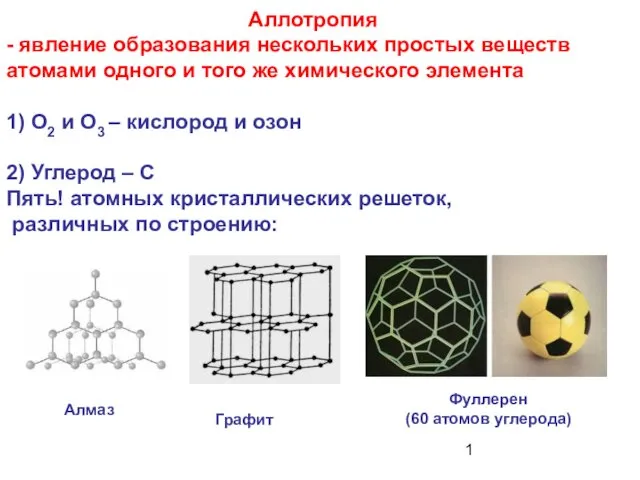 Аллотропия - явление образования нескольких простых веществ атомами одного и того же химического элемента
Аллотропия - явление образования нескольких простых веществ атомами одного и того же химического элемента Соли. 11 класс
Соли. 11 класс Аминокислоты
Аминокислоты Органические и неорганические кислоты
Органические и неорганические кислоты Отложения и коррозия
Отложения и коррозия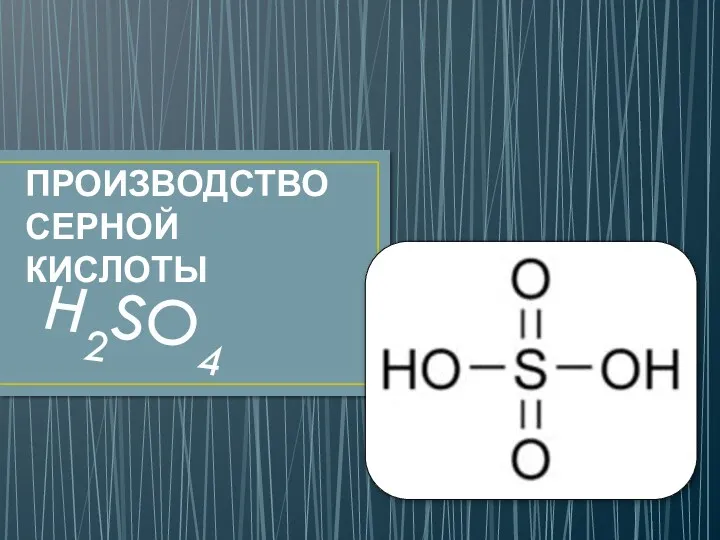 Производство серной кислоты
Производство серной кислоты Метод молекулярных орбиталей
Метод молекулярных орбиталей Водород. Общая характеристика, нахождение в природе. Получение и физические свойства
Водород. Общая характеристика, нахождение в природе. Получение и физические свойства Кисень та хімічні властивості кисню. 7 клас
Кисень та хімічні властивості кисню. 7 клас Химические свойства воды
Химические свойства воды Состав, строение и свойства аминокислот
Состав, строение и свойства аминокислот Сера
Сера Теория твердения минеральных вяжущих веществ
Теория твердения минеральных вяжущих веществ