Содержание
- 2. Характеристика химических реакторов 1. В зависимости от фазового состояния реагирующих веществ 2. По характеру операций питания
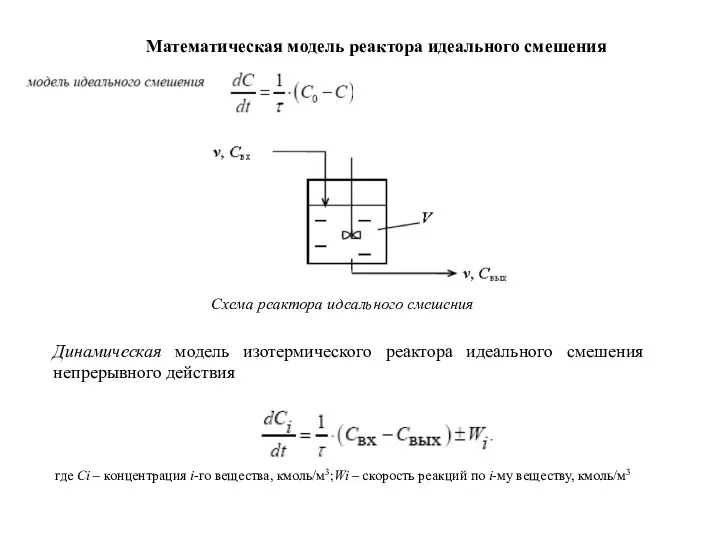
- 3. Математическая модель реактора идеального смешения Схема реактора идеального смешения Динамическая модель изотермического реактора идеального смешения непрерывного
- 4. Математическая модель реактора идеального смешения Математическая модель реактора идеального смешения для реакции для динамического режима работы
- 5. При решении данных уравнений можно найти следующие основные параметры: - время контакта, характеризующее объем аппарата; -
- 6. Уравнение теплового баланса: адиабатический реактор политропический реактор: где Wi – скорость i-й химической реакции; ΔHi –
- 7. Теплоемкость i-го вещества как функция температуры описывается следующим уравнением: Теплоемкость смеси вычисляется по правилу аддитивности: где
- 8. Математическая модель реактора идеального вытеснения Динамическая модель изотермического реактора идеального вытеснения непрерывного действия где Сi –
- 9. Для реакции: В установившемся (стационарном) режиме работы реактора: Тогда уравнения примут следующий вид: Математическая модель реактора
- 10. Так как где τ– время контакта, с При решении системы уравнений можно найти следующие параметры: -
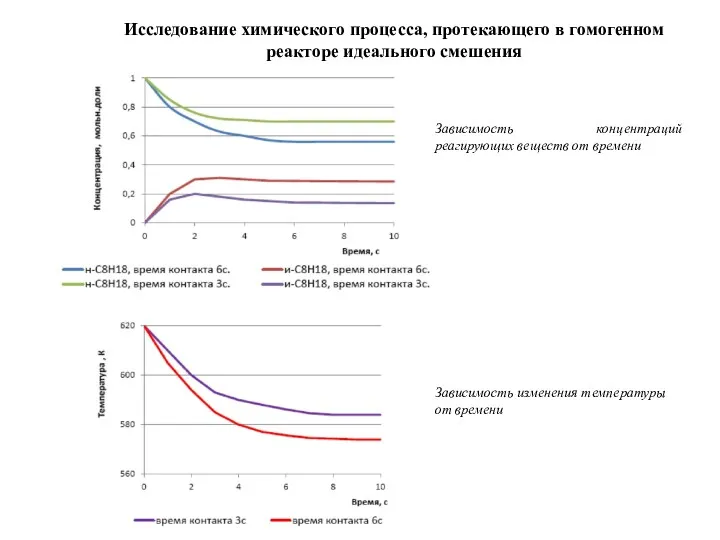
- 11. Исследование химического процесса, протекающего в гомогенном реакторе идеального смешения где ΔH1=-7,03 Дж/моль при (700 К) –
- 12. Начальные условия: при t=0 CА (0)=CА,0;CB(0)=CC(0)=CD(0)=0, R – универсальная газовая постоянная Так как тепловой эффект реакции
- 13. Зависимость концентраций реагирующих веществ от времени Зависимость изменения температуры от времени Исследование химического процесса, протекающего в
- 14. Пусть в реакторе идеального вытеснения (РИВ) протекает химическая реакция Математическая модель химического процесса: где k1, k2
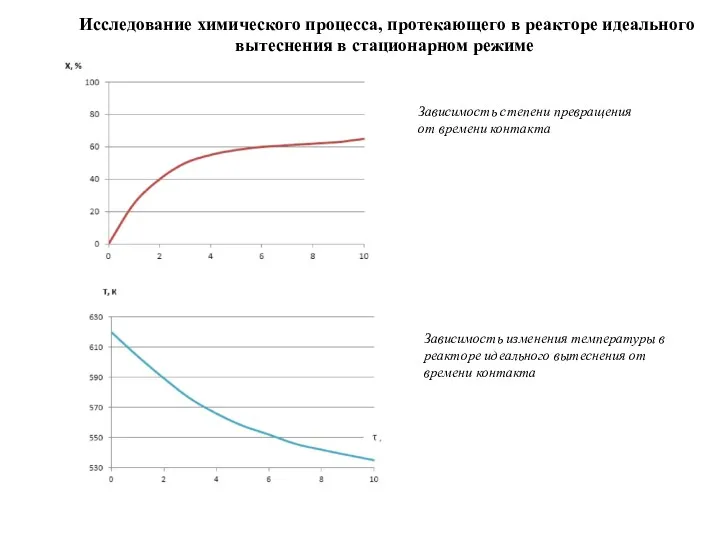
- 15. Зависимость степени превращения от времени контакта Зависимость изменения температуры в реакторе идеального вытеснения от времени контакта
- 17. Скачать презентацию











 Угольная кислота и ее соли. 9 класс
Угольная кислота и ее соли. 9 класс Водород - топливо будущего
Водород - топливо будущего Химические свойства алкенов
Химические свойства алкенов Химические свойства простых металлов, неметаллов и оксидов. Задание 6 по ЕГЭ
Химические свойства простых металлов, неметаллов и оксидов. Задание 6 по ЕГЭ Искусственные каменные материалы
Искусственные каменные материалы Методы прямого секвенирования белков (пептидов)
Методы прямого секвенирования белков (пептидов) Химическая термодинамика. Фазовые равновесия
Химическая термодинамика. Фазовые равновесия Углеводы. Моносахариды. Лекция 5
Углеводы. Моносахариды. Лекция 5 Вода и здоровье
Вода и здоровье Електронні і графічні електронні формули атомів s-, р-, d- елементів. Принцип мінімальної енергії
Електронні і графічні електронні формули атомів s-, р-, d- елементів. Принцип мінімальної енергії Хімічні елементи, їхні назви і символи. Поширеність хімічних елементів у природі
Хімічні елементи, їхні назви і символи. Поширеність хімічних елементів у природі Периодический закон Д.И. Менделеева (лекция 3)
Периодический закон Д.И. Менделеева (лекция 3) Алюминий и его соединения
Алюминий и его соединения Получение и химические свойства оснований
Получение и химические свойства оснований Коллоидная химия. Введение
Коллоидная химия. Введение Халькогены
Халькогены Химические формулы
Химические формулы Свинец
Свинец Нефть - “Кормилица”. 10 класс
Нефть - “Кормилица”. 10 класс Переходные элементы
Переходные элементы fosfor_i_ego_soedineniya
fosfor_i_ego_soedineniya Углерод. Carbon
Углерод. Carbon Литий
Литий Органическая химия в ряду других наук
Органическая химия в ряду других наук Крахмал. Строение вещества
Крахмал. Строение вещества Функциональные производные с простой связью C-“Э”. Часть 2. Галогенпроизводные
Функциональные производные с простой связью C-“Э”. Часть 2. Галогенпроизводные Чистые вещества. Смеси. Способы разделения смесей (7 класс)
Чистые вещества. Смеси. Способы разделения смесей (7 класс) История развития химии
История развития химии