Содержание
- 2. Химические свойства металлов В химических реакциях металлы проявляют только восстановительные свойства, т.е. их атомы отдают электроны,
- 3. 1. Взаимодействуют с неметаллами: а) кислородом (с образованием оксидов) 4Li + O2 = 2Li2O 2Ca +
- 4. Железо, цинк, медь и другие менее активные металлы медленно окисляются на воздухе и активно при нагревании.
- 5. б) водородом (с образованием гидридов) 2Na + H2 = 2NaH Ca + H2 = CaH2
- 6. в) хлором (с образованием хлоридов) 2K + Cl2 = 2KCl Mg + Cl2 = MgCl2 2Al
- 7. г) серой (с образованием сульфидов) 2Na + S = Na2S Hg + S = HgS 2Al
- 8. д) азотом (с образованием нитридов) 6K + N2 = 2K3N 3Mg + N2 = Mg3N2 2Al
- 9. 2. Взаимодействуют со сложными веществами: (использовать ряд Бекетова) Li, K, Ba, Ca, Na, Mg, Al, Mn,
- 10. Магний взаимодействует с водой при кипячении. Mg + 2H2O = Mg(OH) 2 + H2↑ Алюминий при
- 11. б) растворами кислот Металлы, стоящие в ряду до магния и активно реагирующие с водой, не используют
- 12. в) растворами солей правило: Каждый металл вытесняет из растворов солей другие металлы, расположенные в ряду правее
- 13. г) растворами щелочей Взаимодействуют металлы, гидроксиды которых амфотерны. Zn + 2NaOH + 2H2O = Na2 [Zn(OH)
- 14. д) с органическими веществами Щелочные металлы со спиртами и фенолом. 2C2H5OH + 2Na = 2C2H5ONa +
- 15. Неметаллы At, B, Te, H, As, I, Si, P, Se, C, S, Br, Cl, N, O,
- 16. б) в реакциях с неметаллами( смотри ряд электроотрицательности) At, B, Te, H, As, I, Si, P,
- 17. в) в реакциях с некоторыми сложными веществами Окислитель – кислород, реакции горения CH4 + 2O2 =
- 18. 2. Восстановительные свойства а) в реакциях с фтором S + 3F2 = SF6 H2 + F2
- 19. в) в реакциях со сложными веществами – окислителями H2 + CuO = Cu + H2O 6P
- 20. 3. Реакции диспропорционирования: один и тот же неметалл является и окислителем и восстановителем Cl2 + H2O
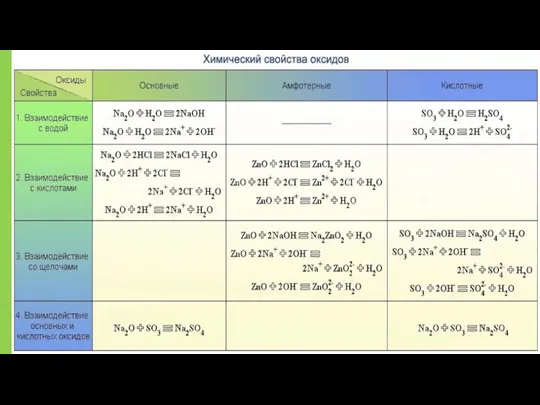
- 21. Оксиды: классификация, получение и химические свойства
- 22. Получение оксидов 1. Взаимодействие простых веществ с кислородом: 1.1. Окисление металлов: 4Al + 3O2 → 2Al2O3
- 23. 1.2. Окисление простых веществ-неметаллов. 4P + 5O2(изб.) → 2P2O5 4P + 3O2(нед.) → 2P2O3 Исключения S
- 24. 2. Окисление сложных веществ (бинарных соединений): сульфидов, гидридов, фосфидов и т.д. 4FeS2 + 11O2 → 2Fe2O3
- 25. 3. Разложение гидроксидов. H2CO3 → H2O + CO2 H2SO3 → H2O + SO2 NH4OH → NH3
- 26. При нагревании H2SiO3 → H2O + SiO2 2Fe(OH)3 → Fe2O3 + 3H2O
- 27. 4. Разложение солей Li2CO3 → H2O + Li2O CaCO3 → CaO + CO2 Запомни (Соли, образованные
- 30. Из предложенного перечня выберите два вещества, с каждым из которых взаимодействует кислород. 1оксид магния 2оксид азота(II)
- 31. Из предложенного перечня пар взаимодействующих между собой веществ выберите две пары, при взаимодействии которых водород не
- 32. Из предложенного перечня выберите два вещества, с каждым из которых взаимодействует медь. 1.хлор 2.водород 3.серная кислота
- 33. Из предложенного перечня выберите два вещества, с каждым из которых вступает в реакцию кремний. 1.магний 2.кислород
- 35. Скачать презентацию































 Галогены (солеобразующие)
Галогены (солеобразующие) Si - Silicon. Distribute Properties
Si - Silicon. Distribute Properties Вещества и материалы. Классификация веществ. Реакции нейтрализации
Вещества и материалы. Классификация веществ. Реакции нейтрализации Непредельные углеводороды ряда этилена. Олефины
Непредельные углеводороды ряда этилена. Олефины Термодинамика химического равновесия
Термодинамика химического равновесия Обмен липидов
Обмен липидов Предмет органической химии. Органические вещества
Предмет органической химии. Органические вещества Электрохимические системы
Электрохимические системы Кислоты. Удивительные факты
Кислоты. Удивительные факты Системи удобрення сільськогосподарських культур
Системи удобрення сільськогосподарських культур Тепловой эффект химических реакций. 8 класс
Тепловой эффект химических реакций. 8 класс Горные породы
Горные породы Лекция 8.3. Реакции окисления и восстановления органических соединений
Лекция 8.3. Реакции окисления и восстановления органических соединений Виведення формул органічних сполук за масовими частками елементів
Виведення формул органічних сполук за масовими частками елементів Основы коррозии и защиты металлов. Опасность локальных видов коррозии
Основы коррозии и защиты металлов. Опасность локальных видов коррозии Свинец (Pb)
Свинец (Pb) Химические волокна
Химические волокна Жиры
Жиры Бензол
Бензол Реакції йонного обміну між електролітами у водних розчинах
Реакції йонного обміну між електролітами у водних розчинах Теплота згоряння. Температура горіння
Теплота згоряння. Температура горіння Мыло и синтетические моющие средства
Мыло и синтетические моющие средства Строение атома и атомного ядра. Изотопы
Строение атома и атомного ядра. Изотопы Периодический закон и периодическая система элементов Д.И. Менделеева
Периодический закон и периодическая система элементов Д.И. Менделеева Окислительно-восстановительные процессы
Окислительно-восстановительные процессы Степень окисления
Степень окисления Композиционные материалы
Композиционные материалы Основы химической кинетики
Основы химической кинетики