Содержание
- 2. Продукты пиролиза нефтяного сырья
- 3. Продукты пиролиза нефтяного сырья
- 4. Сырье Газообразные и жидкие углеводороды: газы, легкие бензиновые фракции, газоконденсаты, рафинаты каталитического риформинга, реже керосино-газойлевые фракции
- 5. Направления использования жидких продуктов пиролиза Получение бензола и других ароматических углеводородов Получение нефтеполимерных смол Получение котельных
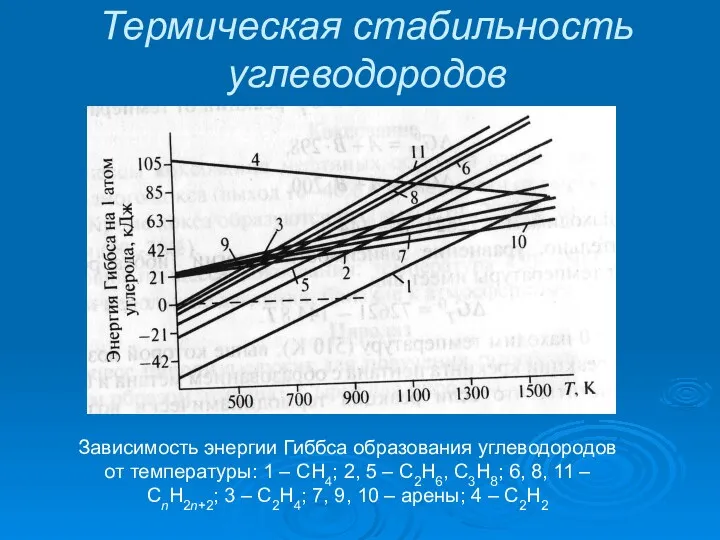
- 6. Термическая стабильность углеводородов Зависимость энергии Гиббса образования углеводородов от температуры: 1 – СН4; 2, 5 –
- 7. Термодинамика реакций крекинга и пиролиза Термодинамическая вероятность протекания химической реакции определяется величиной изменения в процессе свободной
- 8. Кинетика и механизм В настоящее время принят радикально-цепной механизм термической деструкции: инициирование, продолжение и обрыв цепи.
- 9. Основные стадии инициирование – распад углеводородов на радикалы – происходит преимущественно по связи С–С (крекинг), при
- 10. Основные стадии продолжение цепи: а) замещение: б) распад радикалов с образованием ненасыщенных молекул:
- 11. Основные стадии в) присоединение радикалов по кратной связи: г) изомеризация свободных радикалов:
- 12. Основные стадии обрыв цепи: а) реакции рекомбинации: б) реакции диспропорционирования:
- 13. Кинетика Реакции термического разложения обычно описываются уравнением 1-го порядка: где x – доля превращенного сырья; –
- 14. Кинетика процесса с учетом тормозящего влияния продуктов распада β – постоянная, характеризующая степень торможения.
- 15. Основные типы реакций для углеводородов различных классов Превращение алканов – реакция распада по связи С–С с
- 16. Основные типы реакций для углеводородов различных классов в) дегидрирования алкенов: Превращение циклоалканов: а) деалкилирование (или разрыв
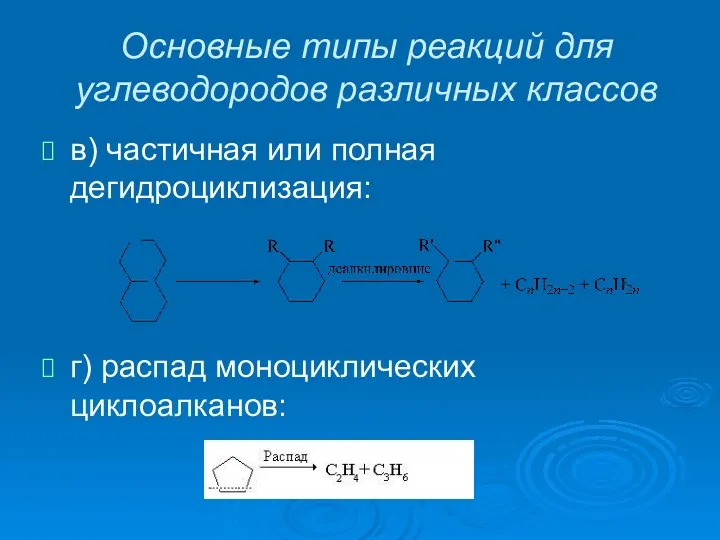
- 17. Основные типы реакций для углеводородов различных классов в) частичная или полная дегидроциклизация: г) распад моноциклических циклоалканов:
- 18. Основные типы реакций для углеводородов различных классов Превращение аренов: деалкилирование преимущественно в β-положение конденсация
- 19. Основные типы реакций для углеводородов различных классов Превращение серосодержащих соединений: разложение с выделением Н2S, меркаптанов и
- 20. Формализованная схема превращений Парафины Олефины Ароматические углеводороды
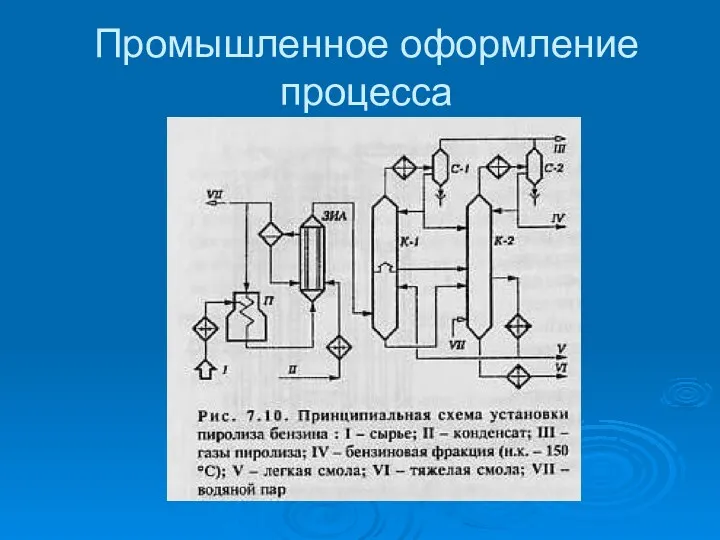
- 22. Промышленное оформление процесса
- 23. Промышленное оформление процесса
- 25. Скачать презентацию















 Разделение неоднородных систем
Разделение неоднородных систем Метанол. Фізичні властивості
Метанол. Фізичні властивості Якісні реакції на деякі йони
Якісні реакції на деякі йони Химия в повседневной жизни человека
Химия в повседневной жизни человека Серная кислота. ОХТ, лекция №7
Серная кислота. ОХТ, лекция №7 Анализ проб воды
Анализ проб воды Mechanistic insights into the aminolysis of 3,4-epoxysulfolane
Mechanistic insights into the aminolysis of 3,4-epoxysulfolane Важнейшие органические вещества пищевых продуктов. Жиры.(Липиды)
Важнейшие органические вещества пищевых продуктов. Жиры.(Липиды) Углеводороды: предельные и непредельные
Углеводороды: предельные и непредельные Алмазы. Бриллианты
Алмазы. Бриллианты Классификация химических реакций по механизму реакции
Классификация химических реакций по механизму реакции Окислительные свойства азотной кислоты
Окислительные свойства азотной кислоты Характеристика неметаллов. Галогены
Характеристика неметаллов. Галогены Электрофоретические и хроматографические методы
Электрофоретические и хроматографические методы Карбоновые кислоты
Карбоновые кислоты Метаморфогенные месторождения
Метаморфогенные месторождения Полімери та їх властивості
Полімери та їх властивості Learning Objectives
Learning Objectives НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Содержание кислорода и углекислого газа в помещениях школы
Содержание кислорода и углекислого газа в помещениях школы Физико-химические основы дезодорации растительных масел
Физико-химические основы дезодорации растительных масел Sm-Nd метод
Sm-Nd метод Ртуть. Применение ртути и ее соединений
Ртуть. Применение ртути и ее соединений Железо и его соединения
Железо и его соединения Тепловой эффект химических реакций. Расчёты по термохимическим уравнениям (ТХУ)
Тепловой эффект химических реакций. Расчёты по термохимическим уравнениям (ТХУ) Химический элемент водород
Химический элемент водород Органічна хімія, частина 1
Органічна хімія, частина 1 БАЗ-дың заманауи, ғылыми классификациясы. 3 Лекция
БАЗ-дың заманауи, ғылыми классификациясы. 3 Лекция