Содержание
- 2. План урока Строение атомов Изменение свойств в группе Соединения, образованные этими элементами Аллотропные модификации Применение (для
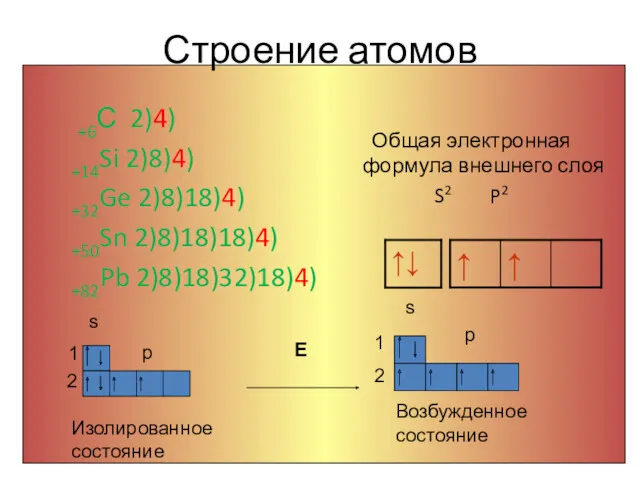
- 3. Строение атомов Общая электронная формула внешнего слоя S2 P2 +6С 2)4) +14Si 2)8)4) +32Ge 2)8)18)4) +50Sn
- 4. Окислительные и восстановительные свойства: Эл0 + 4е → Эл-4 окислитель Эл0 - 4е → Эл+4 восстановитель
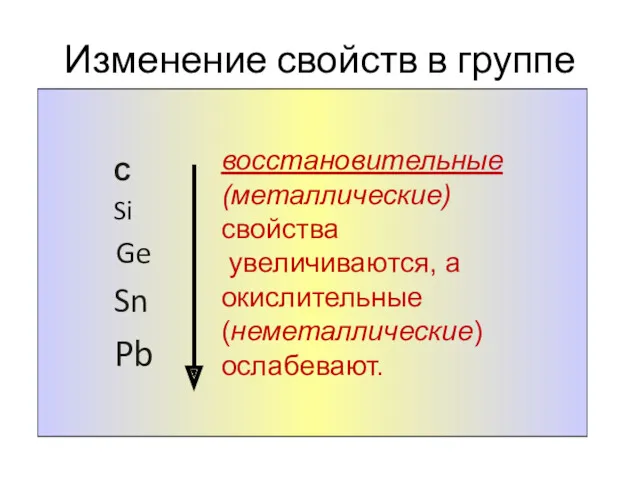
- 5. Изменение свойств в группе С Si Ge Sn Pb восстановительные (металлические) свойства увеличиваются, а окислительные (неметаллические)
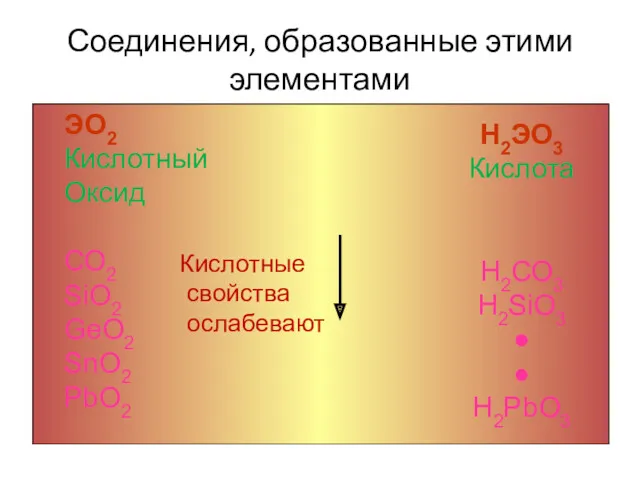
- 6. Соединения, образованные этими элементами ЭО2 Кислотный Оксид СО2 SiO2 GeO2 SnO2 PbO2 Кислотные свойства ослабевают Н2ЭО3
- 7. В природе встречаются в свободном (углерод) и в связанном виде В составе сложных веществ – это
- 8. Углерод в природе
- 9. Аллотропные модификации углерода карбин графит алмазы
- 10. Простое вещество - углерод Алмаз
- 11. АЛМАЗ Один из самых известных алмазов - «Орлов» украшает скипетр русских царей. Это бриллиант чистейшей воды
- 12. Применение алмаза Режущий инструмент Наконечники буров Шлифовальный инструмент Ювелирные изделия
- 13. Простое вещество - углерод Графит
- 14. ГРАФИТ В России в XVII веке графит называли "карандашом" от монгольских слов: "кара" - черный, "таш"
- 15. Стержни в атомных реакторах краски Применение графита Смазочный материал Электроды в электрохимии Грифель для карандашей Литейные
- 16. Взаимопревращение алмаза и графита Алмаз t°=2000°C без доступа воздуха t°=3000°C,Р=50 тыс. атм., катализатор Ni Графит Алмазы,
- 17. Простое вещество - углерод Карбин
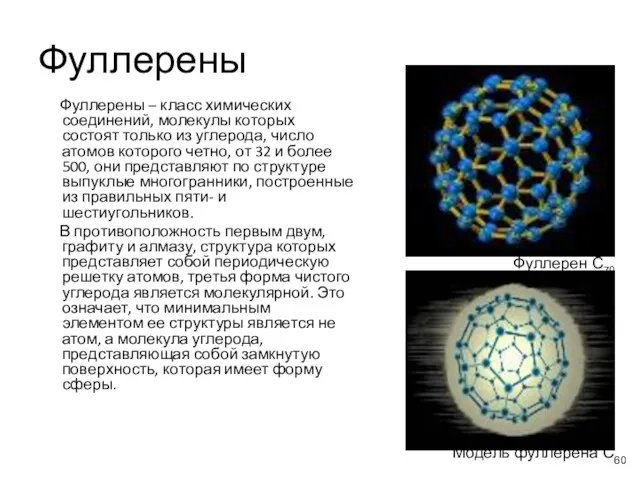
- 18. Фуллерены Фуллерены – класс химических соединений, молекулы которых состоят только из углерода, число атомов которого четно,
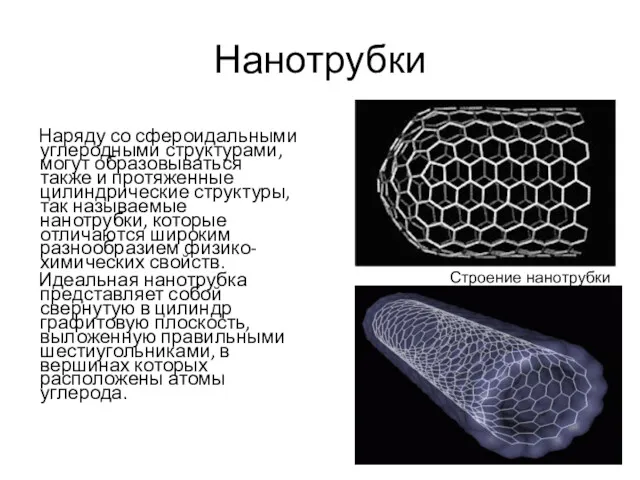
- 19. Нанотрубки Наряду со сфероидальными углеродными структурами, могут образовываться также и протяженные цилиндрические структуры, так называемые нанотрубки,
- 20. Наночастицы В процессе образования фуллеренов из графита образуются также наночастицы. Это замкнутые структуры, подобные фуллеренам, но
- 21. Аморфное состояние углерода Уголь, сажа, кокс - измельченный графит с примесями
- 22. Уголь - аморфный углерод, по структуре напоминающий графит. При обработке его водяным паром поры и каналы
- 23. Применение активированного угля Очистка питьевой воды (фильтры) Карболен- таблетки для выведения токсинов из организма Очистка воздуха
- 24. ЗЕЛИНСКИЙ Николай Дмитриевич (1861-1953) Современный противогаз Изобретатель противогаза
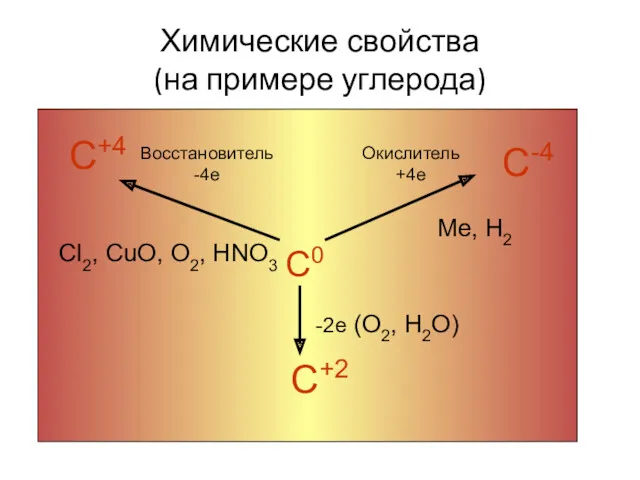
- 25. Химические свойства (на примере углерода) С+4 С0 С-4 С+2 Восстановитель -4е Окислитель +4е -2е (О2, Н2О)
- 26. Химические свойства. C +O2 = CO2 (избыток кислорода) 2С + O2 = 2CO (недостаток кислорода) C
- 27. Химические свойства. 2H2 + C = CH4 метан Ca + 2C = CaC2 карбид кальция Al
- 28. Самый глубокий угольный разрез
- 29. применение Алмазный порошок выглядит как ярко желтый сверкающий песок, а под микроскопом видно, что он состоит
- 30. Графит- самая используемая в технике форма углерода. Он встречается и в самородном виде, но для технических
- 31. В промышленности кремний используется в виде элемента с самой различной чистотой. Поликристаллический кремний технической чистоты (99%),
- 33. Скачать презентацию























 Окисно-відновні реакції. Процеси окиснення, відновлення, окисник та відновник
Окисно-відновні реакції. Процеси окиснення, відновлення, окисник та відновник Растворы. Термодинамика процесса растворения. Способы выражения концентрации. Идеальные растворы. Законы Рауля
Растворы. Термодинамика процесса растворения. Способы выражения концентрации. Идеальные растворы. Законы Рауля Кислородсодержащие соединения серы. Оксиды, кислоты, соли
Кислородсодержащие соединения серы. Оксиды, кислоты, соли Углеводы. Общая формула углеводов Сn(H2O)m
Углеводы. Общая формула углеводов Сn(H2O)m Лекция 1 эквивалент 2
Лекция 1 эквивалент 2 Спирти та їх види
Спирти та їх види Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25)
Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25) Теория электролитической диссоциации
Теория электролитической диссоциации Кислоты. Классификация кислот
Кислоты. Классификация кислот Химическая промышленность
Химическая промышленность Алкалоиды и принципы их классификации
Алкалоиды и принципы их классификации Литология. Кремнистые породы
Литология. Кремнистые породы Природные источники углеводородов
Природные источники углеводородов Общая геохимия. Периодический закон Менделеева. Строение электронных оболочек. Геохимические классификации элементов
Общая геохимия. Периодический закон Менделеева. Строение электронных оболочек. Геохимические классификации элементов Хлороводород и соляная кислота
Хлороводород и соляная кислота Растворы. Классификация
Растворы. Классификация Равновесие в реакциях гидролиза. Лекция 6
Равновесие в реакциях гидролиза. Лекция 6 Ненасыщенные (непредельные) алифатические углеводороды. Алкены
Ненасыщенные (непредельные) алифатические углеводороды. Алкены Натуральный и синтетический каучуки. Резина
Натуральный и синтетический каучуки. Резина Сложные эфиры. Жиры. Мыло
Сложные эфиры. Жиры. Мыло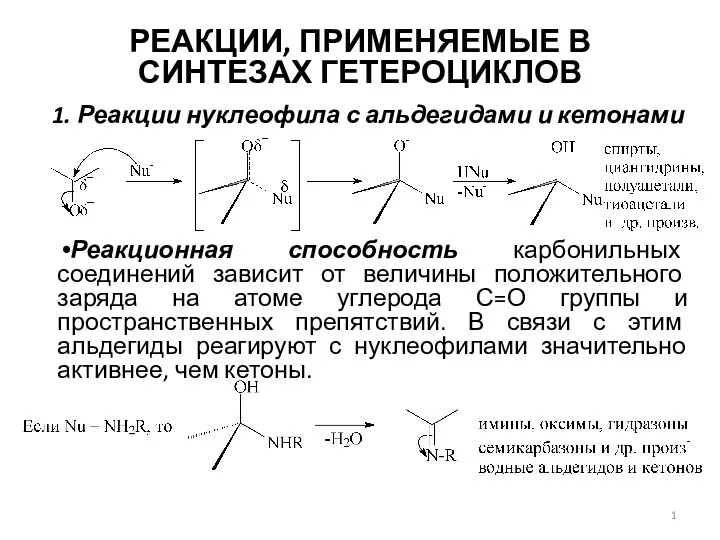 Реакции, применяемые в синтезах гетероциклов
Реакции, применяемые в синтезах гетероциклов Азотная кислота. Соли азотной кислоты. Получение и применение азотной кислоты. Урок 43
Азотная кислота. Соли азотной кислоты. Получение и применение азотной кислоты. Урок 43 Аллотропные модификации углерода. Алмазы
Аллотропные модификации углерода. Алмазы Золото
Золото Химические свойства металлов
Химические свойства металлов Способы выражения концентрации в титриметрическом анализе
Способы выражения концентрации в титриметрическом анализе Щелочи
Щелочи Термический анализ. Прибор синхронного термического анализа
Термический анализ. Прибор синхронного термического анализа