Содержание
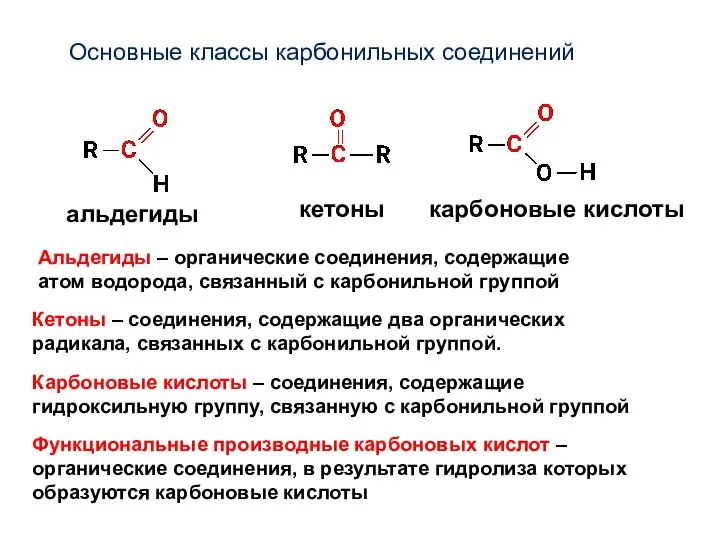
- 2. Основные классы карбонильных соединений альдегиды кетоны карбоновые кислоты Функциональные производные карбоновых кислот – органические соединения, в
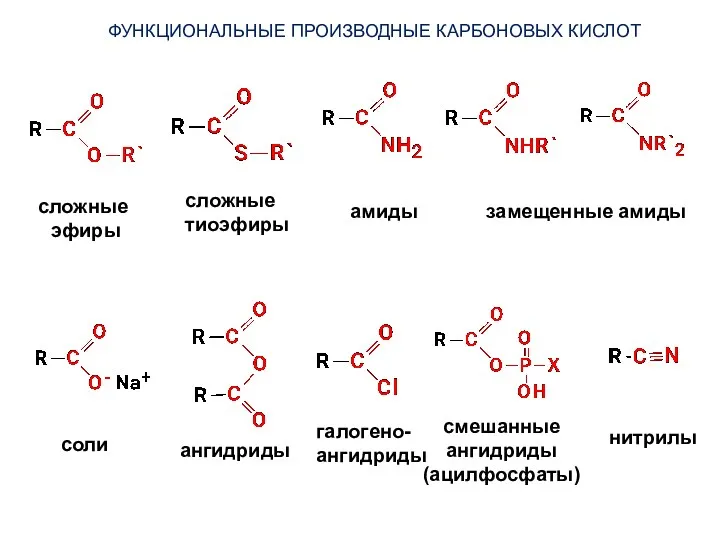
- 3. ФУНКЦИОНАЛЬНЫЕ ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ сложные эфиры сложные тиоэфиры амиды замещенные амиды соли ангидриды галогено- ангидриды смешанные
- 4. Реакционные центры в карбонильных соединениях СН-кислотный центр (атака основанием) Электрофильный центр (атака нуклеофилом) Основный центр (атака
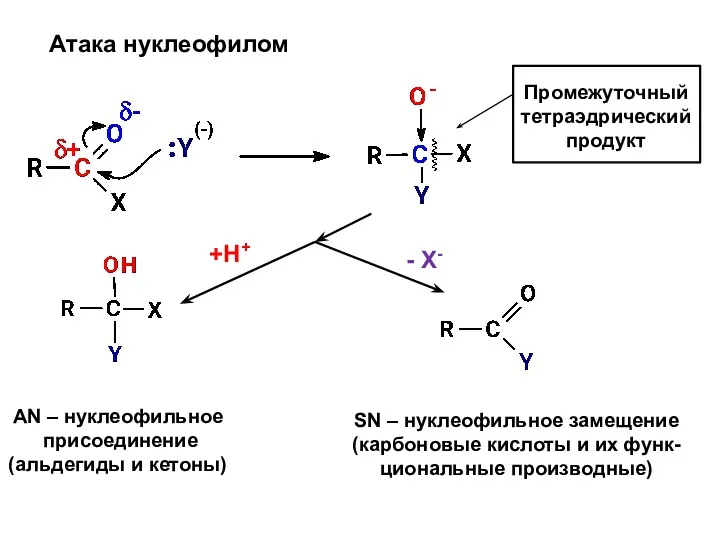
- 5. Атака нуклеофилом Промежуточный тетраэдрический продукт +Н+ - X- AN – нуклеофильное присоединение (альдегиды и кетоны) SN
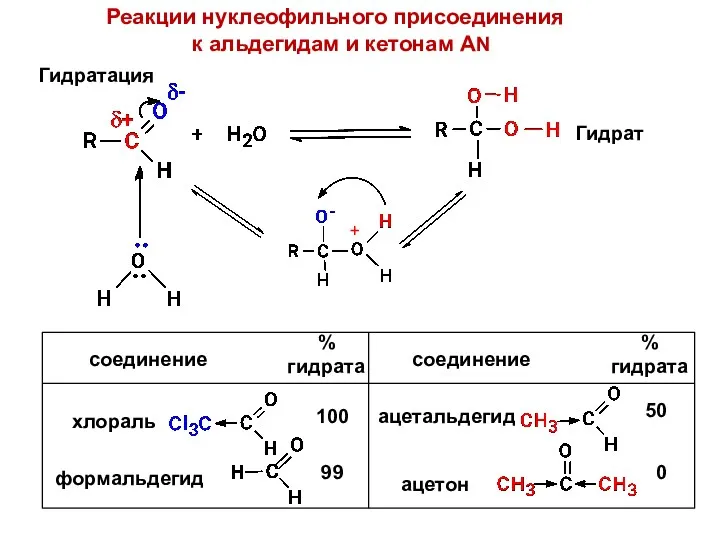
- 6. Реакции нуклеофильного присоединения к альдегидам и кетонам AN Гидратация Гидрат 100 99 50 0 + соединение
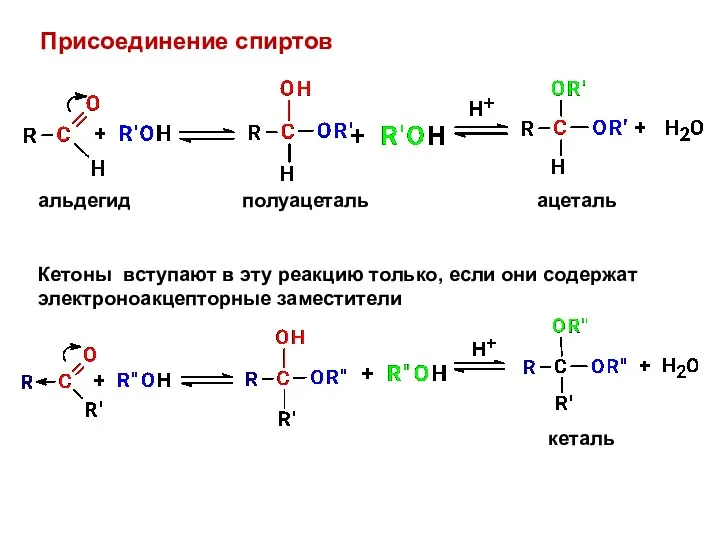
- 7. Присоединение спиртов полуацеталь ацеталь кеталь Кетоны вступают в эту реакцию только, если они содержат электроноакцепторные заместители
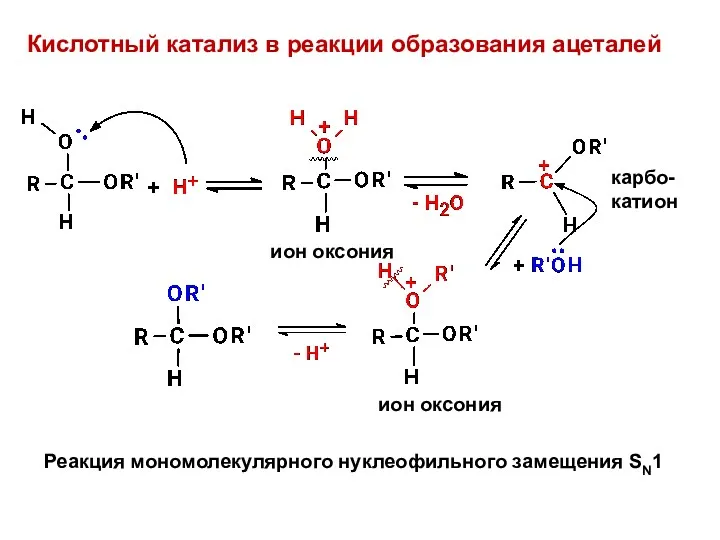
- 8. Кислотный катализ в реакции образования ацеталей Реакция мономолекулярного нуклеофильного замещения SN1 ион оксония карбо- катион ион
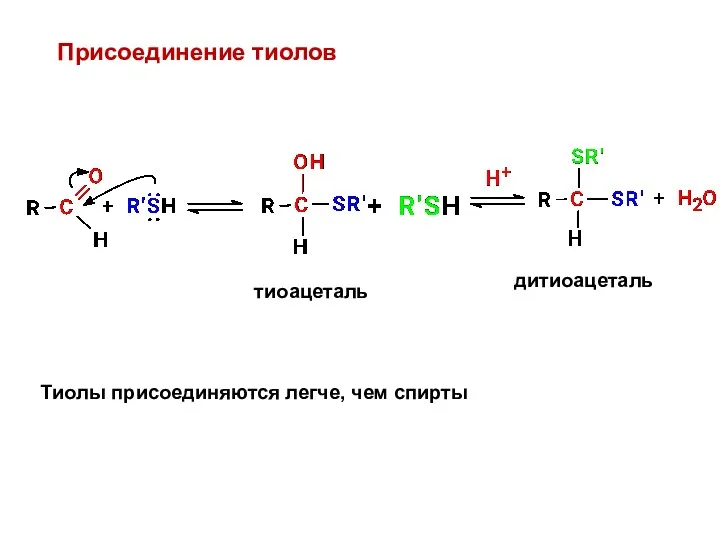
- 9. Присоединение тиолов тиоацеталь дитиоацеталь Тиолы присоединяются легче, чем спирты
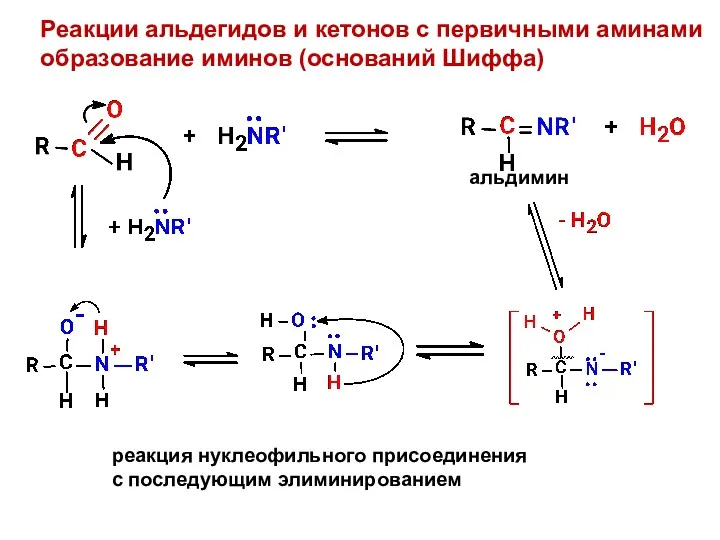
- 10. Реакции альдегидов и кетонов с первичными аминами образование иминов (оснований Шиффа) реакция нуклеофильного присоединения с последующим
- 11. Кислотный катализ в реакциях нуклеофильного присоединения карбокатион Усиление электрофильного центра
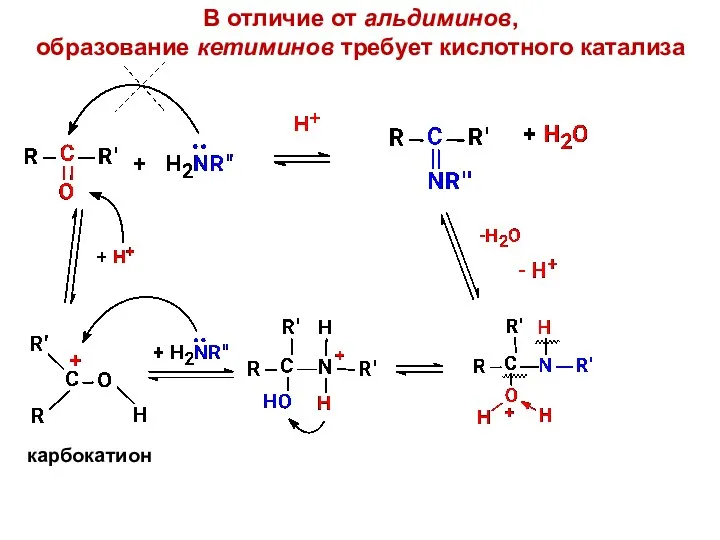
- 12. В отличие от альдиминов, образование кетиминов требует кислотного катализа карбокатион
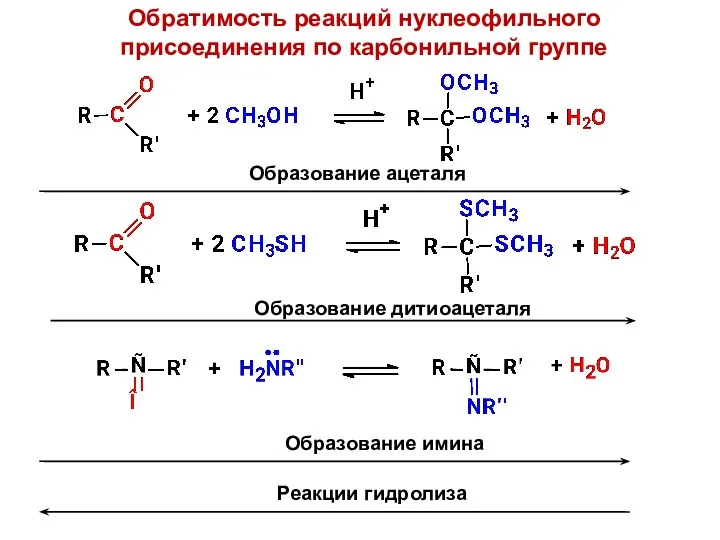
- 13. Обратимость реакций нуклеофильного присоединения по карбонильной группе Образование ацеталя Образование дитиоацеталя Образование имина Реакции гидролиза
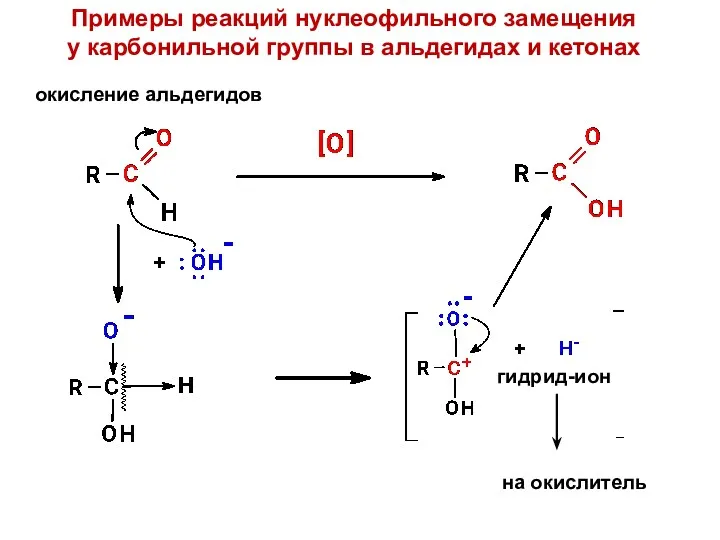
- 14. Примеры реакций нуклеофильного замещения у карбонильной группы в альдегидах и кетонах окисление альдегидов гидрид-ион на окислитель
- 15. Галоформная реакция хлороформ
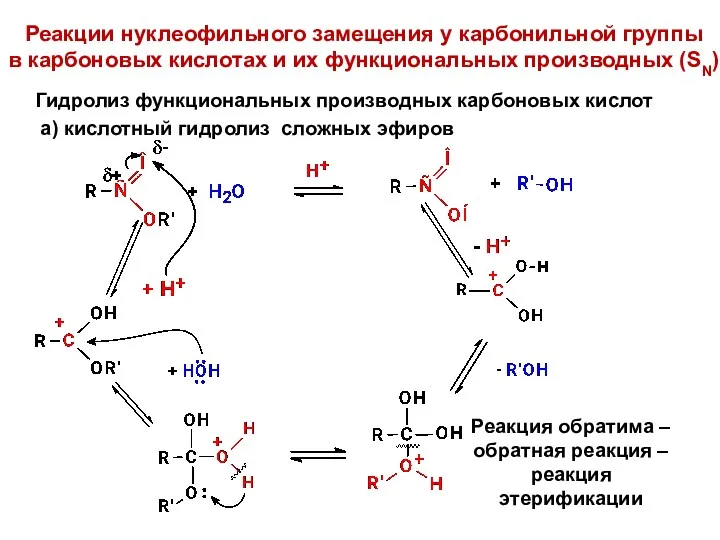
- 16. Реакции нуклеофильного замещения у карбонильной группы в карбоновых кислотах и их функциональных производных (SN) Гидролиз функциональных
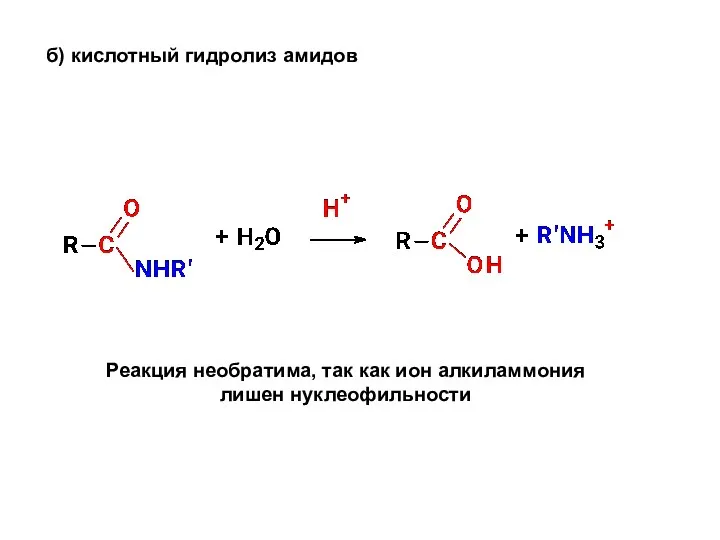
- 17. б) кислотный гидролиз амидов Реакция необратима, так как ион алкиламмония лишен нуклеофильности
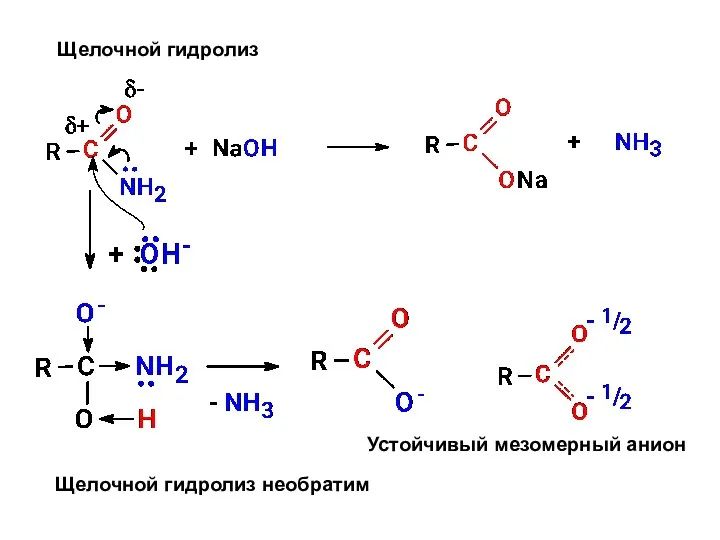
- 18. Щелочной гидролиз Щелочной гидролиз необратим Устойчивый мезомерный анион
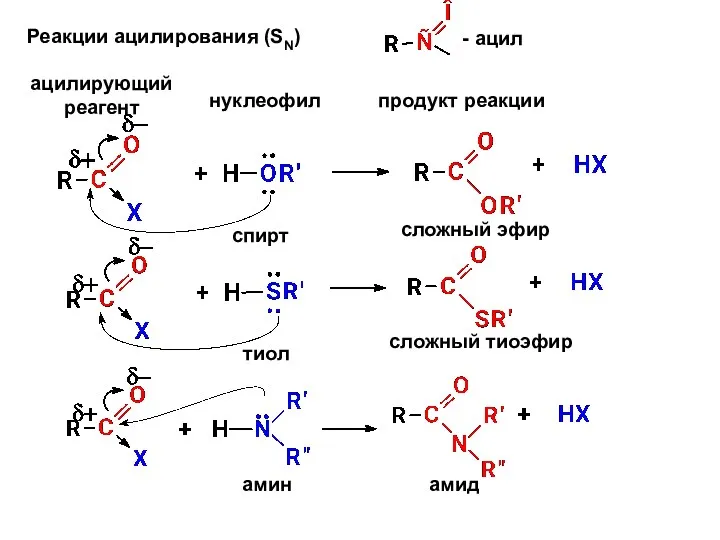
- 19. Реакции ацилирования (SN) ацилирующий реагент нуклеофил продукт реакции спирт сложный эфир - ацил тиол сложный тиоэфир
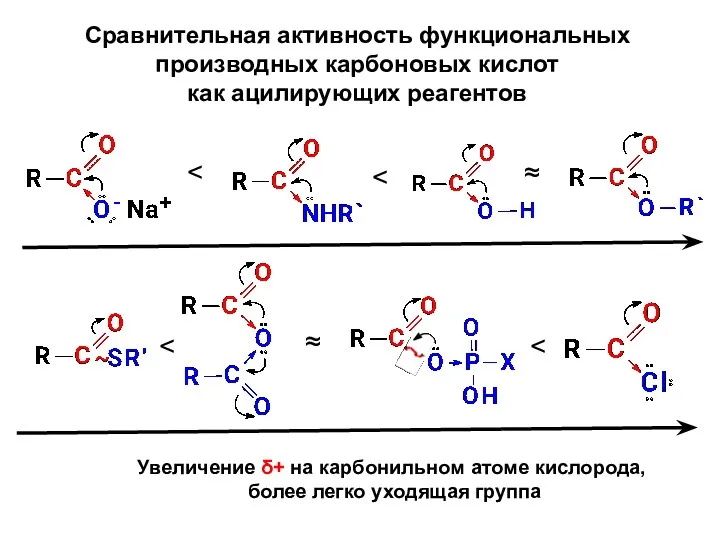
- 20. Сравнительная активность функциональных производных карбоновых кислот как ацилирующих реагентов ≈ ≈ Увеличение δ+ на карбонильном атоме
- 21. Биологически важные ацилирующие реагенты амиды кислот – способны только к гидролизу сложные эфиры – могут ацилировать
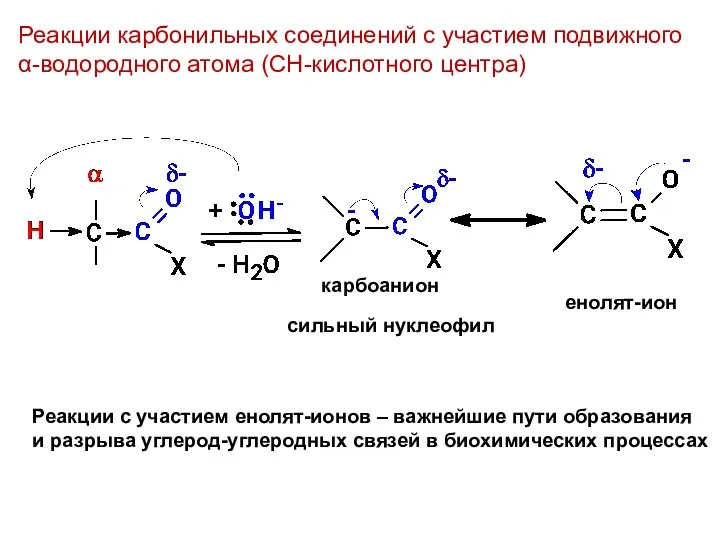
- 22. Реакции карбонильных соединений с участием подвижного α-водородного атома (СН-кислотного центра) енолят-ион карбоанион сильный нуклеофил Реакции с
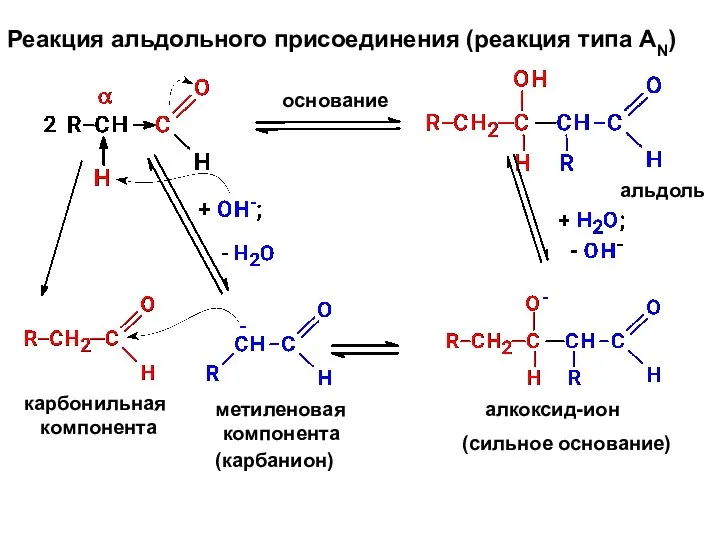
- 23. Реакция альдольного присоединения (реакция типа AN) основание альдоль карбонильная компонента метиленовая компонента (карбанион) алкоксид-ион (сильное основание)
- 24. Карбонильная компонента Метиленовая компонента Альдольное присоединение Альдольное расщепление (ретроальдольный распад)
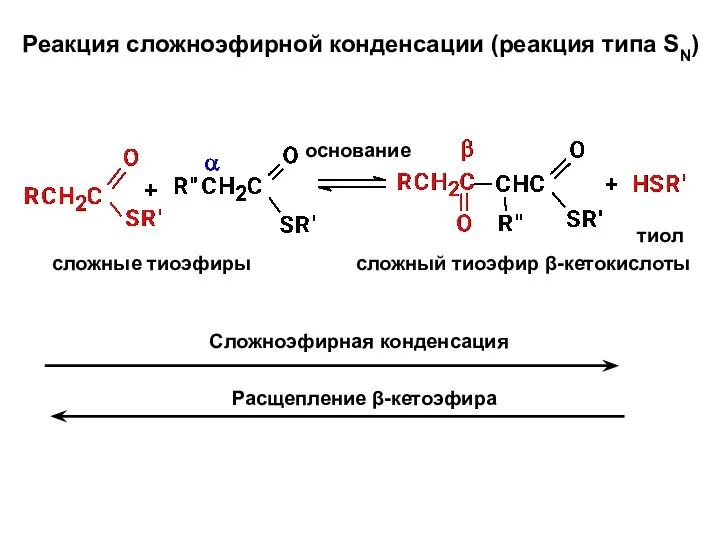
- 25. Реакция сложноэфирной конденсации (реакция типа SN) основание сложные тиоэфиры сложный тиоэфир β-кетокислоты тиол Сложноэфирная конденсация Расщепление
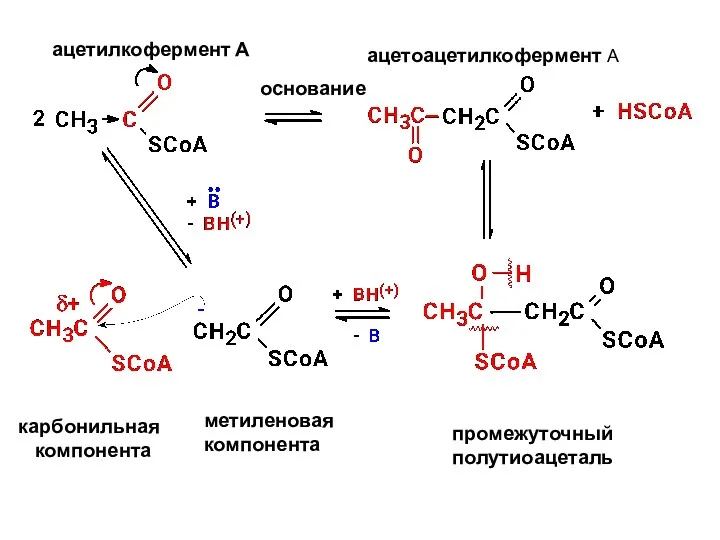
- 26. основание ацетилкофермент А ацетоацетилкофермент А карбонильная компонента метиленовая компонента промежуточный полутиоацеталь
- 28. Скачать презентацию





 Предельные углеводороды. Алканы
Предельные углеводороды. Алканы Гетерофункциональные соединения, участвующие в процессах жизнедеятельности
Гетерофункциональные соединения, участвующие в процессах жизнедеятельности Галогены (солеобразующие)
Галогены (солеобразующие) Общая характеристика неметаллов
Общая характеристика неметаллов Спирттер мен фенолдар
Спирттер мен фенолдар Химия вокруг нас
Химия вокруг нас Методы определения Тст и Тт полимеров
Методы определения Тст и Тт полимеров Гидролиз. Необратимый гидролиз
Гидролиз. Необратимый гидролиз Кислоты. Химические свойства кислот
Кислоты. Химические свойства кислот Пневмовакуум-формование
Пневмовакуум-формование Строение атома. Периодическая таблица Менделеева. Химическая связь
Строение атома. Периодическая таблица Менделеева. Химическая связь Бордың адам ағзасына әсері. Бор дегеніміз не?
Бордың адам ағзасына әсері. Бор дегеніміз не? Карбоновые кислоты. 10 класс
Карбоновые кислоты. 10 класс Жёсткость воды
Жёсткость воды Metal–metal multiple bonded intermediates in catalysis
Metal–metal multiple bonded intermediates in catalysis Химические свойства металлов
Химические свойства металлов Биологическая роль макро и микроэлементов. (Лекция 17)
Биологическая роль макро и микроэлементов. (Лекция 17) Химическая связь и ее типы. (11 класс)
Химическая связь и ее типы. (11 класс) Готовимся к экзамену по химии. 9 класс
Готовимся к экзамену по химии. 9 класс Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25)
Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25) Анализ проб воды
Анализ проб воды Мини-тақталарда немесе дәптерде қатты, сұйық және газтектес заттардың құрылысын сал
Мини-тақталарда немесе дәптерде қатты, сұйық және газтектес заттардың құрылысын сал Растворы. Способы выражения концентраций. Сильные и слабые электролиты. Закон разведения Оствальда
Растворы. Способы выражения концентраций. Сильные и слабые электролиты. Закон разведения Оствальда Минеральные удобрения
Минеральные удобрения Каменный уголь. Физические и химические свойства
Каменный уголь. Физические и химические свойства Preparation for COP
Preparation for COP Методы пробоотбора воздуха. Лекция 2
Методы пробоотбора воздуха. Лекция 2 Периодические системы химических элементов
Периодические системы химических элементов