Содержание
- 2. Строение атома Опыт Эрнеста Резерфорда Модель строения атома Элементарный состав атома Характеристика частиц, входящих в состав
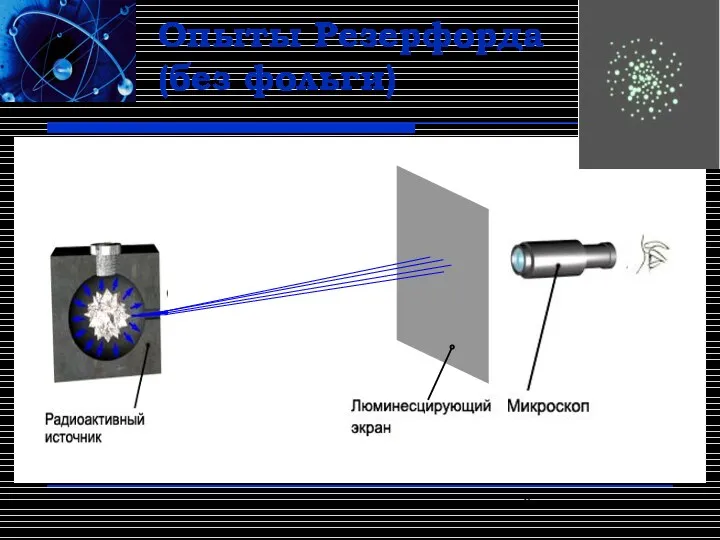
- 3. Опыты Резерфорда (без фольги)
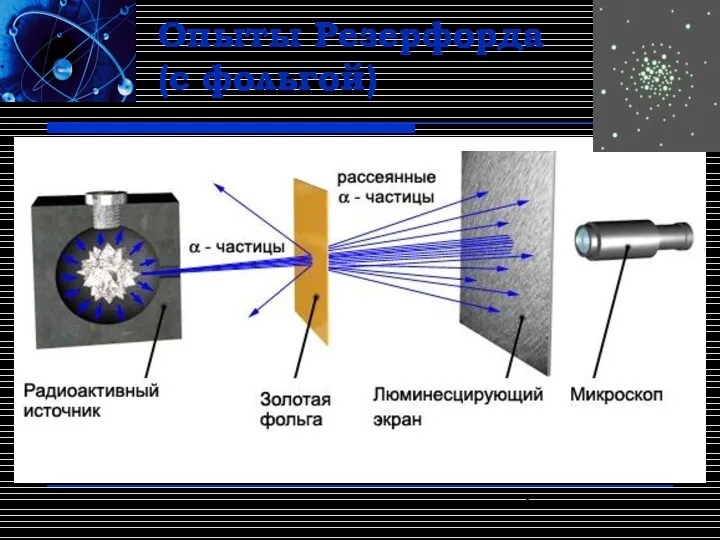
- 4. Опыты Резерфорда (с фольгой)
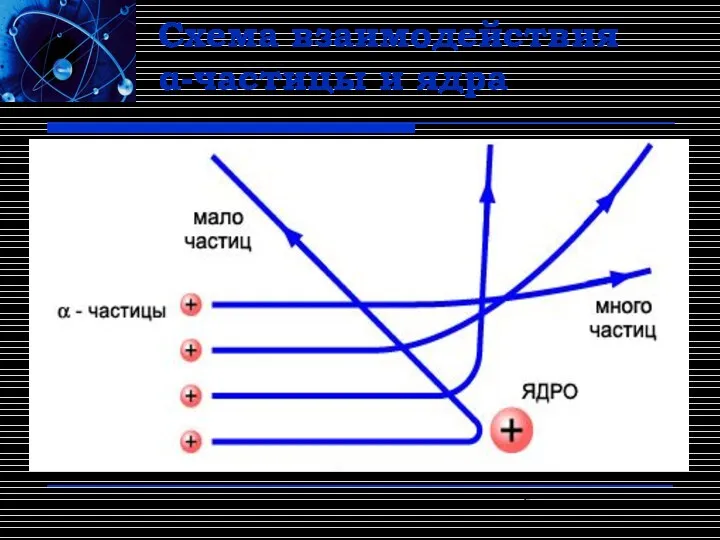
- 5. Схема взаимодействия α-частицы и ядра
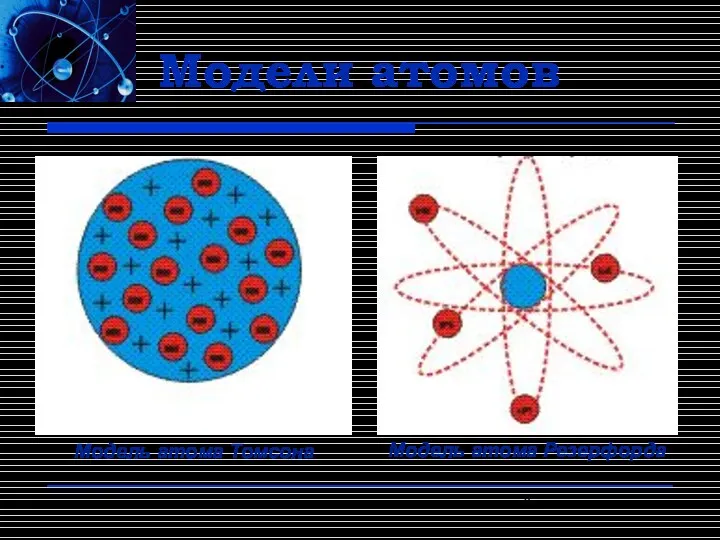
- 6. Модели атомов Модель атома Томсона Модель атома Резерфорда
- 7. Характеристики атомного ядра Z – зарядовое число, A – массовое число, N – число нейтронов в
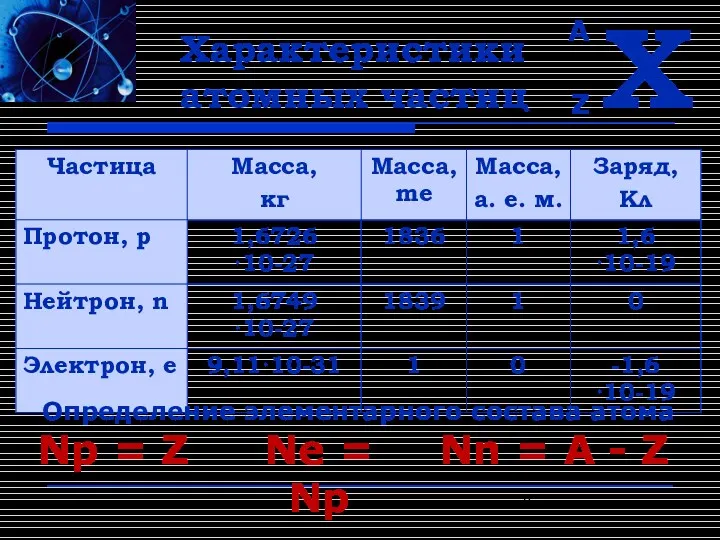
- 8. Характеристики атомных частиц Определение элементарного состава атома Np = Z Ne = Np Nn = A
- 9. Ra 226 88 Rn 222 86 He 4 2 Превращения атомных ядер 226 = 222 +
- 10. Сочинить синквейн по плану: 1 строка – тема или предмет (одно существительное); 2 строка – описание
- 11. Реши задачу 1. Явление радиоактивности, открытое Беккерелем, свидетельствует о том, что … А. Все вещества состоят
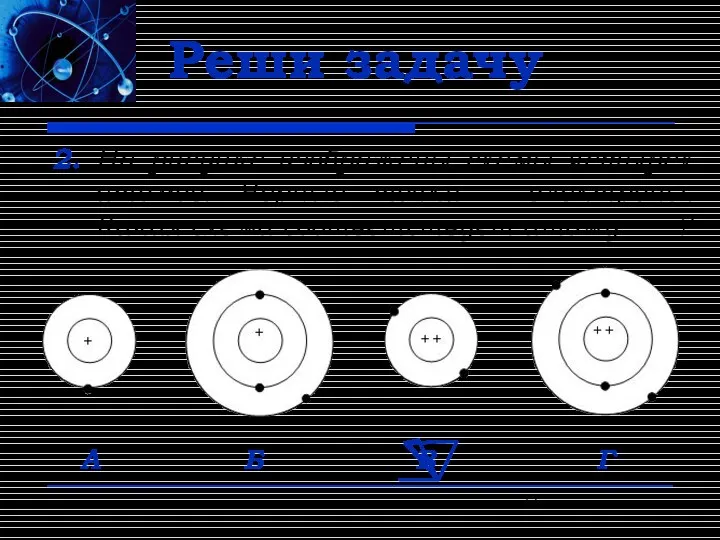
- 12. Реши задачу 2. На рисунке изображены схемы четырех атомов. Черные точки – электроны. Какая схема соответствует
- 13. Реши задачу 3. В состав атома входят следующие частицы: А. Только протоны. Б. Нуклоны и электроны.
- 14. Реши задачу 4. Чему равно массовое число ядра атома марганца Mn? А. 25. Б. 80. В.
- 15. Реши задачу 5. В каких из следующих реакций нарушен закон сохранения заряда? А. Б. В. Г.
- 16. Реши задачу 6. Массы протона и нейтрона … А. Относятся как 1836:1. Б. Приблизительно одинаковы. В.
- 17. Реши задачу 6. В ядре атома кальция содержится … А. 20 нейтронов и 40 протонов. Б.
- 18. Реши задачу 7. Какой вид радиоактивного излучения наиболее опасен при внешнем облучении человека? А. Бета-излучение. Б.
- 19. Домашнее задание § 66, 67. Выполнить (по желанию) творческое задание по теме «Строение атома» : Составить
- 20. Электронные адреса использованных Интернет-ресурсов: Анимация со звуком «Опыт Резерфорда»: Видеоролик - анимация "Планетарная модель атома":
- 21. Томсон Джозеф Джон (1856 - 1940 гг.) Лауреат Нобелевской премии за открытие электрона, предложил одну из
- 22. Эрнест Резерфорд Лауреат Нобелевской премии по химии за исследования по превращению элементов и химии радиоактивных веществ.
- 23. Массовое число – A Общее число нуклонов в ядре называется массовым числом, оно равно массе ядра
- 24. Зарядовое число – Z Число протонов в ядре называется зарядовым числом, оно равно порядковому номеру в
- 25. 1. Радиоактивность Кем было сделано открытие данного явления? Как проводился опыт? Какие выводы были сделаны в
- 26. 2. Демокрит Кто, наряду с Демокритом высказывал предположение о дискретном строении вещества? Как были названы частицы?
- 27. 3. Резерфорд Как проводился опыт по определению состава радиоактивного излучения? Как были названы частицы, входившие в
- 29. Скачать презентацию




















 Свойства и способы получения алкадиенов
Свойства и способы получения алкадиенов Природные источники углеводородов
Природные источники углеводородов Неметаллы: атомы и простые вещества. Воздух. Кислород. Озон
Неметаллы: атомы и простые вещества. Воздух. Кислород. Озон Курс хімії за 11 клас
Курс хімії за 11 клас Методы защиты металлов от электрохимической коррозии. Классификация методов защиты бетона и железобетона
Методы защиты металлов от электрохимической коррозии. Классификация методов защиты бетона и железобетона Общие сведения о полезных ископаемых. (Лекция 2)
Общие сведения о полезных ископаемых. (Лекция 2) Поверхностно-активные вещества (ПАВ)
Поверхностно-активные вещества (ПАВ) Элементы второй группы главной подгруппы
Элементы второй группы главной подгруппы Лекарственные средства, производные барбитуровой кислоты
Лекарственные средства, производные барбитуровой кислоты Медициналық тәжірибедегі потенциометриялар
Медициналық тәжірибедегі потенциометриялар Гравиметрические методы анализа
Гравиметрические методы анализа Фосфор
Фосфор Простые вещества
Простые вещества Закономерность изменений в строении электронных оболочек атома
Закономерность изменений в строении электронных оболочек атома Коррозия металлов
Коррозия металлов Массовая и объемная доля компонентов смеси
Массовая и объемная доля компонентов смеси Осадочные и метаморфические горные породы
Осадочные и метаморфические горные породы Азотистые гетероциклические соединения
Азотистые гетероциклические соединения Кремний и его соединения
Кремний и его соединения Геохимия магматического процесса
Геохимия магматического процесса Характеристика АХОВ и их поражающих факторов
Характеристика АХОВ и их поражающих факторов Камни и Скорпион
Камни и Скорпион Класифікація хімічних реакцій
Класифікація хімічних реакцій Класифікація неорганічних сполук, їхній склад і номенклатура
Класифікація неорганічних сполук, їхній склад і номенклатура Ионная хроматография
Ионная хроматография Окислительно-востановительные реакции в растворах
Окислительно-востановительные реакции в растворах Метаболизм жирных кислот
Метаболизм жирных кислот Физико-химические свойства белков. Электрофоретические и хроматографические методы
Физико-химические свойства белков. Электрофоретические и хроматографические методы