Содержание
- 2. Хроматография История открытия Хроматография - метод разделения и анализа смесей веществ, а также изучения физико-химических свойств
- 3. Хроматография История открытия 1872 Асти (Италия) – 1919 Воронеж (Россия) 1893 — бакалавр физических и естественных
- 4. Хроматография История открытия Работал в Санкт-Петербурге, Варшавском университете, Москве, Нижнем Новгороде, Воронеже 1918 — январь —
- 5. Первая хроматография проведена в 1900 году. М.Цвет использовал колонку, заполненную карбонатом кальция, для разделения пигментов растительного
- 6. Хроматография — метод разделения смесей веществ или частиц, основанный на различиях в скоростях их перемещения в
- 7. Хроматографический процесс – многочисленные циклы сорбции–десорбции
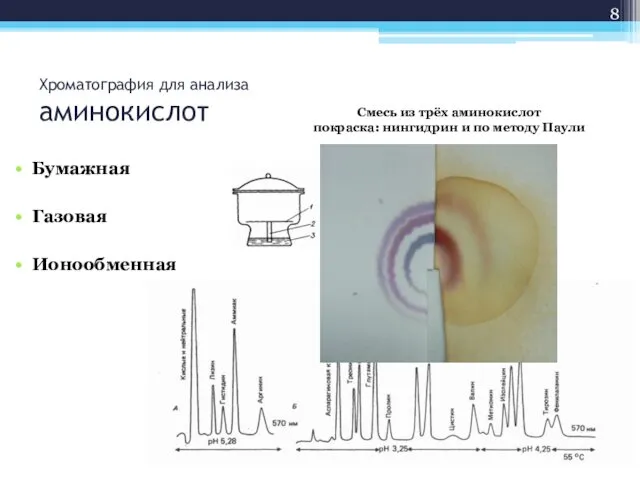
- 8. Хроматография для анализа аминокислот Бумажная Газовая Ионообменная Смесь из трёх аминокислот покраска: нингидрин и по методу
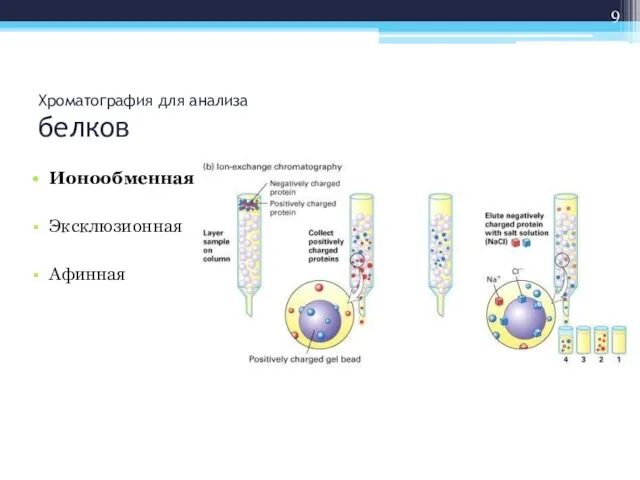
- 9. Хроматография для анализа белков Ионообменная Эксклюзионная Афинная
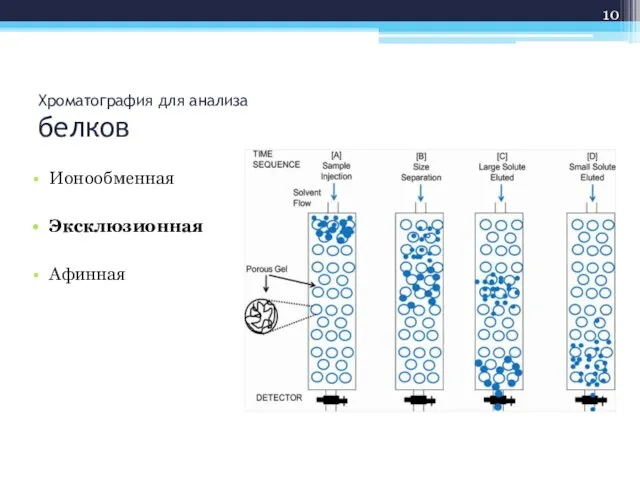
- 10. Хроматография для анализа белков Ионообменная Эксклюзионная Афинная
- 11. Vt = общий объём колонки Vo = объём подвижной фазы снаружи от частиц сефадекса Ve =
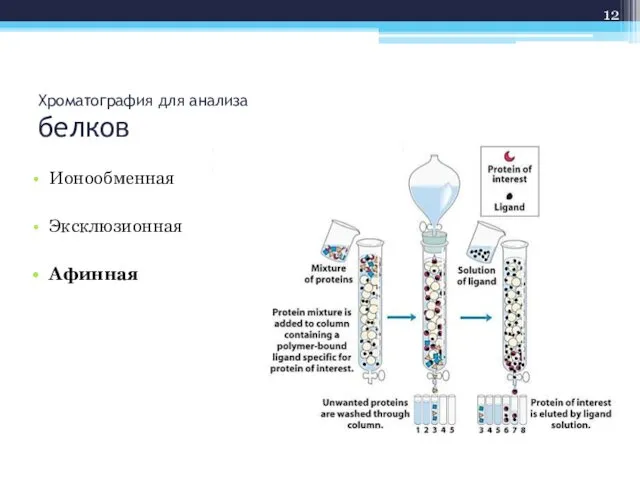
- 12. Хроматография для анализа белков Ионообменная Эксклюзионная Афинная
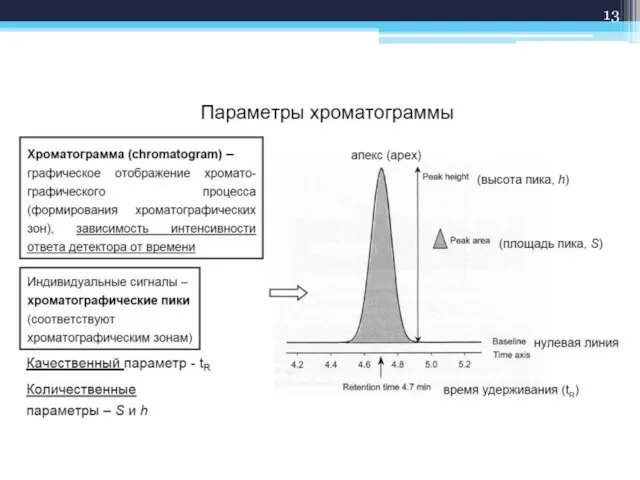
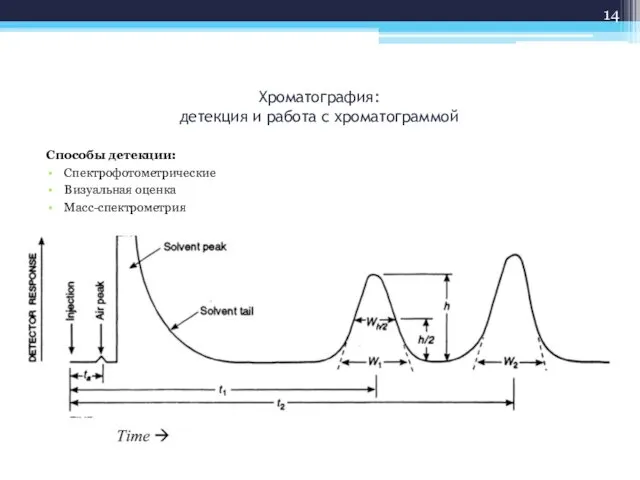
- 14. Хроматография: детекция и работа с хроматограммой Способы детекции: Спектрофотометрические Визуальная оценка Масс-спектрометрия
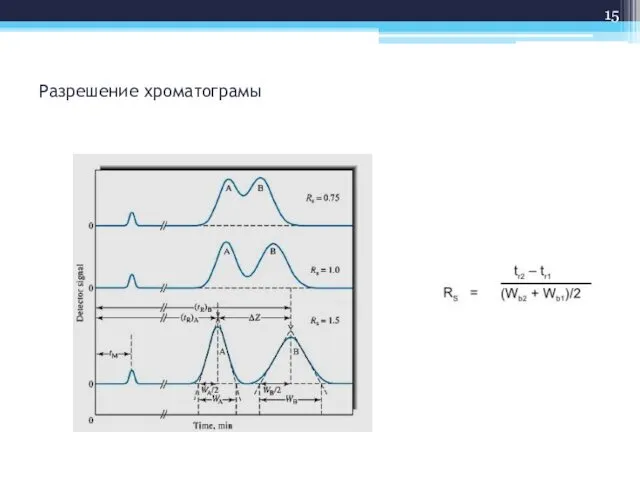
- 15. Разрешение хроматограмы
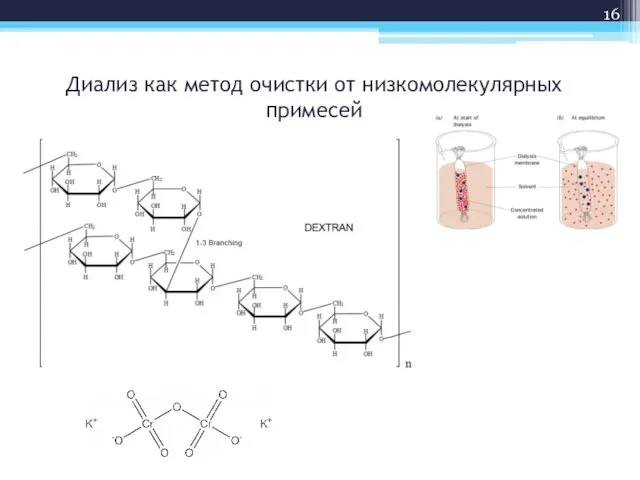
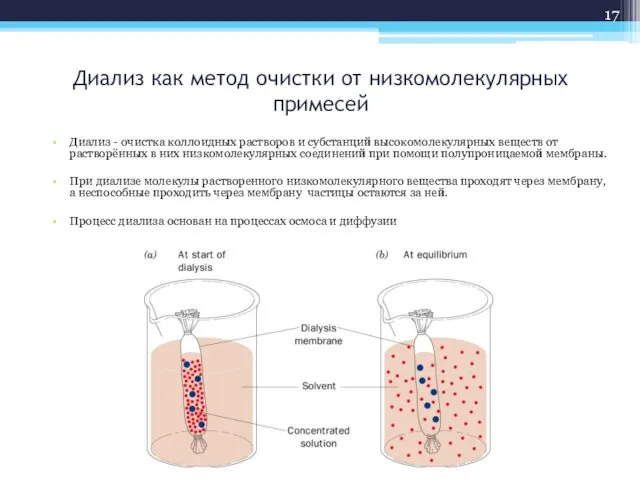
- 16. Диализ как метод очистки от низкомолекулярных примесей
- 17. Диализ как метод очистки от низкомолекулярных примесей Диализ - очистка коллоидных растворов и субстанций высокомолекулярных веществ
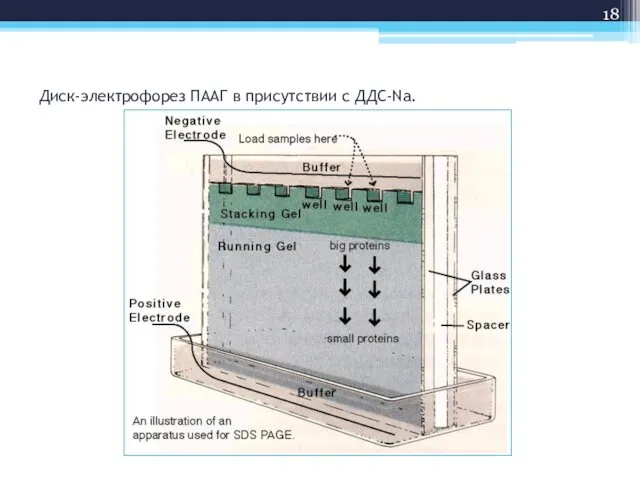
- 18. Диск-электрофорез ПААГ в присутствии с ДДС-Na.
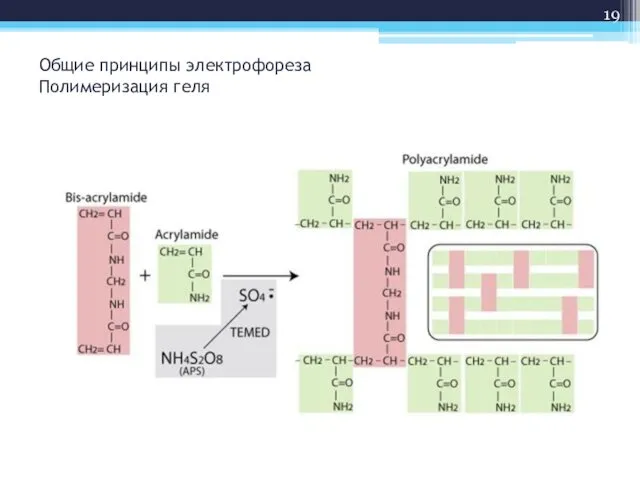
- 19. Общие принципы электрофореза Полимеризация геля
- 21. Скачать презентацию







 Аминокислоты, их строение, изомерия, свойства, применение
Аминокислоты, их строение, изомерия, свойства, применение Изучение процесса коррозии железа (домашний эксперимент)
Изучение процесса коррозии железа (домашний эксперимент) Минералы и горные породы
Минералы и горные породы Сұйықтардағы газ ерітінділері. Генри заңы. Сұйық-сұйық ерітінділердегі бу қысымы. Рауль заңынын ауытқу. Криометрия
Сұйықтардағы газ ерітінділері. Генри заңы. Сұйық-сұйық ерітінділердегі бу қысымы. Рауль заңынын ауытқу. Криометрия Протекание ОВР зависит от рН среды
Протекание ОВР зависит от рН среды Сполуки неметалічних елементів з Гідрогеном
Сполуки неметалічних елементів з Гідрогеном Хром. Химиялық қасиеттері
Хром. Химиялық қасиеттері 20230306_vodorod_ego_fizicheskie_svoystva
20230306_vodorod_ego_fizicheskie_svoystva Закономерности процессов нитрования НЦ
Закономерности процессов нитрования НЦ Основные электрохимические процессы
Основные электрохимические процессы Иодометрия. Комплексиметрия (начало)
Иодометрия. Комплексиметрия (начало) Золото Au (Аурум)
Золото Au (Аурум) Кислородсодержащие органические соединения. Спирты
Кислородсодержащие органические соединения. Спирты Растворение как физико-химический процесс
Растворение как физико-химический процесс Химический анализ веществ
Химический анализ веществ Диагностические свойства минералов. Занятие 3-4
Диагностические свойства минералов. Занятие 3-4 Химия воды
Химия воды Химические свойства основных неорганических соединений в свете ЭД и ОВР
Химические свойства основных неорганических соединений в свете ЭД и ОВР Основные виды химических связей
Основные виды химических связей Занимательные опыты
Занимательные опыты Титриметрический метод анализа
Титриметрический метод анализа Введение в органическую химию
Введение в органическую химию Полиэтилен - термопластичный полимер этилена
Полиэтилен - термопластичный полимер этилена Native elements
Native elements Понятие о солях (8 класс)
Понятие о солях (8 класс) Скорость химической реакции
Скорость химической реакции Состояние радионуклидов в различных фазах и методы его изучения
Состояние радионуклидов в различных фазах и методы его изучения Периодический закон и периодический закон Д.И. Менделеева
Периодический закон и периодический закон Д.И. Менделеева