Содержание
- 2. Тема урока: «Аминокислоты, их строение, изомерия, свойства, применение.»
- 3. Цель урока: дать понятие об аминокислотах как органических амфотерных соединениях; рассмотреть их строение, классификацию, изомерию и
- 4. Аминокислоты NH2 - CH - COOH | R Производные карбоновых кислот, содержащие в своем составе одну
- 5. Аминокислоты Природные Их около 150, они были обнаружены в живых организмах. Около 20 из них входят
- 6. Систематическая номенклатура По систематической номенклатуре названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино- и
- 7. Тривиальная номенклатура Часто используется другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты
- 8. Изомерия аминокислот углеродного скелета ; положения функциональных групп ; межклассовая (нитросоединения); оптическая.
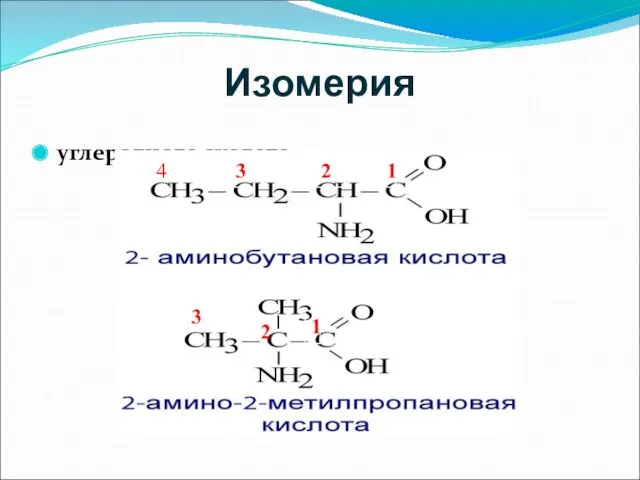
- 9. Изомерия углеродного скелета 1 2 3 1 2 4 3
- 10. Изомерия положения функциональных групп
- 11. Изомерия межклассовая (нитросоединения) 5 4 3 2 1 H3 C – CH2 – CH – CH2
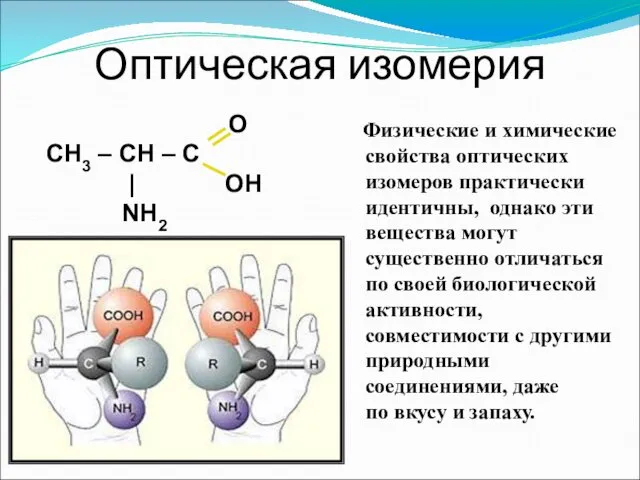
- 12. Оптическая изомерия O CH3 – CH – C | OH NH2 Физические и химические свойства оптических
- 13. Физические свойства Аминокислоты бесцветные; кристаллические; хорошо растворимы в воде, но нерастворимы в эфире; в зависимости от
- 14. Теория химического строения органических соединений А. М. Бутлерова Атомы в молекулах органических веществ связаны в определённой
- 15. Химические свойства Наличие амино- и карбоксильной групп определяет двойственность химических свойств аминокислот. Амфотерность (от греч. amphуteros
- 16. Химические свойства
- 17. Аминокислоты – амфотеры Как кислоты а) с основаниями NH2-CH-COOH + NaOH NH2-CH-COONa + H2O | |
- 18. б) со спиртами NH2-CH-COOH+С2Н5ОН NH2-CH-COOС2Н5 + H2O | | R R этиловый эфир аминокислоты 2) Как
- 19. Реакция поликонденсации H O H O | ║ | ║ …H – N – CH –
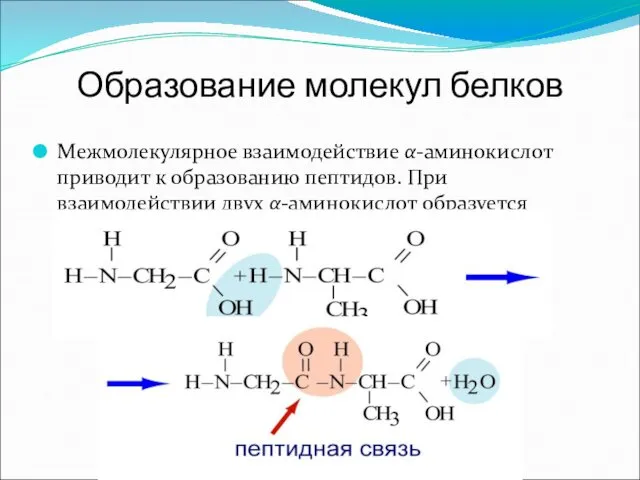
- 20. Образование молекул белков Межмолекулярное взаимодействие α-аминокислот приводит к образованию пептидов. При взаимодействии двух α-аминокислот образуется дипептид.
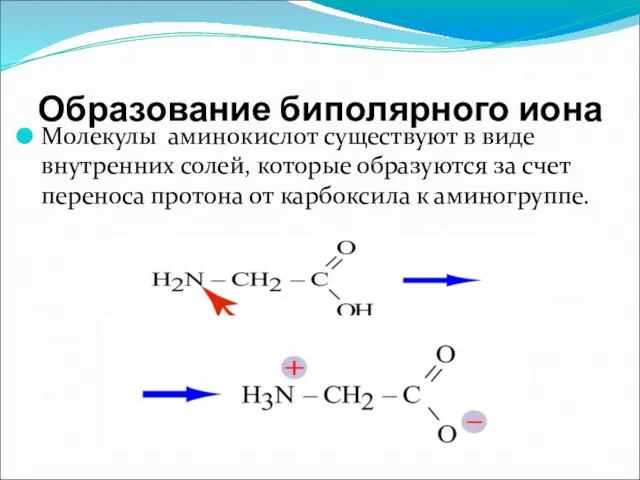
- 21. Образование биполярного иона Молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона
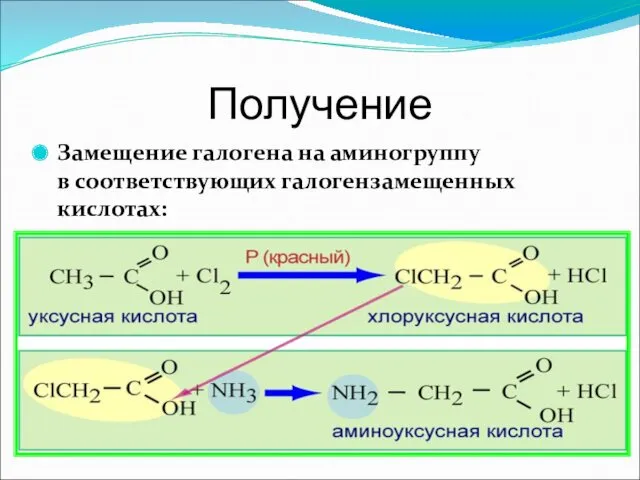
- 22. Получение Замещение галогена на аминогруппу в соответствующих галогензамещенных кислотах:
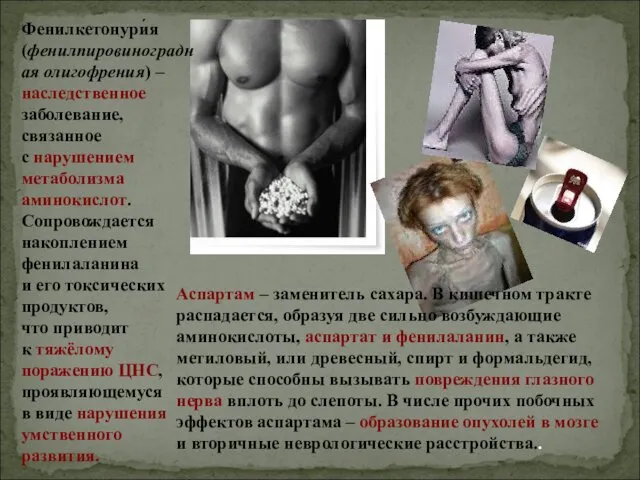
- 23. Фенилкетонури́я (фенилпировиноградная олигофрения) – наследственное заболевание, связанное с нарушением метаболизма аминокислот. Сопровождается накоплением фенилаланина и его
- 24. 1. Напишите структурную формулу аминокислоты по названию и составьте изомер углеродного скелета, изомер положения аминогруппы, межклассовый
- 26. Скачать презентацию

















 Материалы с высокой удельной прочностью
Материалы с высокой удельной прочностью Химические реакторы. Лекция №6
Химические реакторы. Лекция №6 Простые вещества - металлы
Простые вещества - металлы ЕГЭ по химии, задание 2
ЕГЭ по химии, задание 2 Трифенилметановые красители
Трифенилметановые красители Химия. 6я группа элементов. 9 класс
Химия. 6я группа элементов. 9 класс Некоторые структурные особенности макромолекул
Некоторые структурные особенности макромолекул Химические формулы. Относительная атомная и молекулярная масса
Химические формулы. Относительная атомная и молекулярная масса Химиялық байланыс және заттардың құрылымдық түрлі сатылары
Химиялық байланыс және заттардың құрылымдық түрлі сатылары Биогенді элементтер
Биогенді элементтер Актиноиды. Физические и химические свойства
Актиноиды. Физические и химические свойства Көпатомды спирттер. Химиялық қасиеттері
Көпатомды спирттер. Химиялық қасиеттері Сполуки неметалічних елементів з Гідрогеном. Особливості водних розчинів цих сполук, їх застосування
Сполуки неметалічних елементів з Гідрогеном. Особливості водних розчинів цих сполук, їх застосування Электоролиз заңы
Электоролиз заңы Основы органической химии
Основы органической химии Металлы (урок для 8 класса)
Металлы (урок для 8 класса) Вклад М.В. Ломоносова в развитие химии
Вклад М.В. Ломоносова в развитие химии Амины
Амины Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Химическая стойкость тугоплавких металлов в различных реагентах
Химическая стойкость тугоплавких металлов в различных реагентах Кислородсодержащие органические соединения (классификация и номенклатура)
Кислородсодержащие органические соединения (классификация и номенклатура) Подгруппа меди. Элементы 11 группы (Cu,Ag,Au)
Подгруппа меди. Элементы 11 группы (Cu,Ag,Au) Полимеры. Основные понятия
Полимеры. Основные понятия Диеновые углеводороды или алкадиены (тема 4)
Диеновые углеводороды или алкадиены (тема 4) Техника безопасности на уроках химии
Техника безопасности на уроках химии Материаловедение-2
Материаловедение-2 Твердое состояние вещества. Кристаллические и аморфные тела
Твердое состояние вещества. Кристаллические и аморфные тела Супрамолекулярная химия - молекулярная социология
Супрамолекулярная химия - молекулярная социология