Содержание
- 2. Влияние коллектива на индивидуума зависит от: Индивидуума • Типа коллектива • Внешних условий
- 3. ЛЮДИ группа друзей альпинистская группа фирма толпа колонна на параде МОЛЕКУЛЫ раствор • стекло • кристалл
- 4. ЛЮДИ • обстановка в обществе • условия жизни • род занятий МОЛЕКУЛЫ • температура • давление
- 5. Супрамолекулярная химия изучает: • Роль среды в химических реакциях • Молекулы в составе коллективов: • синтез
- 6. Направления исследований (1): • Выявление существования межмолекулярных связей и нахождение их энергетических характеристик (при помощи спектроскопических
- 7. Направления исследований (2): • Использование межмолекулярных взаимодействий в синтезе химических соединений (новые классы сложных органических молекул,
- 8. Направления исследований (3): • Исследование роли межмолекулярных взаимодействий и надмолекулярной организации в формировании физических свойств (анизотропия
- 9. “Реакция неотделима от среды, в которой она протекает” Н. Меншуткин, 1890 г.
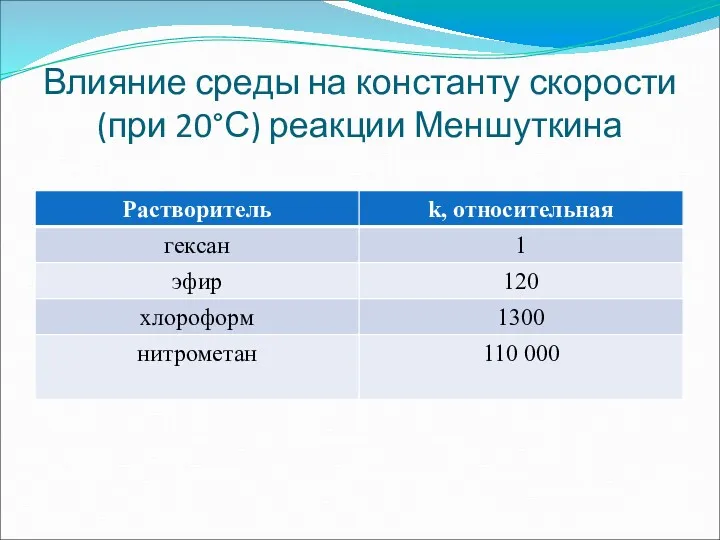
- 10. Влияние среды на константу скорости (при 20°С) реакции Меншуткина
- 11. СРЕДА: • Растворитель • Любые иные ионы / молекулы • Окружение в кристалле • Подложка •
- 12. РОЛЬ ИНДИВИДУУМА H2S H2O Tкип = -62°C Tкип = 100°C
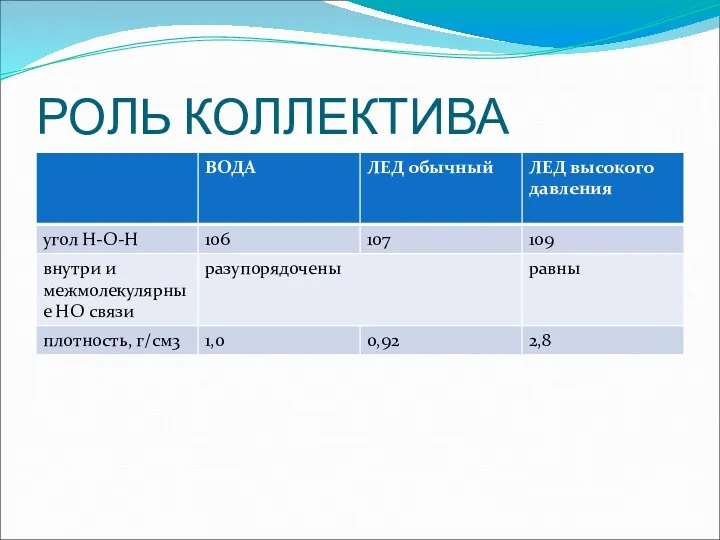
- 13. РОЛЬ УСЛОВИЙ пар • жидкость • 13 видов кристаллических льдов • несколько видов аморфных льдов
- 14. РОЛЬ КОЛЛЕКТИВА
- 15. Влияние среды на индивидуума: • Изменение конформации • Валентная изомеризация • Изменение дипольного момента • Влияние
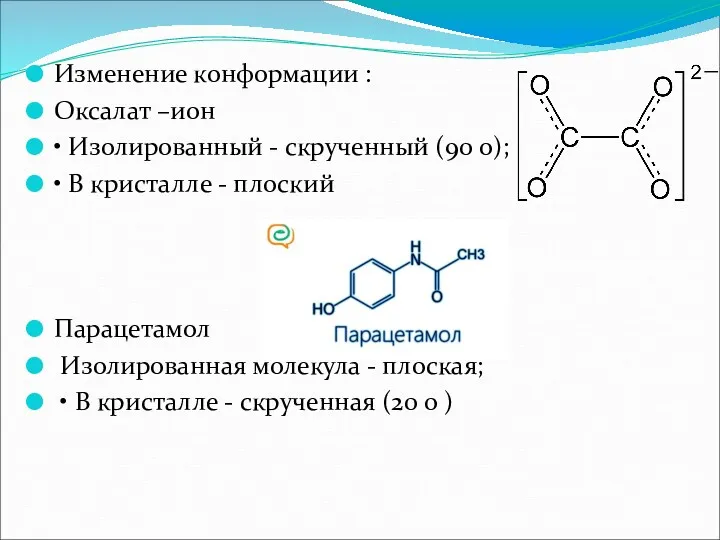
- 16. Изменение конформации : Оксалат –ион • Изолированный - скрученный (90 о); • В кристалле - плоский
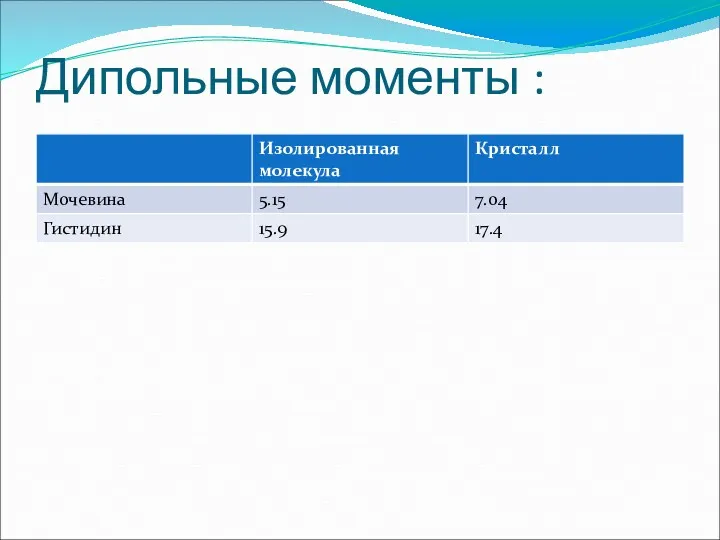
- 17. Дипольные моменты :
- 18. Влияние среды на аминокислоты: Кристаллы, водные растворы цвиттер-ионы H3N+-CHR-COO- Гидрофобные матрицы молекулы H2N-CHR-COOH
- 19. Роль среды в химических реакциях ОТНОСИТЕЛЬНАЯ КИСЛОТНОСТЬ • Газовая фаза: H 2O • Водные растворы: C
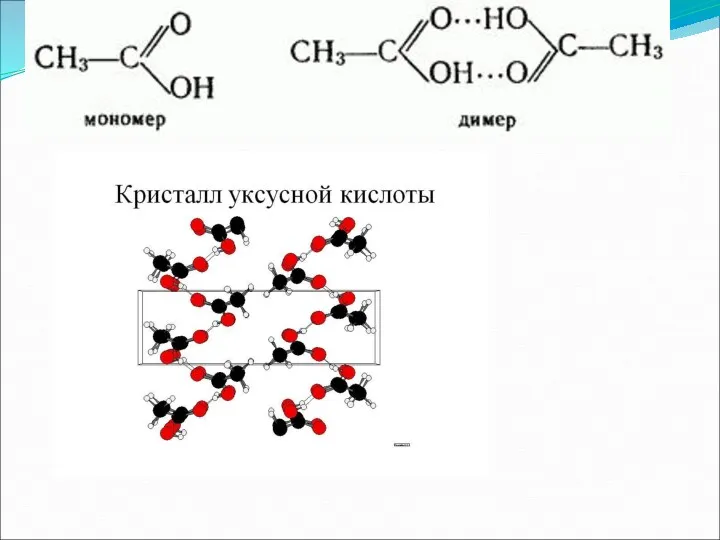
- 20. Молекулярные кристаллы Молекула - в окружении себе подобных Топохимический принцип: Стереохимический ход превращения контролируется взаимодействиями реагирующих
- 21. • Газ: HO- + C6H5CH3 → H2O + (C6H5CH2)- • Водный раствор: H2O + (C6H5CH2)-→ HO-
- 22. • Газ: Большие анионы с делокализованным зарядом • Водный раствор: Малые анионы с более высокой плотностью
- 23. HA + B- ⇔ A- + BH • Газ: Кислотность определяется энергией разрыва связи HA и
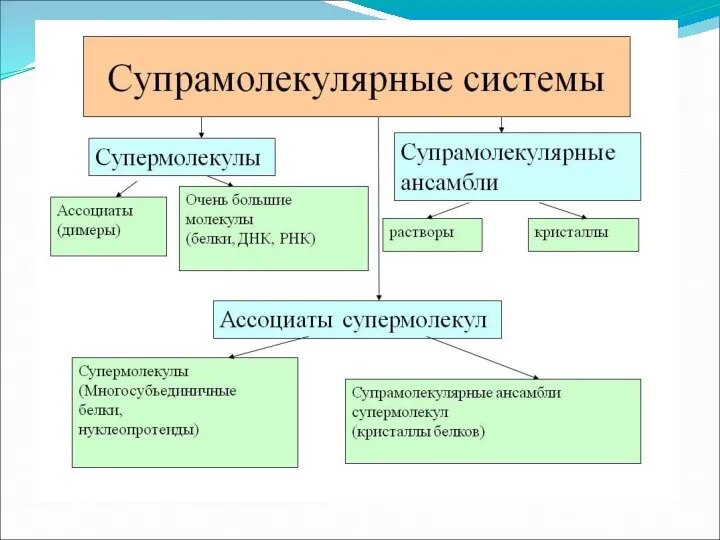
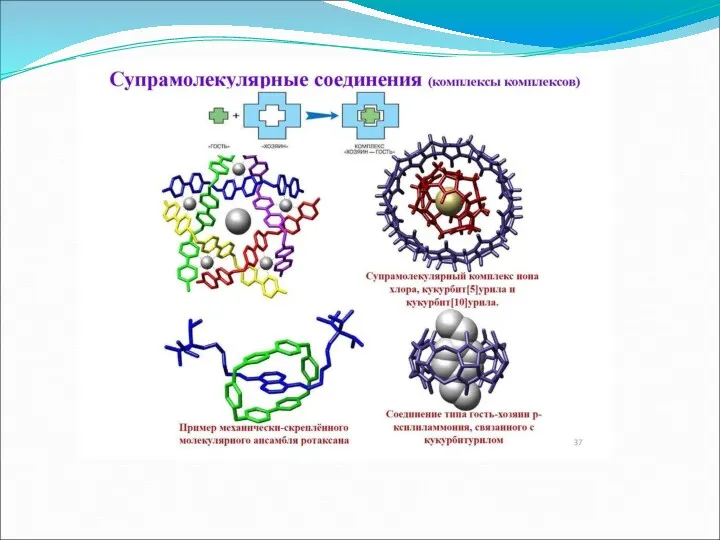
- 25. Супермолекулы: хорошо определенные, дискретные межмолекулярные ассоциаты нескольких компонентов - рецептора и его субстрата (ов), двух и
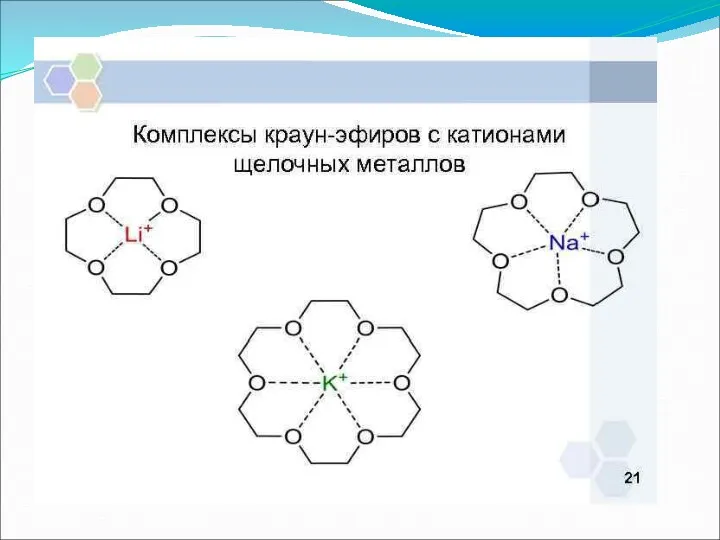
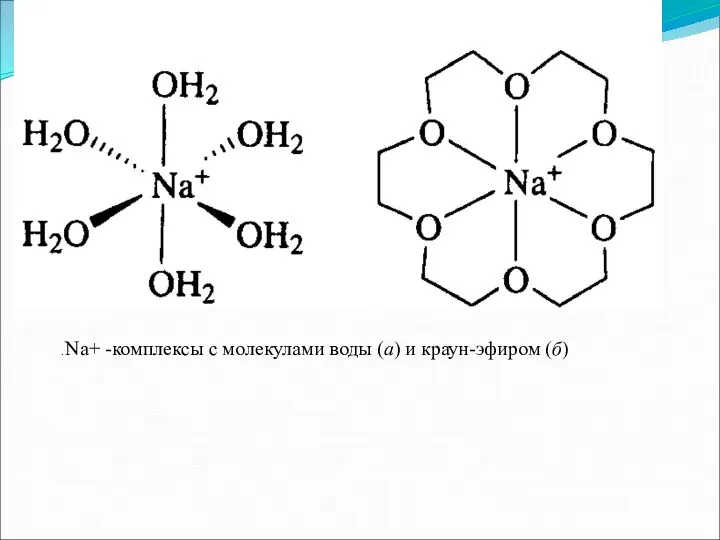
- 29. . Na+ -комплексы с молекулами воды (а) и краун-эфиром (б)
- 32. Примеры больших супермолекул, дендимеры
- 37. В основе синтеза лежат: • Самоорганизация • Молекулярное распознавание • Комплементарность взаимодействий и формы • Принцип
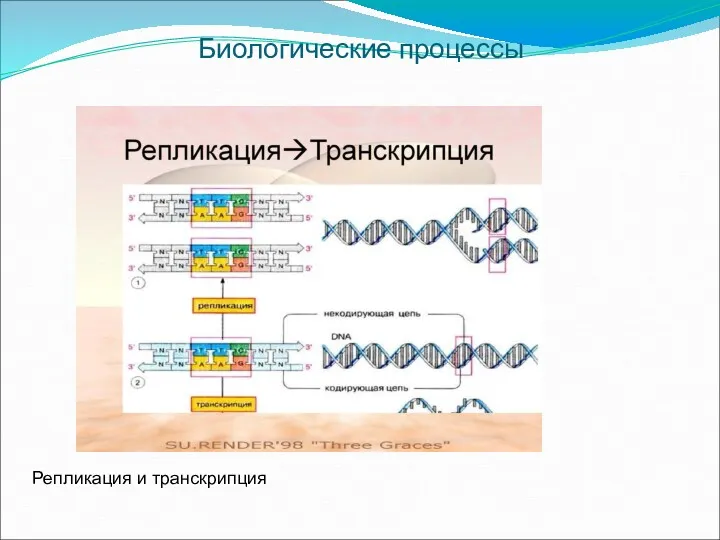
- 38. Биологические процессы Репликация и транскрипция
- 39. За счет селективности достигаются: • Управление составом продуктов • Контроль за полиморфизмом • Контроль за биологическими
- 40. 1. Влияние растворителя на реакции - 19 век 2. Возможность образования молекулярных и ионномолекулярных ассоциатов, не
- 41. Выводы: Реакция неотделима от среды, в которой она происходит Поэтому возникла необходимость перейти от химии индивидуальных
- 42. Выводы: Супрамолекулярная химия имеет дело с супермолекулами и супрамолекулярными ансамблями За образование, структуру и свойства тех
- 44. Скачать презентацию




























 Алканы. Состав, строение, свойства и химические превращения. Экологические последствия. Синтезы генетическая связь
Алканы. Состав, строение, свойства и химические превращения. Экологические последствия. Синтезы генетическая связь Химический элемент. Изотопы. 11 класс
Химический элемент. Изотопы. 11 класс Кислород. Строение молекулы кислорода. Получение кислорода. Взаимодействие с кислородом простых и сложных веществ
Кислород. Строение молекулы кислорода. Получение кислорода. Взаимодействие с кислородом простых и сложных веществ Основные сырьевые материалы для производства портландцемента
Основные сырьевые материалы для производства портландцемента Подземное хранение газа и жидкости
Подземное хранение газа и жидкости Кремний и его соединения
Кремний и его соединения Ионы и ионная химическая связь
Ионы и ионная химическая связь Воспользуйтесь ЛСМ Химические реакции
Воспользуйтесь ЛСМ Химические реакции Металлы. Общая характеристика
Металлы. Общая характеристика Азотная кислота и ее свойства
Азотная кислота и ее свойства Транспортное обеспечение внесения удобрений
Транспортное обеспечение внесения удобрений Развивающие занятия в ГПД Поделочные камни
Развивающие занятия в ГПД Поделочные камни Протолитическая теория кислот и оснований. Протолитическое равновесие. Буферные растворы. Лекция 01
Протолитическая теория кислот и оснований. Протолитическое равновесие. Буферные растворы. Лекция 01 Свойства спирта и воды
Свойства спирта и воды Наноалмазы детонационного синтеза
Наноалмазы детонационного синтеза Этот многоликий цинк
Этот многоликий цинк Изомерия. Виды изомерии
Изомерия. Виды изомерии Диссоциация воды. Водородный и гидроксильный показатели (рН и рОН)
Диссоциация воды. Водородный и гидроксильный показатели (рН и рОН) Соединения кремния
Соединения кремния Введение в кристаллографию
Введение в кристаллографию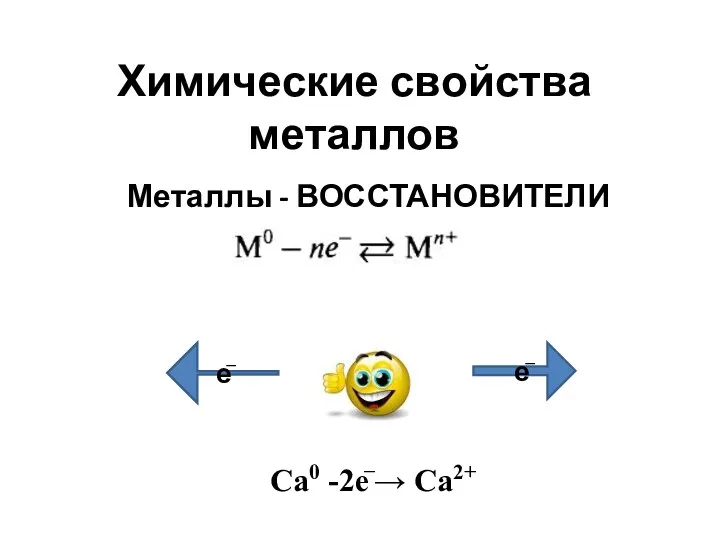 Химические свойства металлов
Химические свойства металлов Методические подходы к решению химических задач. Задание 34
Методические подходы к решению химических задач. Задание 34 Углеводы. Моносахариды
Углеводы. Моносахариды Зеленая химия и проблемы устойчивого развития
Зеленая химия и проблемы устойчивого развития Окислительные методы получения органических соединений
Окислительные методы получения органических соединений Получение уксусной кислоты и опыты с ней
Получение уксусной кислоты и опыты с ней Магний (Mg)
Магний (Mg) Изомерия в органической химии. Изомеры
Изомерия в органической химии. Изомеры