Слайд 2

ЗАДАНИЕ № 1
ЗАПИШИТЕ ФОРМУЛУ СОЕДИНЕНИЯ АЗОТА И ЕГО НАЗВАНИЕ НА ОСНОВАНИИ
ФИЗИЧЕСКИХ СВОЙСТВ
Бесцветный газ с характерным резким запахом, хорошо растворим в воде, легче воздуха.
NH3 - аммиак
Слайд 3

ЗАДАНИЕ № 2
РАСПОЛОЖИТЕ СОЕДИНЕНИЯ АЗОТА В ПОРЯДКЕ ВОЗРАСТАНИЯ СТЕПЕНЕЙ ОКИСЛЕНИЯ.
N2,
NH3, KNO3, NO, HNO2.
-3 0 +2 +3 +5
NH3, N2, NO, HNO2, KNO3.
Слайд 4

АЗОТНАЯ КИСЛОТА И ЕЕ СВОЙСТВА
Слайд 5

I. ФИЗИЧЕСКИЕ СВОЙСТВА
АЗОТНОЙ КИСЛОТЫ
Агрегатное состояние – жидкость;
Цвет – отсутствует;
Запах –
едкий, кислотный;
Растворимость в воде – хорошая;
«Дымит» на воздухе;
«Особые приметы»:
при хранении на свету разлагается, приобретая желтоватый оттенок:
4HNO3=4NO2↑ + O2↑ + 2H2O
Слайд 6

Слайд 7
III. ХИМИЧЕСКИЕ СВОЙСТВА HNO3
Слайд 8
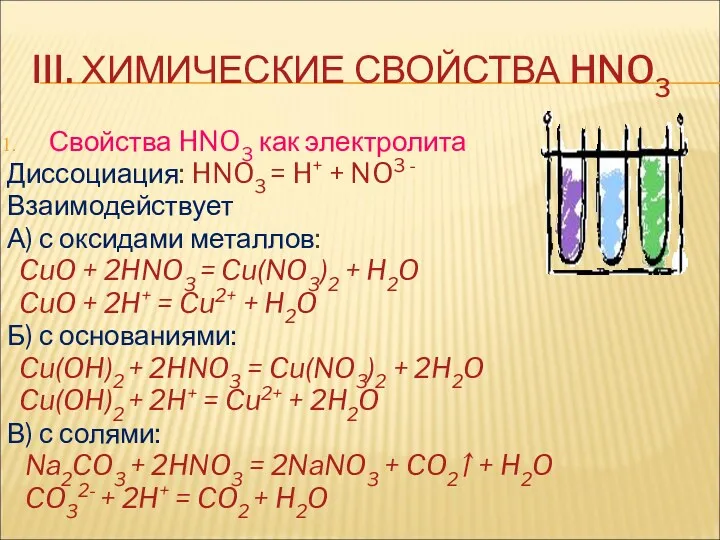
III. ХИМИЧЕСКИЕ СВОЙСТВА HNO3
Свойства HNO3 как электролита
Диссоциация: HNO3 = H+ +
NO3 -
Взаимодействует
А) с оксидами металлов:
CuO + 2HNO3 = Cu(NO3)2 + H2O
CuO + 2H+ = Cu2+ + H2O
Б) с основаниями:
Cu(OH)2 + 2HNO3 = Cu(NO3)2 + 2H2O
Cu(OH)2 + 2H+ = Cu2+ + 2H2O
В) с солями:
Na2CO3 + 2HNO3 = 2NaNO3 + CO2↑ + H2O
CO32- + 2H+ = CO2 + H2O
Слайд 9
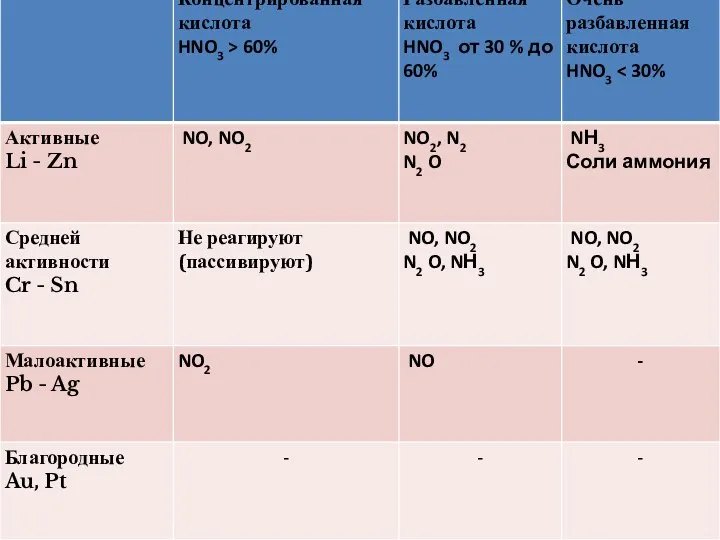
Слайд 10

III. ХИМИЧЕСКИЕ СВОЙСТВА HNO3
2. Окислительные свойства
Взаимодействует с металлами:
K Ca
Na Mg Al Zn Cr Fe Pb H2 Cu Hg Ag Au
Ме + HNO3 → Me(NO3)n + H2O + NxOy
Cu + 4HNO3(конц) = Cu(NO3)2 + 2H2O + 2NO2↑
3Cu + 8HNO3(разб) = 3Cu(NO3)2 + 4H2O + 2NO↑
Me + HNO3 = Me(NO3)2 + H2↑
Слайд 11

ДЕЙСТВИЕ НА ОРГАНИЧЕСКИЕ ВЕЩЕСТВА
Белки при взаимодействии с концентрированной азотной кислотой разрушаются
и приобретают жёлтую окраску .
Под действием азотной кислоты воспламеняются бумага, масло, древесина, уголь.










 Минералды тыңайтқыштар
Минералды тыңайтқыштар Тотығу-тотықсыздану титрлеу әдісі
Тотығу-тотықсыздану титрлеу әдісі Пены. Пенообразование
Пены. Пенообразование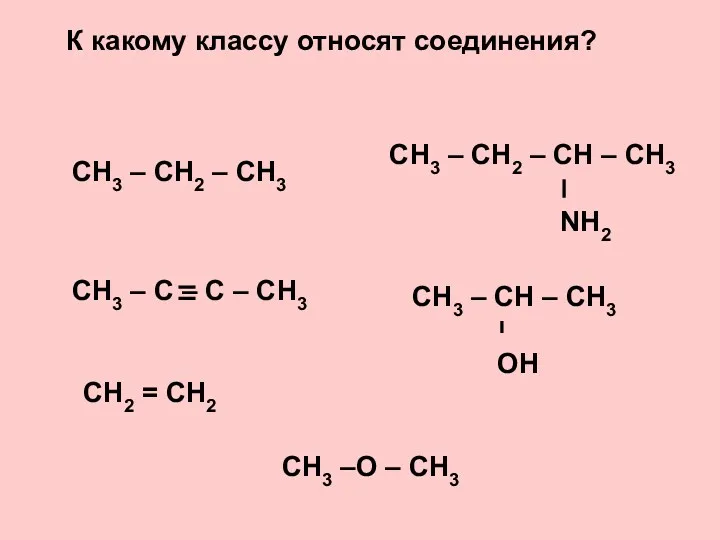 16_OP_05_Alkany
16_OP_05_Alkany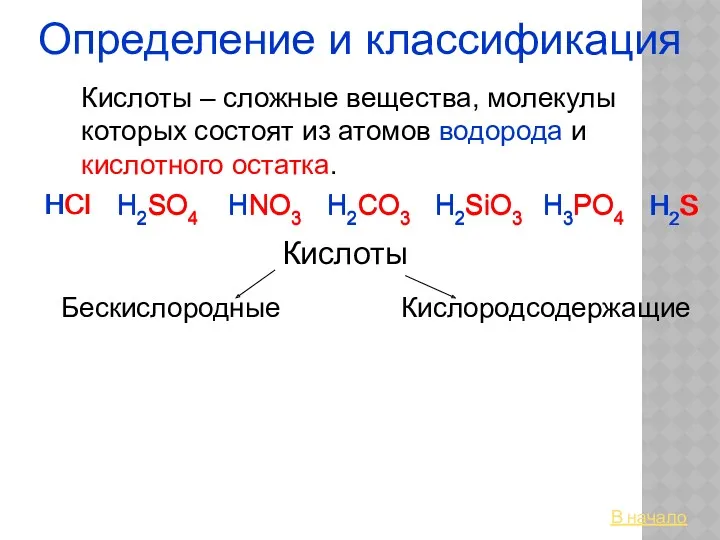 Кислоты. Определение и классификация
Кислоты. Определение и классификация Цикл трикарбоновых кислот (Ц.Кребса). Подсчёт суммарного энергетического эффекта аэробного окисления глюкозы
Цикл трикарбоновых кислот (Ц.Кребса). Подсчёт суммарного энергетического эффекта аэробного окисления глюкозы Квантово-механический подход к описанию строения атомов
Квантово-механический подход к описанию строения атомов d-элементы
d-элементы Химия и живопись
Химия и живопись Ароматические углеводороды (арены)
Ароматические углеводороды (арены)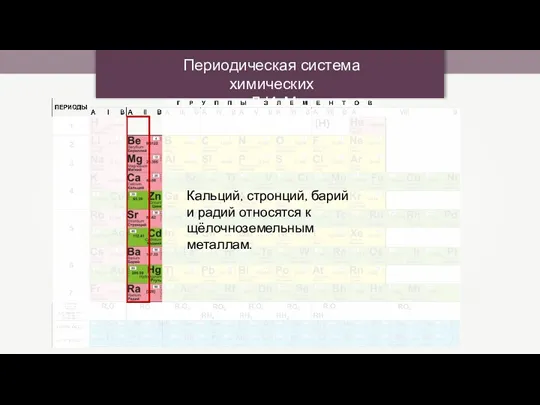 Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Химическое равновесие
Химическое равновесие Тест: полимеры
Тест: полимеры Платина. Физические и химические свойства
Платина. Физические и химические свойства Минералогия с основами кристаллографии
Минералогия с основами кристаллографии Химические реакции
Химические реакции Бордың адам ағзасына әсері
Бордың адам ағзасына әсері Гідроліз солей
Гідроліз солей Гетероциклические соединения природного и синтетического происхождения. Производные фурана и бензофурана. (Лекция 1-2)
Гетероциклические соединения природного и синтетического происхождения. Производные фурана и бензофурана. (Лекция 1-2) Соединения железа. Охарактеризуйте Fe
Соединения железа. Охарактеризуйте Fe Cross-section sample preparation using focused ion beam system (FIB) for transmission electron microscopy (TEM)
Cross-section sample preparation using focused ion beam system (FIB) for transmission electron microscopy (TEM) Вычисление массовой доли растворенного вещества. 8 класс
Вычисление массовой доли растворенного вещества. 8 класс Титриметрические методы количественного определения лекарственных веществ
Титриметрические методы количественного определения лекарственных веществ Structural, substructural properties and chemical composition
Structural, substructural properties and chemical composition Водород
Водород Композиционные материалы
Композиционные материалы Реакции ионного обмена
Реакции ионного обмена Галогенопроизводные углеводородов 1
Галогенопроизводные углеводородов 1