Содержание
- 2. medcollege.ru Изомеры – это вещества, имеющие одинаковый состав (число атомов каждого типа), но разное взаимное расположение
- 3. medcollege.ru Виды изомерии: Различают два основных вида изомерии: структурную и пространственную (стереоизомерию). Структурные изомеры отличаются друг
- 4. medcollege.ru Структурная изомерия: Структурные изомеры – соединения с одинаковым составом, но различным порядком связывания атомов, т.е.
- 5. medcollege.ru 1. Изомерия углеродного скелета: вещества различаются строением углеродной цепи, которая может быть линейная или разветвленная.
- 6. 2. Изомерия положения обусловлена различным положением кратной связи, функциональной группы или заместителя при одинаковом углеродном скелете
- 7. 2.1. Изомерия положения функциональной группы. Например, существует два изомерных предельных спирта с общей формулой С3Н8О: пропанол-1
- 8. 2.2. Изомерия положения кратной связи может быть вызвана различным положением кратной (двойной или тройной) связи в
- 9. 2.3. Межклассовая изомерия – ещё один вид структурной изомерии, когда вещества из разных классов веществ имеют
- 11. Пространственная изомерия: Пространственные изомеры – это вещества с одинаковым составом и химическим строением, но с разным
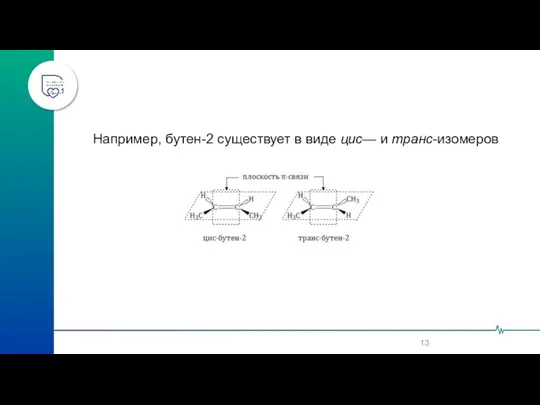
- 12. 1. Геометрическая изомерия (или цис-транс-изомерия). Геометрическая изомерия характерна для соединений, в которых различается положение заместителей относительно
- 13. Например, бутен-2 существует в виде цис— и транс-изомеров
- 14. 1,2-Диметилпропан также образует цис-транс-изомеры: Геометрические изомеры различаются по физическим свойствам (температура кипения и плавления, растворимость, дипольный
- 15. При этом цис—транс-изомерия характерна для соединений, в которых каждый атом углерода при двойной связи С=С (или
- 16. 2. Оптическая изомерия Оптические изомеры – это пространственные изомеры, молекулы которых соотносятся между собой как предмет
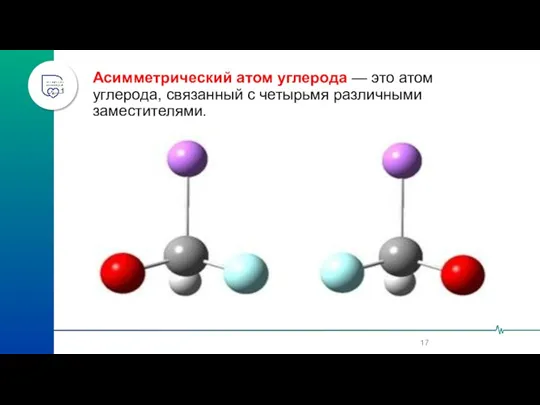
- 17. Асимметрический атом углерода — это атом углерода, связанный с четырьмя различными заместителями.
- 18. Такие молекулы обладают оптической активностью — способностью к вращению плоскости поляризации света при прохождении поляризованного луча
- 19. Метамерия — вид структурной изомерии, для которого характерно различное распределение углеродных атомов между несколькими углеводородными радикалами,
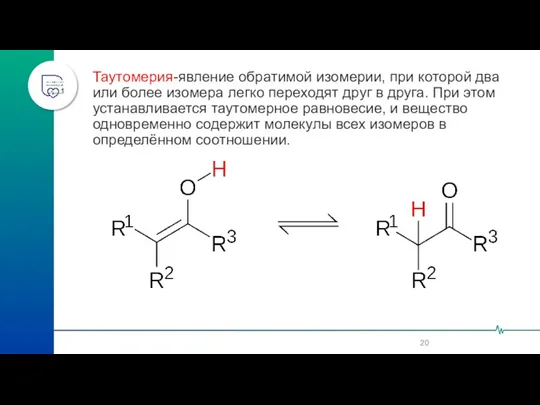
- 20. Таутомерия-явление обратимой изомерии, при которой два или более изомера легко переходят друг в друга. При этом
- 21. Стереохимия - область химической науки, рассматривающая вопросы пространственного строения веществ. Стереохимия играет большую роль в изучении
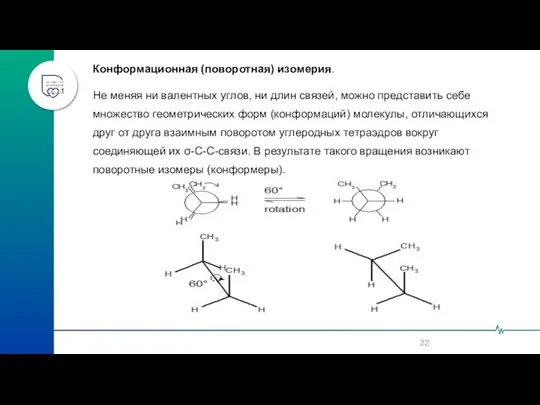
- 22. Конформационная (поворотная) изомерия. Не меняя ни валентных углов, ни длин связей, можно представить себе множество геометрических
- 23. Диастереомеры — стереоизомеры, не являющиеся зеркальными отражениями друг друга. Диастереомерия возникает, когда соединение имеет несколько стереоцентров.
- 25. Скачать презентацию


















 Бензол молекуласында байланыстардың түзілу сызбанұсқасы
Бензол молекуласында байланыстардың түзілу сызбанұсқасы Экспериментально исследовательский проект Соль волшебница
Экспериментально исследовательский проект Соль волшебница Химиялық кинетика және химиялық тепе-теңдік
Химиялық кинетика және химиялық тепе-теңдік Тренувальні вправи. Задачі
Тренувальні вправи. Задачі Техника безопасности в кабинете химии
Техника безопасности в кабинете химии Қалдық мөлшерлер
Қалдық мөлшерлер сложные эфиры
сложные эфиры Закон сохранения массы. Химические уравнения
Закон сохранения массы. Химические уравнения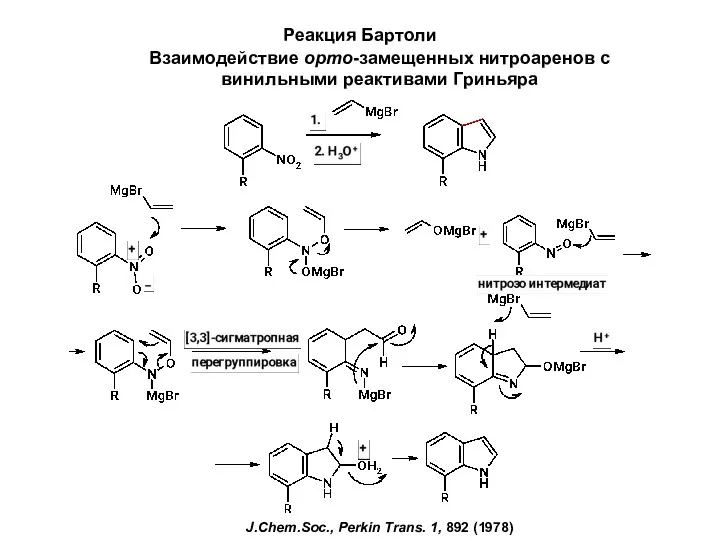 Реакция Бартоли. Взаимодействие орто-замещенных нитроаренов с винильными реактивами Гриньяра
Реакция Бартоли. Взаимодействие орто-замещенных нитроаренов с винильными реактивами Гриньяра Окисно-відновні реакції у природі і промисловості
Окисно-відновні реакції у природі і промисловості Химические свойства толуола
Химические свойства толуола Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Определите положение в ПСХЭ элементов
Определите положение в ПСХЭ элементов Металдарға жалпы сипаттама
Металдарға жалпы сипаттама Complex compounds
Complex compounds Химия - тұрмыста
Химия - тұрмыста p-элементы 17 группы периодической системы: галогены
p-элементы 17 группы периодической системы: галогены Свойства кислорода. Получение кислорода методом вытеснения воздуха
Свойства кислорода. Получение кислорода методом вытеснения воздуха Самородные элементы
Самородные элементы Товары бытовой химии
Товары бытовой химии Реакції йонного обміну між електролітами у водних розчинах
Реакції йонного обміну між електролітами у водних розчинах Вода – растворитель. Растворы. Значение воды
Вода – растворитель. Растворы. Значение воды Окислительно-восстановительные реакции. (лекция №10)
Окислительно-восстановительные реакции. (лекция №10) Узагальнення й систематизація знань з теми Початкові хімічні поняття (1 частина)
Узагальнення й систематизація знань з теми Початкові хімічні поняття (1 частина) Виды присадок к моторным топливам (керосин)
Виды присадок к моторным топливам (керосин) Сера и ее соединения
Сера и ее соединения Кислород. Химия. 8 класс
Кислород. Химия. 8 класс Последствия применения удобрений в сельском хозяйстве
Последствия применения удобрений в сельском хозяйстве