Содержание
- 2. 1.Химиялық реакциялардың энергетикалық сипаттамаларын білу. 2. Кинетика және химиялық реакцияның механизмдері. Вант-Гофф ережесі. Активтендіру энергиясы. Аррениус
- 3. Химиялық кинетика деп химиялық реакциялардың механизмдері жайлы ілімді айтады. Бұл салада әрбір реакция жыл-дамдығы және оған
- 4. Изохора-изотермиялық процесте (V = const, T = const) ▲V = 0 болғандықтан, реакция жылуы ▲U болады,
- 5. Изохора-изотермиялық процесте (V = const, T = const) ▲V = 0 болғандықтан, реакция жылуы ▲U болады,
- 6. Голландия химигі. 1871 жылы Делфт қаласында Политехникалық мектепті бітірген. Лейден және Бонн (Ф.А. Кекуледе) университетерінде, Париждің
- 7. Реакцияға түскіш бөлшектерді активтілер деп, энергетикалық барьерді (асуды) жоюға қажетті энергияны активтендіру энергиясы дейді. Әрекеттесуші заттарды
- 8. Химиялық тепе-теңдік — бір немесе бірнеше қарама-қарсы жүретін қайтымды реакциялар жылдамдықтарының теңескен күйі. Қайтымды реакция аяғына
- 10. . Егер реакция қайтымды болса, белгілі бір уақыт өткен соң кері реакцияның жылдамдығы арта бастайды, себебі
- 12. Скачать презентацию
1.Химиялық реакциялардың энергетикалық сипаттамаларын білу.
2. Кинетика және химиялық реакцияның механизмдері.
1.Химиялық реакциялардың энергетикалық сипаттамаларын білу.
2. Кинетика және химиялық реакцияның механизмдері.
3.Химиялық тепе-теңдік. Қайтымды және қайтымсыз химиялық реакцияларын пайдалану.
4.Тепе-теңдік күйі. Химиялық тепе-теңдікті сипаттауға арналған кинетикалық және термодинамикалық тәсілдерін қолдану.
Химиялық кинетика деп химиялық реакциялардың механизмдері жайлы ілімді айтады. Бұл
Химиялық кинетика деп химиялық реакциялардың механизмдері жайлы ілімді айтады. Бұл
Химиялық реакциялар жылдамдығы түрліше болуы мүмкін. Мысалы, қопарылыс секундтың мыңнан бір бөлігіндей мерзімде жүрсе, ал кейбір реакциялар бірнеше сағат, тәулік, жыл, ғасыр-лар бойына жүреді. Айталық, кәдімгі темір құрғақ ауада ұзақ уақыт таттанбайды. Ал енді осы темірдің бір бөлігін ылғалды ауада ұстаса бір тәулікте, суға салса бірер сағатта-ақ тотықтана-ды. Сол сияқты тау жыныстары мен топырақ құрамындағы реак-циялар ондаған жылдар бойында жүрсе антірацит, мұнай, газ, кө-мір сияқты заттар бірнеше ондаған, жүздеген ғасырлар бойында жүретін күрделі химиялық реакциялар нәтижесінде пайда болады.
Изохора-изотермиялық процесте (V = const, T = const) ▲V = 0 болғандықтан,
Изохора-изотермиялық процесте (V = const, T = const) ▲V = 0 болғандықтан,
▲Нх.р = ∑ ▲Н°түз. - ∑ ▲Н°түс. , түз. және түс. – түзілген, түскен заттар. анықталады, күй функциясы болады:
Qp = ▲H.
Изохора-изотермиялық процесте (V = const, T = const) ▲V = 0 болғандықтан,
Изохора-изотермиялық процесте (V = const, T = const) ▲V = 0 болғандықтан,
▲Нх.р = ∑ ▲Н°түз. - ∑ ▲Н°түс. , түз. және түс. – түзілген, түскен заттар.
Голландия химигі. 1871 жылы Делфт қаласында Политехникалық мектепті бітірген. Лейден және
Голландия химигі. 1871 жылы Делфт қаласында Политехникалық мектепті бітірген. Лейден және
Реакцияға түскіш бөлшектерді активтілер деп, энергетикалық барьерді (асуды) жоюға қажетті энергияны активтендіру энергиясы дейді.
Әрекеттесуші заттарды
Реакцияға түскіш бөлшектерді активтілер деп, энергетикалық барьерді (асуды) жоюға қажетті энергияны активтендіру энергиясы дейді.
Әрекеттесуші заттарды
Жылдамдық константасының активтендіру энергиясына тәуелділігі Аррениус теңдеуіменөрнектелінеді:
К=Z×P×e-Eа/RT
Z –соқтығысқан молекулалар саны әр секунд сайын;
е – натуральді логарифмнің негізі;
Р – бағытталған көбейткіш, молекуланың ыңғайлы орналасуын ескереді.
Оны кДж/кмоль мен өрнектейді. Активтелу энергиясының мәні молекула құрылысына және оның реакцияға түсетініне байланысты, басқа сөзбен айтқанда, әрбір химиялық реакцияның өзіне тән активтелу энергиясының мәні болады. Мысалы:
2НІ → Н2 + І2, Е =185,77
С2Н4 + Н2→ С2Н6 , Е =182,00
Н2 + І2→2НІ , Е=167,36
2NO2→2 NO + О2, Е =133,89
Молекулалардың активтелу энергиясын сыртқы факторлар әсерінен (температураны жоғарылату, жарық энергиясы, катализатор) төмендетуге болады.Активтелу энергиясы молекулаларда әртүрлі көрінеді. Олар қозғалады, атомдар молекулада жоғары энергиямен тербеледі.
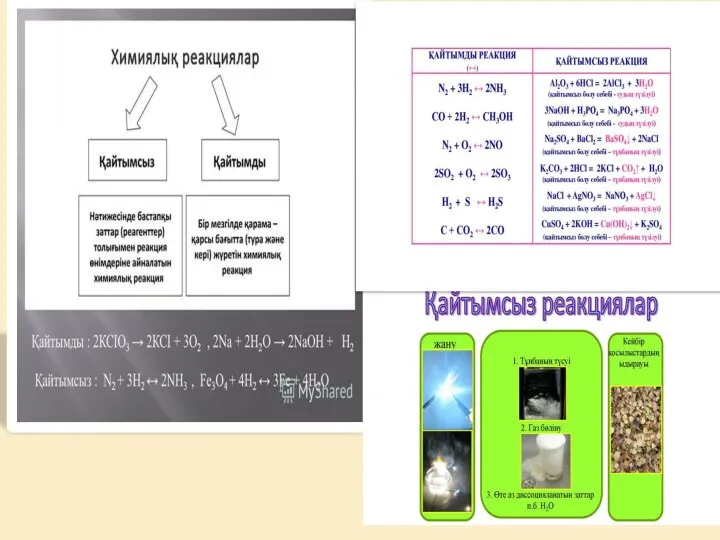
Химиялық тепе-теңдік — бір немесе бірнеше қарама-қарсы жүретін қайтымды реакциялар жылдамдықтарының
Химиялық тепе-теңдік — бір немесе бірнеше қарама-қарсы жүретін қайтымды реакциялар жылдамдықтарының
2КСІО3 → 2КСІ + 3О2, 2Na + 2H2O → 2NaOH + H2.
Химиялық реакция жүрген кезде алғашқы заттардың концентрациялары азаяды, олай болса, әрекеттесуші массалар заңы бойынша реакция жылдамдығы да азаяды. Егер реакция қайтымды болса, белгілі бір уақыт өткен соң кері реакцияның жылдамдығы арта бастайды, себебі реакция нәтижесінде пайда болған заттар концентрациялары артады.
.
Егер реакция қайтымды болса, белгілі бір уақыт өткен соң кері реакцияның
.
Егер реакция қайтымды болса, белгілі бір уақыт өткен соң кері реакцияның
u→ = k→ [A]a × [B]b; u ← = k ← [C]c × [▲]▲ тепе-теңдік кезінде u→ = u ← , олай болса,
k→ [A]a × [B]b = k ← [C]c × [▲]▲ сонда, k→ /k ← = К т – реакцияның тепе-теңдік константасы болады. Тепе-теңдік константасына кіретін концентрацияларды тепе-теңдік концентрациялары деп атайды. Сонымен, тепе-теңдік константасы сол температурада тұрақты шама, реакция нәтижесінде түзілген заттардың тепе-теңдік концентрациялары көбейтіндісінің реакцияға түскен заттардың тепе-теңдік концентрациялары көбейтіндісіне қатынасын көрсетеді:
К т = [C]c × [▲]▲ /[A]a × [B]b
Тепе-теңдік константасы – реакцияның маңызды сипаттамасы, оның мәні көп болған сайын, реакция ↔тереңірек» жүреді, яғни реакция нәтижесінде түзілген заттардың шығымы жоғары болады. Гетерогенді реакциялар үшін тепе-теңдік константасы мәніне де қатты заттардың концентрациясы кірмейді, реакциялар жылдамдығы мәніне кірмеген сияқты. Химиялық тепе-теңдік кезінде реакциялар тоқтамайды, тек қарама-қарсы реакциялардың жылдамдықтары теңеседі, уақыт бірлігінде түзілген заттар молекулаларының саны реакцияға түскен заттар молекулалары санына тең болады.Олай болса, химиялық тепе-теңдік динамикалық, жылжымалы болады.Тепе-теңдік константасы реакцияласатын заттар табиғатына және температураға тәуелді, ал концентрацияларына тәуелді емес.








 Алкины. Химические свойства и способы получения алкинов
Алкины. Химические свойства и способы получения алкинов Индикаторы окислительно-восстановительного титрования и их применение в анализе лекарственных препаратов
Индикаторы окислительно-восстановительного титрования и их применение в анализе лекарственных препаратов Диаграмма состояния Железо – Углерод. Материаловедение. Лекция 2
Диаграмма состояния Железо – Углерод. Материаловедение. Лекция 2 Правила техники безопасности при работе в кабинете химии
Правила техники безопасности при работе в кабинете химии Титан. Хром
Титан. Хром Основные разделы химии
Основные разделы химии Субстраты и продукты биохимических реакций
Субстраты и продукты биохимических реакций Хромотография, явления, атомы и молекулы. 8 класс
Хромотография, явления, атомы и молекулы. 8 класс Дистиляттағы цианидтер, алифаттық қатардағы галоген туындылары, хлороформ, хлоралгидрат, төртхлорлы көміртек
Дистиляттағы цианидтер, алифаттық қатардағы галоген туындылары, хлороформ, хлоралгидрат, төртхлорлы көміртек Ионная хроматография
Ионная хроматография Валентность химических элементов. 8 класс
Валентность химических элементов. 8 класс Щелочные металлы. 9 класс
Щелочные металлы. 9 класс История органической химии. Характерные особенности органических соединений
История органической химии. Характерные особенности органических соединений Асфальтены в тяжелых нефтях и битумах. Химическое строение и влияние на свойства
Асфальтены в тяжелых нефтях и битумах. Химическое строение и влияние на свойства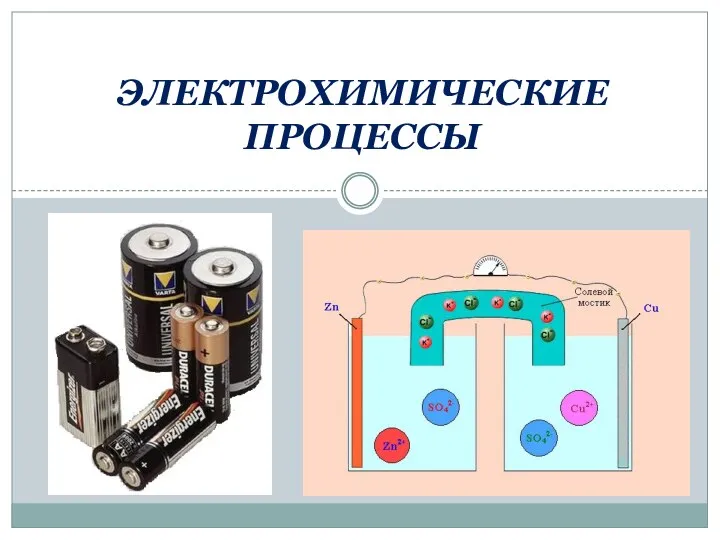 Электрохимические процессы
Электрохимические процессы Alkynes
Alkynes Новые требования к оценке опасности, паспортам безопасности и маркировке химической продукции
Новые требования к оценке опасности, паспортам безопасности и маркировке химической продукции Вуглеводні. Підсумковий урок 9 клас
Вуглеводні. Підсумковий урок 9 клас Теория возникновения электродных и ОВ-потенциалов
Теория возникновения электродных и ОВ-потенциалов Аммиак
Аммиак Урок химии по теме Бериллий, магний и щелочноземельные металлы,9 класс
Урок химии по теме Бериллий, магний и щелочноземельные металлы,9 класс Химические свойства кислот
Химические свойства кислот Взаємодія кисеню зі складними речовинами
Взаємодія кисеню зі складними речовинами Розрахунки за хімічними рівняннями
Розрахунки за хімічними рівняннями Химическая промышленность. 9 класс
Химическая промышленность. 9 класс Наноструктурные и нанокристаллические материалы
Наноструктурные и нанокристаллические материалы Железо. Строение атома, физические и химические свойства простого вещества
Железо. Строение атома, физические и химические свойства простого вещества Влияние этилового спирта на организм детей
Влияние этилового спирта на организм детей