Содержание
- 2. Тест №1. Выберите правильный ответ. 1. Электронная формула внешнего энергетического уровня атома углерода соответствует: 1)…2S22P2; 2)…
- 4. Из меня состоит все живое: Я - графит, антрацит и алмаз. Я на улице, в школе
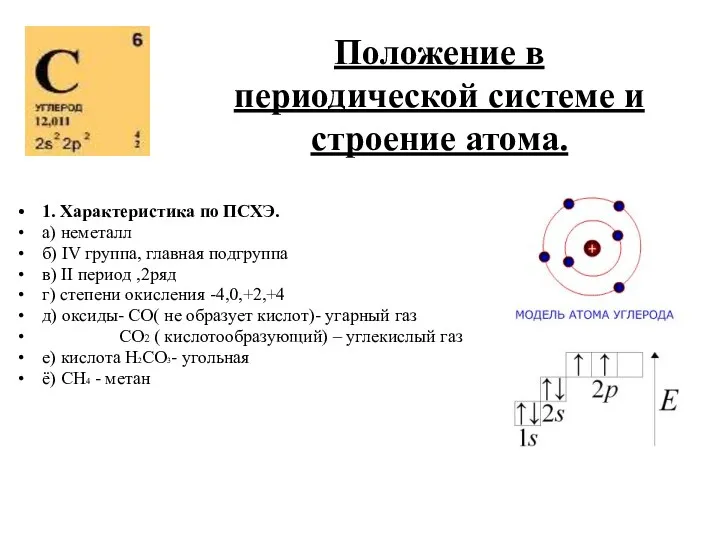
- 5. Положение в периодической системе и строение атома. 1. Характеристика по ПСХЭ. а) неметалл б) IV группа,
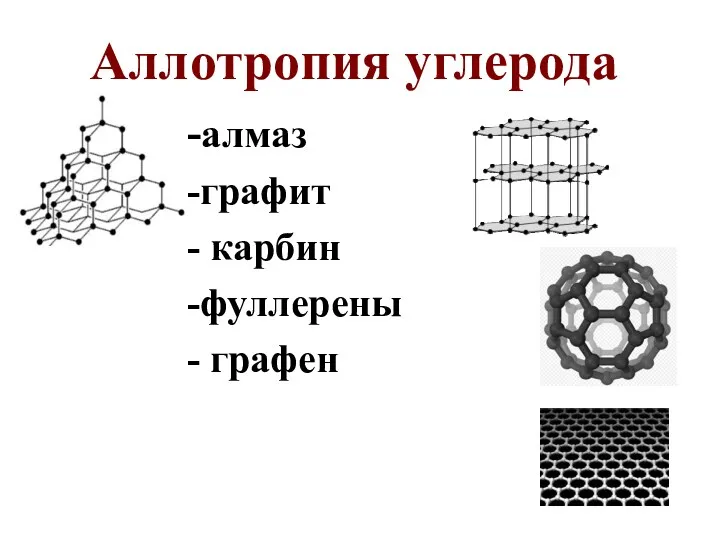
- 6. Аллотропия углерода -алмаз -графит - карбин -фуллерены - графен
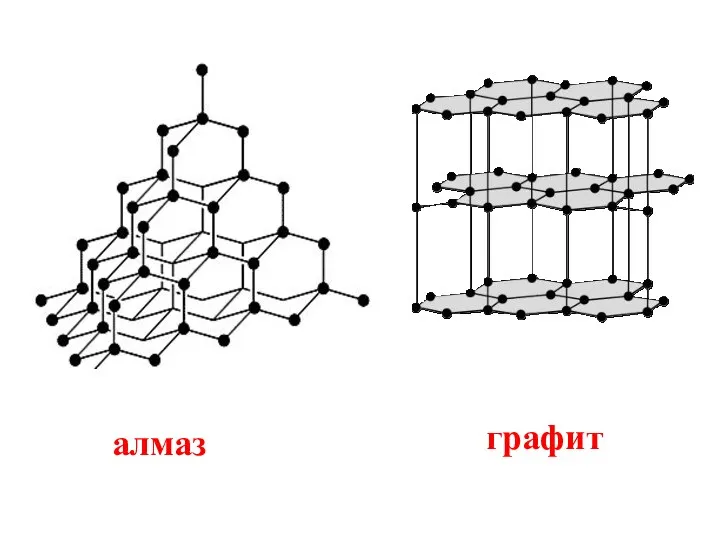
- 7. алмаз графит
- 8. Алмаз Прозрачный кристаллический Тугоплавкий Очень твердый Не проводит электрический ток Высокая светоотражаемость Графит Темно-серый кристалический Тугоплавкий
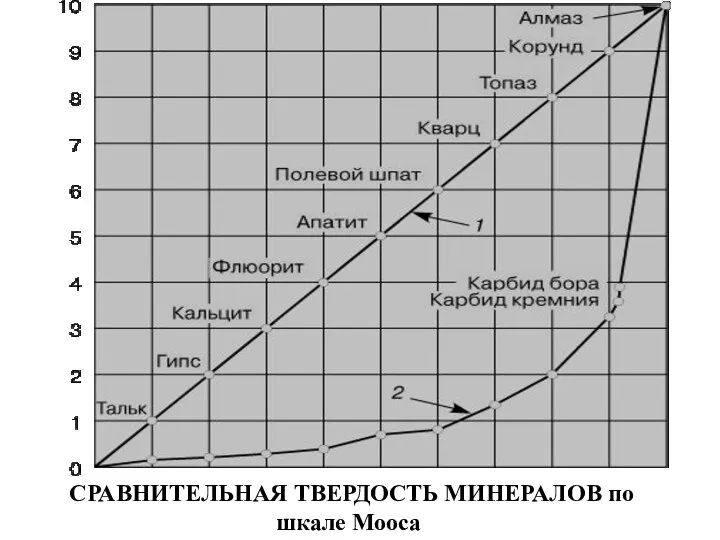
- 9. СРАВНИТЕЛЬНАЯ ТВЕРДОСТЬ МИНЕРАЛОВ по шкале Мооса
- 10. Применение алмазов.
- 11. Применение графита. электроды нагреватели
- 12. электроды В каких изделиях использован графит, а в каких алмаз?
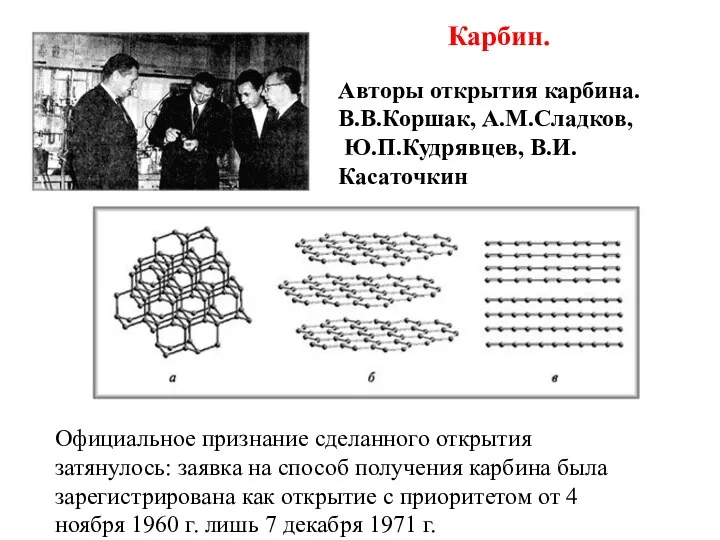
- 13. Авторы открытия карбина. В.В.Коршак, А.М.Сладков, Ю.П.Кудрявцев, В.И.Касаточкин Официальное признание сделанного открытия затянулось: заявка на способ получения
- 14. Фуллерены 1985 год - Ричард Смэлли, Роберт Керл и Гарольд Крото открыли фуллерены. Впервые сумели измерить
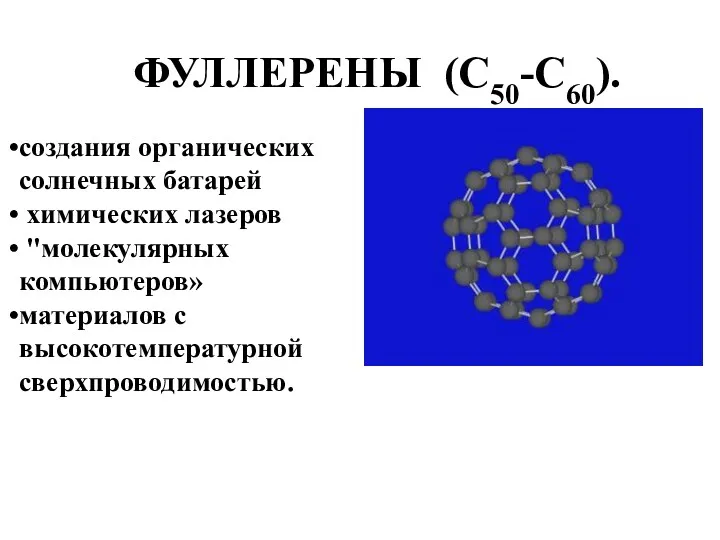
- 15. ФУЛЛЕРЕНЫ (С50-С60). создания органических солнечных батарей химических лазеров "молекулярных компьютеров» материалов с высокотемпературной сверхпроводимостью.
- 16. ДВАДЦАТИЭТАЖНЫЙ ГЕОДЕЗИЧЕСКИЙ КУПОЛ из стали и пластмасс на всемирной выставке в Монреале (1967).
- 18. Количества материала весом всего несколько граммов достаточно для того, чтобы покрыть футбольное поле
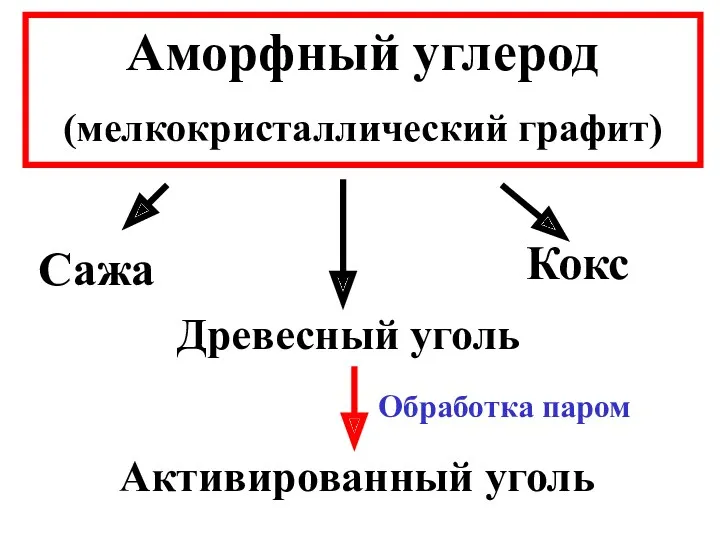
- 19. Аморфный углерод (мелкокристаллический графит) Сажа Кокс Древесный уголь Активированный уголь Обработка паром
- 20. Что вы знаете об активированном угле?
- 21. АДСОРБЦИЯ – способность твердого вещества поглощать газы и растворенные вещества.
- 23. Зелинский Николай Дмитриевич
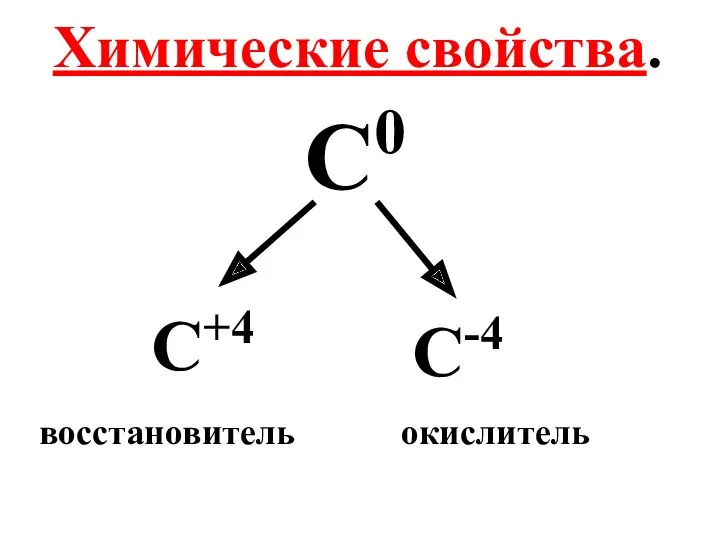
- 24. Химические свойства. С0 С+4 С-4 восстановитель окислитель
- 25. C+2H2→CH4 ( метан) Как изменяется степень окисления углерода в этих реакциях? Какие свойства проявляет углерод? 3C+4Al→Al4C3
- 26. Al4C3 + 12H2O → 4Al(OH)3 + 3CH4↑ CaC2 – карбид кальция CaC2 + 2H2O → Ca(OH)2
- 27. C+O2→CO2 Как изменяется степень окисления углерода в этих реакциях? Как называются продукты этих реакций? 2C+O2→2CO
- 28. ЗАДАЧА. Известно, что легковой автомобиль загрязняет воздух выбросами, на каждые 10 км пути с его выхлопами
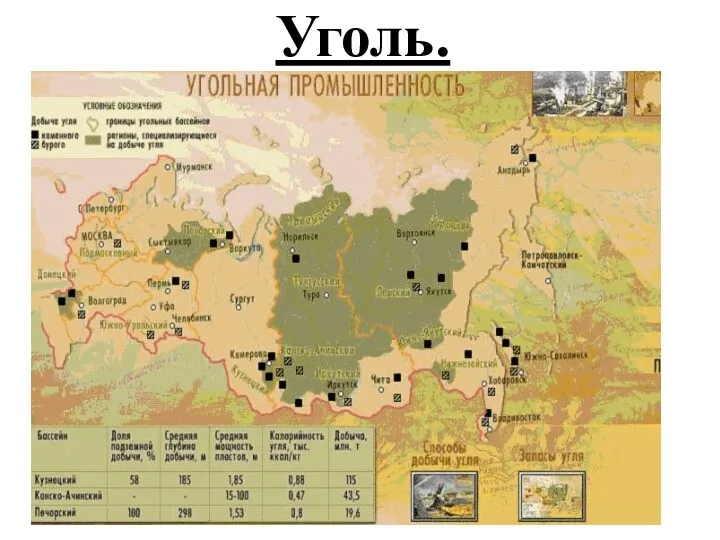
- 29. Уголь.
- 30. Нефть.
- 32. Тест № 2. Выберите правильный ответ. 1. Углерод в химических реакциях может быть: 1) только окислителем;
- 34. Скачать презентацию

















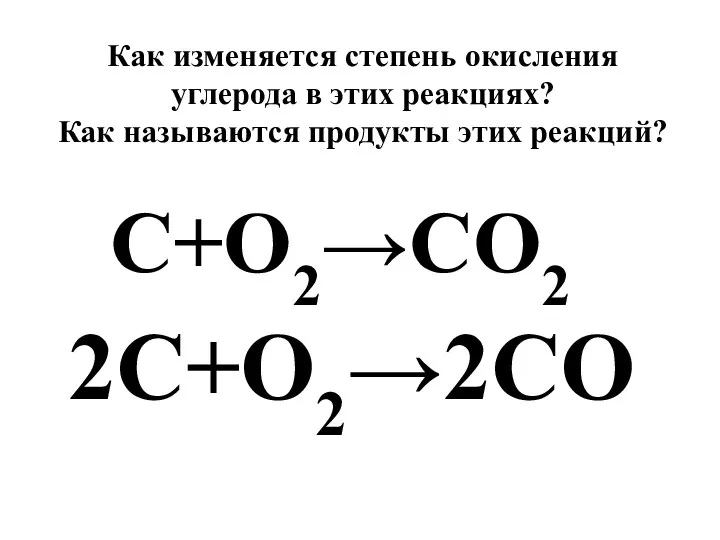



 Соляная кислота и её соли
Соляная кислота и её соли Растворы
Растворы Органическая химия. Этапы развития органической химии
Органическая химия. Этапы развития органической химии Поверхностные явления. Адсорбция
Поверхностные явления. Адсорбция Минеральные удобрения
Минеральные удобрения Химическая связь
Химическая связь Альдегіди і кетони аліфатичного ряду. Альдегіди і кетони ароматичного ряду
Альдегіди і кетони аліфатичного ряду. Альдегіди і кетони ароматичного ряду Фенол и его свойства
Фенол и его свойства Тема 1. Обработка вооружения, техники и обмундирования. Дегазирующие, дезактивирующие и дезинфицирующие вещества и растворы
Тема 1. Обработка вооружения, техники и обмундирования. Дегазирующие, дезактивирующие и дезинфицирующие вещества и растворы Соединения химических элементов
Соединения химических элементов Решение задач по теме: «Электролиз»
Решение задач по теме: «Электролиз» Химическая посуда и ее значение (1)
Химическая посуда и ее значение (1) Классификация неорганических веществ
Классификация неорганических веществ Углерод, как химический элемент и простое вещество
Углерод, как химический элемент и простое вещество АТФ Аденозинтрифосфат
АТФ Аденозинтрифосфат Оксиды, свойства и способы получения
Оксиды, свойства и способы получения Общие сведения о месторождениях полезных ископаемых
Общие сведения о месторождениях полезных ископаемых Золото Au (Аурум)
Золото Au (Аурум) Применение уксусной кислоты
Применение уксусной кислоты Определение качественного состава минеральных вод
Определение качественного состава минеральных вод Химическое равновесие. Азот и Фосфор. 9 класс
Химическое равновесие. Азот и Фосфор. 9 класс Корбонаттар көмір қышқылынның тұздары
Корбонаттар көмір қышқылынның тұздары Химическая промышленность
Химическая промышленность Алюминий. Строение
Алюминий. Строение Свойства металлов
Свойства металлов Коррозия металлов
Коррозия металлов Механизм реакции
Механизм реакции Основные виды химических связей
Основные виды химических связей