Содержание
- 2. План 1. Понятие об углеводах. Классификация. 2. Моносахариды 3. Олигосахариды (дисахариды) 5. Полисахариды 2
- 3. Углеводы - обширный класс природных соединений, которые играют важную роль в жизни человека, животных и растений
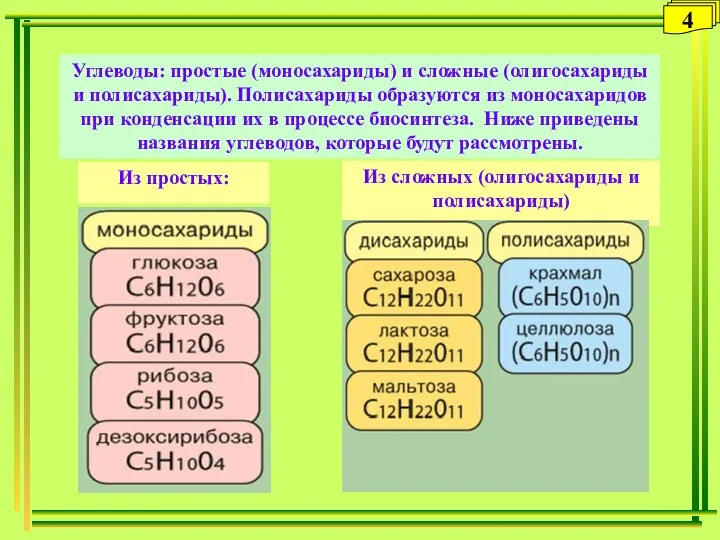
- 4. Углеводы: простые (моносахариды) и сложные (олигосахариды и полисахариды). Полисахариды образуются из моносахаридов при конденсации их в
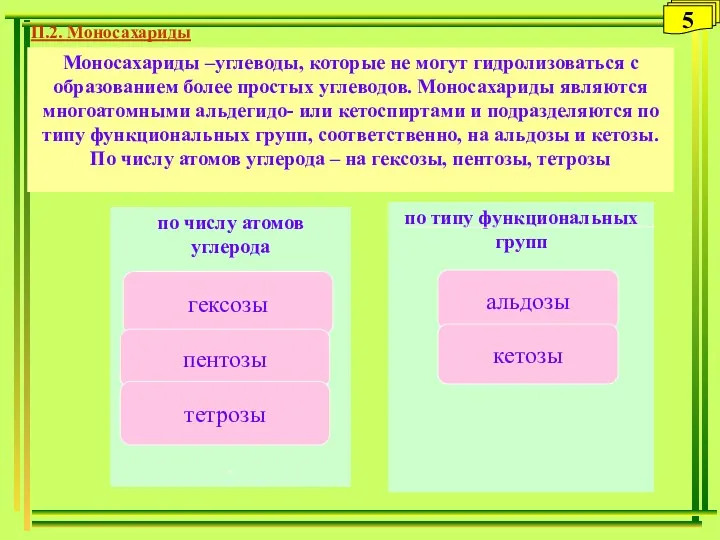
- 5. Моносахариды –углеводы, которые не могут гидролизоваться с образованием более простых углеводов. Моносахариды являются многоатомными альдегидо- или
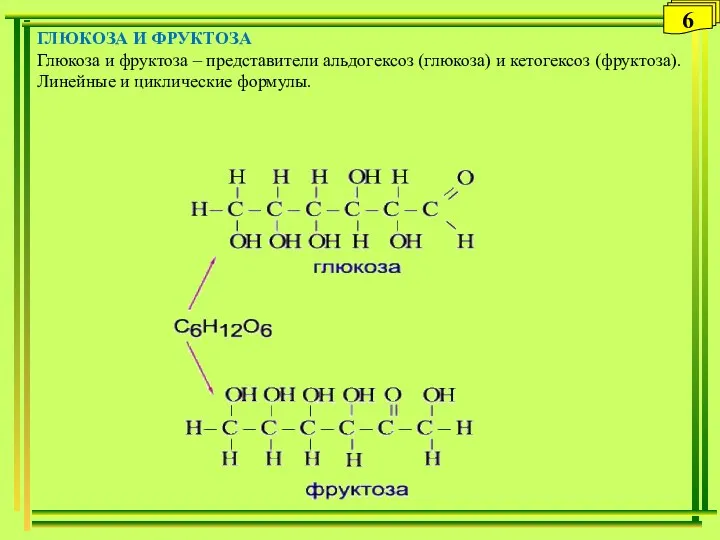
- 6. ГЛЮКОЗА И ФРУКТОЗА Глюкоза и фруктоза – представители альдогексоз (глюкоза) и кетогексоз (фруктоза). Линейные и циклические
- 7. Пространственная изомерия Изомеры - вещества, имеющие один и тот же качественный и количественный состав молекулы (брутто-формулу),
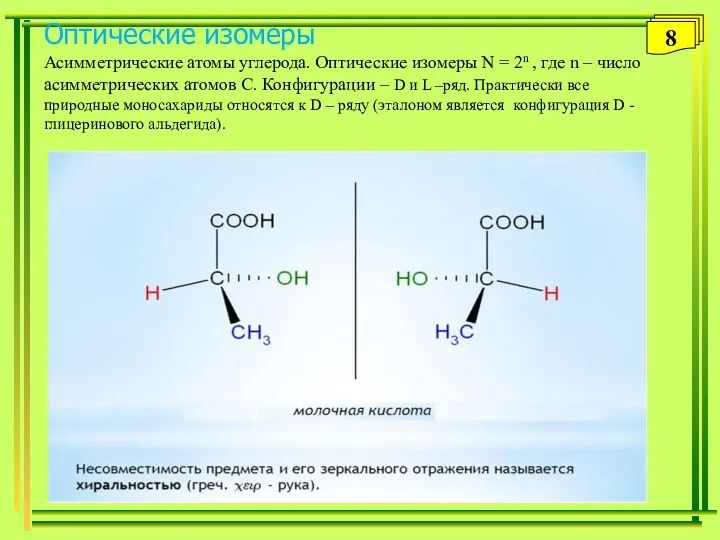
- 8. Оптические изомеры Асимметрические атомы углерода. Оптические изомеры N = 2n , где n – число асимметрических
- 9. 9
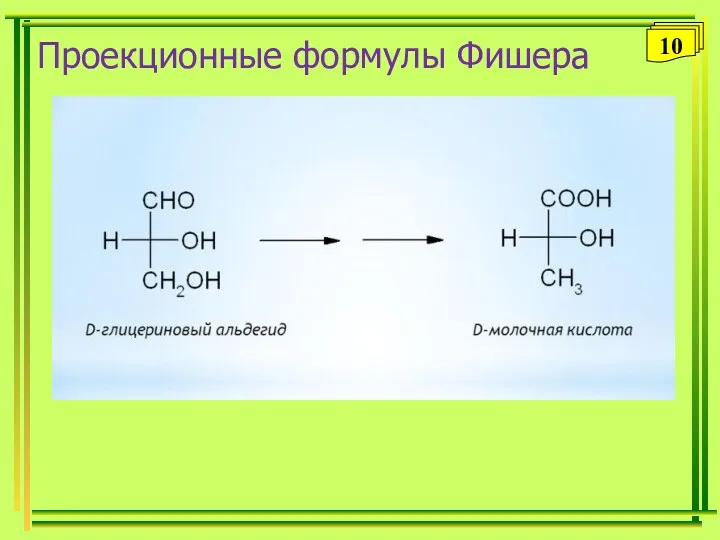
- 10. Проекционные формулы Фишера 10
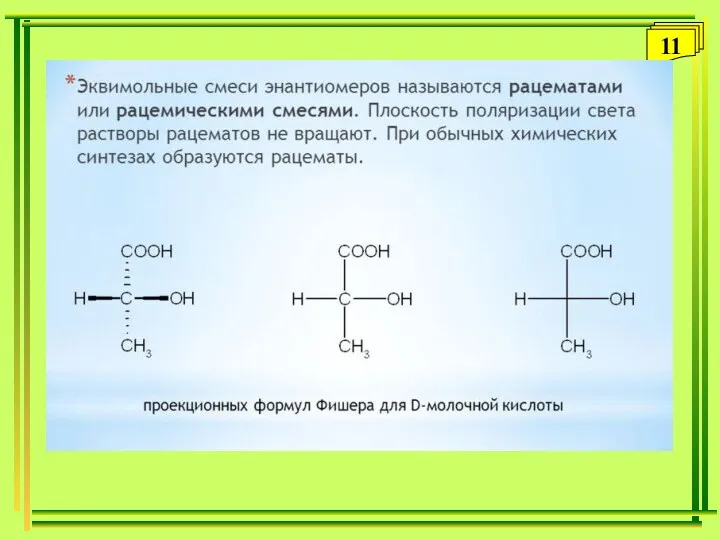
- 11. 11
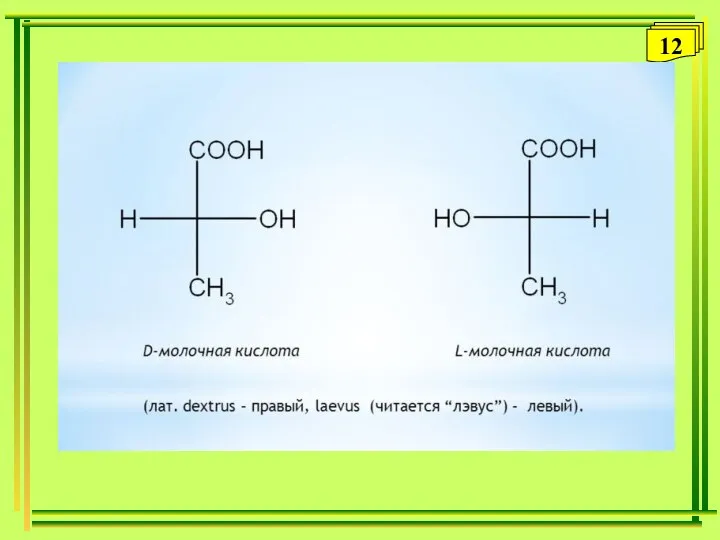
- 12. 12
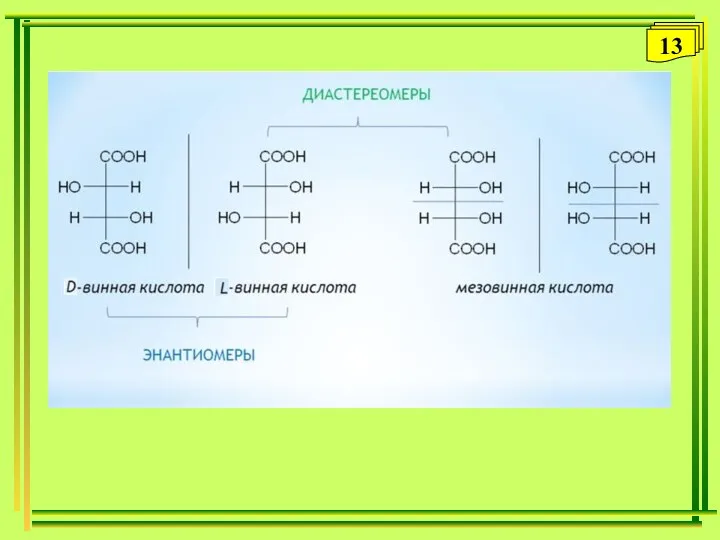
- 13. 13
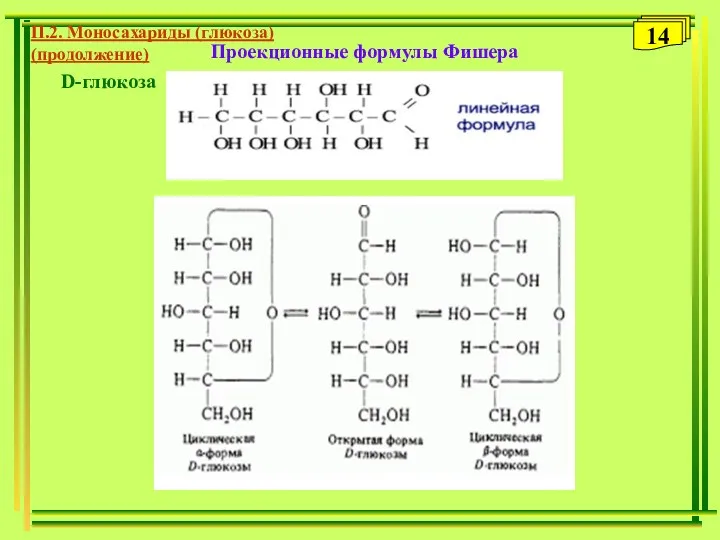
- 14. Проекционные формулы Фишера П.2. Моносахариды (глюкоза) (продолжение) 14 D-глюкоза
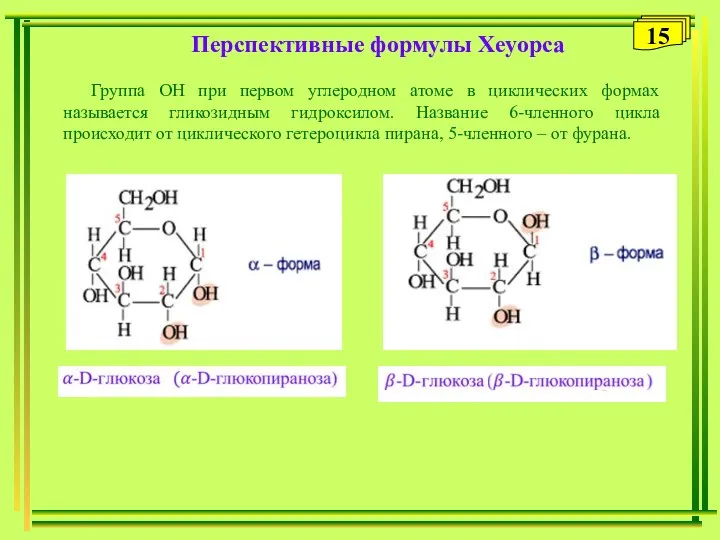
- 15. Перспективные формулы Хеуорса 15 Группа ОН при первом углеродном атоме в циклических формах называется гликозидным гидроксилом.
- 16. Моносахариды – бифункциональные соединения, поэтому их химические свойства обусловлены наличием как карбонильных (в линейной форме), так
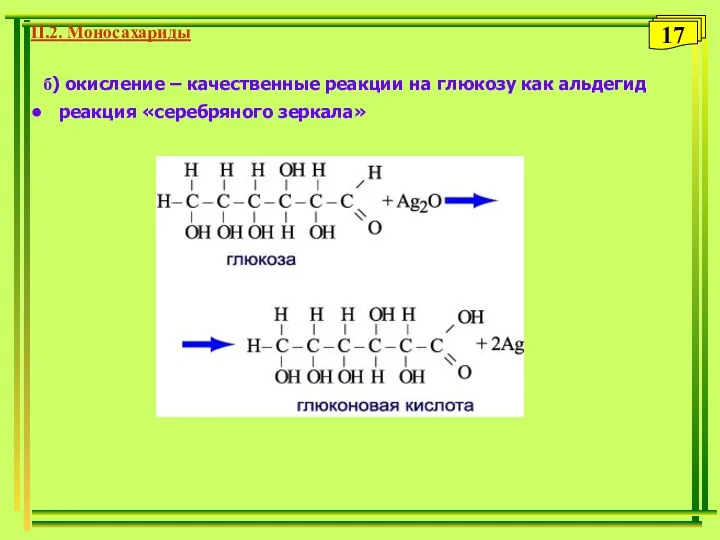
- 17. б) окисление – качественные реакции на глюкозу как альдегид реакция «серебряного зеркала» П.2. Моносахариды 17
- 18. реакция с гидроксидом меди (II) Cu(OH)2 , при температуре образуется красно-бурый осадок. 18
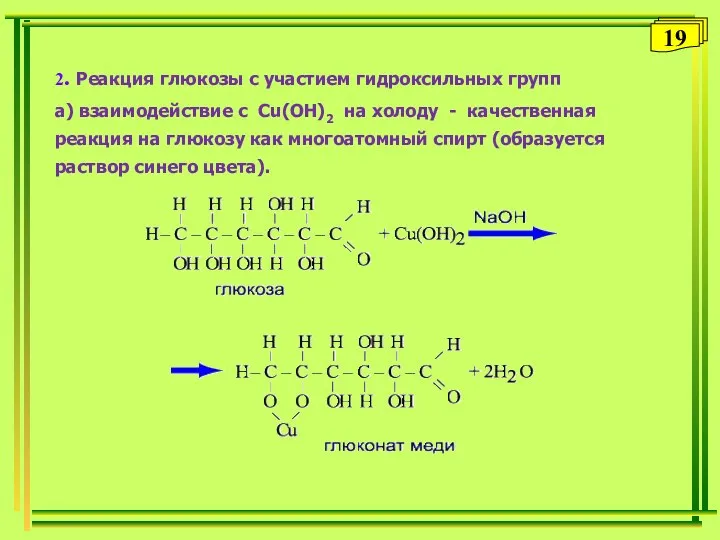
- 19. 2. Реакция глюкозы с участием гидроксильных групп а) взаимодействие с Cu(OH)2 на холоду - качественная реакция
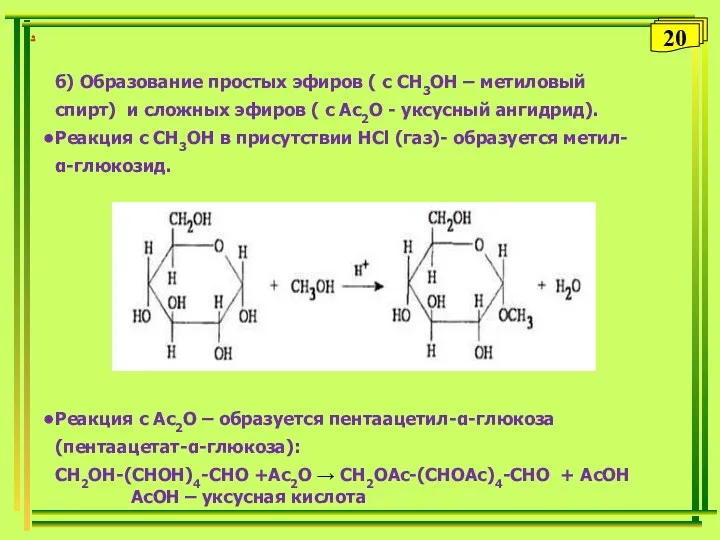
- 20. б) Образование простых эфиров ( с СН3ОH – метиловый спирт) и сложных эфиров ( с Ac2O
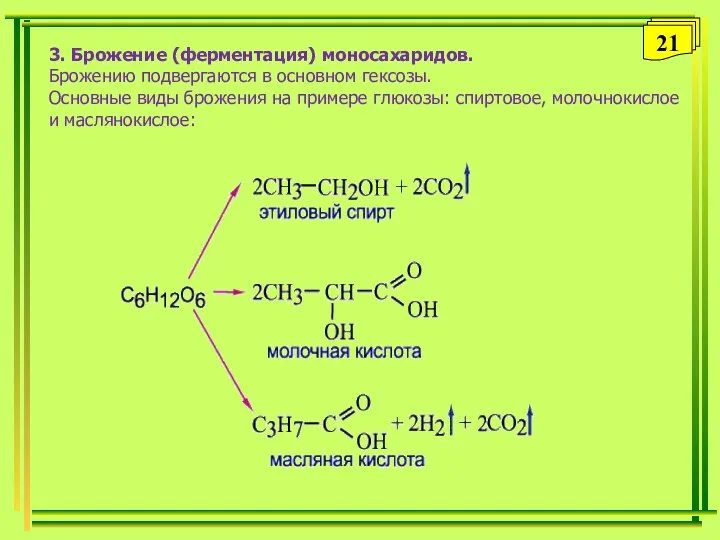
- 21. 3. Брожение (ферментация) моносахаридов. Брожению подвергаются в основном гексозы. Основные виды брожения на примере глюкозы: спиртовое,
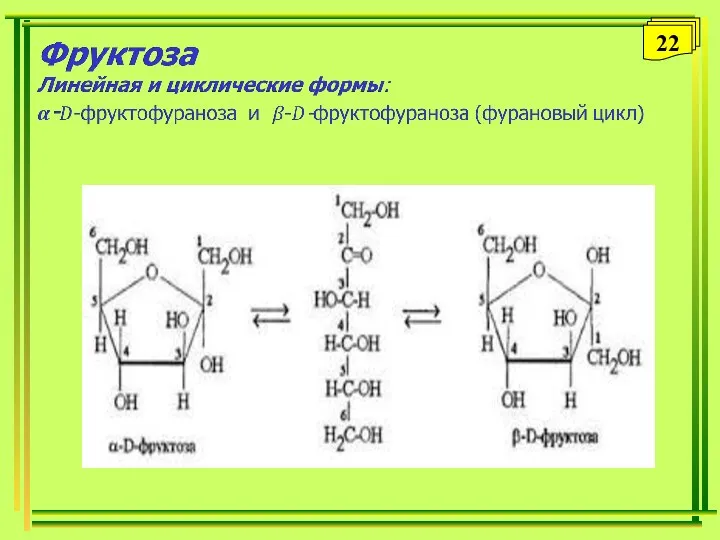
- 22. 22
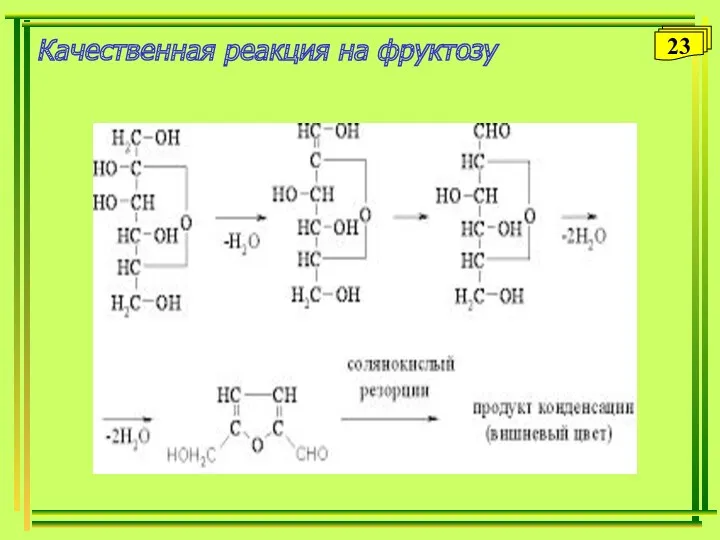
- 23. Качественная реакция на фруктозу 23
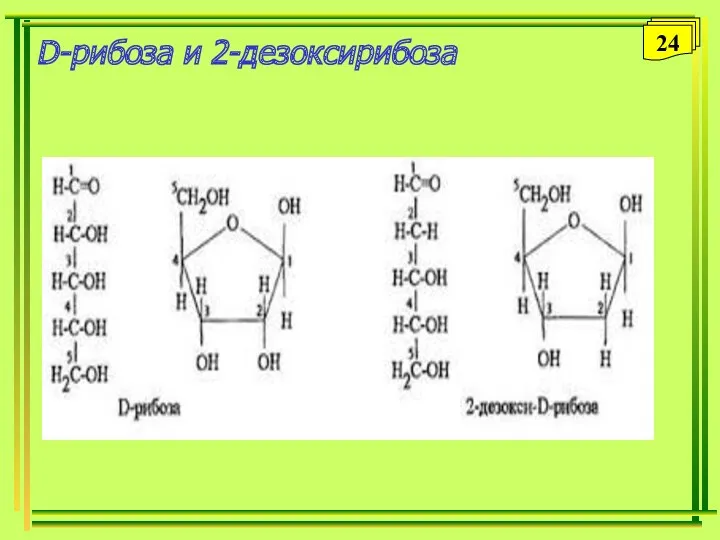
- 24. D-рибоза и 2-дезоксирибоза 24
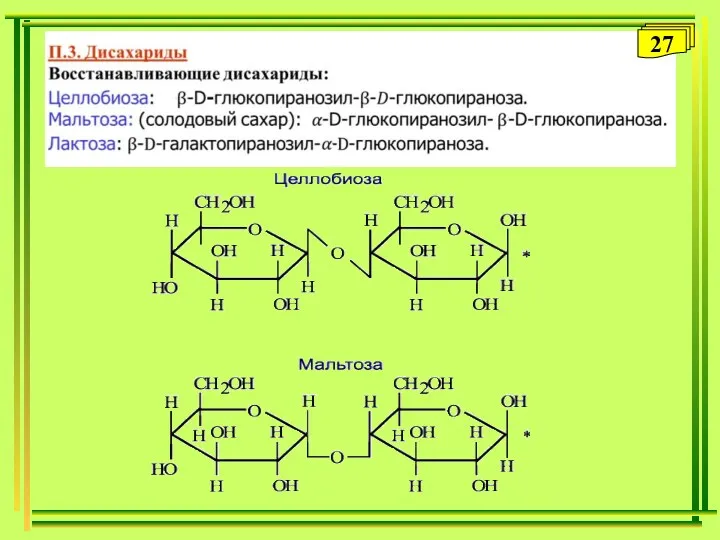
- 25. П.3. Дисахариды 25
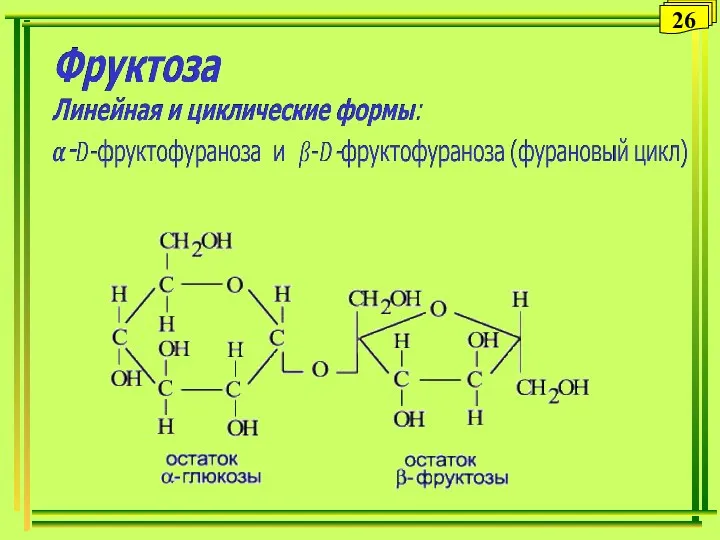
- 26. 26
- 27. 27
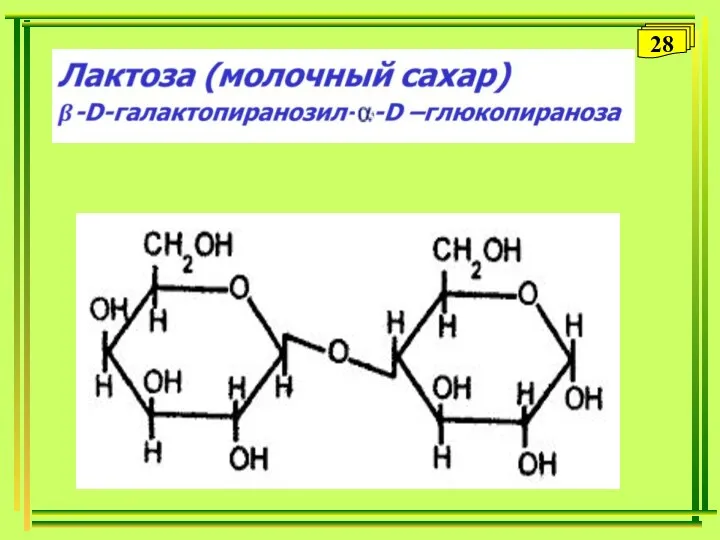
- 28. 28
- 29. Химические свойства дисахаридов Дисахариды, в молекулах которых сохраняется полуацетальный гидроксил (мальтоза, лактоза, целлобиоза) – восстанавливающие –
- 30. 3. Гидролиз 2. Все дисахариды являются многоатомными спиртами, для них характерны свойства многоатомных спиртов, они дают
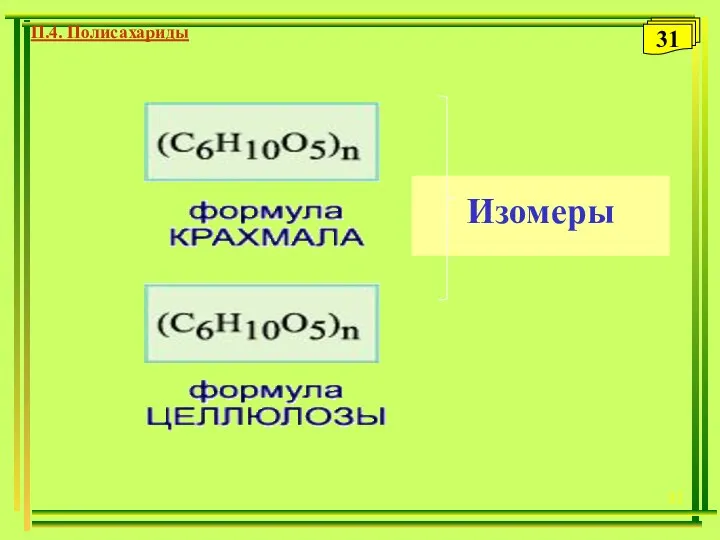
- 31. П.4. Полисахариды Изомеры 31
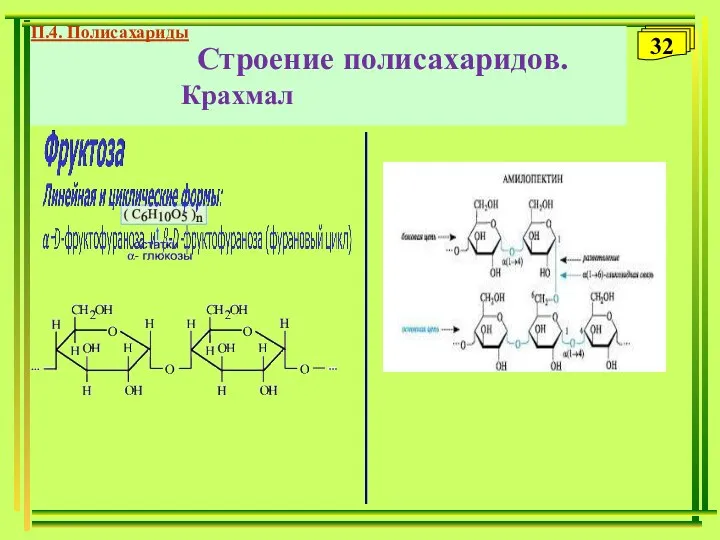
- 32. Строение полисахаридов. Крахмал П.4. Полисахариды 32
- 33. Химические свойства крахмала П.4. Полисахариды 1. Гидролиз 2. Качественная реакция на крахмал (С6Н10О5)n + I2 комплексное
- 34. 3. Горение: 4. Термическое разложение без доступа воздуха: (С6Н10О5)n древесный уголь + Н2О + летучие органические
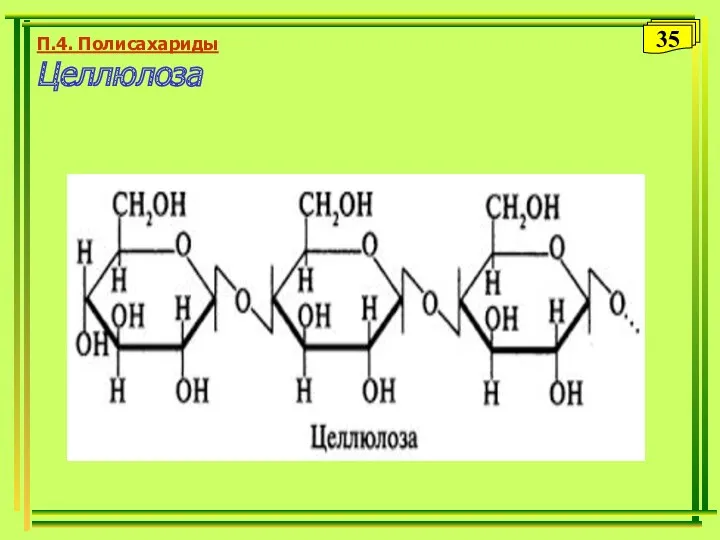
- 35. П.4. Полисахариды Целлюлоза 35
- 37. Скачать презентацию











 Топливо и топливосжигающие устройства
Топливо и топливосжигающие устройства большая стирка
большая стирка Бытовая химия. Правила безопасного обращения со средствами бытовой химии
Бытовая химия. Правила безопасного обращения со средствами бытовой химии Redox reactions
Redox reactions Железо. Fe (лат. Феррум)
Железо. Fe (лат. Феррум) Фармацевтическая химия натрия гидрокарбоната
Фармацевтическая химия натрия гидрокарбоната Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады) Диссоциация воды. Водородный и гидроксильный показатели (рН и рОН)
Диссоциация воды. Водородный и гидроксильный показатели (рН и рОН) Теоретические аспекты химического осаждения из газовой фазы
Теоретические аспекты химического осаждения из газовой фазы Занимательные опыты
Занимательные опыты Валентність. Хімія. 7 клас
Валентність. Хімія. 7 клас Химические уравнения. Типы химических реакций. А что такое химическая реакция?
Химические уравнения. Типы химических реакций. А что такое химическая реакция? Электронные конфигурации атомов
Электронные конфигурации атомов Общая характеристика неметаллов
Общая характеристика неметаллов Кремний и его соединения
Кремний и его соединения Химия нефти и газа
Химия нефти и газа яжелые металлы полезны или вредны?
яжелые металлы полезны или вредны? Metal–metal multiple bonded intermediates in catalysis
Metal–metal multiple bonded intermediates in catalysis Закон сохранения массы веществ
Закон сохранения массы веществ Методические проблемы преподавания органической химии и ее основные теоретические понятия
Методические проблемы преподавания органической химии и ее основные теоретические понятия Щелочноземельные металлы
Щелочноземельные металлы Значення хімії у повсякденному житті
Значення хімії у повсякденному житті Неорганические строительные материалы. Стекло
Неорганические строительные материалы. Стекло Теория растворов электролитов и неэлектролитов
Теория растворов электролитов и неэлектролитов Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Кремний и его соединения
Кремний и его соединения Химическая связь и ее типы
Химическая связь и ее типы Превращение веществ
Превращение веществ