Содержание
- 2. Эти нежелательные явления могут быть устранены путем: наиболее рационального выбора состава пластмассы, удаления вредных примесей, регулирования
- 3. Реакции ингибированного окисления InH – молекула ингибитора
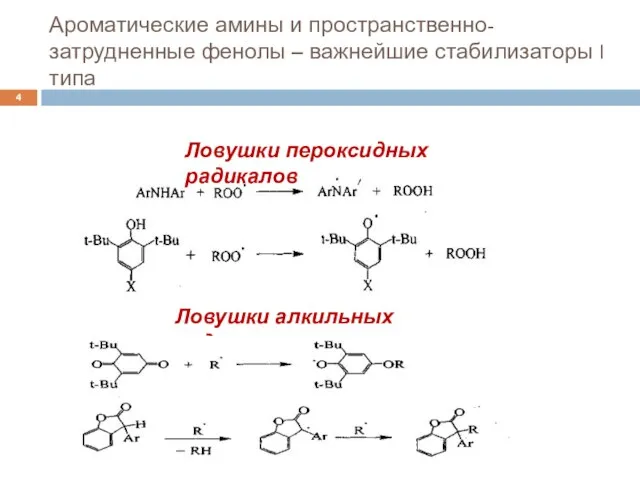
- 4. Ароматические амины и пространственно-затрудненные фенолы – важнейшие стабилизаторы I типа Ловушки пероксидных радикалов Ловушки алкильных радикалов
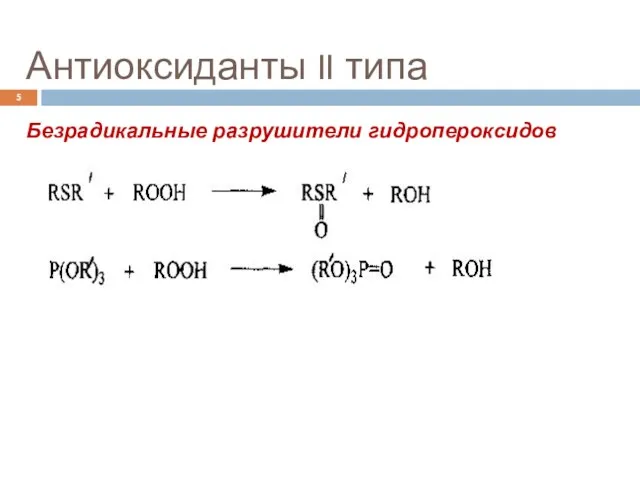
- 5. Антиоксиданты II типа Безрадикальные разрушители гидропероксидов
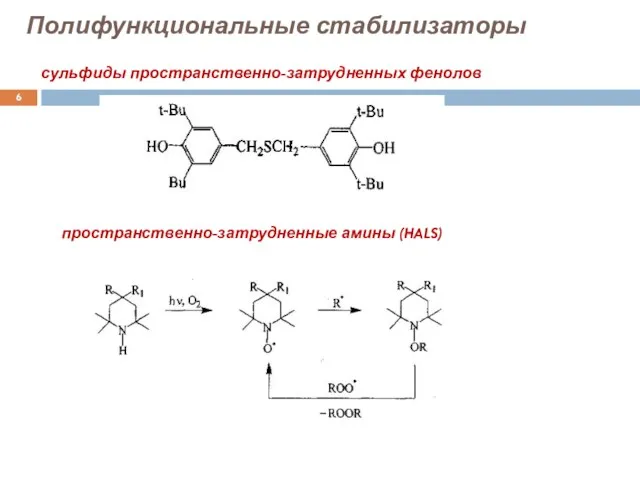
- 6. Полифункциональные стабилизаторы пространственно-затрудненные амины (HALS) сульфиды пространственно-затрудненных фенолов
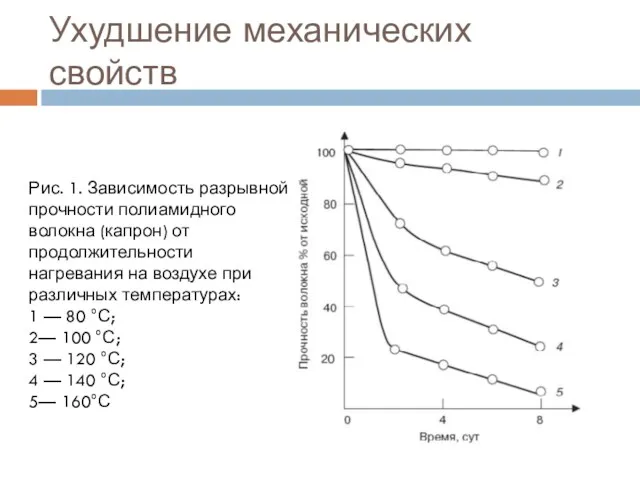
- 7. Ухудшение механических свойств Рис. 1. Зависимость разрывной прочности полиамидного волокна (капрон) от продолжительности нагревания на воздухе
- 8. Термоокислительной деструкцией называют разрушение макромолекул при одновременном воздействии тепла и кислорода. Условия, при которых возможно окисление:
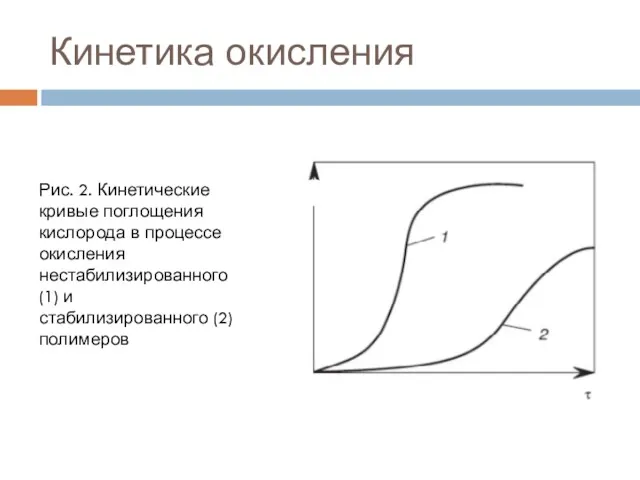
- 9. Кинетика окисления Рис. 2. Кинетические кривые поглощения кислорода в процессе окисления нестабилизированного (1) и стабилизированного (2)
- 10. Стадии процесса окисления 1) Инициирование кинетических цепей 2) Продолжение кинетической цепи 3) Разветвление кинетической цепи 4)
- 11. Инициирование кинетических цепей Процесс зарождения кинетических цепей происходит но следующей схеме: RH + O2 → R∙
- 12. Продолжение цепи Эта стадия включает в себя чередующиеся реакции: 1) R∙ + O2 → RO2∙ 2)
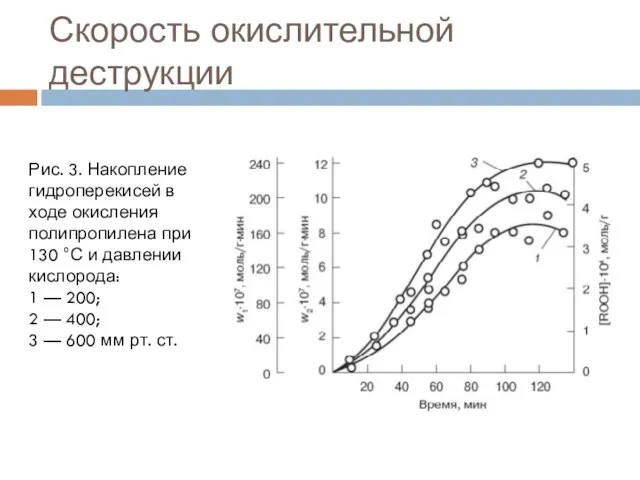
- 13. Скорость окислительной деструкции Рис. 3. Накопление гидроперекисей в ходе окисления полипропилена при 130 °С и давлении
- 14. Разветвление кинетической цепи ROOH → RO∙ + ∙OH (I) ROOH + RH → RO∙ + H2O
- 15. Обрыв кинетической цепи Уравнения скорости поглощения кислорода полимеров: - для квадратичного обрыва цепи - для линейного
- 16. Принципы стабилизации полимеров В процессе переработки в готовые изделия полимеры подвергаются воздействию высоких температур и значительных
- 17. Термостабилизаторы 1) Акцепотры низкомолекулярных продуктов деструкции (HCl, H2O, CH2O и др.) 2) Акцепторы свободных радикалов а)
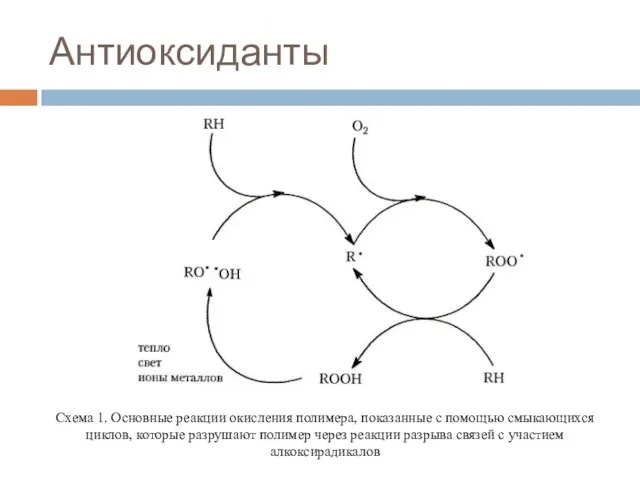
- 18. Антиоксиданты Схема 1. Основные реакции окисления полимера, показанные с помощью смыкающихся циклов, которые разрушают полимер через
- 19. Ароматические ингибиторы В качестве ингибиторов можно использовать: Фенолы, нафтолы, ароматические амины, аминофенолы, диамины ROO∙ + InH
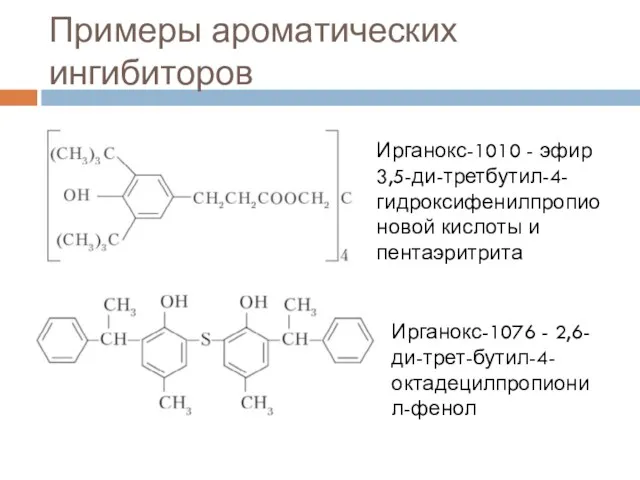
- 20. Примеры ароматических ингибиторов Ирганокс-1010 - эфир 3,5-ди-третбутил-4-гидроксифенилпропионовой кислоты и пентаэритрита Ирганокс-1076 - 2,6-ди-трет-бутил-4-октадецилпропионил-фенол
- 21. Стабилизаторы, разрушающие инициаторы
- 22. Примеры стабилизаторов, разрушающих инициаторы Бис-(2-окси-5-метил-3-третбутилфенил)-сульфид Бис-[2-окси-5-метил-3-α-метнлбензил)-фенил]-сульфид
- 23. Эффективность стабилизаторов в полимерах зависит от ряда факторов, таких, как влияние полимера на реакционную способность стабилизатора,
- 24. Формулы расхода антиоксиданта и концентрации активных центров n - концентрация активных центров n - расход антиоксиданта
- 25. Критическая концентрация антиоксиданта Если фактор автокатализа больше kx, окисление ускоряется; если меньше окисление протекает с постоянной
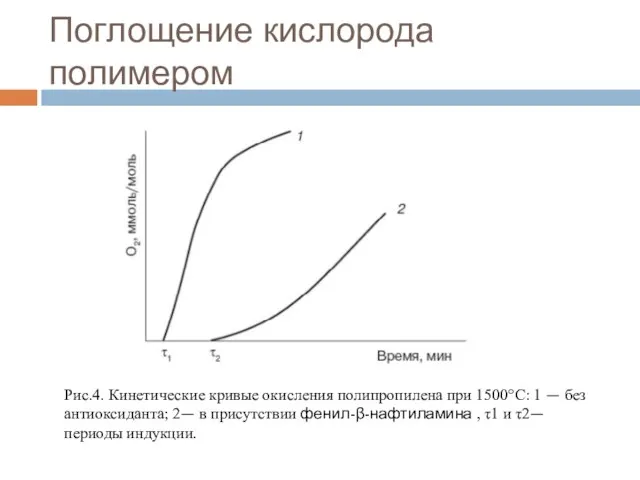
- 26. Поглощение кислорода полимером Рис.4. Кинетические кривые окисления полипропилена при 1500°С: 1 — без антиоксиданта; 2— в
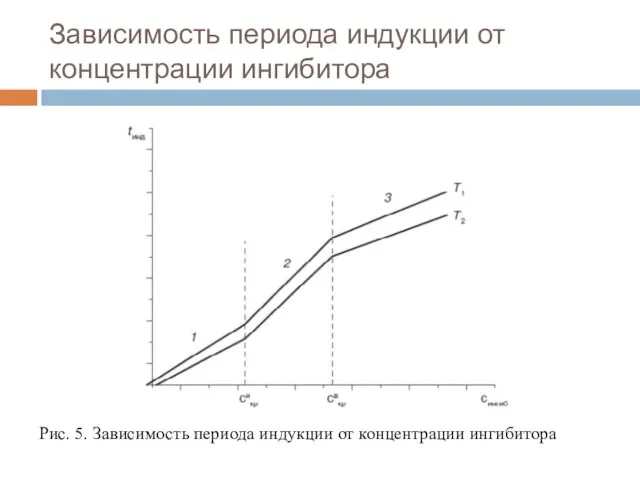
- 27. Зависимость периода индукции от концентрации ингибитора Рис. 5. Зависимость периода индукции от концентрации ингибитора
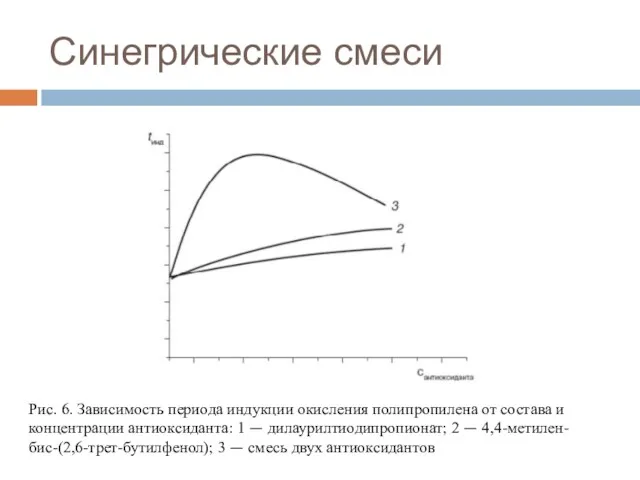
- 28. Синегрические смеси Рис. 6. Зависимость периода индукции окисления полипропилена от состава и концентрации антиоксиданта: 1 —
- 30. Скачать презентацию












![Примеры стабилизаторов, разрушающих инициаторы Бис-(2-окси-5-метил-3-третбутилфенил)-сульфид Бис-[2-окси-5-метил-3-α-метнлбензил)-фенил]-сульфид](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/429320/slide-21.jpg)



 Фосфор и его соединения
Фосфор и его соединения Химиялық байланыс және заттардың құрылымдық түрлі сатылары
Химиялық байланыс және заттардың құрылымдық түрлі сатылары Дистилляция и ректификация
Дистилляция и ректификация Металлы и их соединения
Металлы и их соединения Оксиды. Классификация, номенклатура, свойства оксидов, получение, применение
Оксиды. Классификация, номенклатура, свойства оксидов, получение, применение Кислородосодержащие производные углеводородов. Спирты. Фенолы. Простые эфиры
Кислородосодержащие производные углеводородов. Спирты. Фенолы. Простые эфиры Углеводы
Углеводы Металлическая связь
Металлическая связь Карбоновые кислоты. (Лекция 6.3)
Карбоновые кислоты. (Лекция 6.3) Стирка по научному
Стирка по научному Углеводы (особенности строения, реакционной способности и методы синтеза альдегидо- и кетоспиртов)
Углеводы (особенности строения, реакционной способности и методы синтеза альдегидо- и кетоспиртов) Спирты. Классификация, номенклатура, изомерия спиртов
Спирты. Классификация, номенклатура, изомерия спиртов Строение атома
Строение атома Углеводы, монозы, биозы. Лекция 15
Углеводы, монозы, биозы. Лекция 15 Атом – сложная частица
Атом – сложная частица Элементы пятой-А группы. Азот и фосфор
Элементы пятой-А группы. Азот и фосфор Идеальные и реальные кристаллы
Идеальные и реальные кристаллы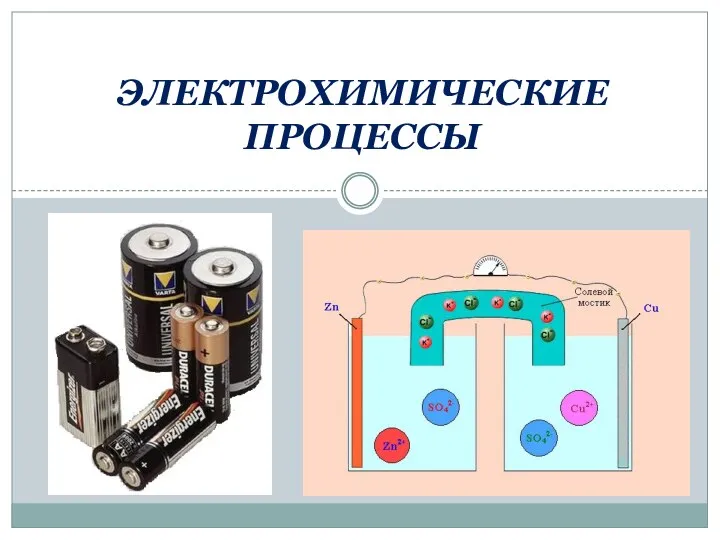 Электрохимические процессы
Электрохимические процессы Ядерное топливо
Ядерное топливо Кислород. Оксиды. Валентность
Кислород. Оксиды. Валентность Палладий. История открытия химических веществ
Палладий. История открытия химических веществ Качественные реакции
Качественные реакции 20230219_prezentatsiya_k_uroku_neft
20230219_prezentatsiya_k_uroku_neft Аминокислоты, как структурные компоненты белков
Аминокислоты, как структурные компоненты белков Степень окисления. Составление химических формул бинарных соединений
Степень окисления. Составление химических формул бинарных соединений Основи. Фізичні властивості основ
Основи. Фізичні властивості основ Внеклассное мероприятие по химии. 9 класс
Внеклассное мероприятие по химии. 9 класс Водород. Характеристика положения водорода в ПСХЭ, строение атома и молекулы (8 класс)
Водород. Характеристика положения водорода в ПСХЭ, строение атома и молекулы (8 класс)