Содержание
- 2. План лекции Принципы метода Основные узлы жидкостных хроматографов Сорбенты для ВЭЖХ Наиболее распространенные виды современной ВЭЖХ
- 3. Подвижная фаза – жидкость Неподвижная фаза – твердое вещество Часто присутствуют одновременно несколько механизмов. При классификации
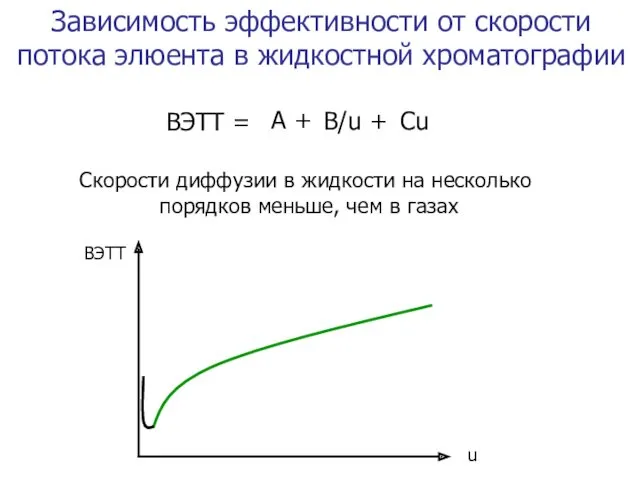
- 4. ВЭТТ = A + B/u + Cu Зависимость эффективности от скорости потока элюента в жидкостной хроматографии
- 5. Высокоэффективная жидкостная хроматография (ВЭЖХ или HPLC) – современные (преимущественно колоночные) варианты жидкостной хроматографии с целью обеспечения
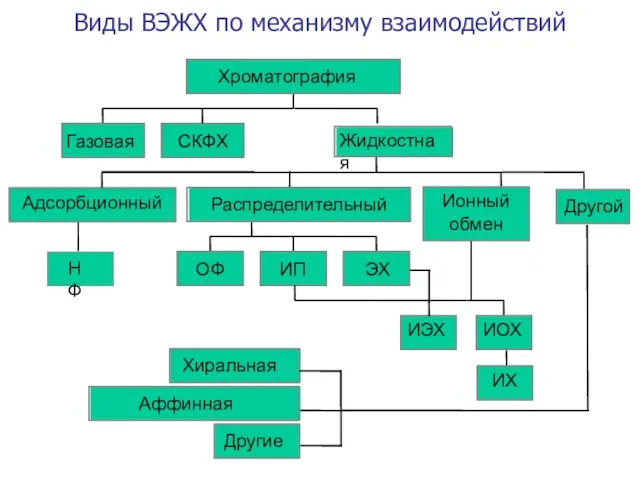
- 6. Виды ВЭЖХ по механизму взаимодействий
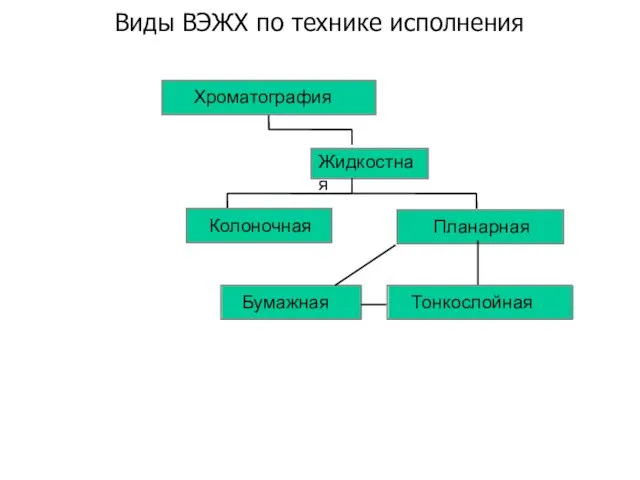
- 7. Виды ВЭЖХ по технике исполнения Хроматография
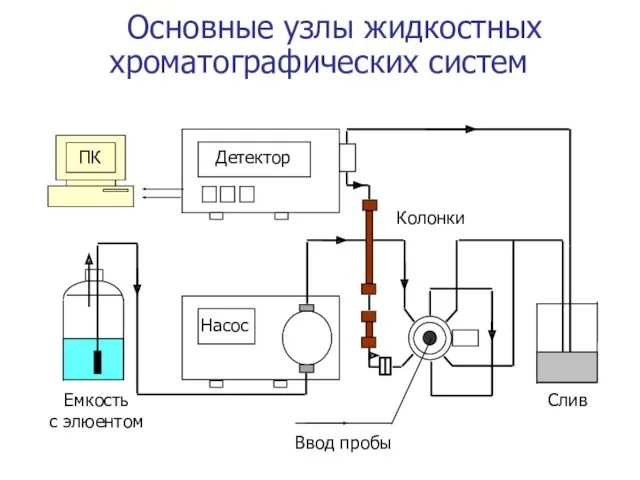
- 8. Основные узлы жидкостных хроматографических систем
- 9. Требования к подвижной фазе Смачивать сорбент, но не взаимодействовать с ним химически Растворять вещества пробы Не
- 10. Элюирующая сила растворителей Способность растворителей элюировать компоненты пробы характеризуется элюирующей силой. Расположение растворителей в порядке увеличения
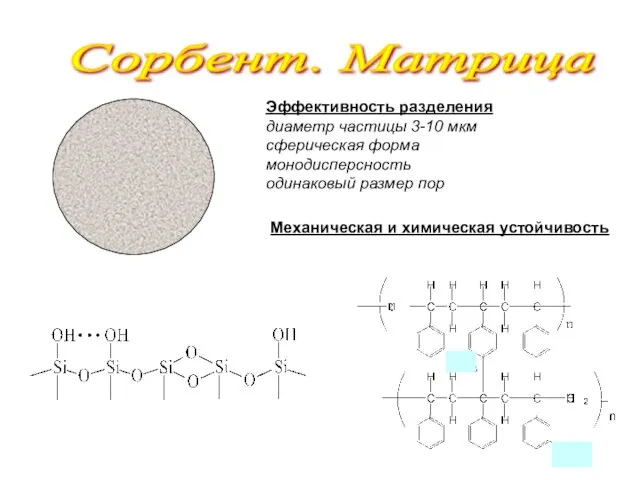
- 11. Сорбент. Матрица Эффективность разделения диаметр частицы 3-10 мкм сферическая форма монодисперсность одинаковый размер пор Механическая и
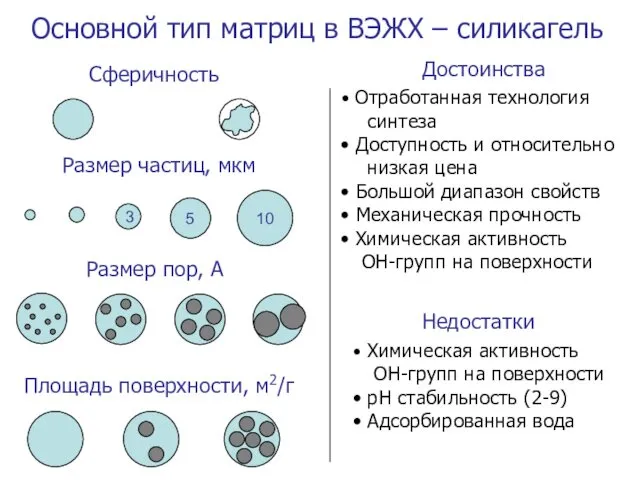
- 12. Основной тип матриц в ВЭЖХ – силикагель Достоинства Недостатки Отработанная технология синтеза Доступность и относительно низкая
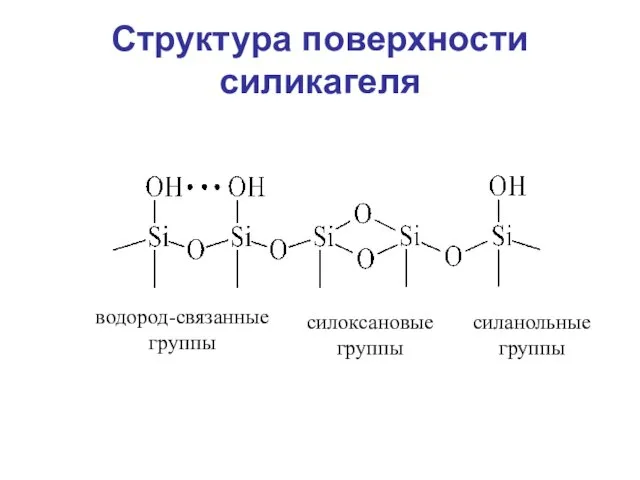
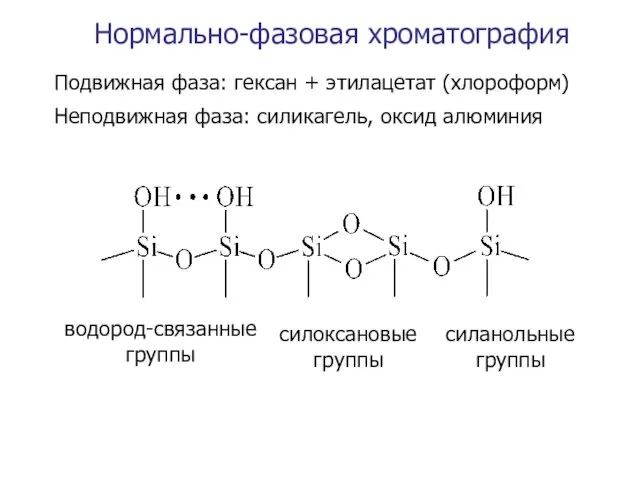
- 13. Структура поверхности силикагеля водород-связанные группы силоксановые группы силанольные группы
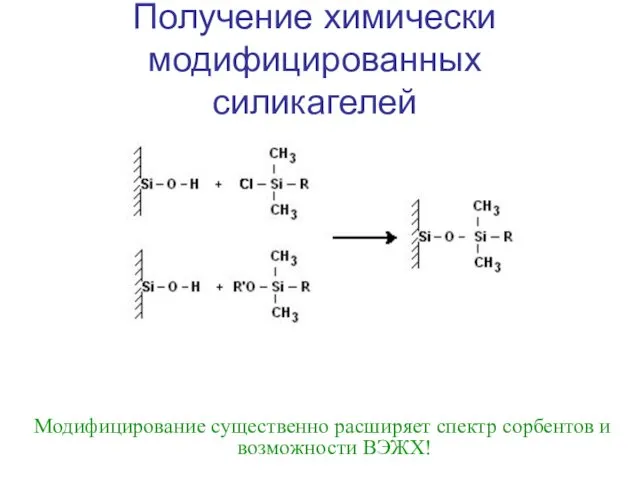
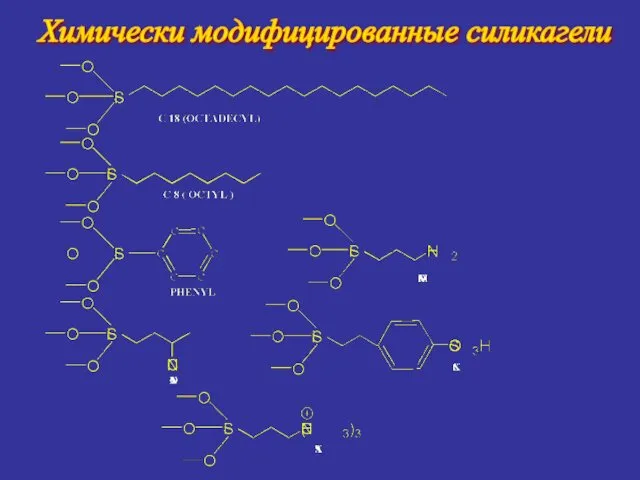
- 14. Получение химически модифицированных силикагелей Модифицирование существенно расширяет спектр сорбентов и возможности ВЭЖХ!
- 15. Химически модифицированные силикагели
- 16. Рекомендации по применению химически модифицированных силикагелей
- 17. Рекомендации по применению химически модифицированных силикагелей
- 18. Силикагель Сорбенты для ВЭЖХ Недостатки: Структура поверхности зависит от условий синтеза (термообработка, промывка кислотными и щелочными
- 19. Основные виды ВЭЖХ Нормально-фазовая Обращенно-фазовая Гидрофильная Ион-парная Эксклюзионная Ультра-ВЭЖХ
- 20. Нормально-фазовая хроматография
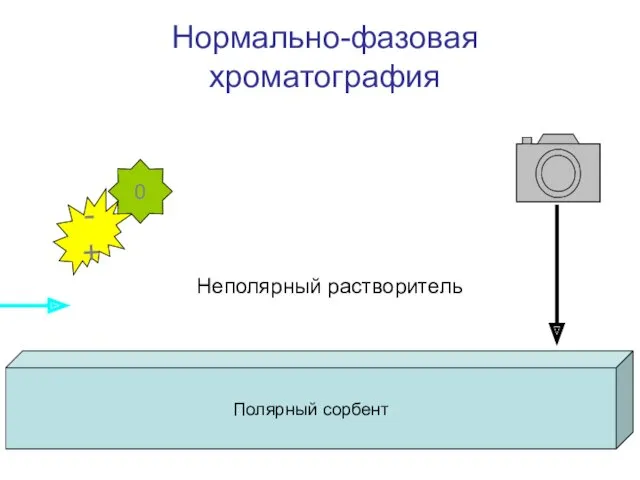
- 21. Нормально-фазовая хроматография Полярный сорбент - + 0 Неполярный растворитель
- 22. Подвижная фаза: гексан + этилацетат (хлороформ) Неподвижная фаза: силикагель, оксид алюминия Нормально-фазовая хроматография
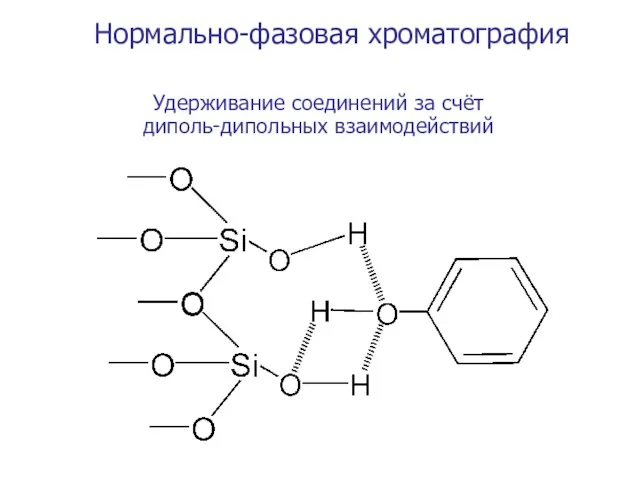
- 23. Нормально-фазовая хроматография Удерживание соединений за счёт диполь-дипольных взаимодействий
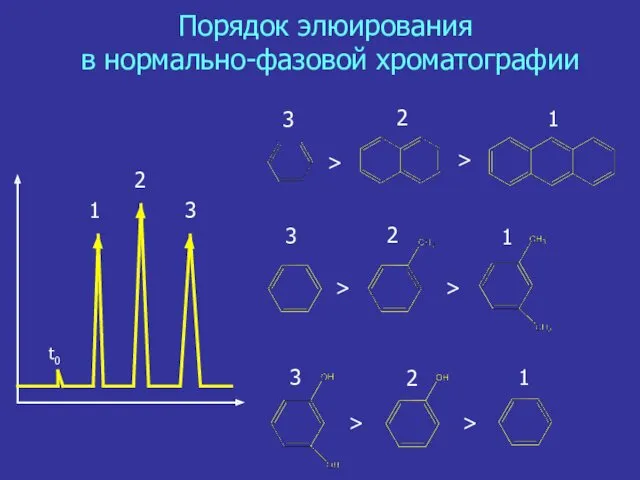
- 24. Закономерности удерживания Полярные соединения удерживаются сильнее, чем неполярные Гомологи, (вещества, различающиеся различным количеством метиленовых звеньев), разделяются
- 25. Порядок элюирования в нормально-фазовой хроматографии
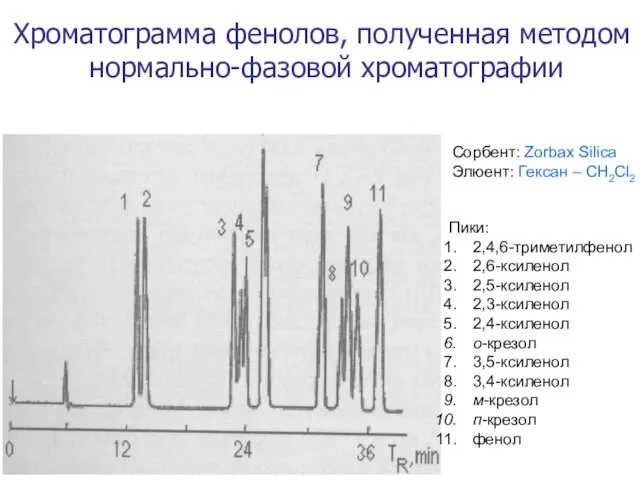
- 26. Хроматограмма фенолов, полученная методом нормально-фазовой хроматографии Сорбент: Zorbax Silica Элюент: Гексан – CH2Cl2 Пики: 2,4,6-триметилфенол 2,6-ксиленол
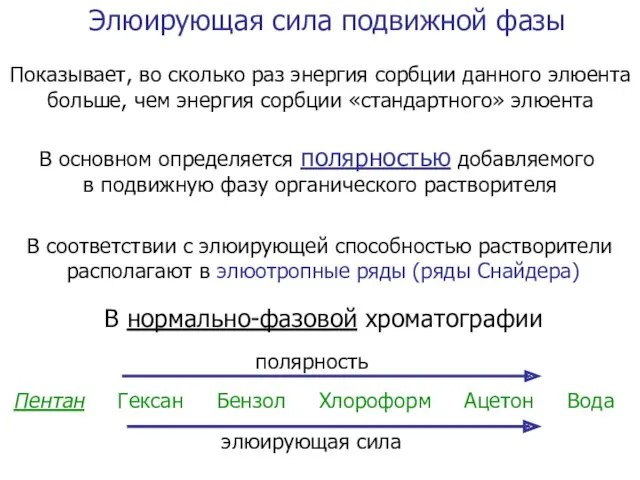
- 27. Элюирующая сила подвижной фазы Показывает, во сколько раз энергия сорбции данного элюента больше, чем энергия сорбции
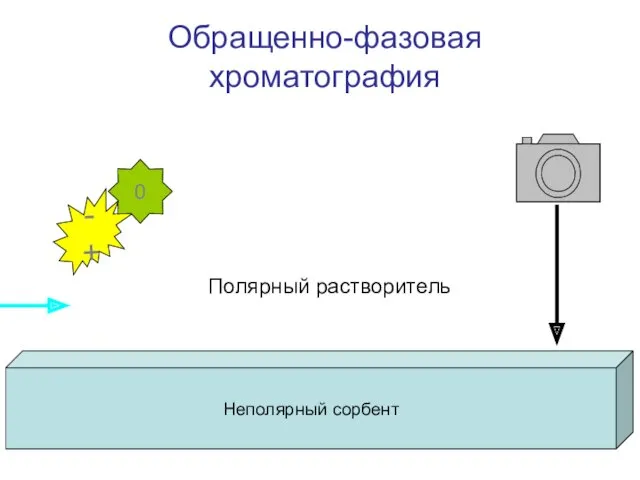
- 28. Обращенно-фазовая хроматография
- 29. Обращенно-фазовая хроматография Неполярный сорбент - + 0 Полярный растворитель
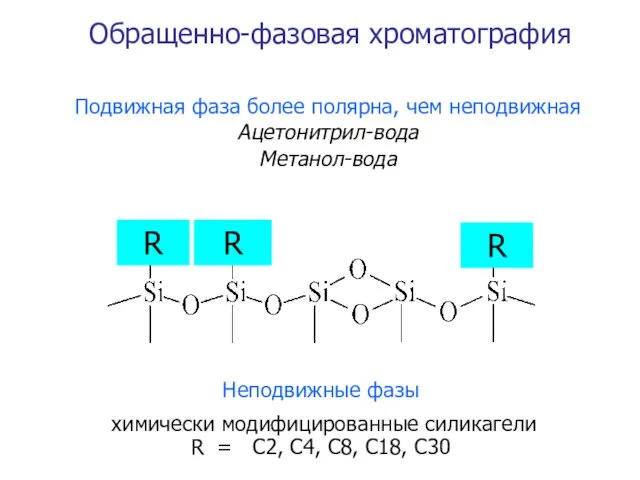
- 30. Подвижная фаза более полярна, чем неподвижная Ацетонитрил-вода Метанол-вода Неподвижные фазы химически модифицированные силикагели R = С2,
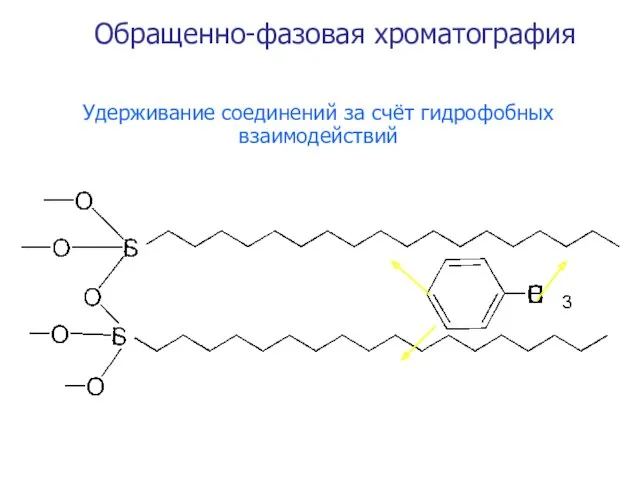
- 31. Удерживание соединений за счёт гидрофобных взаимодействий Обращенно-фазовая хроматография
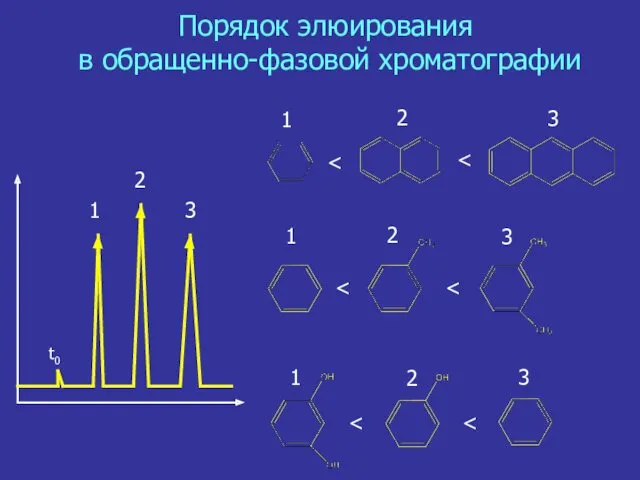
- 32. Порядок элюирования в обращенно-фазовой хроматографии
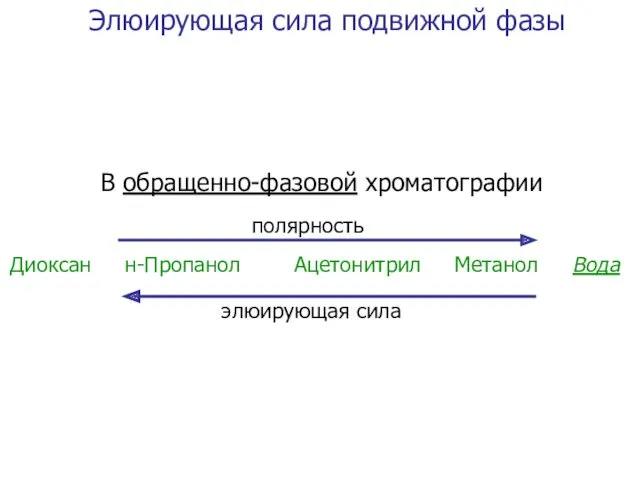
- 33. Элюирующая сила подвижной фазы
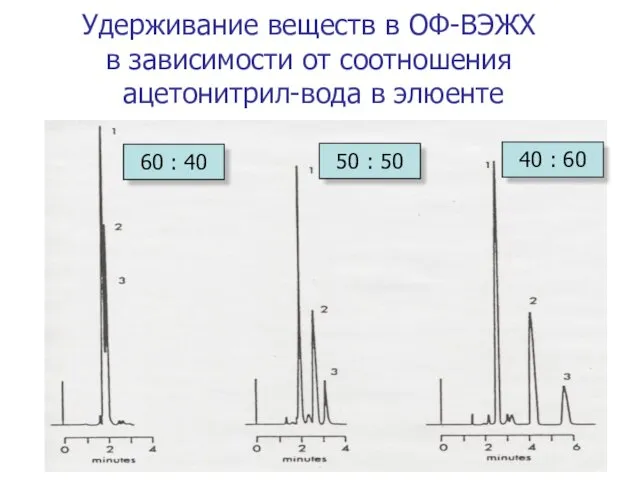
- 34. Удерживание веществ в ОФ-ВЭЖХ в зависимости от соотношения ацетонитрил-вода в элюенте
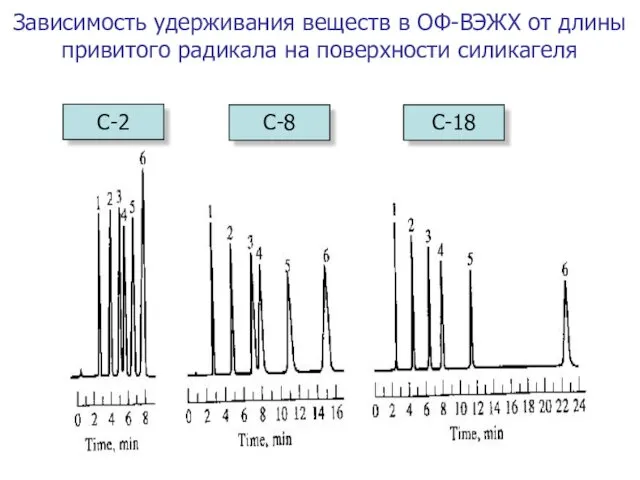
- 35. Зависимость удерживания веществ в ОФ-ВЭЖХ от длины привитого радикала на поверхности силикагеля С-2 С-8 С-18
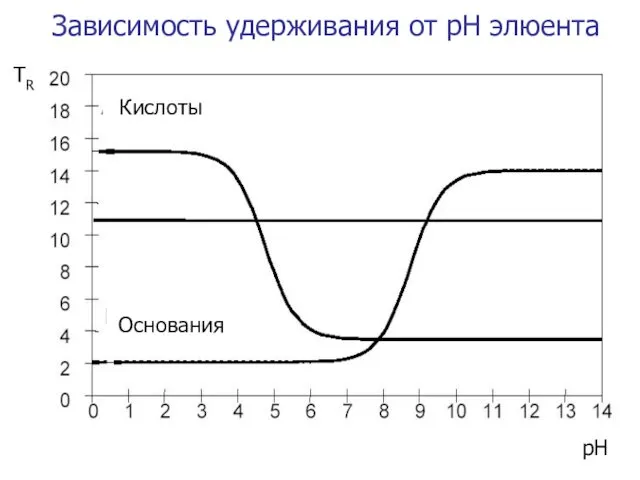
- 36. Зависимость удерживания от рН элюента
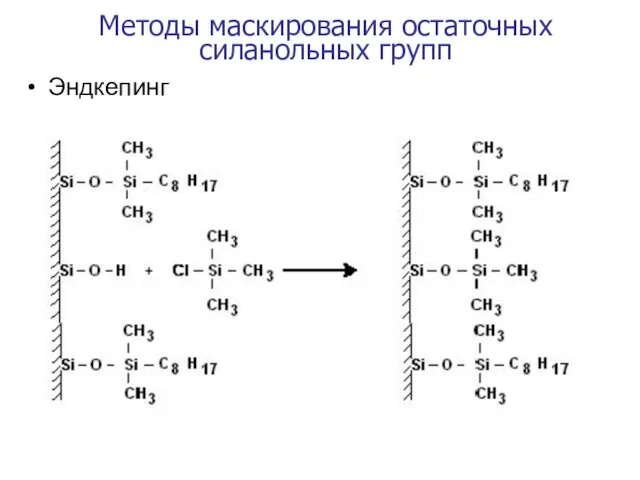
- 37. Методы маскирования остаточных силанольных групп Эндкепинг
- 38. Основные проблемы ОФ ВЭЖХ
- 39. Удерживание возрастает с появлением неполярных заместителей (CH3, CH2, Cl, Br, I) Удерживание уменьшается с появлением полярных
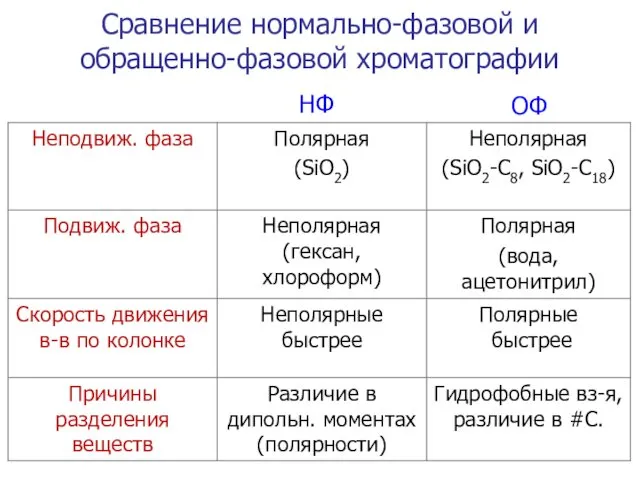
- 40. Сравнение нормально-фазовой и обращенно-фазовой хроматографии
- 41. Хроматография гидрофильных взаимодействий HILIC Идея: использовать механизм нормально-фазовой хроматографии с менее токсичными растворителями Достоинства Многие вещества
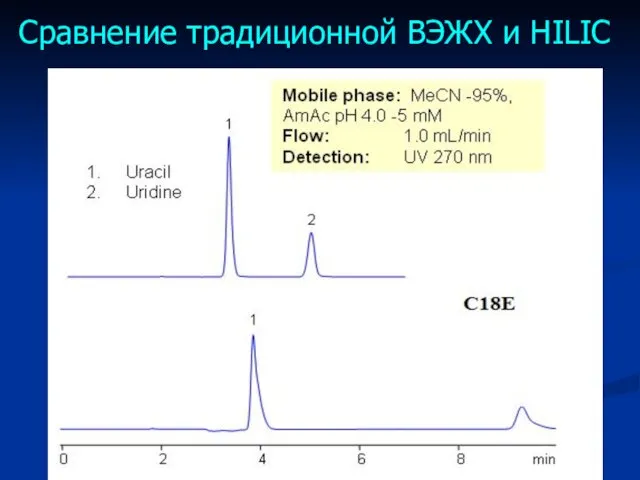
- 42. Сравнение традиционной ВЭЖХ и HILIC
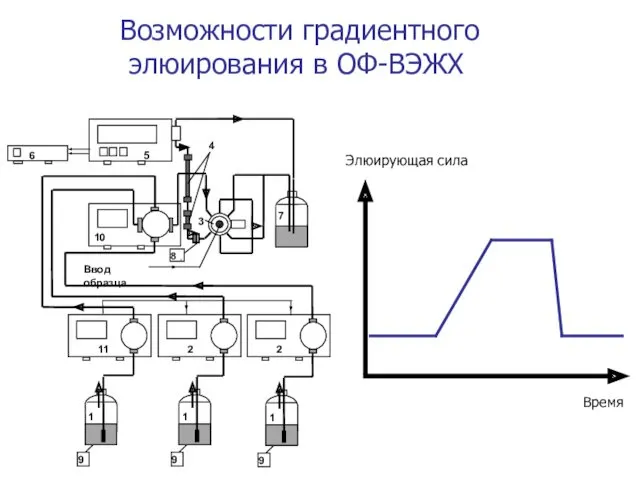
- 43. Возможности градиентного элюирования в ОФ-ВЭЖХ
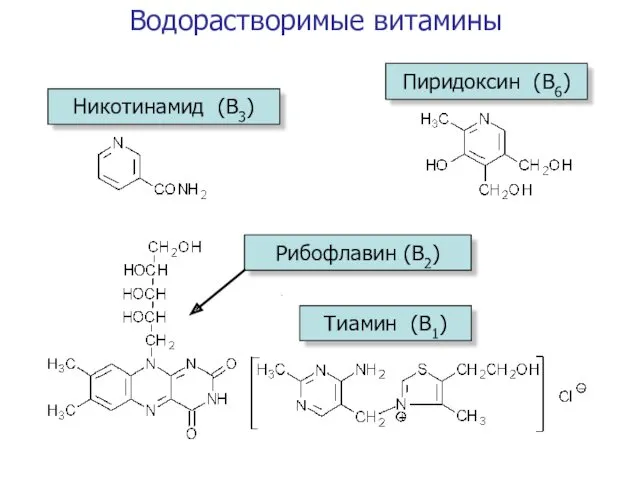
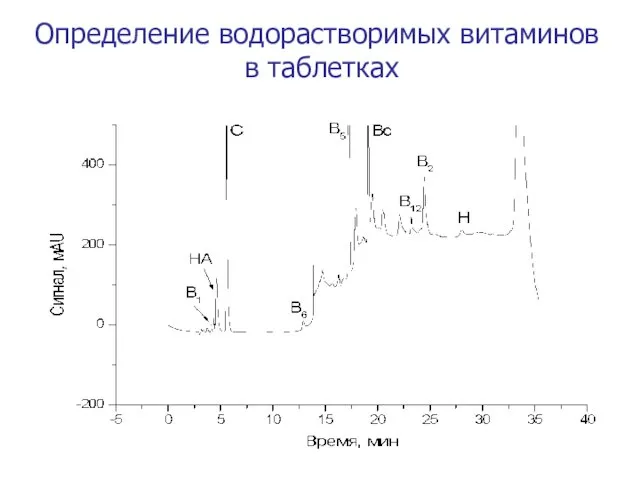
- 44. Водорастворимые витамины
- 45. Определение водорастворимых витаминов в таблетках
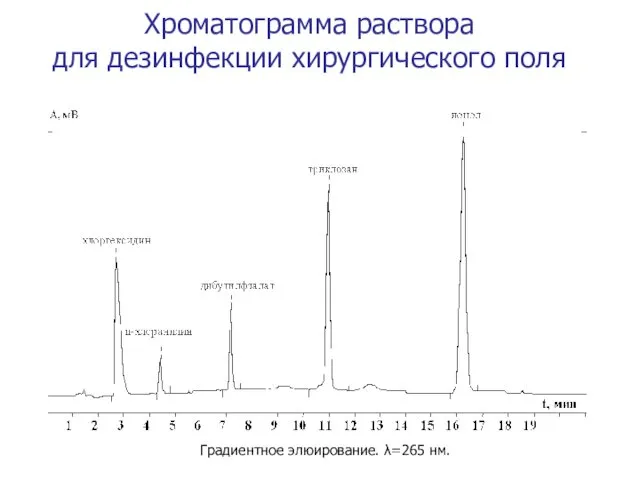
- 46. Хроматограмма раствора для дезинфекции хирургического поля Градиентное элюирование. λ=265 нм.
- 47. Ион-парная хроматография
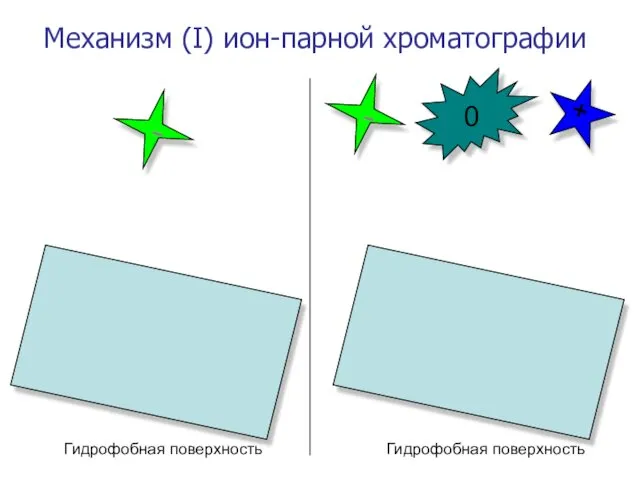
- 48. Механизм (I) ион-парной хроматографии - - + 0
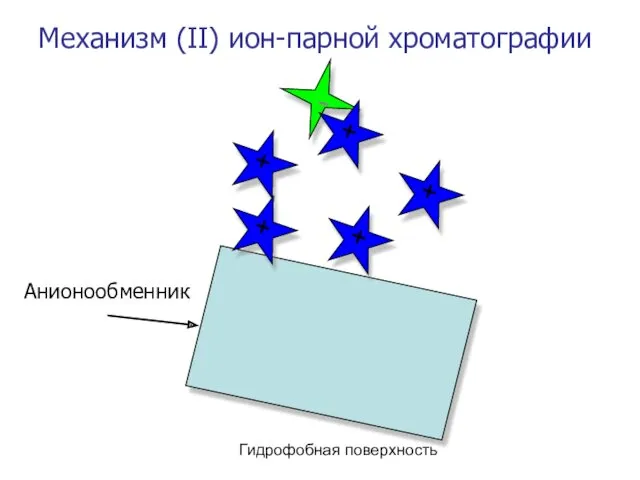
- 49. Механизм (II) ион-парной хроматографии - + + + + +
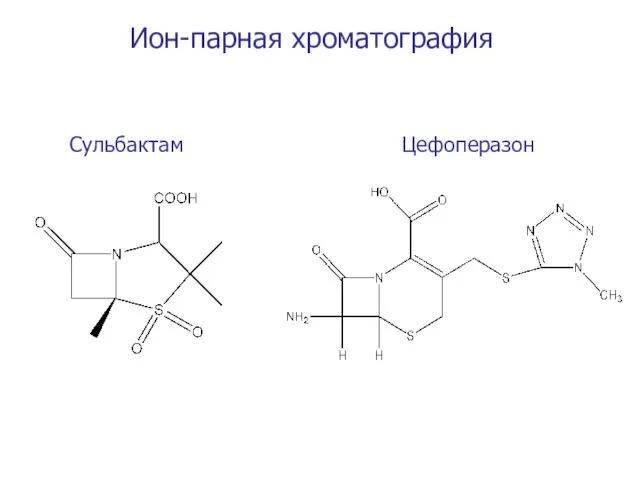
- 50. Ион-парная хроматография Сульбактам Цефоперазон
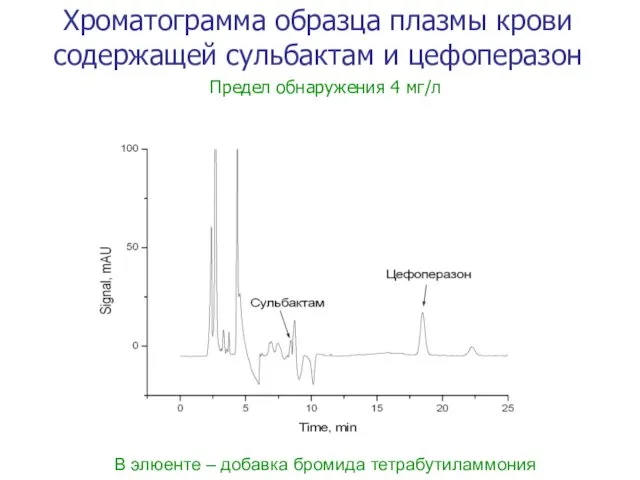
- 51. В элюенте – добавка бромида тетрабутиламмония Хроматограмма образца плазмы крови содержащей сульбактам и цефоперазон Предел обнаружения
- 52. Эксклюзионная хроматография
- 53. Эксклюзионная хроматография Основана на проникновении (диффузии) молекул в гелевую матрицу (полиакриламиды, агароза и др.), содержащую поры
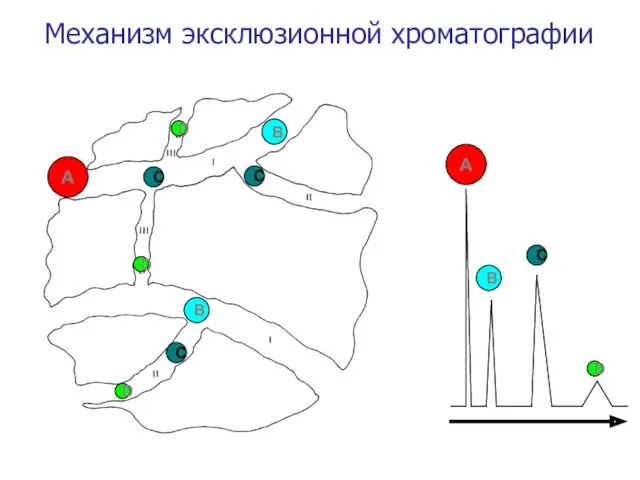
- 54. Механизм эксклюзионной хроматографии
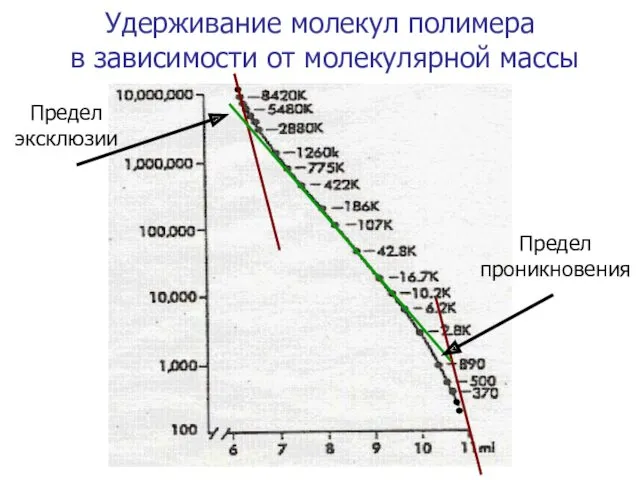
- 55. Удерживание молекул полимера в зависимости от молекулярной массы
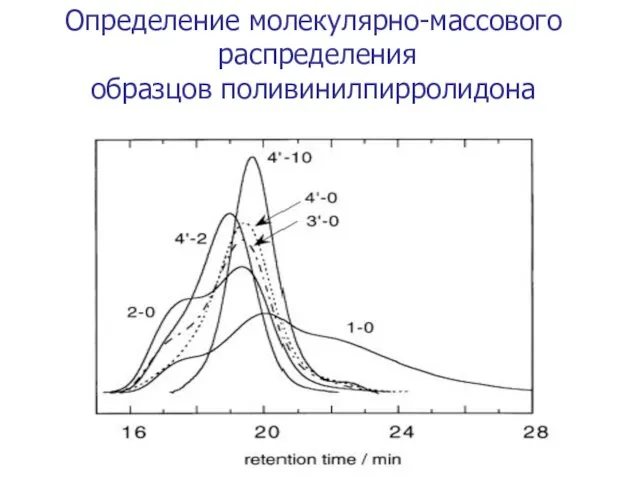
- 56. Определение молекулярно-массового распределения образцов поливинилпирролидона
- 57. Жидкостная хроматография специфических взаимодействий
- 58. Неподвижная фаза для разделения стереоизомеров Хиральная хроматография (Разделение стереоизомеров)
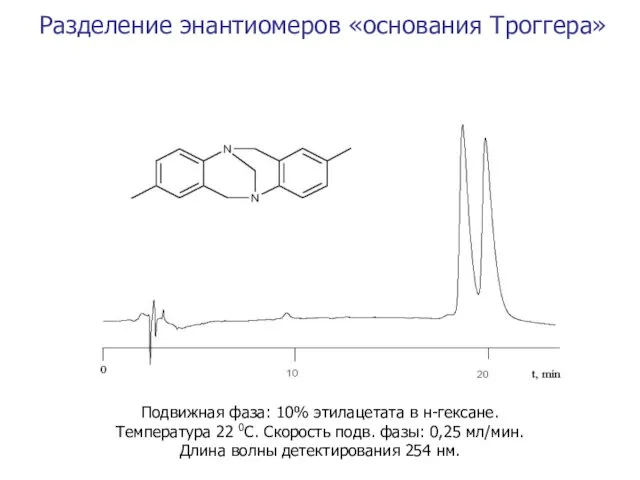
- 59. Разделение энантиомеров «основания Троггера» Подвижная фаза: 10% этилацетата в н-гексане. Температура 22 0С. Скорость подв. фазы:
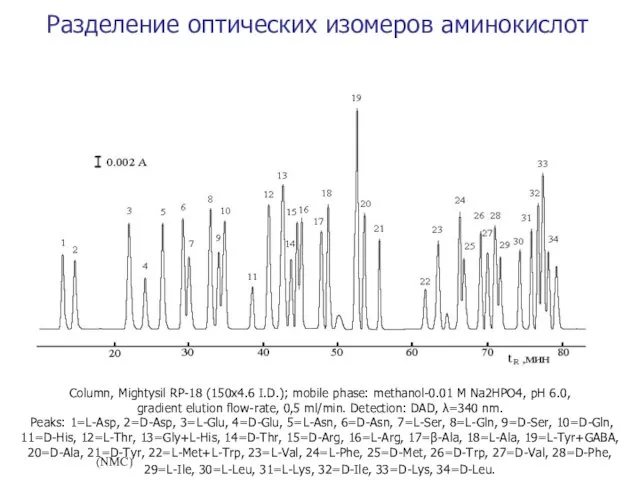
- 60. Разделение оптических изомеров аминокислот (IBLC) (NMC) Column, Mightysil RP-18 (150x4.6 I.D.); mobile phase: methanol-0.01 M Na2HPO4,
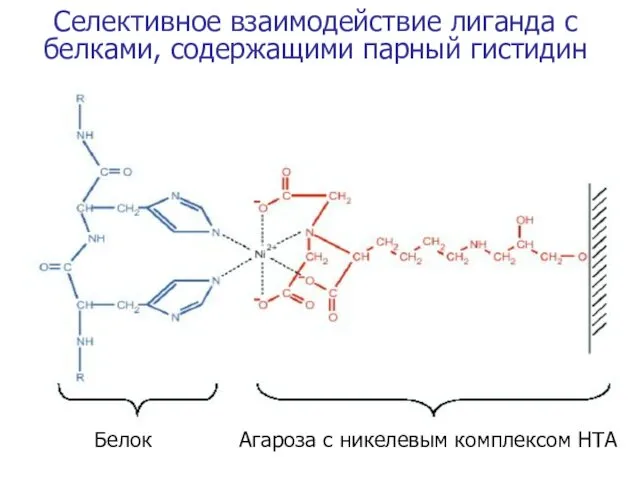
- 61. Аффинная хроматография (избирательное связывание) Основана на способности некоторых веществ (в основном – белков) нековалентно связываться со
- 62. Селективное взаимодействие лиганда с белками, содержащими парный гистидин
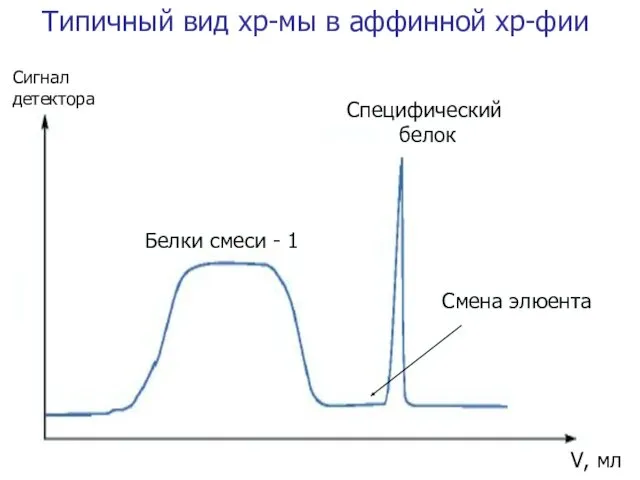
- 63. Сигнал детектора V, мл Специфический белок Белки смеси - 1 Смена элюента Типичный вид хр-мы в
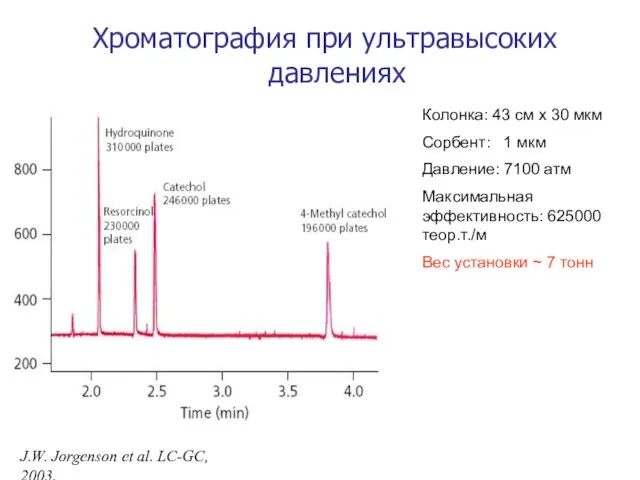
- 64. Хроматография при ультравысоких давлениях Колонка: 43 см х 30 мкм Сорбент: 1 мкм Давление: 7100 атм
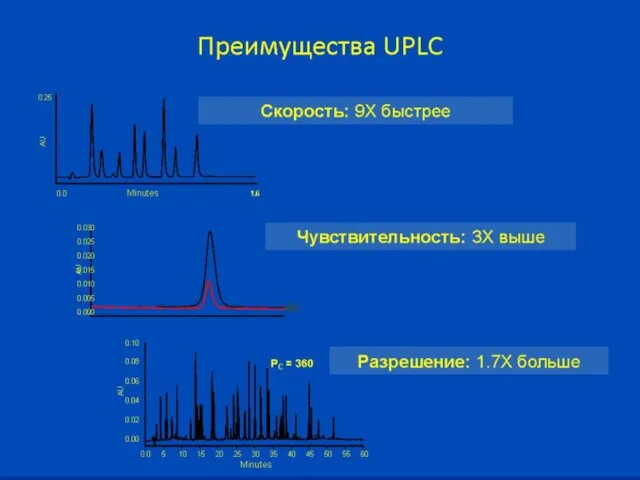
- 65. Быстрая жидкостная хроматография (2004 г.) (UHPLC, RRLC, UPLC, RSLC) Диаметр зерна сорбента менее 2 мкм Меньшие
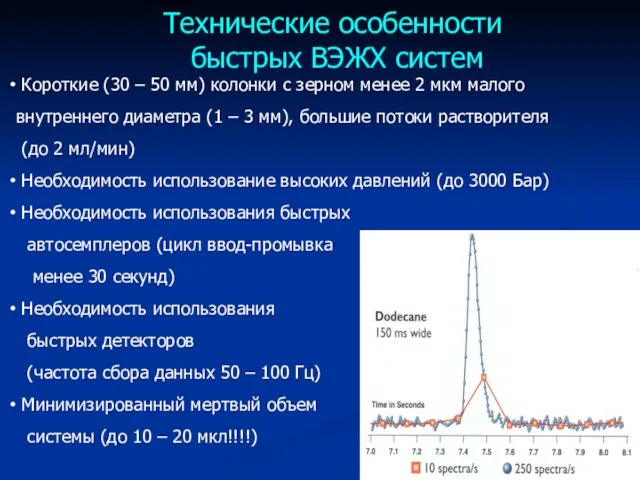
- 67. Технические особенности быстрых ВЭЖХ систем Короткие (30 – 50 мм) колонки с зерном менее 2 мкм
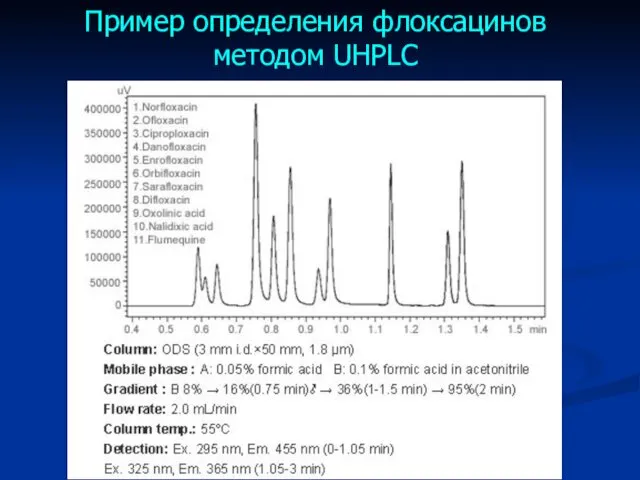
- 68. Пример определения флоксацинов методом UHPLC
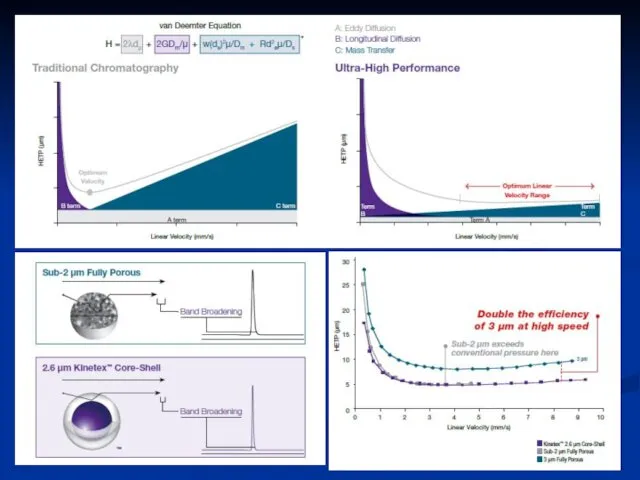
- 69. Повышение характеристик хроматографического разделения Core – Shell технология
- 72. Скачать презентацию





















 Металлы
Металлы Нефть и способы её переработки
Нефть и способы её переработки Хімічні явища у природі
Хімічні явища у природі Химиялық реакциялардың жылдамдығы
Химиялық реакциялардың жылдамдығы Выдающиеся открытия в области химии
Выдающиеся открытия в области химии Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів
Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів Окислительно-восстановительные реакции. Основные положения электронной теории ОВР
Окислительно-восстановительные реакции. Основные положения электронной теории ОВР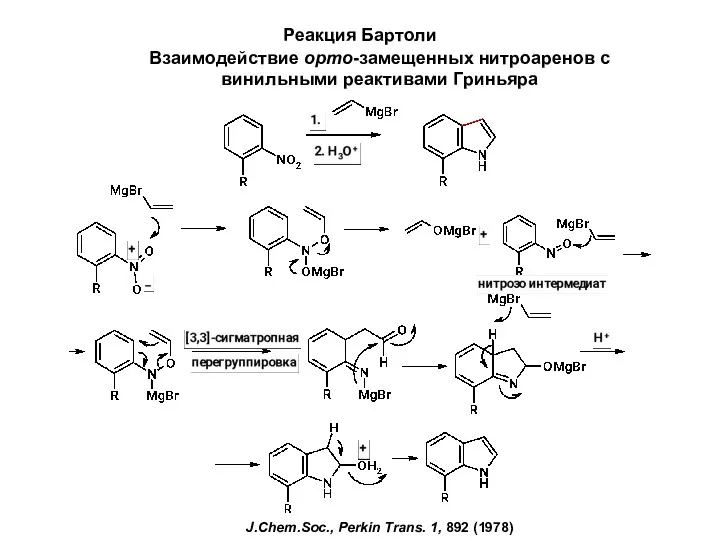 Реакция Бартоли. Взаимодействие орто-замещенных нитроаренов с винильными реактивами Гриньяра
Реакция Бартоли. Взаимодействие орто-замещенных нитроаренов с винильными реактивами Гриньяра Наноструктурные и нанокристаллические материалы
Наноструктурные и нанокристаллические материалы Хімія запаху і смаку
Хімія запаху і смаку Азот. Нахождение азота в природе
Азот. Нахождение азота в природе Азот и его свойства
Азот и его свойства Циклоалканы
Циклоалканы Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки 6-я группа элементов. 9 класс
6-я группа элементов. 9 класс Таблицы. Определение характера оксидов
Таблицы. Определение характера оксидов Оксиды, их классификация и свойства
Оксиды, их классификация и свойства Получение высокодисперсных проводящих оксидов - носителей платинового катализатора для низкотемпературных топливных элементов
Получение высокодисперсных проводящих оксидов - носителей платинового катализатора для низкотемпературных топливных элементов Биотыңайтқыштар
Биотыңайтқыштар Йод. Химические свойства
Йод. Химические свойства Использование кубового остатка ректификации стирола в процессах получения нефтяных дорожных битумов
Использование кубового остатка ректификации стирола в процессах получения нефтяных дорожных битумов Гетерофункциональные производные бензольного ряда как лекарственные средства
Гетерофункциональные производные бензольного ряда как лекарственные средства Химические уравнения
Химические уравнения Химический турнир
Химический турнир Химические свойства оксидов
Химические свойства оксидов Химическая термодинамика
Химическая термодинамика Химия в повседневной жизни человека
Химия в повседневной жизни человека