Содержание
- 2. Номенклатура различных форм кислорода
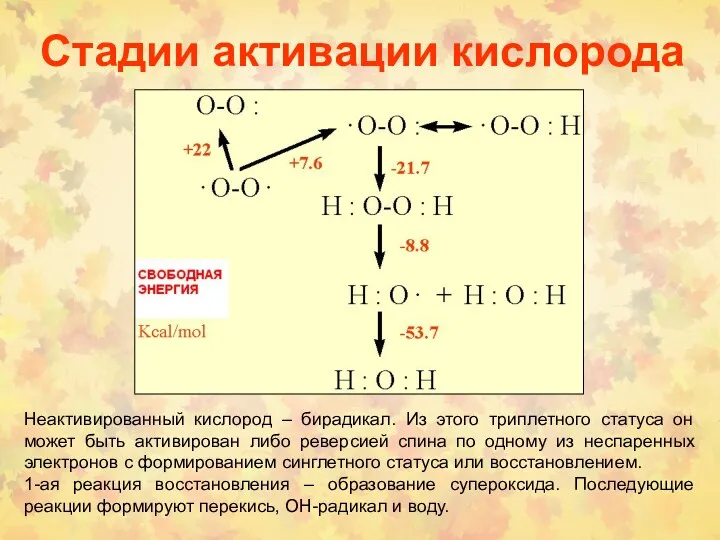
- 3. Стадии активации кислорода Неактивированный кислород – бирадикал. Из этого триплетного статуса он может быть активирован либо
- 4. Источники радикалов кислорода - эндогенные - экзогенные
- 5. 1. Эндогенные источники А. Реакция Фентона
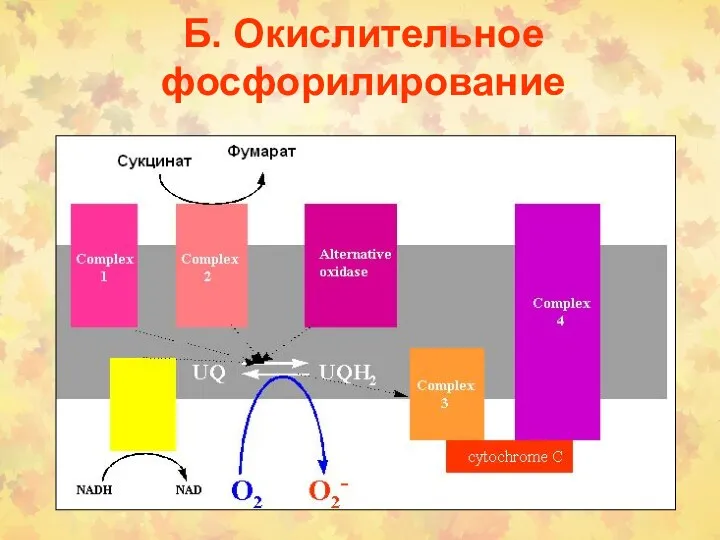
- 6. Б. Окислительное фосфорилирование
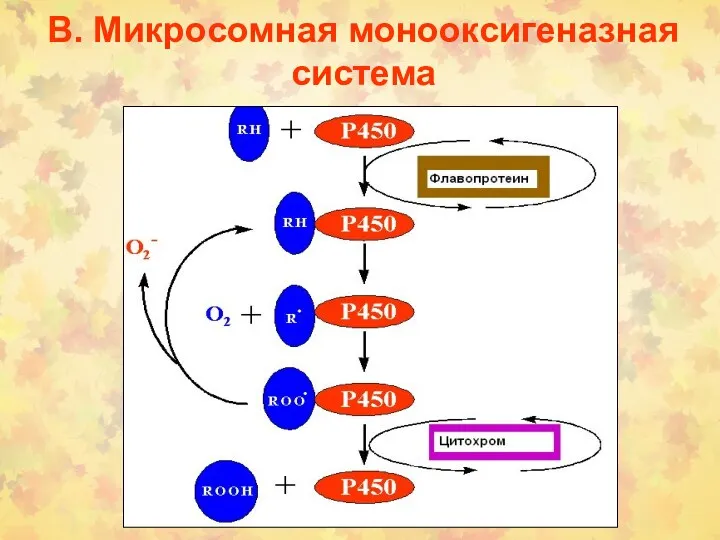
- 7. В. Микросомная монооксигеназная система
- 8. Г. Пероксисомы и глиоксисомы - окисление жирных кислот - цикл глиоксильной кислоты: гликолат оксидаза – продуцирует
- 9. Полиморфноядерные лейкоциты имеют три ферментативные системы генерации АКМ : NАDPН-оксидазу (мембраносвязанную), пероксидазы - миелопероксидаза (МПО) в
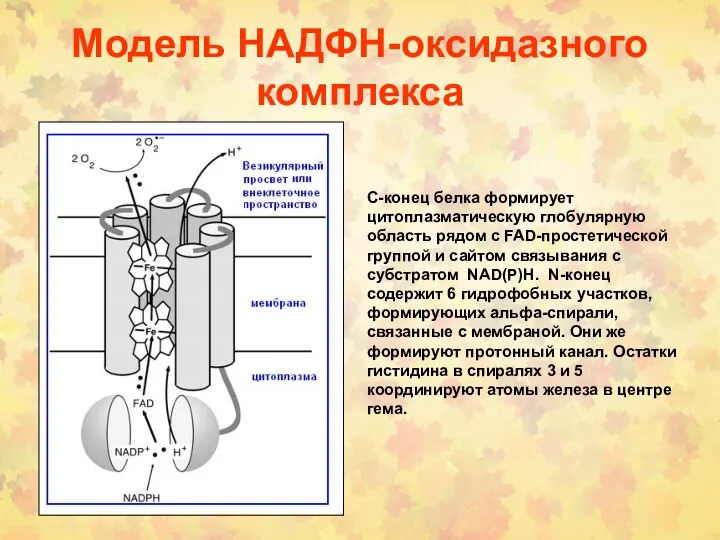
- 10. Модель НАДФН-оксидазного комплекса С-конец белка формирует цитоплазматическую глобулярную область рядом с FAD-простетической группой и сайтом связывания
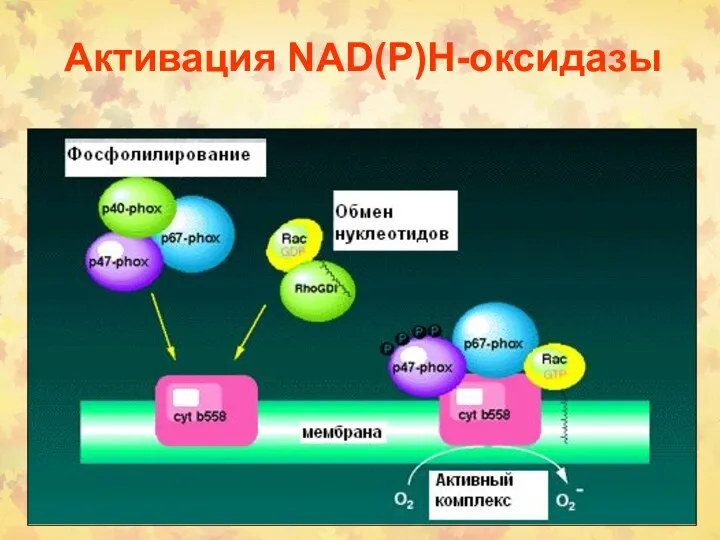
- 11. Активация NАD(P)Н-оксидазы
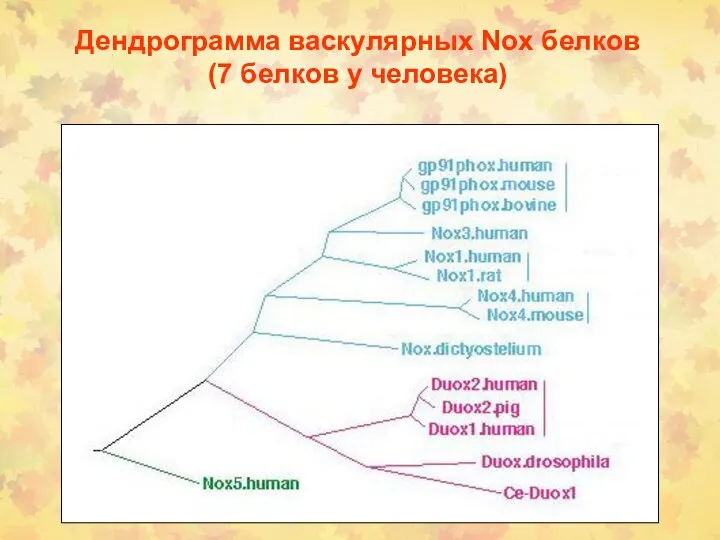
- 12. Дендрограмма васкулярных Nox белков (7 белков у человека)
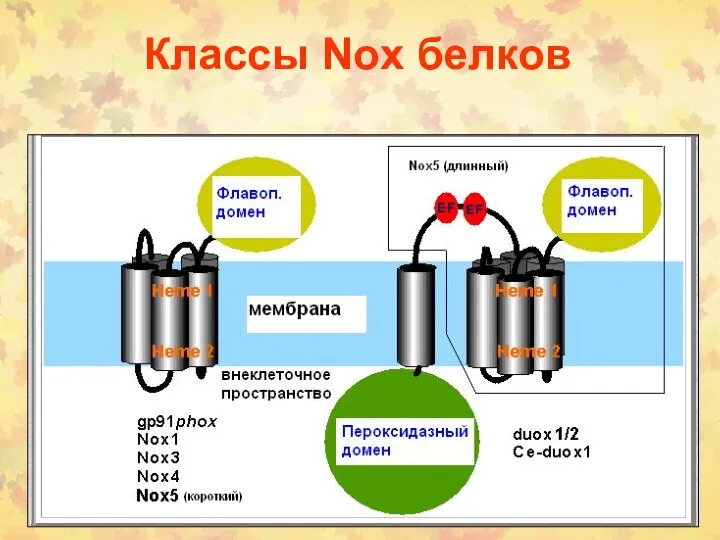
- 13. Классы Nox белков
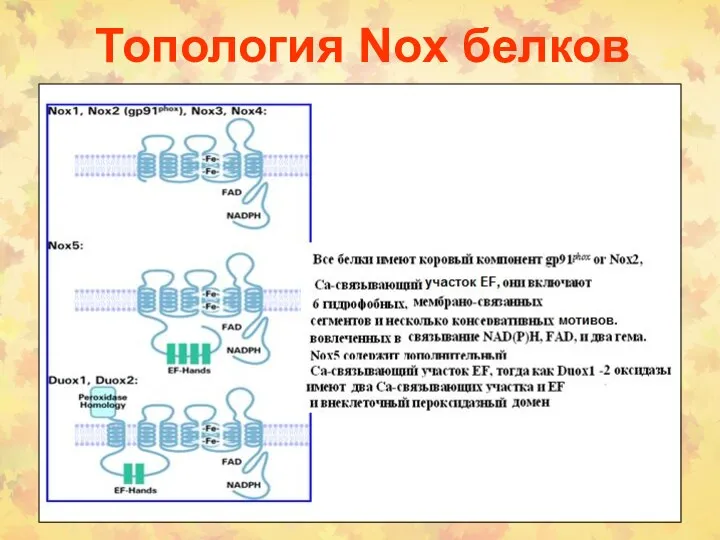
- 14. Топология Nox белков
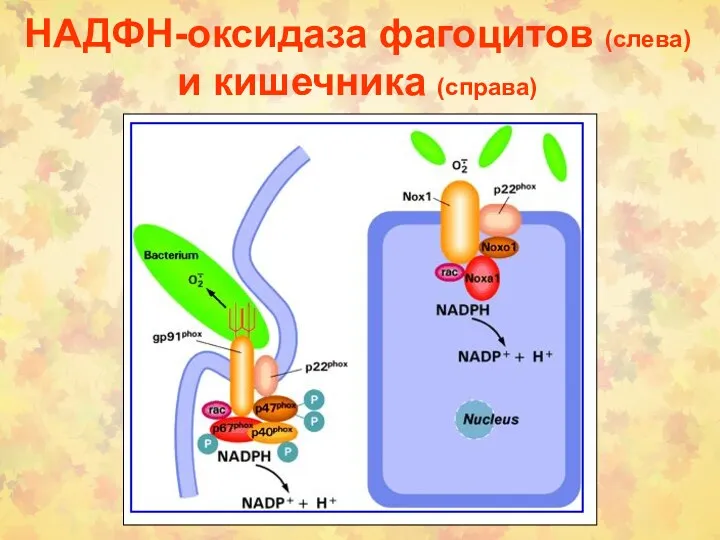
- 15. НАДФН-оксидаза фагоцитов (слева) и кишечника (справа)
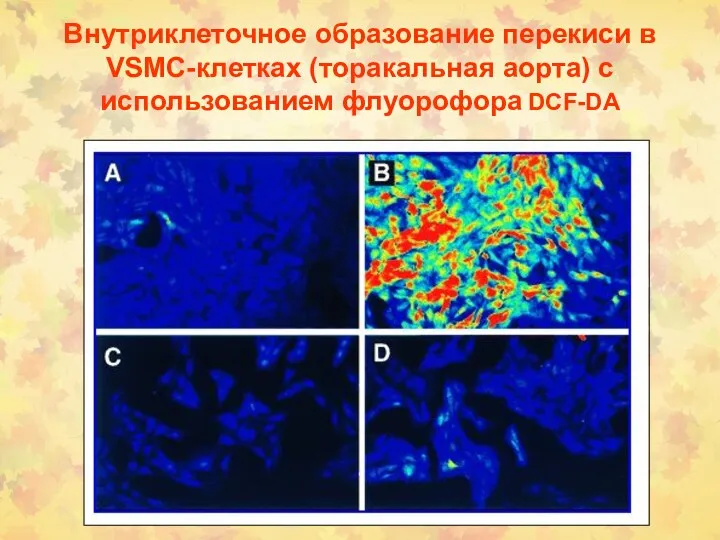
- 16. Внутриклеточное образование перекиси в VSMC-клетках (торакальная аорта) с использованием флуорофора DCF-DA
- 17. 2. Экзогенные источники - Оксиды азота в сигаретном дыме (1000ррм) - Соли Fe и Cu -
- 18. Механизмы действия. Мишени для РФК и РФА Липиды клеточной мембраны ДНК Белки
- 19. 1. Окислительное повреждение липидов
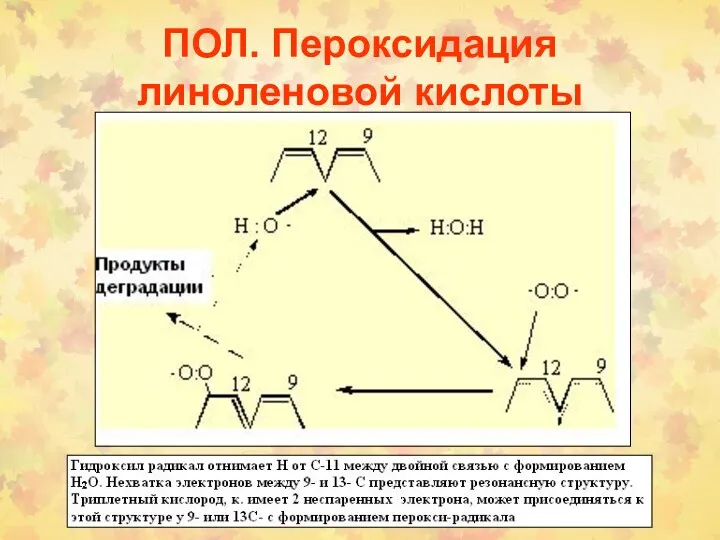
- 20. ПОЛ. Пероксидация линоленовой кислоты
- 21. Терминация ПОЛ
- 22. 2. Окислительное повреждение белков Оксидативная атака на белки вызывает: - сайт-специфичные модификации аминокислот - фрагментацию пептидной
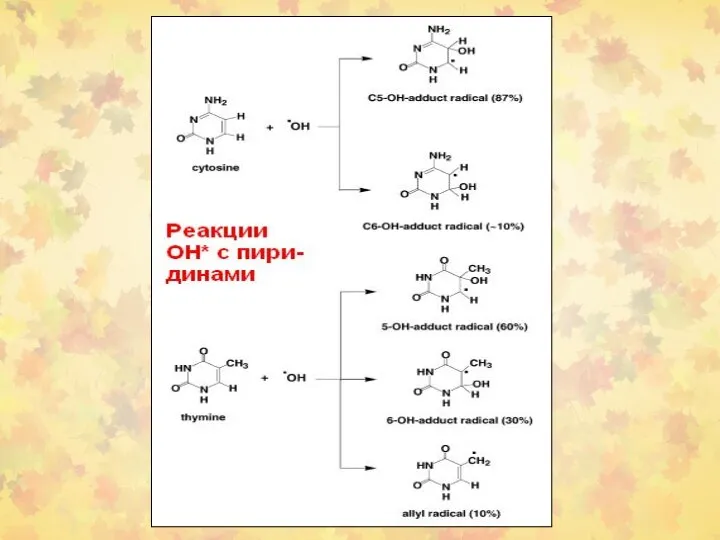
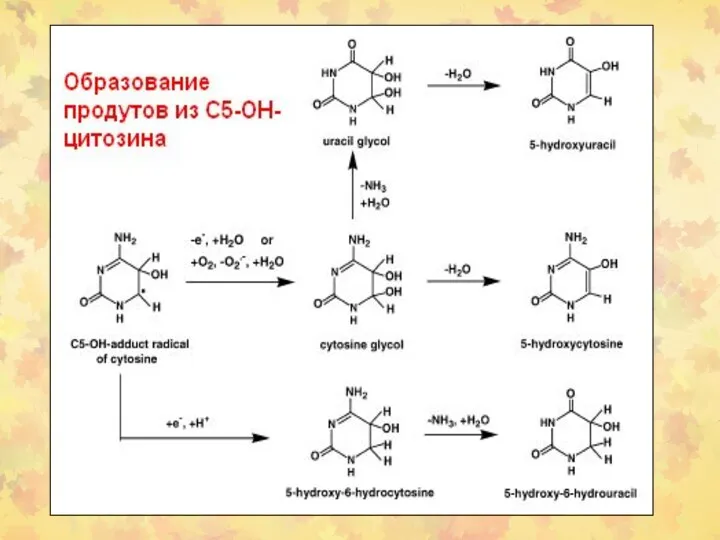
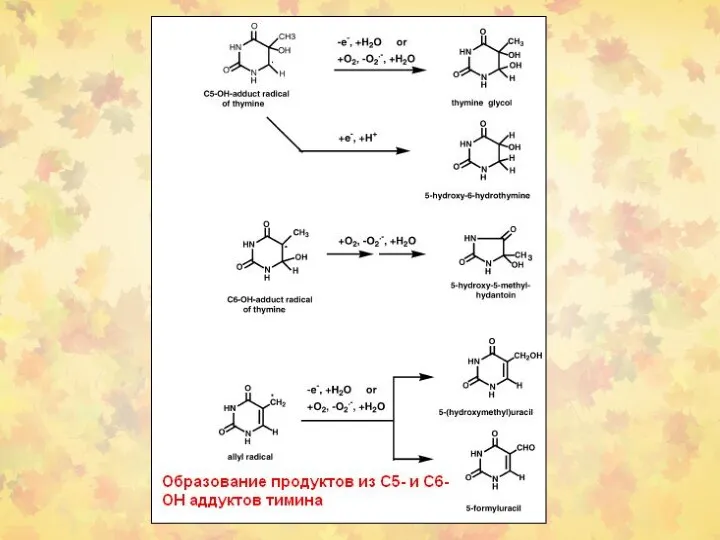
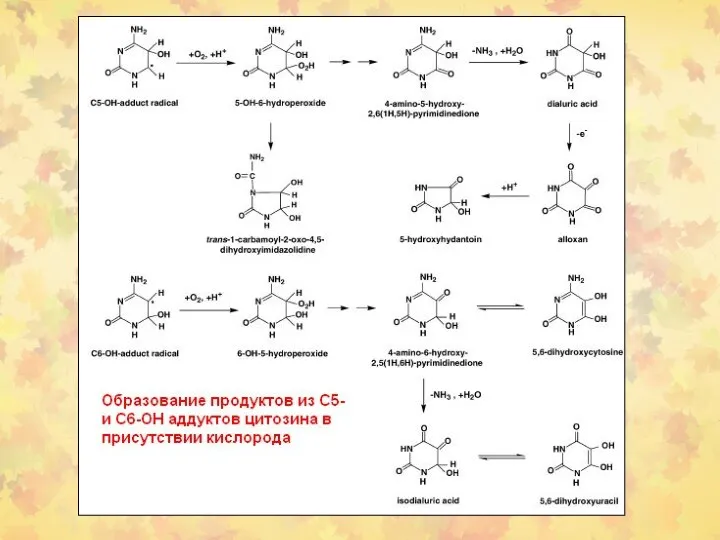
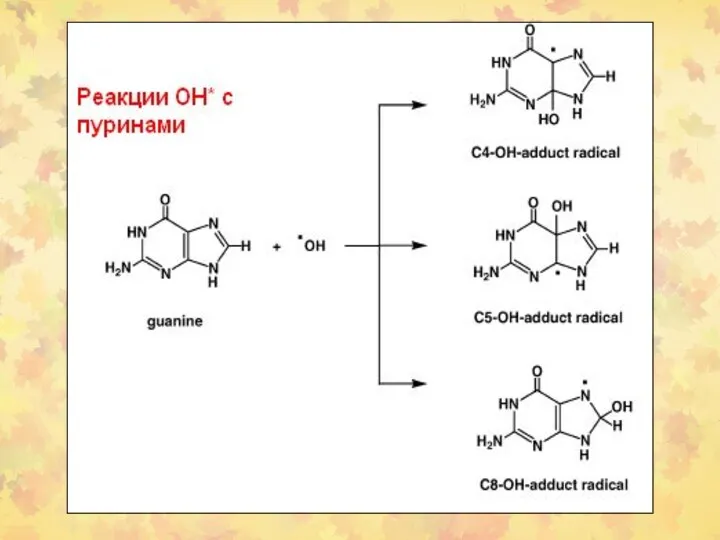
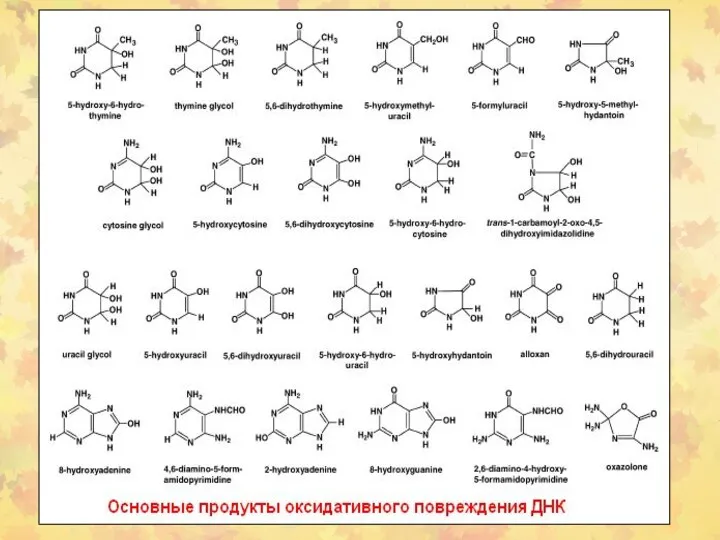
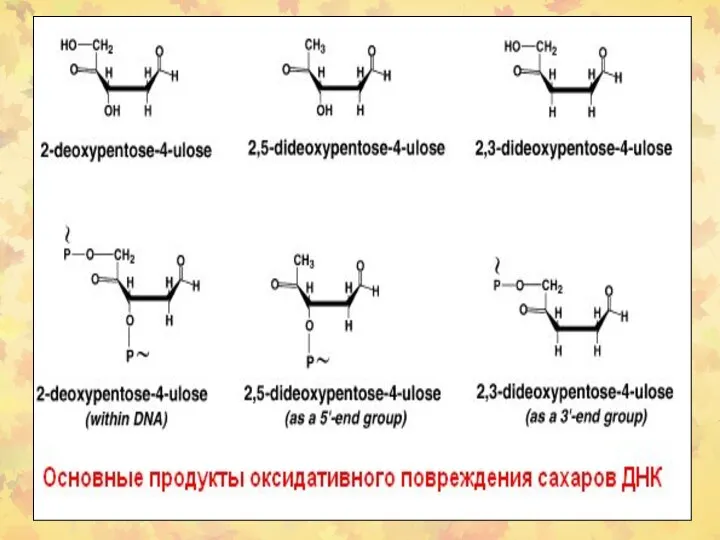
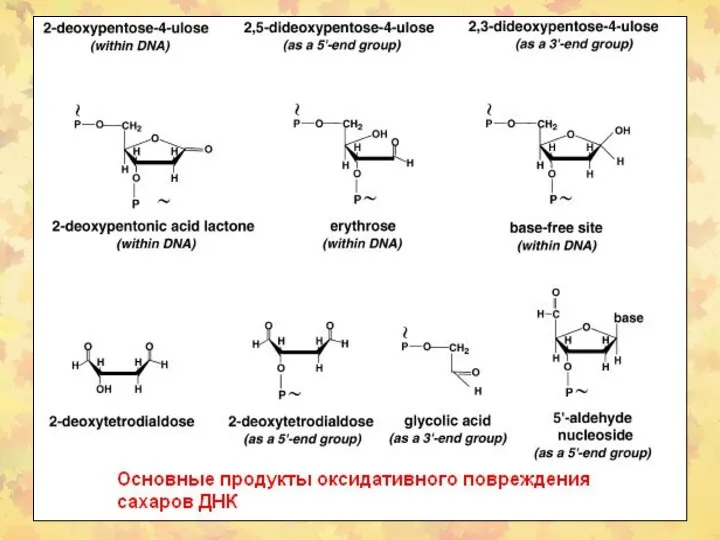
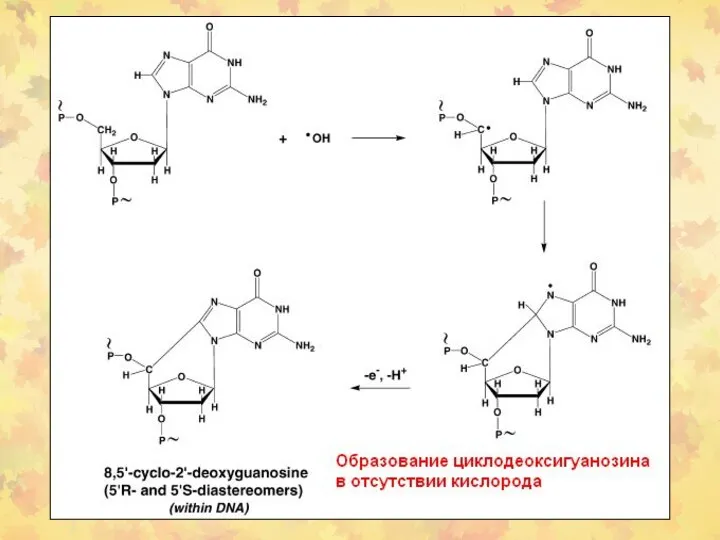
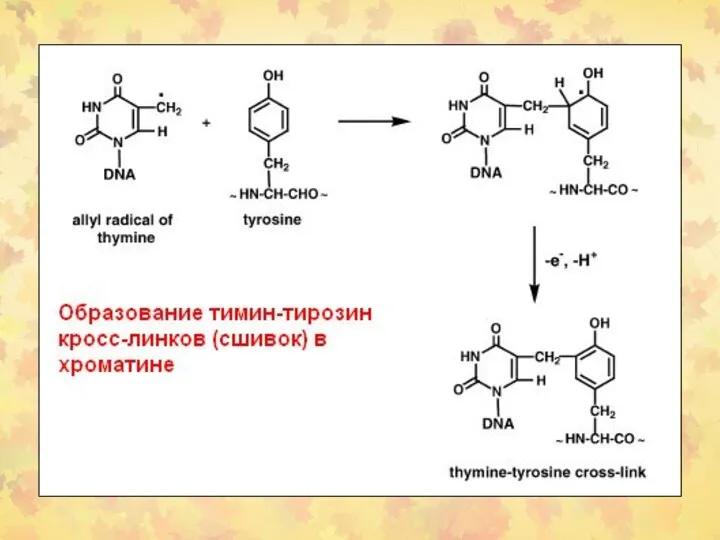
- 23. 3. Окислительное повреждение ДНК Множественные повреждения, как сахаров, так и оснований. Индуцируются мутации, в том числе
- 34. Антиоксидантная защита - ферментативная - химическая
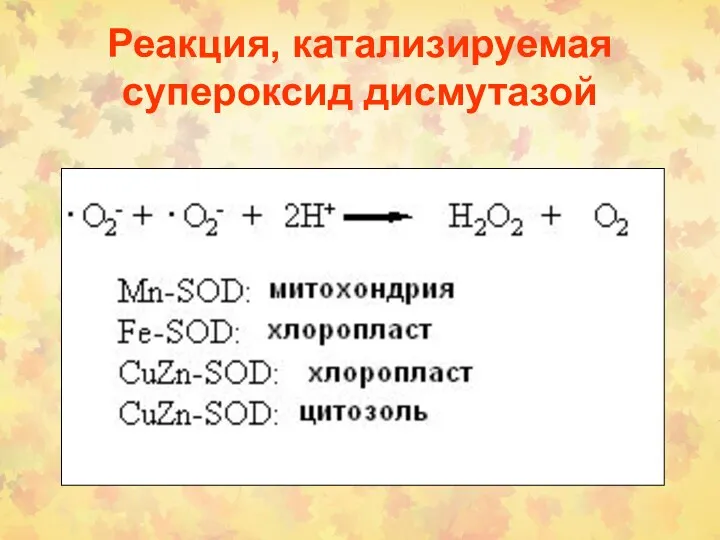
- 35. Реакция, катализируемая супероксид дисмутазой
- 36. Другие ферменты
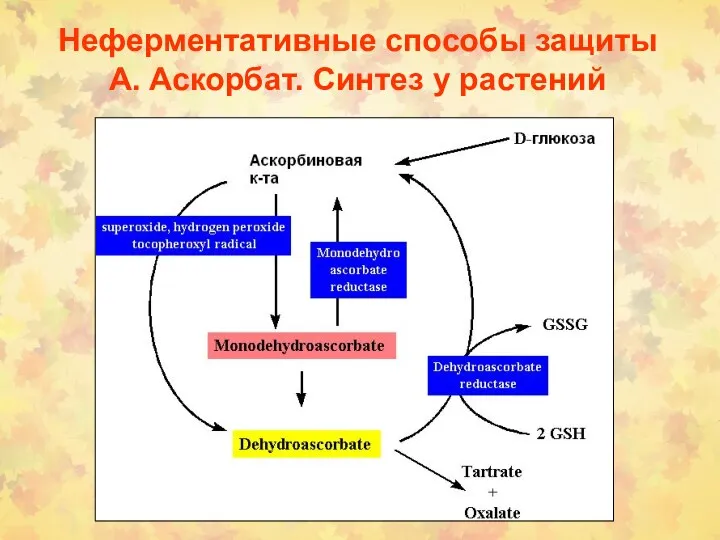
- 37. Неферментативные способы защиты А. Аскорбат. Синтез у растений
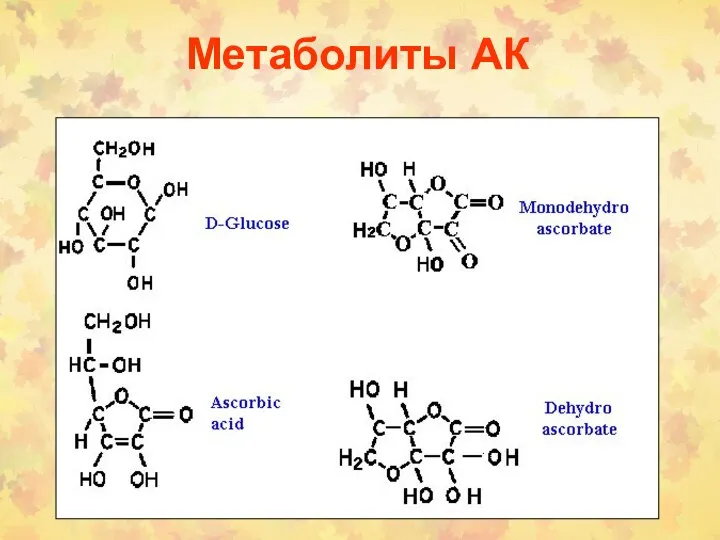
- 38. Метаболиты АК
- 39. Некоторые реакции с участием аскорбата
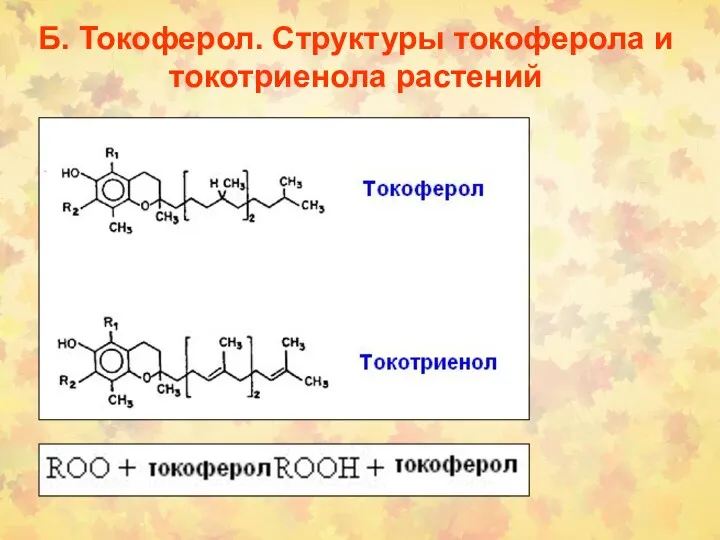
- 40. Б. Токоферол. Структуры токоферола и токотриенола растений
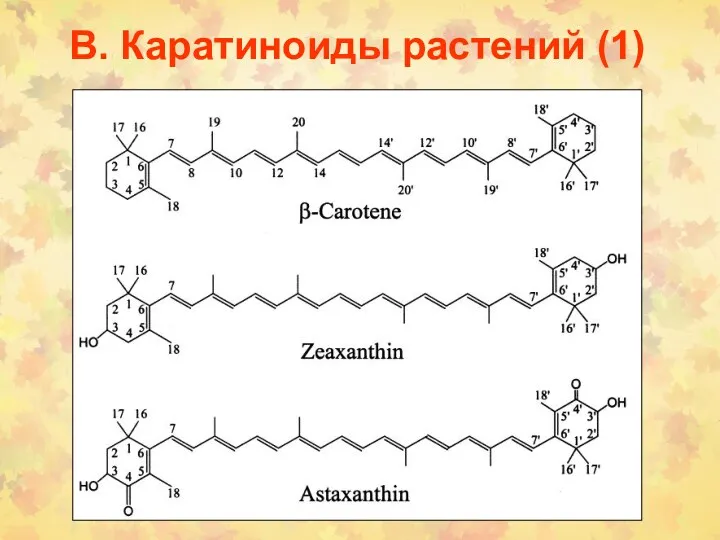
- 41. В. Каратиноиды растений (1)
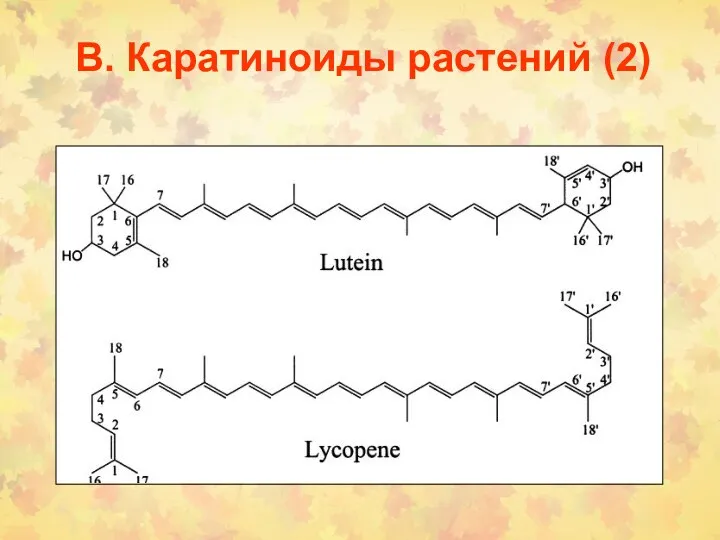
- 42. В. Каратиноиды растений (2)
- 43. Методы изучения антиоксидантной активности каратиноидов
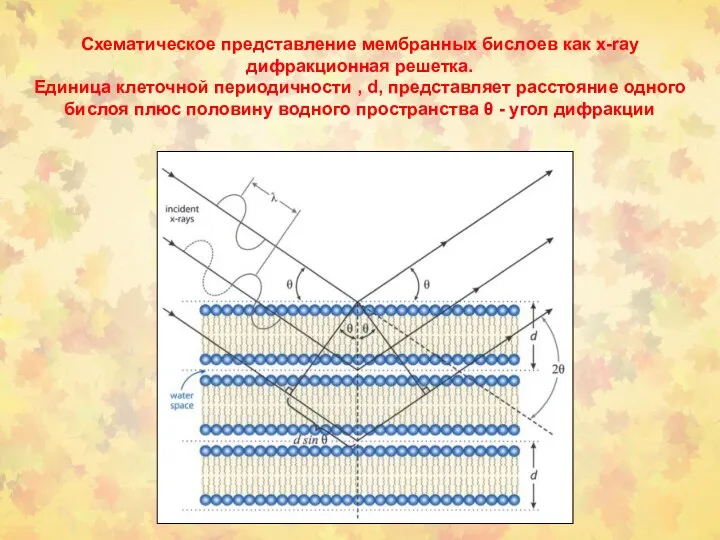
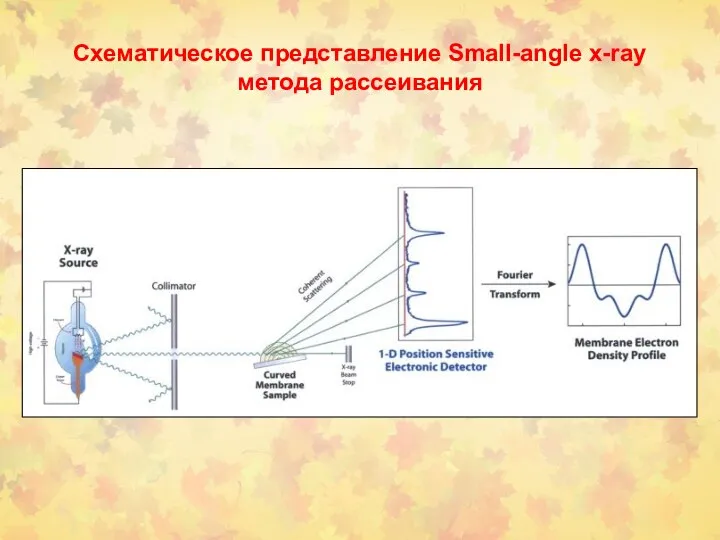
- 44. Схематическое представление мембранных бислоев как x-ray дифракционная решетка. Единица клеточной периодичности , d, представляет расстояние одного
- 45. Схематическое представление Small-angle x-ray метода рассеивания
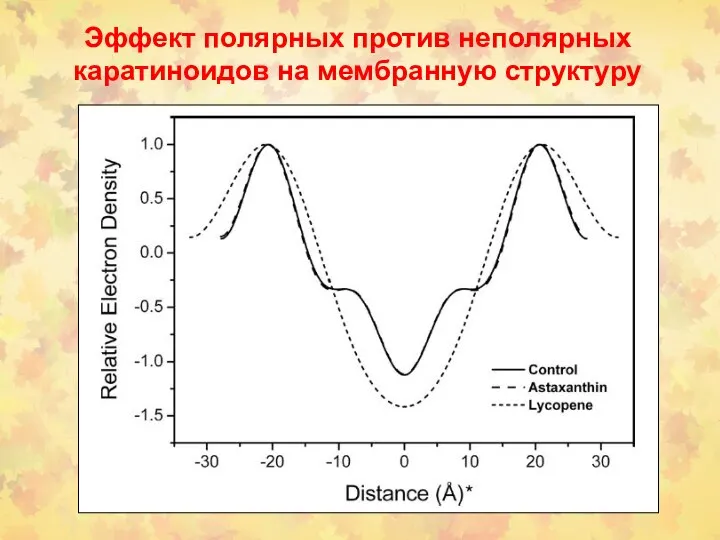
- 46. Эффект полярных против неполярных каратиноидов на мембранную структуру
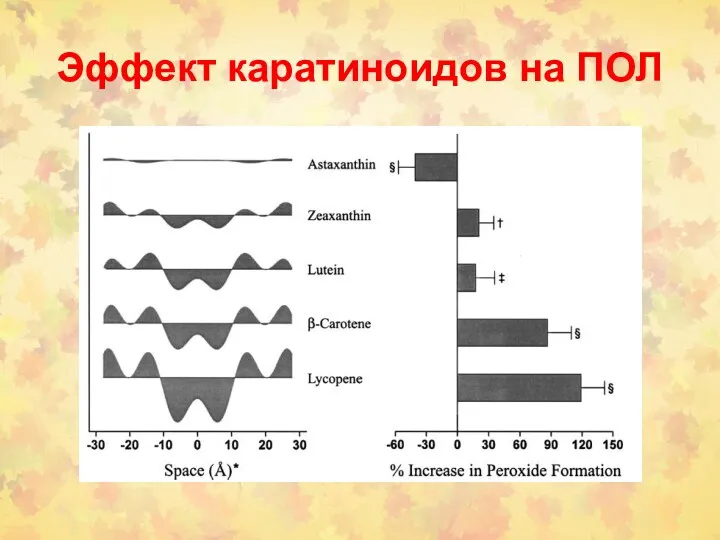
- 47. Эффект каратиноидов на ПОЛ
- 48. Полифенолы (ПФ) растений Антиоксидантная активность: 1. Взаимодействие с ROS, роль «ловушка» 2. Предотвращение образования радикалов (связывание
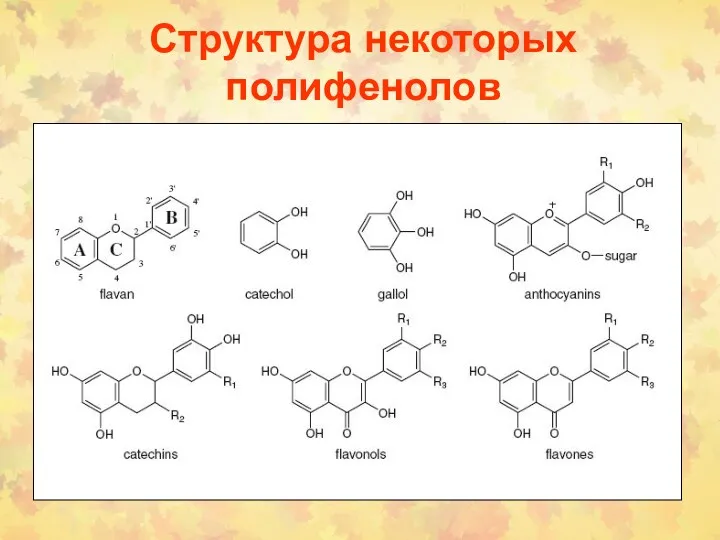
- 49. Структура некоторых полифенолов
- 50. Механизм действия ПФ 1. «Тушение» радикалов Несколько способов измерения: trolox-equivalent antioxidant activity (TEAC) oxygen radical absorbance
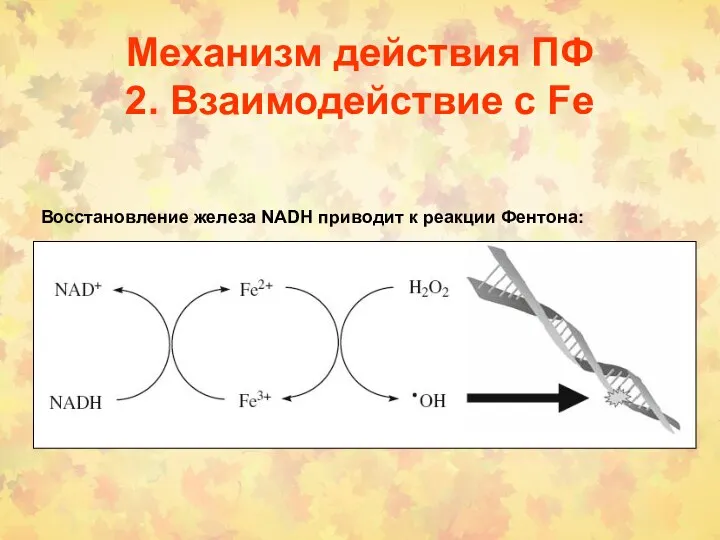
- 51. Механизм действия ПФ 2. Взаимодействие с Fe Восстановление железа NADH приводит к реакции Фентона:
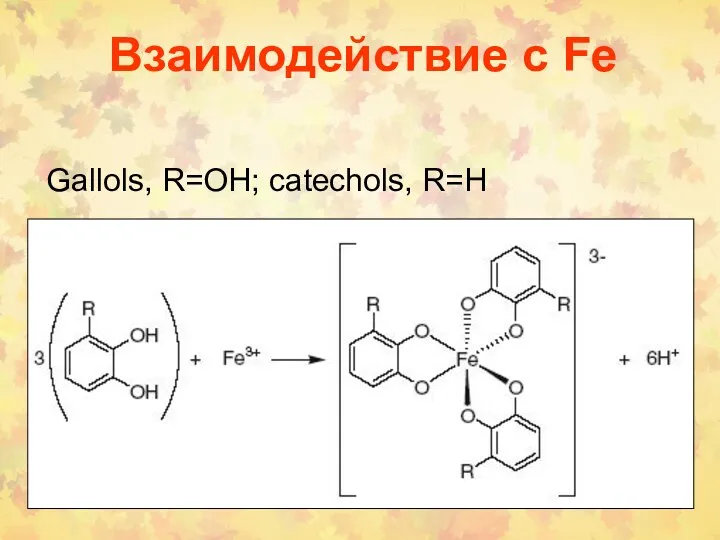
- 52. Взаимодействие с Fe Gallols, R=OH; catechols, R=H
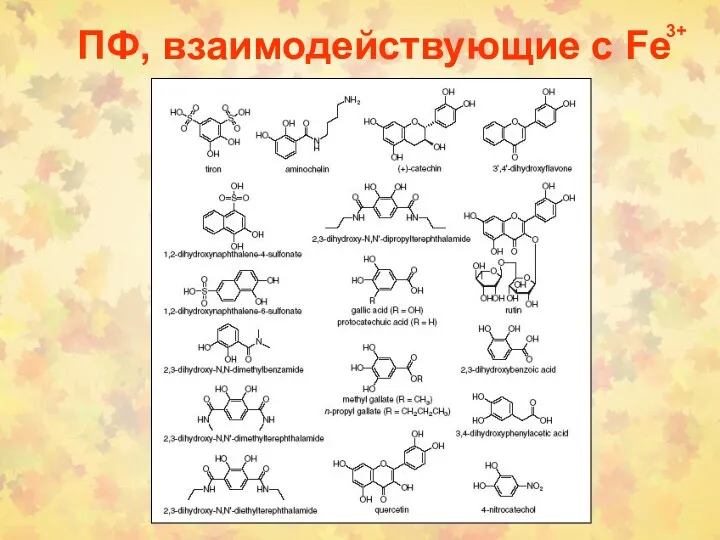
- 53. ПФ, взаимодействующие с Fe 3+
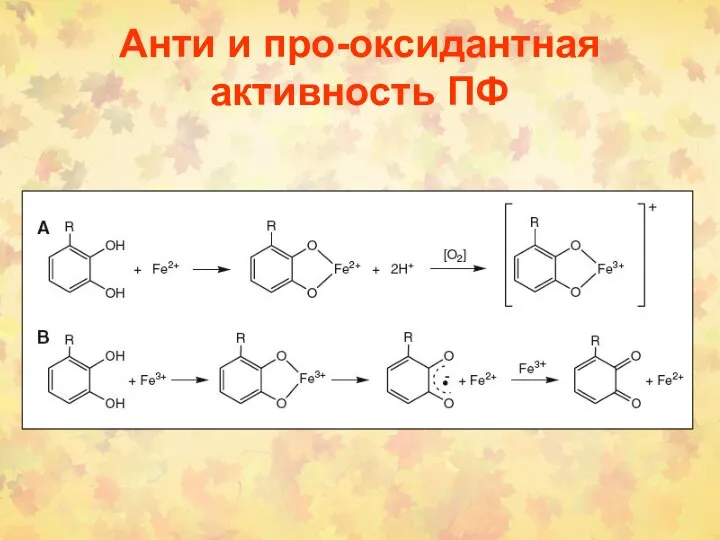
- 54. Анти и про-оксидантная активность ПФ
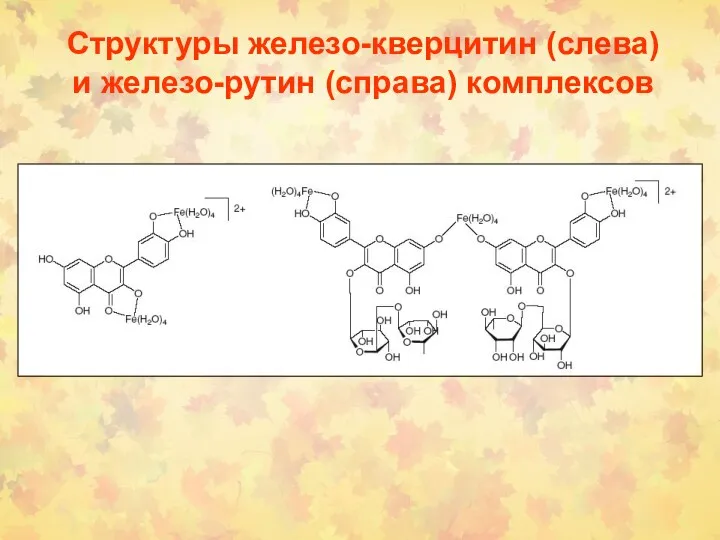
- 55. Структуры железо-кверцитин (слева) и железо-рутин (справа) комплексов
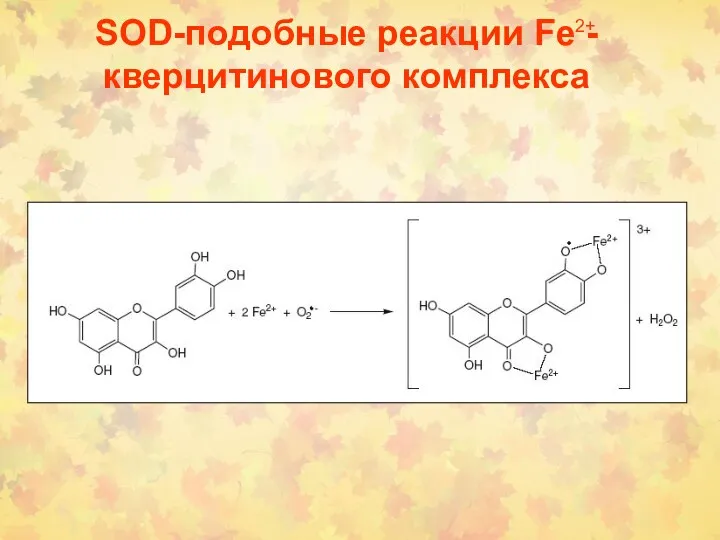
- 56. SOD-подобные реакции Fe - кверцитинового комплекса 2+
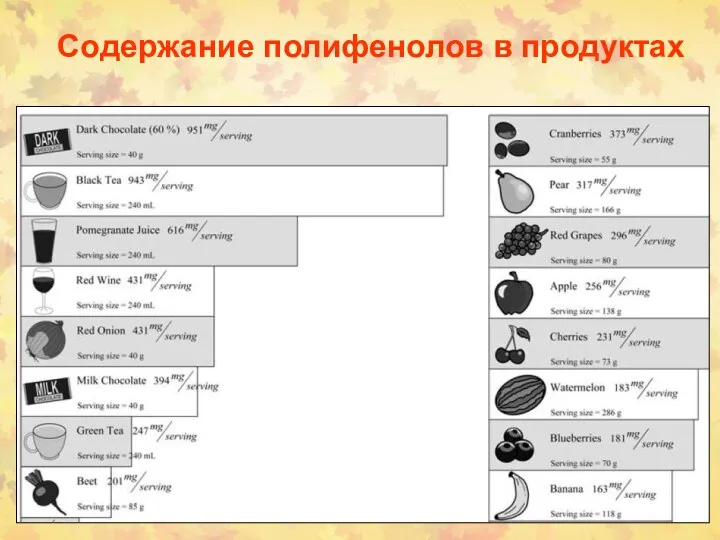
- 57. Содержание полифенолов в продуктах
- 58. Содержание полифенолов в продуктах
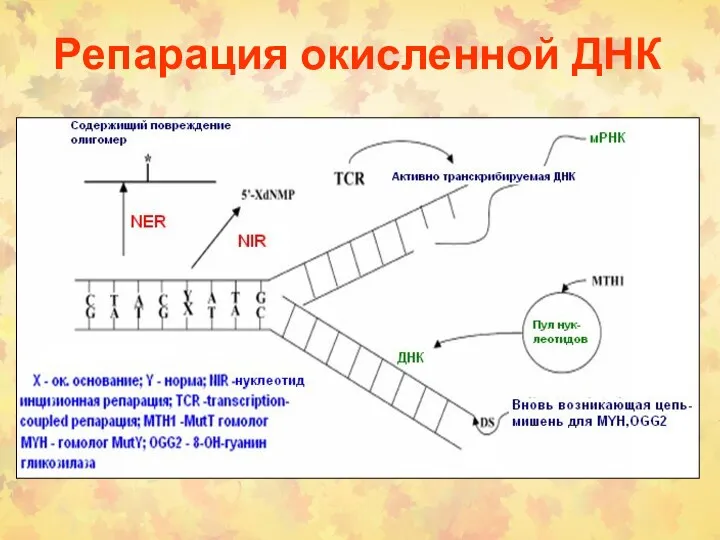
- 59. Репарация окисленной ДНК
- 61. Скачать презентацию


















 Ожирение среди подростков. Ожирение - хроническое заболевание
Ожирение среди подростков. Ожирение - хроническое заболевание Эмфизема легких, дыхательная недостаточность, хлс
Эмфизема легких, дыхательная недостаточность, хлс Жүйелі қателер туралы ұғым
Жүйелі қателер туралы ұғым Синтетические противомикробные средства
Синтетические противомикробные средства Помощь при укусах и отравлениях
Помощь при укусах и отравлениях Рентгенанатомия, физиология, развитие и рост опорно – двигательного аппарата
Рентгенанатомия, физиология, развитие и рост опорно – двигательного аппарата Природне вигодовування дітей раннього віку
Природне вигодовування дітей раннього віку Использование средств изобразительной деятельности в коррекции фонетико-фонематического недоразвития
Использование средств изобразительной деятельности в коррекции фонетико-фонематического недоразвития Анестезиологическое обеспечение лапароскопических операций
Анестезиологическое обеспечение лапароскопических операций Ана сүтімен қоректендірудің маңызы
Ана сүтімен қоректендірудің маңызы Нарушения периферического кровообращения
Нарушения периферического кровообращения Исследование эякулята
Исследование эякулята Травматический шок
Травматический шок Вибрационная болезнь
Вибрационная болезнь Расстройства кровообращения: гемостаз, стаз, тромбоз, ДВС-синдром, эмболия, ишемия, инфаркт
Расстройства кровообращения: гемостаз, стаз, тромбоз, ДВС-синдром, эмболия, ишемия, инфаркт Рак кожи. Меланома
Рак кожи. Меланома Бейімделудің физиологиялық негізі
Бейімделудің физиологиялық негізі Burns
Burns Внутриэпителиальный рак. Болезнь Боуэна, эритроплазия Кейра
Внутриэпителиальный рак. Болезнь Боуэна, эритроплазия Кейра Теплолечение (термотерапия)
Теплолечение (термотерапия) Итоги деятельности службы медицинской профилактики за 2018 год, приоритетные направления на 2019 год
Итоги деятельности службы медицинской профилактики за 2018 год, приоритетные направления на 2019 год Очаговые тени. Рентгенопульмонология
Очаговые тени. Рентгенопульмонология Вирусы – возбудители гриппа, парагриппа, ОРВИ, паротита и кори
Вирусы – возбудители гриппа, парагриппа, ОРВИ, паротита и кори Оперативные доступы к органам брюшной полости
Оперативные доступы к органам брюшной полости Факоматозы. Туберозный склероз (болезнь Бурневилля - Прингла). Нейрофиброматоз
Факоматозы. Туберозный склероз (болезнь Бурневилля - Прингла). Нейрофиброматоз Геморрагическая лихорадка Эбола
Геморрагическая лихорадка Эбола Type of Imaging Modalities In Radiology
Type of Imaging Modalities In Radiology Регуляция сосудистого тонуса. Особенности регионарного кровообращения
Регуляция сосудистого тонуса. Особенности регионарного кровообращения