Содержание
- 2. 1. Дисоціація води 2. Водневе число 3. Водневий показник 4. Загальна й активна кислотність 5. Індикатори
- 3. 8. Буферні розчини 9. Властивості буферних розчинів 10. Визначення рН буферним методом 11. Значення рН і
- 4. Дисоціація води
- 6. Вода – універсальний розчинник для більшості мінеральних і органічних речовин.
- 7. Організм тварини в середньому містить 65,9 % води, жива клітина — 85, кора головного мозку —
- 8. Величина константи дисоціації води при 25 °С дорівнює 1,8•10-16. Методом електропровідності встановлено, що концентрація іонів водню
- 9. Концентрації іонів Н+ і ОН- — величини сполучені. Щоб визначити реакцію середовища розчину, необхідно знати концентрацію
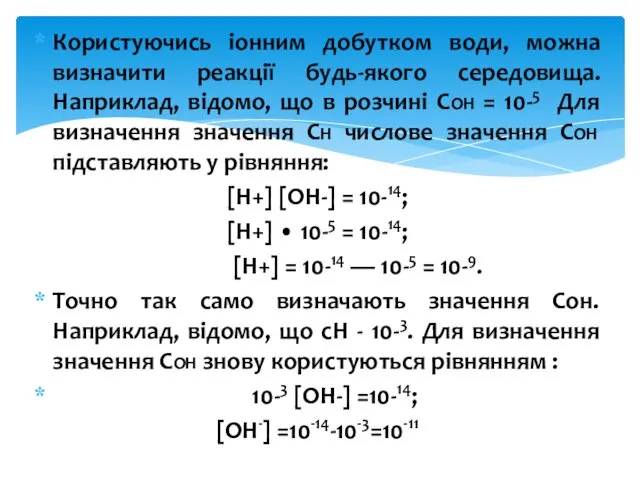
- 10. Користуючись іонним добутком води, можна визначити реакції будь-якого середовища. Наприклад, відомо, що в розчині СОН =
- 11. Визначення СН за допомогою лакмусового папірця дозволяє виділити три середовища: кисле (від 0° до 10-6,9),- нейтральне
- 12. Водневий показник рн — величина, що характеризує концентрацію (активність) іонів водню в розчинах. Він чисельно дорівнює
- 13. У різних розчинах міститься неоднакова кількість іонів Н+ і ОН-. При нейтралізації кислоти лугом іони Н+
- 14. Загальна кислотність нормальних розчинів усіх кислот однакова, вона дорівнює 1 моль кислотного водню в 1 л
- 15. Концентрація іонів кислотного водню дорівнює загальній концентрації кислоти в 1 л, помноженої на ступінь дисоціації. Для
- 16. Розчини основ відрізняються один від іншого концентрацією іонів ОН-. Як і в розчинах кислот, розрізняють загальну,
- 17. Індикатори (від лат. indico — указую) — речовини за допомогою яких визначають рн середовища, установлюють крапку
- 19. Найбільший інтерес представляють кислотно-лужні індикатори. Вони застосовуються для колориметричного методу визначення рн і в хімічному аналізі
- 20. За допомогою індикатора можна визначити значення рН. Область значення рН, у межах якої відбувається помітна неозброєним
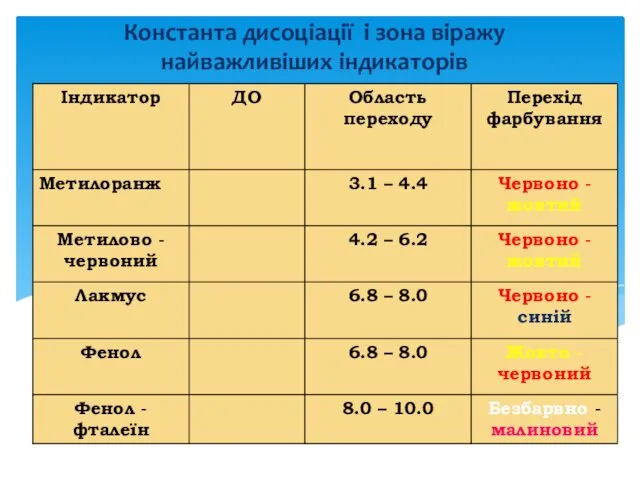
- 21. Константа дисоціації і зона віражу найважливіших індикаторів
- 22. Водневий показник, дорівнює показнику константи дисоціації індикатора, називається крапкою переходу. Індикатор у крапці переходу приймає проміжне
- 23. Колориметричний (від лат. color — колір і греч. metric — вимірюю, визначаю) метод визначення рН заснований
- 25. З даного закону випливає, що при рівному поглинанні світла двома розчинами 'з який концентрація одного відома
- 26. Електрометричний метод визначення рн заснований на вимірі електрорушійної сили (э.д. с.), що виникає в результаті різниці
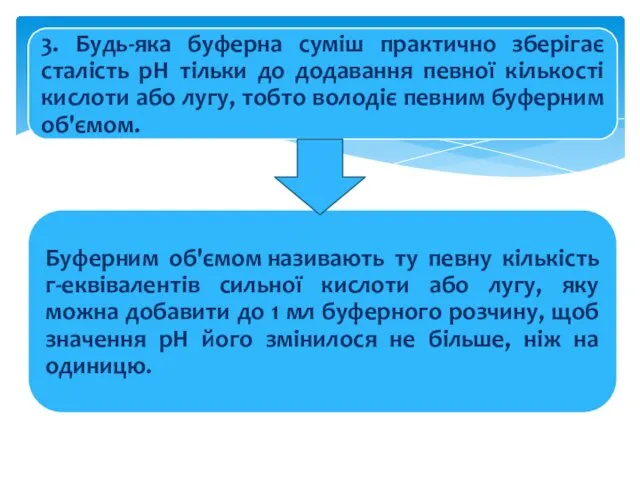
- 27. Буферні розчини — це розчини, що містять буферні системи. Буферними системами називаються суміші, у складі яких
- 28. Буферні розчини знаходяться у водах світового океану, ґрунтових розчинах і живих організмах. Буферні розчини виконують таку
- 29. Також розрізняють природні і штучні буферні розчини: Природним буферним розчином є кров, що містить гідрокарбонатну, фосфатну,
- 30. Властивості буферних розчинів
- 33. Буферні розчини застосовуються для визначення рн. По таблицях готують ряд стандартних буферних розчинів з поступово зростаючим
- 34. Концентрація іонів Н+ має важливе значення для плину багатьох біохімічних процесів в організмах тварин і рослин.
- 35. Дані про оптимум рН для розвитку хвороботворних мікробів варто враховувати при розробці мір боротьби з різними
- 37. Скачать презентацию






























 Строительство физкультурно-оздоровительного комплекса
Строительство физкультурно-оздоровительного комплекса Судовая паросиловая установка
Судовая паросиловая установка Дискретные структуры. Комбинаторный анализ. Сочетания. Размещения
Дискретные структуры. Комбинаторный анализ. Сочетания. Размещения Синтез САР
Синтез САР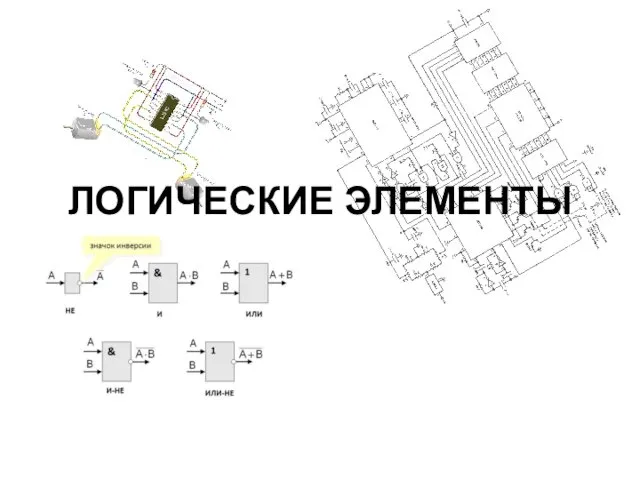 Логические элементы
Логические элементы Аддитивные технологии
Аддитивные технологии Викторина о грибах
Викторина о грибах Россия - наша Родина
Россия - наша Родина Урок по физике -химии для 5 класса Строение вещества. Химические элементы
Урок по физике -химии для 5 класса Строение вещества. Химические элементы Вторичные дистонии
Вторичные дистонии Роль иностранного капитала в экономике России XIX-XX веков
Роль иностранного капитала в экономике России XIX-XX веков Базовые технологии локальных сетей
Базовые технологии локальных сетей Магнитное поле, его характеритики, виды
Магнитное поле, его характеритики, виды Презентация для родителей Артикуляционная и пальчиковая гимнастика.
Презентация для родителей Артикуляционная и пальчиковая гимнастика. БИОНИКА_АЭРОДИНАМИЧЕСКИЕ ПРОТОТИПЫ - презентация из серии БИОНИКА
БИОНИКА_АЭРОДИНАМИЧЕСКИЕ ПРОТОТИПЫ - презентация из серии БИОНИКА Производство пеллет
Производство пеллет 24 марта - Всемирный день борьбы с туберкулезом
24 марта - Всемирный день борьбы с туберкулезом კონსტიტუცია. ძირითადი კანონი
კონსტიტუცია. ძირითადი კანონი Лишайники
Лишайники Порядок и основные этапы создания субъектов предпринимательского права
Порядок и основные этапы создания субъектов предпринимательского права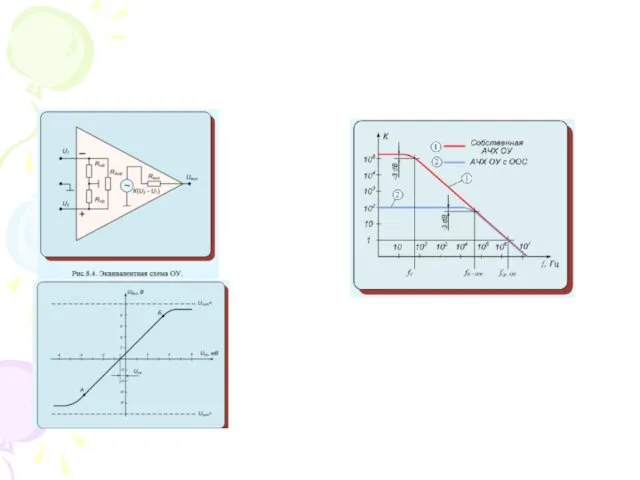 Операционные усилители
Операционные усилители Перегрузочные комплексы универсального назначения с крановыми схемами механизации
Перегрузочные комплексы универсального назначения с крановыми схемами механизации Проектирование поста обслуживания трансмиссий легковых автомобилей
Проектирование поста обслуживания трансмиссий легковых автомобилей Сборка графического компьютера за 50 тысяч рублей
Сборка графического компьютера за 50 тысяч рублей Павловопосадские платки. Статья и презентация
Павловопосадские платки. Статья и презентация Мой классный коллектив…Каким ему быть?
Мой классный коллектив…Каким ему быть? Сложение двоичных чисел с фиксированной запятой
Сложение двоичных чисел с фиксированной запятой Балансировка роторов
Балансировка роторов